角膜胶原交联术后无菌性角膜炎的临床特征及治疗转归
2023-10-07顾宇伟庞辰久任胜卫杨凯丽徐丽妍王树林
顾宇伟 庞辰久 任胜卫 杨凯丽 范 棋 徐丽妍 张 波 王树林 李 金
圆锥角膜是一种以角膜基质进行性变薄、角膜中央或角膜旁中央扩张向前呈锥形突起为特征的眼病[1-2],常于青春期发病,进行性进展,发病机制为角膜胶原排列紊乱、角膜生物力学下降,通过增加角膜生物力学强度,可控制该病的进展[3]。角膜胶原交联术(CXL)以核黄素作为光敏剂,用365 nm的紫外线对角膜局部进行照射,通过增加角膜胶原纤维之间的化学链接,提高角膜基质的硬度,从而控制或延缓圆锥角膜的发展[2]。CXL安全、有效[4-7],但也存在一些并发症,文献报告的并发症有角膜混浊、基质水肿、内皮损伤、无菌性角膜炎及感染性角膜炎等[8-10],其中无菌性角膜炎报道较少,国外报道发病率为0.97%~7.60%[11-14],国内文献尚未见报道。本研究对行CXL的387只圆锥角膜眼进行观察,计算CXL术后无菌性角膜炎的发生率,分析其临床特征及其诊疗过程,以期为临床工作提供指导。
1 资料与方法
1.1 研究对象
选择2018年1月至2020年9月在河南省立眼科医院屈光手术中心行CXL的圆锥角膜患者(281例387眼)进行回顾性分析。所有患者均进行术前检查,包括裸眼视力、主觉验光、最佳矫正视力(BCVA)、三维眼前节分析系统、角膜生物力学分析仪、傅里叶光学相干断层扫描仪(RTVue-OCT)、频域眼前节光学相干断层成像(SS-1000 OCT)、角膜内皮细胞显微镜、眼轴、眼压、裂隙灯显微镜及眼底检查等。
1.2 CXL患者入选与排除标准
CXL患者入选标准:(1)年龄<40岁;(2)符合圆锥角膜诊断标准[1-2],并处于进展阶段:角膜地形图在12个月内连续两次的观察中发现角膜最大曲率(Kmax)增加>1 D;主觉验光或散光增加>1 D[12];(3)角膜最薄点厚度(TCT)>400 μm;(4)CXL前至少已停戴硬性透氧性角膜接触镜≥4周。排除标准:伴其他眼部活动性病变者,既往有角膜手术史、角膜瘢痕以及TCT低于 400 μm者。
CXL术后发生无菌性角膜炎的圆锥角膜患者为炎症组(9例11眼),并选取同期CXL术后无并发症的圆锥角膜患者为对照组(23例30眼)。所有患者均进行术前常规检查,术前均被告知手术过程及相关并发症,患者本人或其监护人均签署知情同意书。本研究符合《赫尔辛基宣言》的伦理标准,并经河南省立眼科医院医学研究伦理委员会批准[批文号:HNEECKY-2019 (5)]。
1.3 手术方法
所有患者均于术前3 d开始滴5 g·L-1左氧氟沙星滴眼液,每天4次,使用紫外光照射系统对患者进行快速角膜去上皮CXL 或跨上皮CXL(使用RTVue-OCT测量,角膜基质厚度>400 μm行去上皮CXL,其余行跨上皮CXL)。(1)去上皮CXL:使用体积分数20%新鲜乙醇浸泡角膜20 s,去除角膜中央直径9 mm区的上皮,1.0 g·L-1核黄素(ViberX Rapid)充分湿润裸露基质10 min,生理盐水冲洗残余核黄素,光照强度30 mW·cm-2的紫外光照射4 min,总能量7.2 J·cm-2。术毕,予1滴5 g·L-1左氧氟沙星滴眼液和1 g·L-1氟米龙滴眼液,戴角膜绷带镜。(2)跨上皮CXL:2.5 g·L-1核黄素(Paracel)充分湿润角膜4 min,再用2.2 g·L-1核黄素(Viber-Xtra)充分湿润角膜6 min,生理盐水冲洗残余核黄素,光照强度45 mW·cm-2紫外光脉冲式1:1 照射5 min 20 s,总能量7.2 J·cm-2。术毕,给予1滴5 g·L-1左氧氟沙星滴眼液和1 g·L-1氟米龙滴眼液,戴角膜绷带镜。
术后5 g·L-1左氧氟沙星滴眼液滴眼,每天4次,每次1滴,每天复查直至上皮愈合后摘除角膜绷带镜;1 g·L-1氟米龙滴眼液滴眼,术后第1周每天4次,每次1滴,逐周递减共持续 4~8周;3 g·L-1玻璃酸钠滴眼液滴眼,每天4~6次,每次1滴,持续3~6个月。
1.4 无菌性角膜炎的诊断
1.4.1 症状
因CXL术后会有眼痛、异物感、畏光、流泪等症状,术后早期出现无菌性角膜炎的患者通常自觉症状不明显。角膜上皮愈合后出现无菌性角膜炎患者可伴有疼痛、异物感、烧灼感、畏光、流泪增多等症状。
1.4.2 体征
裂隙灯显微镜检查可见:病灶呈灰白色,边界较清晰,多发生在角膜周边部、交联治疗区范围以外,部分病灶呈弧形(环形)或孤立圆形,病灶与角膜缘间可有一透明区,少数病灶位于角膜旁中央区、甚至角膜中央区;部分病灶角膜上皮完整,伴睫状充血;严重者可伴前房闪辉,甚至前房积脓。病灶多于CXL术后1周内出现。
1.4.3 辅助检查
病变部位上皮完整的患者可以联合前节OCT及共聚焦显微镜辅助诊断。病变部位有溃疡形成的患者应立即行角膜刮片、细菌培养及药敏检查,并可联合共聚焦显微镜及前节OCT辅助诊断。
1.5 无菌性角膜炎的治疗
发现患者出现无菌性角膜炎后,立即摘除角膜绷带镜,1 g·L-1氟米龙滴眼液滴眼,每天6次,每次1滴;5 g·L-1左氧氟沙星滴眼液滴眼,每天4次,每次1滴;玻璃酸钠滴眼液滴眼,每天4~6次,每次1滴;病情缓解后1 g·L-1氟米龙滴眼液逐步减量。若角膜上皮尚未愈合,1 g·L-1氟米龙滴眼液滴眼,每天2次,每次1滴,上皮愈合后增加为每天6次。
1.6 检测指标
对炎症组及对照组患者的临床资料进行分析,包括临床特征、治疗及愈后等,并记录两组患者的术前平坦角膜曲率(K1)、陡峭角膜曲率(K2)、散光(Astig)及TCT等参数。
1.7 统计学分析
采用SPSS 23.0对相关资料进行统计分析。数据不符合正态分布者,采用中位数及四分位数间距M(P25,P75)表示。炎症组和对照组患者TCT、K1、K2及Astig的比较采用非参数秩和检验,性别构成采用χ2检验。采用多因素Logistic回归分析无菌性角膜炎发生的影响因素。所有统计学检验均为双侧检验,检验水准:α=0.05。
2 结果
行CXL的圆锥角膜患者281例387眼,其中行去上皮CXL的圆锥角膜患者107例130眼,跨上皮CXL的圆锥角膜患者187例257眼,13例患者的双眼行不同手术(一眼行去上皮CXL,一眼行跨上皮CXL)。术后发生无菌性角膜炎患者9例11眼,发生率为2.84%。其中男5例6眼,女4例5眼;双眼发病者2例,单眼发病者7例;右眼3例,左眼8例。
2.1 无菌性角膜炎患者临床特点与治疗
9例11眼无菌性角膜炎患者发病时间为术后2~6 d,其中4眼术后2 d发病,4眼术后3 d发病,2眼术后5 d发病,1眼术后6 d发病(表1)。1眼同时累及角膜中央区、旁中央区及周边部,1眼累及角膜旁中央区,其余9眼均位于角膜周边部。10眼为圆形孤立病灶,1眼为周边多发病灶,后相互融合呈类弧形灶;所有病灶呈灰白色,边界清晰,伴有睫状充血;11眼中大部分病灶上皮完整,且均位于角膜浅基质层。综合以上病例临床表现,将其分为3类,分别是周边单个病灶,周边多发病灶,累及角膜中央、旁中央的多发病灶。

表1 无菌性角膜炎患者临床特点
无菌性角膜炎患者均予1 g·L-1氟米龙滴眼,5 g·L-1左氧氟沙星及玻璃酸钠滴眼液辅助治疗后迅速好转并治愈。药物治疗后,病灶均于1~4 d内明显好转,最终8眼遗留角膜云翳,3眼角膜完全透明,视力几乎不受影响。
图1示周边部孤立病灶(病例8),术后2 d复查时诉左眼酸涩、异物感,裂隙灯显微镜检查发现左眼睫状充血,角膜缘4点钟位灰白色孤立病灶,该处上皮被覆,边界清晰,位于浅基质层。治疗后遗留角膜云翳。
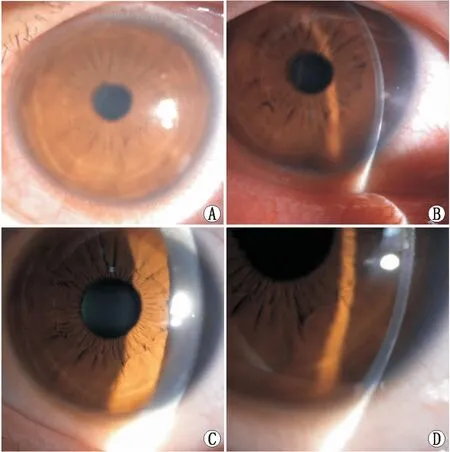
A:治疗前裂隙灯显微镜照相,角膜缘4点钟位1处孤立病灶;B:治疗前裂隙灯显微镜照相,病灶位于浅基质层,上皮完整;C:治疗后裂隙灯显微镜照相,病灶愈后遗留角膜云翳;D:治疗后裂隙灯显微镜照相,云翳位于角膜浅基质层。图1 病例8无菌性角膜炎病灶特征
图2示周边多发病灶(病例2),术后3 d复查无不适,裂隙灯显微镜检查发现左眼睫状充血,角膜缘12~1点钟位见3处孤立灰白病灶,上皮部分缺失,共聚焦显微镜检查结果阴性,未见真菌菌丝及阿米巴样物,药物治疗后好转,遗留角膜云翳,前节OCT检查显示病灶位于浅基质层。
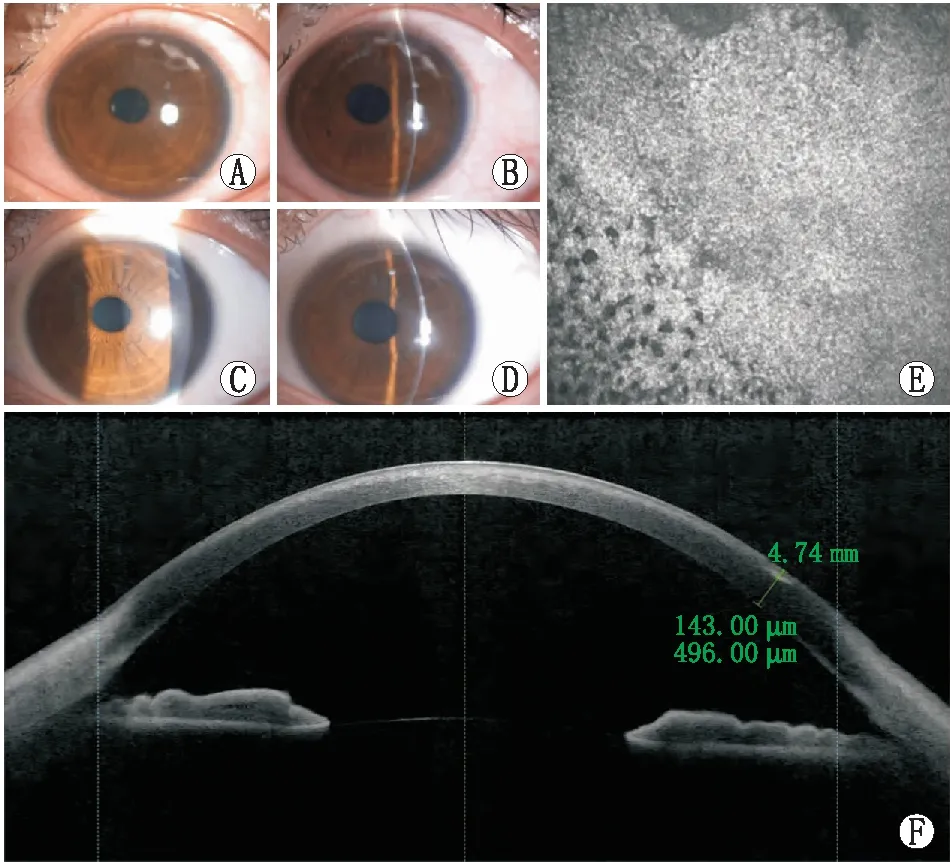
A:治疗前裂隙灯显微镜照相,角膜缘12~1点钟位3处孤立病灶;B:治疗前裂隙灯显微镜照相,病灶位于浅基质层;C:治疗后裂隙灯显微镜照相,病灶处遗留角膜云翳;D:治疗后裂隙灯显微镜照相,角膜云翳位于角膜浅基质层;E:治疗前共聚焦显微镜检查,高反光坏死组织伴大量炎症细胞聚集;F:治疗后前节OCT扫描,病灶深度143.00 μm,边界清晰。图2 病例2无菌性角膜炎病灶特征
图3示累及角膜中央区、旁中央区及周边部的多发病灶(病例1),患者术后3 d复查诉左眼畏光,异物感明显,裂隙灯显微镜检查发现左眼角膜中央区、旁中央区及周边部各1处灰白色孤立病灶,立即摘除角膜绷带镜,共聚焦显微镜检查结果未检出真菌菌丝及阿米巴样物,角膜刮片镜检未见典型真菌菌丝及细菌,病原微生物培养阴性。药物治疗后遗留角膜云翳。
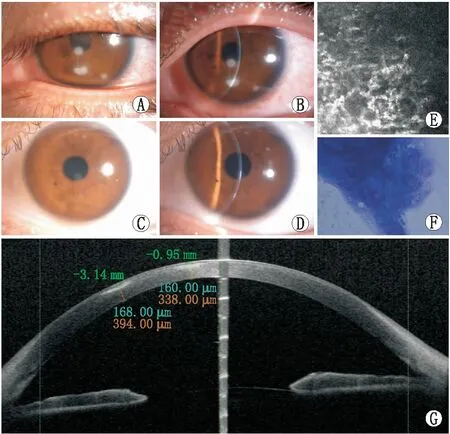
A:治疗前裂隙灯显微镜照相,角膜中央、旁中央及周边部3处孤立病灶;B:治疗前裂隙灯显微镜照相,病灶位于浅基质层;C:治疗后裂隙灯显微镜照相,病灶愈后遗留角膜云翳;D:治疗后裂隙灯显微镜照相,角膜云翳位于浅基质层;E:治疗前共聚焦显微镜检查,浅基质层大量炎症细胞聚集;F:角膜刮片镜检未见典型真菌菌丝,未见细菌;G:治疗后前节OCT扫描,2处病灶深度分别为168.00 μm和160.00 μm,边界清晰。图3 病例1无菌性角膜炎病灶特征
2.2 临床检查指标比较
炎症组和对照组患者年龄、性别、K1、K2、Astig及TCT差异均无统计学意义(均为P>0.05)(表2)。
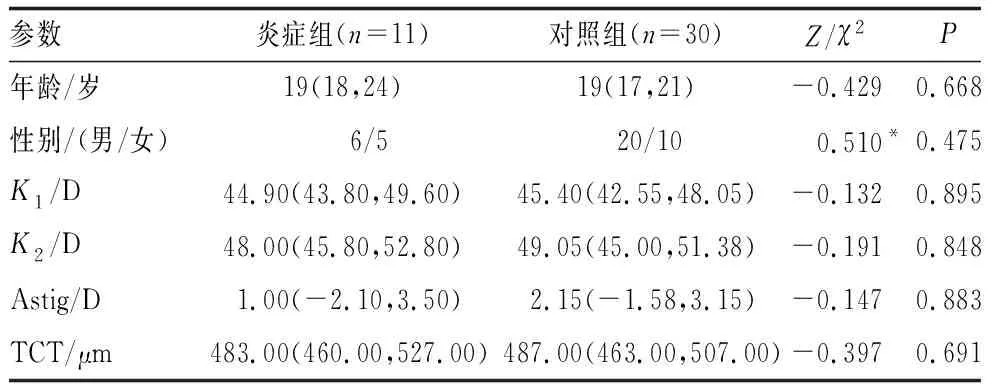
表2 炎症组与对照组患者临床检查指标比较
2.3 Logistic回归分析结果
多因素Logistic回归分析结果显示,年龄、性别、K1、K2、Astig及TCT均不是无菌性角膜炎发生的危险因素(均为P>0.05)(表3)。
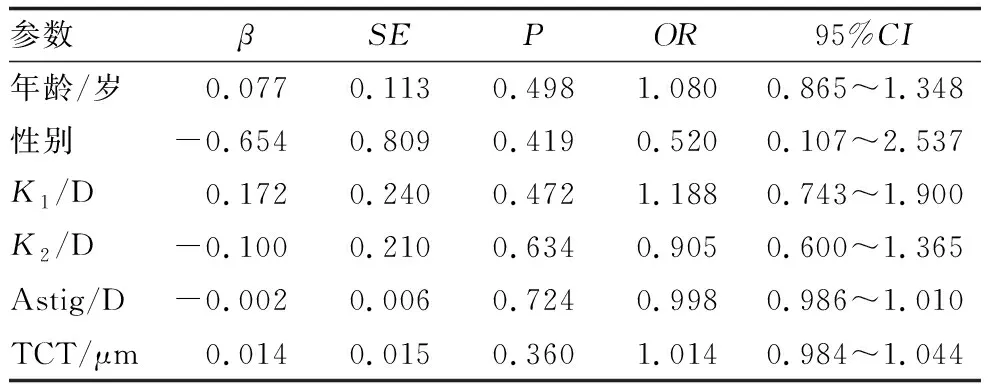
表3 多因素Logistic回归分析结果
3 讨论
无菌性角膜炎可发生在多种角膜屈光术后[15],也可发生在配戴角膜接触镜后[16]。CXL手术是一种通过增加角膜硬度阻止圆锥角膜进展的方法,无菌性角膜炎在CXL术后也有出现[11,17]。2009年Angunawela等[17]首次报道CXL术后出现的无菌性角膜炎,目前国内尚无文献报道。本研究结果发现,无菌性角膜炎均发生在去上皮CXL术后,发生率为 2.84%,与既往研究相比,除Lam等[13]的病例研究中是去除部分上皮外,其余病例均发生在去上皮CXL术后,与本研究结果一致。Cerman等[12]报道CXL术后无菌性角膜炎多发生在术后2~4 d,Lam等[13]研究发现,发生无菌性角膜炎的患者发病时间均为CXL术后1周内,与本研究中患者发病时间(术后2~6 d)一致。本研究中9眼病灶位于角膜周边部浅基质层,与角膜缘间有一透明区;1眼病灶位于角膜旁中央区;1眼累及角膜中央区,均为圆形孤立病灶,呈灰白色,大部分病例上皮完整,边界较清晰,伴有睫状充血。本研究未见环形病灶及前房反应,可能与本研究中病灶发现较早,多在病灶未融合前发现并及时治疗有关[11-13]。该病主要与感染性角膜炎相鉴别,上皮完整的患者可以联合前节OCT及共聚焦显微镜辅助诊断。病灶有溃疡形成的患者应立即行角膜刮片、细菌培养及药敏检查,并可使用共聚焦显微镜检查及前节OCT辅助诊断。此外,在Kodavoor等[18]的研究中,1例基质环植入联合CXL的患者出现了2处无菌性病灶并伴前房积脓,因此,应警惕CXL术后前房炎症反应的出现。
该病起病隐匿,既往文献中患者多为复查摘除角膜接触镜时发现,本研究中部分患者发病无自觉症状,部分患者伴有疼痛、异物感、烧灼感、畏光、流泪增多等症状。临床治疗中皮质类固醇激素的可选种类较多,建议根据患者病情轻重程度进行相应选择。Ghanem等[11]报道的无菌性角膜炎多为环形浸润,多使用5 g·L-1氯替泼诺及10 g·L-1泼尼松龙滴眼治疗等,Angunawela等[17]的研究中使用1 g·L-1地塞米松频繁滴眼治疗无菌性角膜炎,本研究中患者病灶发现早,病情较轻,治疗及时,1 g·L-1氟米龙即可获得良好的治疗效果。本研究中无菌性角膜炎治愈后多遗留角膜云翳,对视力几乎没有影响,既往文献中除García de Oteyza等[19]的研究中因为角膜瘢痕行角膜移植手术外,局部使用类固醇类的药物治疗一般均能获得良好效果。因此,临床医师应重视患者行CXL术后的复查,及早发现无菌性角膜炎等CXL术后并发症,制定个性化的治疗方案,有利于患者的预后。
该病的发病原因目前并未完全清楚,主要推测有以下几个方面:Angunawela等[17]研究认为,CXL术后无菌性角膜炎可能与角膜绷带镜下泪液中的葡萄球菌的抗原引起的细胞免疫有关。Ghanem等[11]提出了CXL过程中紫外光照射对角膜基质产生的光毒性可能是引起无菌性角膜炎的主要机制,此外CXL后的蛋白抗原性改变引起的自体免疫与CXL术后的无菌性角膜炎有关。有学者在研究中发现去上皮导致的上皮损伤可能是CXL术后无菌性角膜炎发生的主要机制,并且术后使用非甾体类抗炎药可以增加无菌性角膜炎的发生率[12];也有研究认为厚度更薄、曲率更陡峭的角膜更容易发生无菌性角膜炎[13,18]。本研究通过对炎症组与对照组归纳分析发现,无菌性角膜炎的发生与TCT、曲率陡峭程度无关,但未能针对免疫方面进行深入研究,因此,未来的研究中需要增加样本量及相关检查,进一步研究该病的发生机制。
4 结论
无菌性角膜炎是CXL 术后的主要并发症之一,因此,在临床工作中,对于去上皮CXL的患者,术后一定严格随访,定期复查,早发现、早诊断和早治疗,避免出现严重的无菌性角膜炎,提高患者的视觉质量。
