胰管括约肌切开联合胰管支架在胆管微结石性急性特发性胰腺炎中的应用研究
2023-09-29胡浔科余亚平
胡浔科 余亚平
【摘要】 目的 探讨胰管括约肌切开(EPS)联合胰管支架在胆管微结石(BML)性急性特发性胰腺炎(AIP)中的应用效果。方法 回顾性分析2020年4月—2021年10月景德镇市第二人民医院收治的BML性AIP患者,根据治疗方式将其分为2组,其中30例接受EPS联合胰管支架治疗的患者为研究组,另30例接受内镜下乳头括约肌切开(EST)联合胆管清理治疗的患者为对照组。对比2组住院费用与住院时间,术后并发症情况、术前与术后1 d时2组实验室检查指标;随访6个月,统计2组术后胰腺炎(PEP)与胆管并发症的发生率。结果 2组患者住院费用与住院时间对比,差异无统计学意义(P>0.05);2组术后并发症对比,差异无统计学意义(P>0.05)。术后1 d时,研究组白细胞、血淀粉酶较对照组低(P<0.05),2组ALT、总胆红素、CRP差异无统计学意义(P>0.05)。随访6个月,2组PEP发生率对比,差异无统计学意义(P>0.05);研究组胆管并发症发生率低于对照组(P<0.05)。结论 EPS与胰管支架联合治疗BML性AIP效果确切,能够保留胆管括约肌功能,降低胆道并发症风险,具有临床推广价值。
【关键词】 急性特发性胰腺炎;胆管微结石;胰管括约肌切开;胰管支架;治疗效果
中图分类号:R576 文献标识码:A
文章编号:1672-1721(2023)13-0041-03
DOI:10.19435/j.1672-1721.2023.13.013
急性胰腺炎(AP)在临床十分常见,其发病原因尚未完全明确,多数患者与胆石症、高脂血症与酒精因素有关,而约10%~30%的患者经病史、实验室检查、体检与常规影像学评估后仍难以确定病因,此类AP可以认定为急性特发性胰腺炎(AIP)[1]。一些研究发现,胆管微结石(BML)与AIP发病密切相关,即微结石一过性地嵌顿于十二指肠头所致[2]。目前,内镜下乳头括约肌切开(EST)以及清理胆管是治疗胆源性AIP的主要手段,但其对于乳头括约肌损伤较重,继而增加了胆管并发症风险,影响预后。胰管括约肌切开术(EPS)对胆管括约肌功能具有一定的保留,继而抑制了胆管并发症。然而,有研究认为EST 与EPS存在经内镜逆行胰胆管造影(ERCP)术后胰腺炎(PEP)风险[3]。胰管支架预防性置入则为EPS 治疗BML性AIP提供了有利的支持,其可以缓解胰管压力,促使胰液引流通畅,胰管内的消化酶排空调节自我消化问题,继而降低了PEP风险。本研究回顾性分析60例BML性AIP患者的临床资料,对比EST并胆管清理与EPS并胰管支架的疗效,报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2020年4月—2021年10月景德镇市第二人民医院收治的BML性AIP患者资料,根据治疗方式将其分为2组,其中30例接受EPS联合胰管支架治疗的患者为研究组,另30例接受EST联合胆管清理治疗的患者为对照组。对照组:男17例,女13例;年龄22~75岁,平均年龄(50.65±7.78)岁;AIP分类为轻度27例,中度3例;急性生理及慢性健康状况(APACHEⅡ)评分为3~10分,平均(5.62±1.25)分。研究组男18例,女12例;年龄25~73岁,平均年龄(50.60±7.68)岁;AIP分类为轻度28例,中度2例; APACHEⅡ评分为3~10分,平均(5.60±1.34)分。2组一般资料对比无明显差异(P>0.05)。本次研究方案已取得该医院医学伦理委员会批准。
1.2 选取标准 纳入标准:符合《中国急性胰腺炎诊治指南》[4]对于AIP的诊断与分类标准,经肝胆超声、MRI、CT、免疫学指标、血脂、血钙、病史等检查证实;胆管超声或显微镜下胆汁分析检查明确存在BML,且结石或泥沙样结石直径<2 mm,临床资料完整。排除标准:其他原因所致的AP;慢性胰腺炎;ERCP检查排除胰腺分裂、壶腹肿瘤、Oddi括约肌功能障碍、胰胆管汇流异常;患有其他消化系统疾病;恶性肿瘤;免疫与血液系统疾病。
1.3 方法 对照组行EST与胆管清理治疗,方法:患者取左侧俯卧位,全麻,十二指肠镜置入至十二指肠降段,探寻到十二指肠乳头,导丝引导下胆管插管,行乳头括约肌切开。之后通过取石球囊对胆管进行清理,留置鼻胆管引流。研究组行EPS联合胰管支架治疗方法:十二指肠镜置入至十二指肠降段,探查并调整乳头位置,在导丝引导下胰管插管,行胰管括约肌切开,之后沿导丝缓慢向胰管中段放置胰管支架,近端位于十二指胰内1 cm,退出导丝,镜下对胰液外溢情况予以观察,并通过X线透视明确支架部位。术后1~2个月拍摄腹部平片,并在十二指肠镜下将胰管支架取出。2组术后常规补液、禁食,并予以抑酶、抑酸、抗炎等对症治疗3 d。
1.4 观察指标 (1)住院费用与住院时间。(2)术后并发症,包括:术后出血、感染、穿孔等。(3)术前与术后1 d时2组實验室检查指标:白细胞、血淀粉酶、丙氨酸转氨酶(ALT)、总胆红素、C反应蛋白(CRP)。(4)随访6个月(门诊随访与电话随访方式),对比2组PEP与胆管并发症的发生率。PEP诊断标准[5]:(1)术后上腹部疼痛症状;(2)24 h血清淀粉酶>正常值的3倍;(3)有胰腺炎影像学特征,上述指标符合2条即可确诊。胆管并发症包括胆管结石、胆管炎、胆囊结石、胆囊增大胆囊炎等。
1.5 统计学方法 使用SPSS 23.0统计学软件进行数据处理,计量资料以x±s表示,采用t检验,计数资料以百分比表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
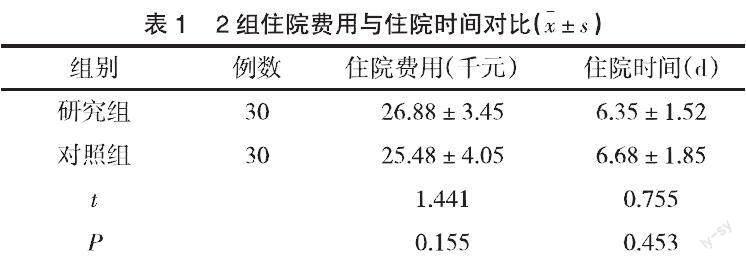
2.1 2组住院费用与住院时间对比 2组住院费用与住院时间差异无统计学意义(P>0.05),见表1。
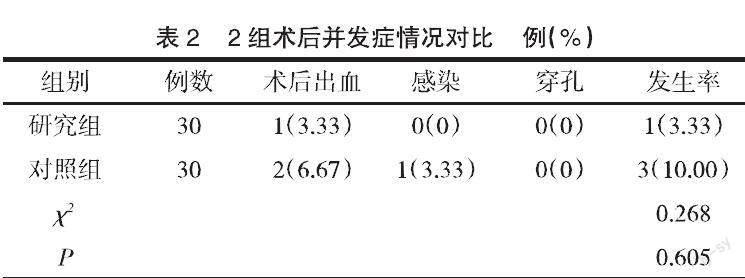
2.2 2组术后并发症比较 2组术后并发症发生率差异无统计学意义(P>0.05),见表2。
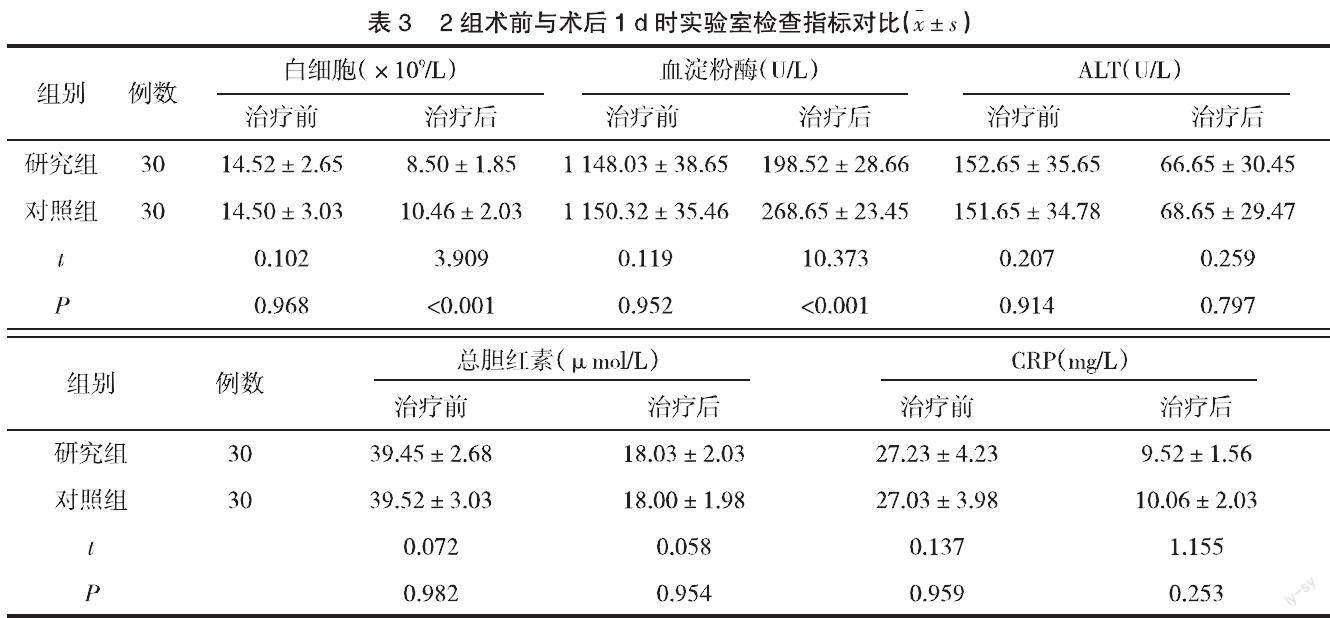
2.3 2组术前与术后1 d时实验室检查指标对比 2组术前白细胞、血淀粉酶、ALT、总胆红素、CRP比较,差异无统计学意义(P>0.05);术后1 d,研究组白细胞、血淀粉酶较对照组低(P<0.05),2组ALT、总胆红素、CRP差异无统计学意义(P>0.05),见表3。
2.4 2组随访6个月PEP与胆管并发症发生率对比 随访6个月,2组PEP发生率差异无统计学意义(P>0.05);研究组胆管并发症发生率较对照组低(P<0.05),见表4。
3 讨论
AIP是AP的一种类型,多数患者症状反复发作,对健康与生活质量造成了严重影响,甚至危及生命。有研究发现,约80%的AIP与BML有关,即胆泥或微结石嵌顿在十二指肠乳头诱发[5]。现阶段,胆源性AP主要采用EST与胆管取石协同治疗,然而胆源性AP的发病机制是胆结石嵌顿于胆管,极易造成堵塞乳头开口,或导致开口狭窄,不通畅的胆管进一步增加了胆管的压力,使胆汁向胰管反流,继而诱发AP[6]。BML性AIP的发病机制与胆源性AP有所差异,胆管内微结石具有流动性,能够进入十二指肠,刺激Oddi括约肌,诱发充血、水肿、痉挛等症状,甚至导致功能紊乱与逆向收缩,最终造成AIP发作。因此,临床治疗BML性AIP时不仅在于取出结石解除胆管梗阻,還应保持胰管畅通。
随着医疗技术与内镜设备的发展,ERCP与EST联合胆管清理成为治疗BML性AIP的主要手段,能够解除微结石对于十二指肠乳头的不良刺激。EST术中解除胆胰管壶腹部位梗阻是治疗本病的关键,乳头梗阻持续时间与胰腺炎的严重度、并发症发生率密切相关,尽早解除梗阻,恢复引流通畅利于改善BML性AIP患者的预后。然而,EST术中乳头括约肌切开与鼻胆管引流,易引起胰液或肠内容物向胆管反流,长期作用下增加了胆管并发症,甚至胆管黏膜恶性病变的风险。同时,EST与内镜鼻胆管引流处理了胆管梗阻问题,但小结石仍能够堵塞胰管,胰管高压未得到完全解决,胰液持续渗出易加重病情。有研究发现,早期内镜干预主要集中在胆管清理中,而BML性AIP的致病因素却发生在腺泡细胞与胰管[7]。多数学者认为,腺泡过度刺激与胰管梗阻在BML性AIP早期发挥着重要的作用,胰管破坏与压力增加与发病密切相关[8]。EPS基于BML性AIP的发病机制进行干预,保留了胆管括约肌功能,利于缓解胆管远期并发症。同时,随着医疗材料的发展,胰管支架在AIP的治疗中发挥出了重要的作用。胰管支架能够缓解胰管压力,保证胰液的引流畅通,且促进了胰管内消化酶排空,抑制自我消化作用,继而改善AP症状。本研究对比EST并胆管清理与EPS并胰管支架治疗BML性AIP的效果,结果显示在住院费用、住院时间、术后并发症对比中,2组未见明显差异(P>0.05)。可见,相较于EST联合胆管清理治疗,EPS联合胰管支架治疗的住院费用与时间相当,且未增加术后并发症风险。
有研究认为,EST联合胆管清理治疗BML性AIP的效果较为理想,但术中操作造成了乳头括约肌损伤,由其所致的胆管并发症问题不容忽视[9]。本次研究随访6个月,结果显示研究组胆管并发症发生率低于对照组(P<0.05)。EST操作时将胆总管末端与壶腹括约肌切开,抑制了括约肌相关功能,抗反流屏障受到强烈的干扰后无法抵挡十二指肠内容物逆流至胆管,进一步增加细菌定植与感染概率,而细菌感染也促进了炎症与结石的复发。EPS切开的胰管末端括约肌有限,能够保留胆管括约肌,极大程度上降低了胆管并发症风险。有研究发现,胆管插管困难是PEP的独立危险因素,但预防性置入胰管支架能够避免Oddi括约肌痉挛及壶腹部损伤,缓解胰管高压[10]。本研究随访发现,2组PEP发生率对比无明显差异(P>0.05)。EST已被证实是胰腺炎的独立风险因素,特别是小乳头括约肌切开、反复插管、针刀乳头括约肌预切开等致内镜操作困难时,能够加重乳头水肿,抑制胰液流动,引起PEP及原有胰腺炎进展。EPS联合支架不仅处理了BML,且可以缓解胰管压力,利于胰管引流,排空胰管内的消化酶抑制自我消化,实现胆胰管开口分离,避免结石对胰管开口的过度刺激,改善PEP症状。本研究中虽然2组患者的PEP发生率以及术后1 d时ALT、总胆红素、CRP对比差异无统计学意义(P>0.05),但研究组白细胞、血淀粉酶较对照组低(P<0.05)。可见,经EPS与胰管支架治疗后,BML性AIP患者白细胞与血淀粉酶明显降低,说明其对胰腺炎控制具有明显作用。
综上所述,EPS与胰管支架联合治疗BML性AIP效果确切,能够保留胆管括约肌功能,降低胆管并发症风险,具有临床推广价值。
参考文献
[1] 张其伟,刘念洲.临时胰管支架在急性胆源性胰腺炎治疗中的疗效评估[J].国际外科学杂志,2022,49(1):23-28.
[2] 李谦益,姚文飞,祁洋,等.胰管支架表面括约肌预切开在ERCP困难胆管插管中的应用效果[J].肝胆胰外科杂志,2022,34(3):129-133.
[3] 叶玲,俞佩伶,李国华,等.ERCP术后胰腺炎的发生率及相关危险因素分析[J].南昌大学学报(医学版),2019,59(5):52-55.
[4] 中华医学会消化病学分会胰腺疾病学组,中华胰腺病杂志编辑委员会,中华消化杂志编辑委员会.中国急性胰腺炎诊治指南(2013年,上海)[J].临床肝胆病杂志,2013,29(9):656-660.
[5] 宛星宇,毛屏,赵晟南,等.ERCP联合EST治疗的胆管梗阻患者术后发生急性胰腺炎危险因素分析[J].山东医药,2021,61(21):64-67.
[6] 杨帆,段建峰,丁建龙,等.胰管内支架置入术联合腹腔镜胆囊切除术治疗急性胆源性胰腺炎的临床疗效[J].腹腔镜外科杂志,2021,26(11):843-846.
[7] 张玉琴,陈卫玲,陈章兴.十二指肠乳头旁憩室对括约肌切开术治疗胰管结石的影响[J].胃肠病学和肝病学杂志,2019,28(5):556-558.
[8] 张诚,杨玉龙,何川琦.胰管支架置入联合生长抑素预防内镜逆行胰胆管造影术后急性胰腺炎的疗效评价[J].中华医学杂志,2021,101(4):276-279.
[9] 唐睿,丁俊,李甫,等.早期经胰管方向Oddi括约肌预切开可减少ERCP术后胰腺炎发生[J].外科理论与实践,2020,25(4):306-310.
[10] 李运红,王云,刘加宁,等.双导丝技术联合胰管支架预防经内镜逆行胰胆管造影术后急性胰腺炎的初步研究[J].中华消化内镜杂志,2021,38(9):740-743.
(收稿日期:2023-02-15)
