基于整合药理学及正交试验优选助孕I号直肠导入方的提取工艺研究
2023-09-27黄金珠袁强华周航刘莉夏宛廷曾倩
黄金珠,袁强华,周航,刘莉,夏宛廷▲,曾倩▲
(1.成都中医药大学 护理学院,四川 成都 611137;2.成都中医药大学附属医院,四川 成都 610072;3.成都中医药大学 基础医学院,四川 成都 611137)
补肾活血“助孕I号方” (国家发明专利:ZL2014 1 0390113.7)是国家重点学科成都中医药大学中医妇科团队不孕方向学术带头人、四川省名中医曾倩主任医师基于中医“肾主生殖”藏象理论结合三十余年临证经验,以补肾活血法所立助孕临床协定方。该方由《摄生众妙方》五子衍宗丸化裁而成,由续断、丹参、菟丝子、枸杞子、覆盆子、山药、丝瓜络、山楂8味药组成。补肾精佐以活血,补中有行,诸药合用共奏补肾填精,活血通络之功效。直肠导入法能有效避免肝肠循环,增加盆腔局部血药浓度,是治疗妇科疾病效优、直接的给药途径。研究团队应用助孕I号方水煎药液直肠导入治疗肾虚血瘀不孕症/辅助生殖技术失败患者数千例(年使用2 000余次),结果显示可有效改善子宫内膜容受性、提高自然妊娠率及临床妊娠率。
水煎提取是中药复方临床应用最为传统及广泛的形式,中药复方水煎煮提取有效性需得到充分验证,现代中药复方制剂工艺研究常以多种成分含量或提取率为评价指标,并结合现代数据分析方法来优选提取工艺参数,但由于缺乏相应的药效学试验验证,导致处方的开发应用出现偏差[1]。本研究以处方的临床应用为基础,再结合现代药物制剂研究的定量分析及药理研究手段,将有利于中药复方制剂研究的标准化,进而促进中药临床经验方向的成果转化。基于临床应用基础,以水为提取溶媒,首先采用HPLC-MS/MS结合网络药理学预测筛选本方核心活性成分;再采用正交试验法,以丹酚酸B、川续断皂苷Ⅵ含量及干膏率为指标进行综合加权评分,确定本方的最佳水提工艺参数;再以肾虚血瘀-子宫内膜容受性不良(RDBS-PER)模型大鼠的药效学试验验证助孕I号直肠导入方水提物的疗效,为下一步研究开发提供依据,研究思路框架见图1。
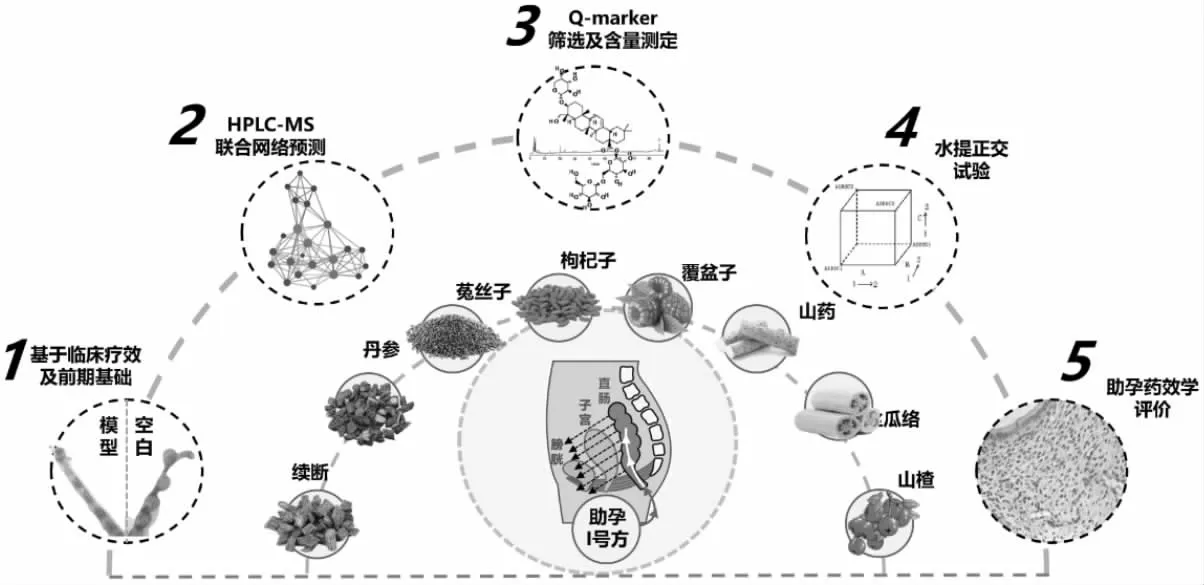
图1 研究思路框架
1 仪器与材料
1.1 仪器
HPLC色谱仪(Agilent 1260),Agilent;电子天平(BP211D型),Sartorius;数控超声波提取器(KH-250B型),昆山和创;数字控温电热套(98-1-C型),电热恒温水浴锅(DK-98-Ⅱ型),泰斯特;恒温培养箱(YZB/USA1802-2009型),Thermo;高速低温台式离心机(型号:5424R),Eppendorf;酶标仪(Synergy H1MF型),BioTek;显微镜(ECLIPSE Ci型),日本尼康株式会社等;数字切片扫描仪(VS200型),OLYM-PUS。
1.2 实验动物
购买无特定病原体动物(SPF)级SD雌性大鼠,体质量(220±10)g,共80只,SD雄性大鼠20只,体质量 (240±10)g(用于交配实验),实验动物购买合格证号:SCXK(川)2020-030,实验动物使用许可证号:SYXK(川)2020-124。实验方案符合动物实验伦理要求,动物伦理审批号:2019DL-006。
1.3 药材、试剂与样品
1.3.1 中药饮片与对照品
酒续断 (批号:1901043),丹参 (批号:1905089),盐大菟丝子(批号:1811023),盐覆盆 子 (批 号:1903029), 枸 杞 子 (批 号:1904004),山药(批号:1903077),山楂(批号:1903043),丝瓜络(批号:1903056),上述饮片均购于四川新荷花中药饮片股份有限公司,符合《中国药典》2020年版相关规定;丹酚酸B(Salvianolic Acid B)对照品 (批号:111562-201716,质量分数:94.1%);川续断皂苷Ⅵ(Dipsacoside VI)对照品(批号:111685-201707,质量分数:90.9%),上述对照品均来源于中国食品药品检定研究院。
1.3.2 试剂
雌二醇(E2)、孕酮(P)、D2聚体(D-Dimer)的ELISA试剂盒(货号F15321、F16576、F15820,均购于上海西唐);E-钙黏蛋白(E-cad),兔多克隆抗体,1∶100(浓度),ER63312,华安生物;IGFBP-1,兔克隆抗体,1∶50(浓度),ER1091-37,华安生物;苏木精染色液;伊红染色液;戊二醛;PBS;PMA;Fix&Perm Kit固定破膜剂;Flow cytometry Staining buffer;流式染色缓冲液。
2 方法
2.1 HPLC-MS/MS结合网络预测筛选助孕I号方活性成分
成分获取:选取助孕I号方按临床常用煎煮方法提取后,取50 mg于2.0 mL离心管中,加800μL 80%甲醇,65 HZ,涡旋振荡充分混匀;4℃超声30 min;于-20℃静置1 h;于4℃,12 000 rpm下离心15 min(离心力×3 000 g);移取200μL上清,加入内标0.14 mg/mL二氯苯丙氨酸5μL,混匀后转入进样小瓶中。使用LC-MS/MS技术进行检测。色谱分离条件:柱温为40℃;流速0.3 mL/min;流动相组成A:水+0.05%甲酸,B:乙腈;进样量:5μL,自动进样器温度4℃。质谱检测参数:正模式:加热器温度300℃;鞘气流速:45 arb;辅助气流速:15 arb;尾气流速:1 arb;电喷雾电压:3.0 KV;毛细管温度:350℃;S-Lens RF Level,30%。负模式:加热器温度300℃;鞘气流速:45 arb;辅助气流速:15 arb;尾气流速:1 arb;电喷雾电压:3.2 KV;毛细管温度:350℃;S-Lens RF Level,60%。通过Analysis Base File Converter软件将LC-MS获得的原始数据转换成ABF格式,MS-DIAL 4.60软件预处理,包括峰提取、去噪音、反卷积,峰对齐,导出CSV格式的原始数据矩阵。提取的峰信息与mz Valult数据库及参考文献进行比对,对匹配结果进行参数过滤:Area≥30 000 000,mzCloud Best Match≥85。
网络预测:通过GeneCards数据库筛选不孕症靶点,通过Swiss Target prediction数据库、BATMAN预测数据库以及本草组鉴数据库结合文献检索,预测助孕I号方对不孕症靶点进行匹配评估,通过Cytoscape构建“方药-成分-靶点-疾病”预测网络。
2.2 丹酚酸B与川续断皂苷含量测定
2.2.1 色谱条件
安捷伦SB-C18色谱柱(250 mm×4.6 mm,5μm);流动相:以乙腈(A)-0.2%磷酸溶液(B)梯度进行洗脱 (0~8 min,5%A;8~18 min,5%→11%A;18~35 min,11%→13%A;35~45 min,13%→20%A;45~60 min,20%→21%A;60~65 min,21%→22%A;65~75 min,22%A;75~80 min,22%→30%A;80~90 min,30% →35% A;后 运 行5 min);检 测 波 长:212 nm;流速:1.0 mL·min-1;进样量:5μL;柱温箱:20℃。
2.2.2 丹酚酸B与川续断皂苷Ⅵ对照品混合溶液的制备
(1)对照品储备溶液制备 精密称取对照品丹酚酸B、川续断皂苷Ⅵ21.24 mg、19.28mg,分别转移至25 mL容量瓶,加甲醇溶解并定容至刻度,摇匀,作为丹酚酸B、川续断皂苷Ⅵ对照品储备溶液。(2)对照品混合溶液制备 精密吸取丹酚酸B与川续断皂苷Ⅵ对照品储备溶液各1 mL,置10 mL量瓶,加甲醇至刻度,摇匀,即可。
2.2.3 全方供试品溶液制备
(1)全方药液制备 按处方比例称取盐大菟丝子等8味饮片220.38 g,加7倍水煎煮2次(第一次多加1倍吸水量,浸泡40 min),每次煎煮30 min,过滤,滤液减压浓缩至2000 mL,2℃~8℃冷藏,备用;(2)全方供试品溶液制备 精密吸取全方药液5 mL,置于25 mL容量瓶中,加甲醇至约23 mL,超声处理10 min,放冷,加甲醇至刻度,摇匀,滤膜(PTFE,0.45μm)过滤,取续滤液,即得。
2.2.4 阴性供试品溶液
按处方比例,称取缺丹参组方饮片200.17 g、缺川续断组方饮片180.12 g,按“2.2.3(2)”项下方法制得阴性供试品溶液。
2.3 干膏率测定
精密吸取药液50 mL(V取液量),分别置已干燥至恒重的蒸发皿中(m),水浴蒸干,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量(M),计算干膏率。
2.4 水提正交试验
采用L9(34)正交试验法对加水量、煎煮时间及煎煮次数等主要影响因素进行考察筛选,采用L9(34)正交试验法优选本方水提工艺。按处方比例取全方中药饮片9份(约220 g/份),浸泡30 min,按表1进行操作,滤过,滤液减压浓缩至2 000 mL(V总药液量);按“2.2.3”项下方法制备供试品溶液,照“2.2.1”项下色 谱条件测定丹酚酸B、川续断皂苷Ⅵ含量;照“2.3”项下方法测定干膏率。

表1 水提L9(34)正交因素-水平设计表
2.5 肾虚血瘀PER动物模型建立及助孕I号方药效学试验验证方法
2.5.1 肾虚血瘀-子宫内膜容受性不良大鼠模型(RDBS-PER)建立
RDBS-PER方案综合参照课题组前期预实验及相关文献方法[2-3]建立,空白组予同等体积0.9%氯化钠注射液假干预处理。模型组大鼠毛发枯槁无光泽,懒动反应迟钝,大便稀软等,光镜下观察模型大鼠种植窗期子宫内膜上皮菲薄,上皮细胞数目明显减少、内膜间质排列紧密且紊乱,较空白组螺旋微、细、小动脉偏少,炎症浸润严重,提示RDBS-PER模型构建成功。
2.5.2 干预及标本获取
大鼠经阴道涂片筛选动情前期时入组,分为空白组、模型组、助孕I号方低剂量组(简称助低组)、中剂量组(简称助中组)、高剂量组(简称助高组)以及对照组(每组n=10只),羟基脲造模开始当日同时予以助孕I号方干预:分别予以低剂量(0.65 g/mL)、中剂量(1.30 g/mL)、高剂量(2.60 g/mL)直肠导入[4]连续10 d,对照组予阿司匹林[5](4.81mg/Kg·d)进行干预。第11天开始,各组筛选动情期大鼠雌雄交配,次日早晨进行阴道涂片,以发现阴栓或者光镜下查见精子视为妊娠第1天(1.0 dpc)。于6.0 dpc上午予以0.3%戊巴比妥钠麻醉后固定,取外周血上清液进行ELISA检测,取左侧上1/2段子宫组织存入4%甲醛中进行HE染色,下1/2段置于戊二醛固定,扫描电镜(SEM)检测;将右侧子宫组织存于甲醛中进行免疫组化监测。
2.5.3 助孕药效学观察指标
观察各组大鼠6.0 dpc一般状态,麻醉后迅速剖离子宫,观察子宫形态并进行着床点计数;按曹蕾等方法[6]进行胞饮突评分和内膜容受性判断;采用ELISA法检测各组大鼠外周血雌二醇(E2)、孕酮(P)、D2聚体表达水平;免疫组化法检测各组大鼠子宫组织中胰岛素样生长因子结合蛋白1(IGFBP-1)、E-钙黏蛋白(E-Cadherin)相对蛋白表达。
3 结果
3.1 利用HPLC-MS联合网络预测筛选助孕I号方核心成分
通过HPLC-MS结合数据库筛选出助孕I号方11个活性成分(图2A-B,表2),对筛选出来的成分进行活性成分作用靶点预测,将不孕症靶点与复方预测靶点进行交集,共获得58个共同作用靶点,通过Cytoscape构建“中药-成分-靶点”网络图(图2C)发现川续断皂苷VI(17个潜在调控靶点,以下简略)、山奈酚 (17)、丹酚酸B(15)、隐丹参酮(12)、山楂酸(6)等成分对不孕症靶点具有良好的调控作用,此外,结合中药复方质量标记物(Q-marker)五原则,考虑成分的独特性、有效性、质量传递及配伍环境,排除广泛存在的非特异性成分,课题组选择助孕I号方中的丹酚酸B和川续断皂苷Ⅵ进行下一步研究。
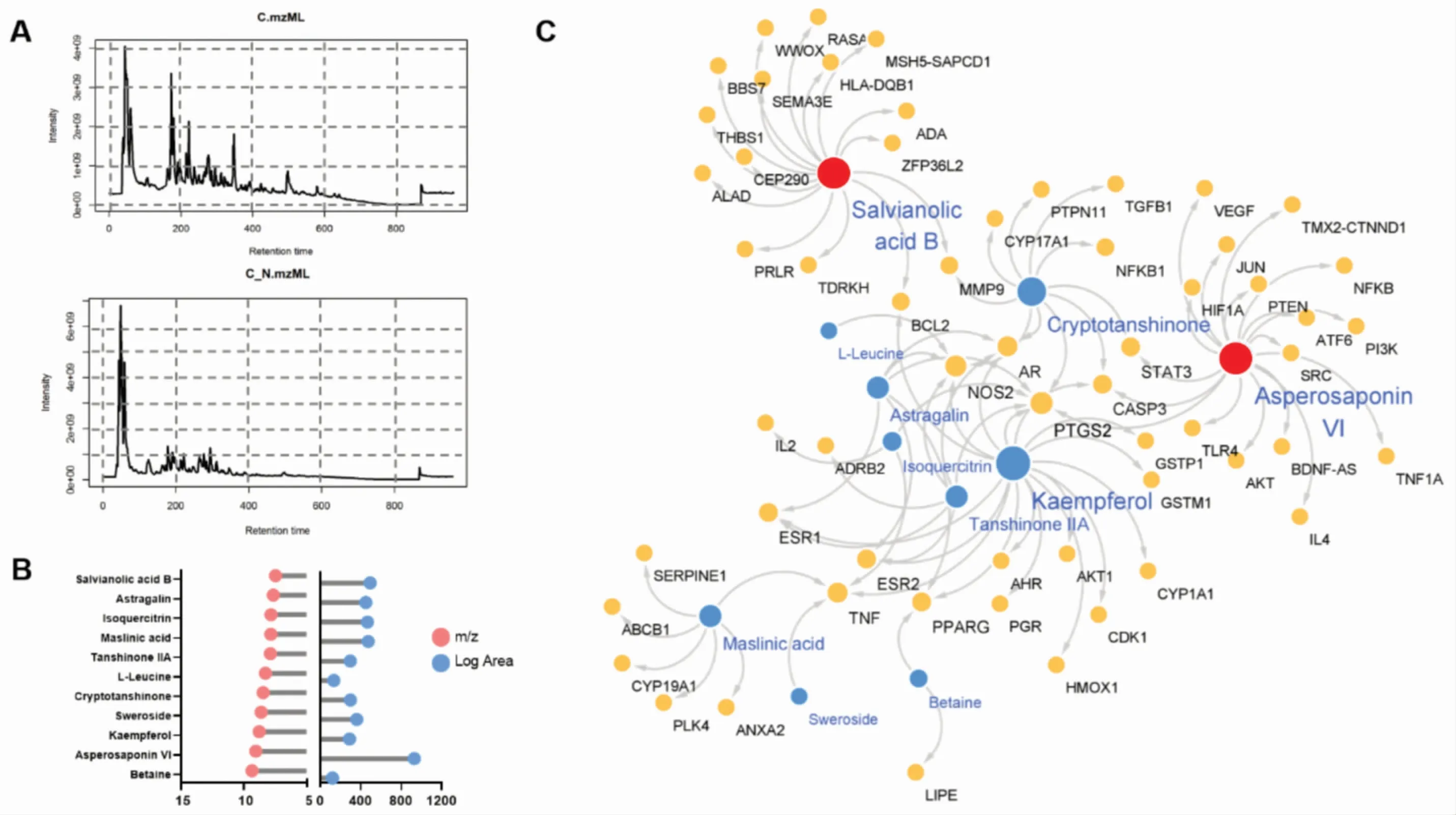
图2 助孕I号方活性成分鉴定及网络预测
3.2 丹酚酸B与川续断皂苷Ⅵ含量测定方法学考察结果
3.2.1 专属性试验
分别精密吸取供试品溶液、混合对照品溶液及各阴性供试品溶液5 μL,注入HPLC,照“2.2.1”项下色谱条件测定,记录色谱图 (图3)。结果显示,缺丹参、缺川续断阴性供试品图谱中丹酚酸B、川续断皂苷Ⅵ无干扰峰出现,且丹酚酸B、川续断皂苷Ⅵ分离度大于1.5,结果表明两种待测成分专属性良好。

图3 专属性试验色谱图
3.2.2 线性范围
分别精密吸取“2.2.2(1)”项下丹酚酸B对照品储备溶液与川续断皂苷Ⅵ对照品储备溶液1、1、1、3、1、2 mL,分 别 置100、50、25、50、10、10 mL量瓶,加甲醇至刻度,摇匀,作为6种不同浓度的丹酚酸B与川续断皂苷Ⅵ对照品混合溶液;精密吸取上述6种浓度的对照品混合溶液各5μL,注入HPLC,照“2.2.1”项下色谱条件测定,以峰面积为纵坐标、进样浓度(μg·mL-1)为横坐标绘制标准曲线,结果见表3。

表3 助孕I号方2种成分的回归方程及线性范围

表4 正交试验结果

表5 方差分析表
表6 各组大鼠外周血D2聚体、雌孕激素表达及子宫组织IGFBP-1、E-Cadherin表达(±s,n=6)

表6 各组大鼠外周血D2聚体、雌孕激素表达及子宫组织IGFBP-1、E-Cadherin表达(±s,n=6)
注:与模型组比较,*P<0.05,**P<0.01
组别外周血雌二醇(E2)/pg·mL-1孕酮(P)/ng·mL-1 D2聚体/ng·mL-1子宫组织IGFBP-1/平均光密度E-Cadherin/平均光密度空白组 67.63±4.48 5.18±0.45** 154.76±45.57**0.23±0.01 0.19±0.03模型组 23.63±1.00 3.76±0.94 245.88±14.09 0.2±0.01 0.25±0.01助低组 41.62±17.72** 4.21±0.80** 242.55±41.63 0.21±0.01 0.25±0.02助中组 67.63±12.12** 4.69±0.67 175.2±57.92* 0.21±0.01 0.22±0.01助高组 57.70±11.34* 4.18±1.45 212.55±31.63 0.21±0.01 0.23±0.01阳性组 71.62±17.72** 5.58±0.45**232.55±46.63 0.22±0.01 0.24±0.02
3.2.3 精密度试验
精密吸取“2.2.2(2)”项下丹酚酸B与川续断皂苷Ⅵ对照品混合溶液5μL,连续进样测定6次,照“2.2.1”项下色谱条件测定,结果见表丹酚酸B、川续断皂苷Ⅵ平均峰面积依此为3 523.0、415.8,RSD依此为0.81%、0.21%,表明仪器精密度良好。
3.2.4 稳定性试验
精密吸取 “2.2.2(2)”项下供试品溶液5μL,分别于0、4、8、12、24 h注入HPLC,照“2.2.1”项下色谱条件测定,结果见表丹酚酸B、川续断皂苷Ⅵ平均峰面积依此为1 551.1、318.0,RSD依此为0.88%、1.00% ,表明供试品溶液在室温条件下24 h内稳定。
3.2.5 重复性试验
精密吸取“2.2.3”项下全方药液10 mL,共6份,置25 mL量瓶中,照“2.2.3(2)”项下方法制备成供试品溶液,精密吸取5μL,注入HPLC,照“2.2.1”项下色谱条件测定,结果见表丹酚酸B、川续断皂苷Ⅵ平均峰面积依此为1 545.8、317.8,RSD 依此为1.36%、0.88%,表明供试品溶液在室温条件下12 h内稳定。
3.2.6 加样回收试验
精密吸取“2.2.3”项下全方药液(每mL含丹酚酸B 0.1 806 mg、川续断皂苷Ⅵ0.264 5 mg)5 mL,共9份,分别置50mL量瓶中,均分为3组,每组分别加入丹酚酸B与川续断皂苷Ⅵ对照品混合溶液(每mL含丹酚酸B 0.450 2 mg、川续断皂苷Ⅵ0.657 0 mg)1、2、3 mL,加甲醇至约45 mL,超声处理10 min,放冷,加甲醇至刻度,摇匀,滤膜(PTFE,0.45μm)过滤,精密吸取续滤液5μL,注入HPLC,照“2.2.1”项下色谱条件测定,计算丹酚酸B、川续断皂苷Ⅵ平均加样回收率依此为98.77%、98.46%,RSD依此为2.00%、2.15%,表明该方法准确度较好,可行。
3.3 正交试验结果
以综合评分为指标,在所选因素水平范围内,各影响因素作用顺序为煎煮次数(C) >加水量(A) >提取时间(B),得出第5号结果综合评分最高,初步优选工艺为A2B2C3;方差分析可知,A因素对煎煮效果呈显著影响(P<0.05),B因素对煎煮效果无显著影响(P>0.05),C因素对煎煮效果呈极显著影响(P<0.01),故在直观分析结果基础上,将提取工艺调整为A2B1C3,即加10倍量水,煎煮3次,40 min/次。
3.4 水提工艺验证
优选出最佳工艺后,按照优选条件进行验证试验,测定丹酚酸B、川续断皂苷Ⅵ及干膏率,已验证优选工艺的重复性及可行性。结果见表7,验证所得各指标RSD均小于3%,表明该工艺稳定可行。
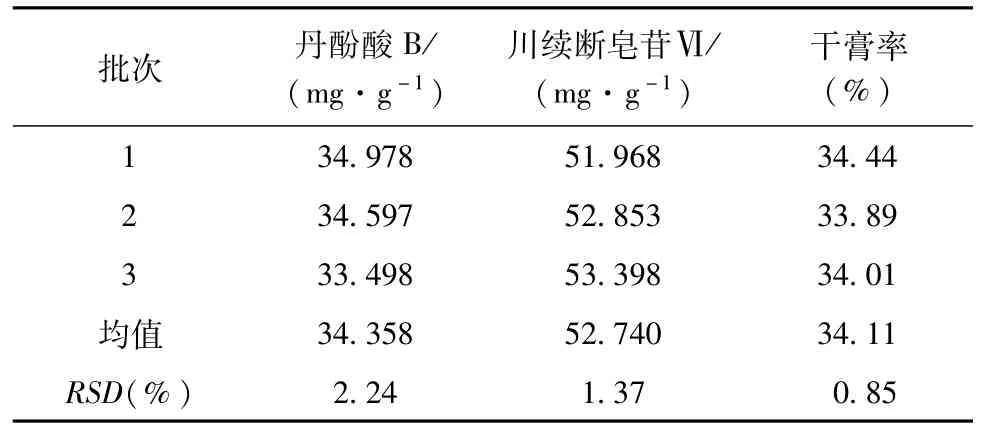
表7 水提工艺验证结果(n=3)
3.5 助孕I号方对RDBS-PER大鼠相关药效学指标测定
3.5.1 各组大鼠着床点数及子宫内膜形态学变化
实验过程中无大鼠死亡,与空白组相比,RDBSPER大鼠着床点数明显降低,差异显著(P <0.001),提示RDBS-PER大鼠子宫发育及胚胎着床明显受到干扰。而助孕I号方各剂量组和对照组大鼠着床点均显著多于RDBS-PER大鼠(P<0.05);光镜下子宫内膜形态:助孕I号方各剂量组大鼠子宫内膜被覆上皮较模型组有明显改善。透射电镜子宫内膜超微结构提示:与空白组相比,RDBS-PER大鼠内膜绒毛稀疏、破损严重,仅见少量小胞饮突表达,胞饮突评分明显下降(P<0.001);助孕I号方各组、对照组胞饮突评分均高于RDBS-PER大鼠(P<0.05),助高组评分显著高于RDBS-PER大鼠(P<0.001)(详见图4)。以上结果提示助孕I号方有改善RDBS-PER模型大鼠“胚-膜”发育不良的作用。

图4 助孕I号方对肾虚血瘀-PER模型大鼠的药效学研究结果
3.5.2 各组大鼠外周血雌二醇(E2)、孕酮(P)、D2聚体及子宫IFGBP-1、ECAD表达水平比较
与空白对照组比较,模型组大鼠外周血E2、P表达明显减弱(P<0.05),D2聚体升高;与模型对照组比较,助孕I号方各剂量组E2、P表达显著性上调(P<0.05),D2聚体表达出现不同程度的下降,以助中组疗效最佳。与空白对照组比较,模型组大鼠子宫组织IGFBP-1表达明显下调(P<0.05)、ECadherin表达明显上调(P<0.05)。与模型对照组比较,助孕I号方各剂量组的子宫组织IGFBP-1表达均著性上调(P<0.05),助孕I号方各剂量组组间差异不明晰,而E-Cadherin表达均明显下调,助中组表型差异更大(详见表6、图5)。

图5 助孕I号方对肾虚血瘀-PER模型大鼠子宫IGFBP-1、E-Cadherin研究结果
4 讨论
研究显示,自然受孕条件下,人类30%的妊娠失败是胚胎着床失败导致,反复着床失败也是辅助生殖技术中的难点。《傅青主女科》云:“精满则子宫易于摄精,血足则子宫易于容物”,精血同源、母子相生,肾精亏虚、津枯血燥,血液则易黏滞而成瘀,胞脉瘀阻则有碍肾中精气化生,且辅助生殖技术反复金刃之邪伤及胞脉胞络、耗损肾气,因此肾虚血瘀是导致胎元不固的主要病机。本研究团队以补肾活血法立方的助孕I号直肠导入方治疗肾虚血瘀不孕症/辅助生殖技术失败患者疗效确切,该协定方的开发、应用、推广具有重要价值。
本研究旨在确定助孕I号直肠导入方的最佳提取工艺,并探讨其对RDBS-PER模型大鼠的子宫内膜组织形态学、着床率、E2、P、D2聚体、IGFBP-1、E-Cadherin表达的影响。本研究通过HPLC-MS联合网络预测揭示丹酚酸B和川续断皂苷Ⅵ是助孕I号方重要的活性成分,前者为丹参主要的水溶性药效成分,具有活血化瘀、抗氧化等药理作用[7-9],后者为续断的主要药效成分,具有抗炎镇痛、治疗先兆性流产等药理作用[10-12],与处方的功能主治一致。
综合考虑多个成分含量和出膏率,通过正交试验筛选出最优的提取工艺,并采用了急毒和药效实验相结合的方法进行了验证。①在优化提取工艺方面,通过正交试验筛选出加10倍量水,煎煮3次,40 min/次的最优提取工艺方案。这些结果表明,最优提取工艺可以使助孕I号方的有效成分得到充分提取。②急毒实验结果表明,所有大鼠在最佳提取方案下均健康存活,未出现明显的毒性反应。这表明最佳提取方案安全无毒,可以用于后续的临床应用和研究。③药效实验结果显示,采用最佳提取方案的助孕I号方中剂量组(1.30 g/mL的)能够显著改善RDBS-PER大鼠的性激素和子宫组织IGFBP-1、E-CAD 表达。IGFBP1作为子宫内膜蜕膜化的重要标志物之一,其表达可用以衡量着床期子宫内膜蜕膜化程度的高低[12]。E-cadherin属于Ⅰ类经典钙黏素,是跨膜糖蛋白的一种,介导上皮细胞之间的黏附,对维持细胞连接有重要作用,对参与着床期上皮-间充质转化(EMT)具有重要作用,从而利于胚胎植入成功[13]。以上结果表明,采用最优提取工艺方案,助孕I号直肠导入方可显著改善模型大鼠子宫内膜容受性,为其后续开发提供了基础依据。
综上,本研究所采用的药效筛选和正交试验方法具有很好的可重复性和可扩展性,可提高中药方剂的提取效率和药效。本研究确定了最佳的提取工艺方案,验证了助孕I号方水提物具有改善肾虚血瘀子宫内膜容受性不良的作用,为助孕I号直肠导入方的下一步研究提供了基础数据和依据。
