氨茶碱联合百令胶囊对稳定期慢性阻塞性肺疾病气道功能及相关指标的影响
2023-09-13李竺宜彭俊杰杨从意姚楷南
李竺宜,彭俊杰,杨从意,吕 莹,姚楷南
深圳市宝安区中医院感染性疾病科,深圳 518000
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)具有不完全可逆气流受限的特征,病情呈进行性发展。COPD的临床表现以气道阻塞为主,患者肺部存在慢性炎症,肺脏受损,在全球死亡原因中居第四位[1]。COPD的主要病理改变为气道重塑,这也是影响患者预后的关键。常规支气管扩张药物吸入难以抑制气道重塑的进展。氨茶碱是临床治疗COPD的常用药,可有效舒张支气管平滑肌,且具有一定抗感染及免疫调节作用[2-3]。百令胶囊为补肺益气中成药,善治由肺肾两虚引起的气喘、咳嗽,其在稳定期COPD患者治疗中的应用日益增多。本院在稳定期COPD的临床治疗中联合应用氨茶碱和百令胶囊取得了较好的效果,本研究拟探讨该治疗方案对患者气道重塑的影响,以明确其作用机制。
1 一般资料
选取收治的稳定期COPD患者作为研究对象。
纳入标准:年龄为18~80岁;满足COPD诊断标准(《慢性阻塞性肺疾病诊治指南》[4])且病情处于稳定期;慢性阻塞性肺疾病全球倡议(global initiative for chronic obstructive lung disease,GOLD)分级≤Ⅲ级;规律接受常规西药治疗6个月以上;患者能积极配合治疗,且均获随访。
排除标准:对试验用药过敏者;伴有急、慢性肺炎者;存在恶性肿瘤疾病者;肺功能Ⅳ级者;呼吸衰竭者;精神病患者;严重神经功能缺损者;无法配合研究者;由其他疾病(如囊性纤维化、肺结核、支气管扩张等)导致气流受限者;存在免疫系统疾病者;近期应用过免疫抑制剂者;中途退出研究者。根据纳入标准与排除标准,本研究共纳入96例患者。用随机数字表法将患者分为对照组、A组和B组,每组32例。本研究通过了医院伦理委员会批准,患者知情了解并签署了知情同意书。
2 方法
2.1 治疗方案
对照组患者接受常规西药治疗,包括对GOLD分级Ⅰ~Ⅱ级者给予硫酸沙丁胺醇吸入气雾剂(山东京卫制药有限公司,规格为100 μg×200掀)吸入,每日2次,每次1吸,对GOLD Ⅲ级者给予布地奈德福莫特罗吸入粉雾剂[瑞典AstraZeneca AB,规格为布地奈德(160 μg·吸-1),富马酸福莫特罗(4.5 μg·吸-1)]吸入,每日2次,每次1吸。另外,对合并高血压、糖尿病者给予降压、降糖等对症治疗。持续治疗8周。
A组在对照组治疗的基础上加用氨茶碱缓释片(西南药业股份有限公司,规格为0.1 g),每次0.1 g,每日2次,口服给药,持续用药8周。
B组在对照组治疗的基础上加用氨茶碱缓释片(西南药业股份有限公司,规格为0.1 g)和百令胶囊(杭州中美华东制药有限公司,规格为0.5 g),持续用药8周。氨茶碱用法、用量与A组相同。百令胶囊剂量为每次5片,每日3次。
2.2 检测方法
(1)血清指标检测:治疗前3 d及治疗结束后3 d,分别采集患者的空腹肘静脉血5 mL,抗凝保存并静置分层。用高速离心机以2 000 r·min-1离心5 min后,取上清液,置于-70 ℃保存待检。使用酶联免疫吸附试验测定血清白细胞介素-2(interleukin-2,IL-2)、白细胞介素-18(interleukin-18,IL-18)、血管内皮生长因子(vascular endothelial growth factor,VEGF)、神经生长因子(nerve growth factor,NGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,b-FGF)、转化生长因子-β1(transforming growth factor-β1,TGF-β1)、核因子-κB(nuclear factor- κB,NF-κB)、烟酰胺腺嘌呤二核苷酸磷酸氧化酶4(nicotinamide adenine dinucleotide phosphate oxidase 4,NOX4)、基质金属蛋白酶-9(matrix metalloproteinase-9,MMP-9)水平。
(2)气道功能检测:治疗前3 d及治疗结束后3 d,分别用肺功能仪测定1次气道功能参数。检查前需停用支气管扩张剂及糖皮质激素等药物24 h以上。测定指标包括第1秒用力呼气容积(forced expiratory volume in 1 second,FEV1)、第1秒用力呼气容积与用力肺活量比值(forced expiratory volume in 1 second/forced vital capacity,FEV1/FVC)、50%肺活量最大呼气流速(maximal expiratory flow after 50% of the FVC has been not exhaled,MEF50)、中段呼气流速(maximal expiratory flow after 25%~75% of the FVC has been not exhaled,MEF25~75)及25%肺活量用力呼气流速(maximal expiratory flow after 25% of the FVC has been not exhaled,MEF25)。
2.3 观察指标
①比较3组治疗前后的血清炎症因子、生长因子及气道重塑相关指标水平的变化情况;②比较3组患者治疗前后的气道功能参数变化情况;③治疗前、治疗结束当天及治疗后1个月,分别用简化36医疗结局研究量表[5](36-item short form survey instrument,SF-36)对患者的生活质量进行评价,量表满分为100分,得分越高表示生活质量越好;④记录、比较3组治疗期间药物不良反应的发生情况。
2.4 统计学方法

3 结果
3.1 基线资料的比较
3组患者的性别、平均年龄、平均病程及GOLD分级比较,差异均无统计学意义(P>0.05)。见表1。

表1 3组患者基线资料的比较
3.2 治疗前后的气道功能参数的比较
治疗前,3组的各气道功能参数比较,差异无统计学意义(P>0.05)。治疗后,3组的FEV1、FEV1/FVC、MEF50、MEF25~75和MEF25均明显升高(P<0.05),3组的各气道功能参数比较差异有统计学意义,FEV1、FEV1/FVC、MEF50、MEF25~75和MEF25均为B组>A组>对照组,组间两两比较差异均有统计学意义(P<0.05)。见表2。
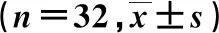
表2 3组患者治疗前后气道功能参数的比较
3.3 治疗前后血清炎症因子水平的比较
治疗前,3组患者的血清IL-2和IL-18水平比较,差异均无统计学意义(P>0.05)。治疗后,3组患者的血清IL-2和IL-18水平均明显降低(P<0.05),3组患者的血清IL-2、IL-18水平比较差异有统计学意义,血清IL-2和IL-18水平均为B组 表3 3组患者治疗前后血清炎症因子水平的比较 治疗前,3组患者的血清VEGF、NGF及b-FGF水平比较,差异均无统计学意义(P>0.05)。治疗后,3组患者的血清VEGF、NGF及b-FGF水平均明显降低(P<0.05),3组患者的血清VEGF、NGF及b-FGF水平比较差异有统计学意义,血清VEGF、NGF及b-FGF水平均为B组 表4 3组患者治疗前后血清生长因子水平的比较 治疗前,3组的各气道重塑分子水平比较,差异无统计学意义(P>0.05)。治疗后,3组的TGF-β1、NOX4、NF-κB及MMP-9水平均明显降低(P<0.05),且TGF-β1、NOX4、NF-κB及MMP-9水平均为B组 表5 3组患者治疗前后气道重塑分子水平的比较 治疗期间,对照组有1例(3.13%)出现恶心,A组有2例(6.25%)发生不良反应(轻度恶心1例,咽喉不适1例),B组有2例(6.25%)发生不良反应(恶心1例,口干1例)。3组的不良反应发生率比较,差异无统计学意义(χ2=0.354,P>0.05)。 与治疗前比较,治疗结束当天3组的SF-36评分均显著升高(P<0.05),但组间比较差异无统计学意义(P>0.05)。治疗后1个月,3组的SF-36评分均高于治疗结束当天(P<0.05),组间比较为B组>A组>对照组,组间两两比较差异有统计学意义(P<0.05)。见表6。 表6 3组患者治疗前后的SF-36评分 COPD作为气流受限的不完全可逆性呼吸系统疾病,即使患者处于病情稳定期,机体仍存在一定的气道炎症,这种气道炎症状态会对气道黏膜、软骨组织等造成缓慢损伤,进而为急性气道病原菌感染创造有利条件。研究指出[6],当血茶碱质量浓度>5 mg·L-1时可发挥治疗作用,但质量浓度>15 mg·L-1即可增加不良反应发生的风险,血茶碱质量浓度≤10 mg·L-1时具有一定的免疫调节及抗感染作用,能抑制嗜酸性粒细胞浸润,释放毒性蛋白,减弱外周血嗜酸性细胞阳离子蛋白对气道上皮的毒性作用。茶碱还能抑制Th2细胞信使RNA表达,减少支气管黏膜中多种炎症因子的表达,进而缓解气道炎症,改善气道高反应性[7-8]。近期有研究显示[9],低剂量茶碱治疗COPD具有显著的抗感染作用。 本研究结果显示,加用氨茶碱缓释片治疗的A组患者,治疗后的血清炎症因子IL-2、IL-8水平均显著低于常规应用吸入型糖皮质激素的对照组,并且A组治疗后肺功能参数、气道重塑分子、血清生长因子的改善效果均优于对照组。这与同类文献报道[10-11]的结果基本一致,其作用机制可能是氨茶碱的抗感染作用机制有别于激素类药物,但氨茶碱可以增强激素的抗感染作用,氨茶碱与糖皮质激素可通过不同的途径发挥作用,二者起到协同作用,有助于气道炎症的控制、解除支气管平滑肌痉挛,从而获得较好的抗炎、解痉效果。 稳定期COPD患者经规律对症药物治疗后,气道相关病理改变可达到停滞状态,但最新研究发现,单纯支气管扩张药物维持治疗并不能逆转气道重塑过程。气道炎症是气道重塑的基石,炎症反应反复发作-修复的过程会引起组织增生,引发不可逆或可逆性较差气道通气功能障碍、气道高反应性[12]。气道重塑进程的持续加剧是COPD患者病情进展的主要机制,近期越来越多的学者推荐在稳定期COPD治疗中加入中成药百令胶囊[13]。百令胶囊由冬虫夏草菌丝制成,具有补肺益气的功效。现代药理研究显示[14],百令胶囊的氨基酸、甘露醇、核酸及微量元素含量丰富,有良好的抗炎、调节免疫、抗肿瘤等作用。本研究结果表明,相比A组,联用百令胶囊和氨茶碱缓释出的B组治疗后气道功能参数(FEV1、FEV1/FVC、MEF50、MEF25~75、MEF25)升高的幅度更明显,表明氨茶碱缓释片与百令胶囊的联合使用能有效改善COPD患者的大气道功能及小气道功能。 直径<2 mm的小气道是气道重塑的主要场所,COPD患者的早期表现以黏液腺及上皮细胞增生为主,随着病情进展可发生杯状细胞增多及管腔黏液分泌增加,小气道管壁结缔组织成分沉积,管壁平滑肌增厚,气道壁血管增生,并最终发生纤维化,造成小气道阻力增加、气流受限,进而使病情加重。气道阻塞、呼吸受阻与气道重塑密切相关,COPD患者的气道重塑会随着病情的发展而不断加重。在呼吸道重塑过程中,TGF-β1/Smade信号通路被激活是一个重要的作用机制[15]。NF-κB为TGF-β1上游分子,中性粒细胞弹性蛋白酶经NF-κB途径可促使气道平滑肌表达TGF-β1,而TGF-β1为致纤维化生长因子,其具有促进肌成纤维细胞增殖、生成细胞外基质,加快呼吸道重塑的作用[16]。高表达的NOX4可促进平滑肌增生、细胞外基质胶原蛋白Ⅳ沉积,从而引发气道重塑。另外,MMP-9在呼吸道重塑过程中也发挥着重要作用,MMP-9可降解细胞外基质,促使基底膜上的气道上皮脱落,炎症细胞穿越血管壁到达炎症部位,从而造成气道损伤,引起气道重塑。血清生长因子b-FGF能调控细胞的增殖、分化,能通过促进肥大细胞增殖来促进气道重塑。NGF由支气管肺泡巨噬细胞分泌,可加快中性粒细胞的分化、生长及趋化。VEGF则能通过结合相关受体来促进巨噬细胞、肥大细胞及中性粒细胞合成,促进气道平滑肌增殖[17]。 本研究结果显示,B组治疗后的气道重塑分子、血清炎症因子及生长因子(b-FGF、NGF及VEGF)水平降幅均比另外2组更明显。这一结果与曹利静等[18-19]的研究结果一致,表明百令胶囊联用氨茶碱可进一步增强抗炎作用,缓解气道炎症,抑制气道上皮细胞增殖,延缓气道重塑。本研究结果还显示,B组治疗后1个月的SF-36得分显著高于另外2组,表明百令胶囊联合氨茶碱治疗稳定期COPD能通过缓解气道炎症、解除呼吸肌痉挛、抑制气道重塑及改善患者呼吸功能来提高患者的生活质量,这与刘艳等[20]的报道相符。 综上所述,对稳定期COPD患者联用氨茶碱和百令胶囊可有效发挥抗炎作用,改善患者的气道功能,抑制气道上皮细胞增殖,延缓气道重塑进程,且安全性好,是治疗稳定期COPD的理想方案。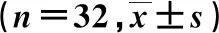
3.4 治疗前后血清生长因子水平的比较
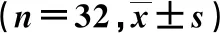
3.5 治疗前后气道重塑分子水平的比较
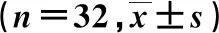
3.6 不良反应发生情况的比较
3.7 生活质量评分的比较

4 讨论
