LC-MS/MS法同时测定诺氟沙星胶囊中的3种杂质
2023-09-13王群葆
曹 旭, 张 琤,刘 涛,王群葆
1.邢台市食品药品检验所,邢台 054000;2. 邢台市第五医院,邢台 054000
诺氟沙星(norfloxacin),别名氟哌酸,化学名称为1-乙基-6-氟-1,4-二氢-4-氧代-7-(1-哌嗪基)-3-喹啉羧酸,是第三代喹诺酮类抗菌药,可选择性抑制消化道内致病菌DNA合成中起作用的DNA促旋酶,从而干扰细菌DNA的复制、转录和修复重组,使细菌无法传代。诺氟沙星胶囊为诺氟沙星常用制剂,主要辅料为淀粉、羟甲基纤维素等,其生产和使用在我国具有广泛性和普遍性。但有研究结果表明,喹诺酮类化合物药物的杂质会引起恶心、头痛、头晕、高血压、光毒性等不良反应[1]。因此,有必要对诺氟沙星胶囊进行杂质分析和有关物质检查。
诺氟沙星原料中的主要杂质为:杂质A(7位取代基为氯,化学名为1-乙基-6-氟-7-氯-4-氧代-1,4-二氢-3-喹啉羧酸);杂质E[氯哌酸,化学名为1-乙基-7-氯-1,4-二氢-4-氧代-6-(1-哌嗪基)-3-喹啉羧酸];杂质K[1位取代基位甲基,化学名为1-甲基-6-氟-1,4-二氢-4-氧代-7-(1-哌嗪基)-3-喹啉羧酸]。它们均为诺氟沙星原料在合成过程中产生的工艺杂质。这些杂质会少量带入诺氟沙星制剂中,从而显著降低其质量。因此,杂质的分离和测定对质量控制、工艺开发过程的反应监测都具有重要意义[2]。诺氟沙星胶囊现行质量标准为2020年版《中华人民共和国药典》(以下简称《中国药典》)二部[3],有关物质项下用高效液相色谱法(high performance liquid chromatography,HPLC)在双波长下对诺氟沙星杂质A和总杂质进行检测并规定了限度要求。《美国药典》(the United States Pharmacopieial,USP)41 版(USP41)[4]、《欧洲药典》(the European Pharmacopoeia,EP)9.3版(EP9.3)[5]未收录诺氟沙星胶囊,但对诺氟沙星原料药中杂质A、杂质E、杂质K均做了限度要求。因标准方法灵敏度有限,各杂质之间分离度达不到要求[6],根据药品杂质分析指导原则和人用药品技术要求国际协调理事会(the international council for harmonisation of technical requirement for pharmaceuticals for human use,ICH)相关规定[7-9],并参考有关文献[10-23]建立了本方法。各杂质结构式见图1。
1 仪器与试药
1.1 仪器
ACQUITY UPLC H-Class TQS液质联用仪(美国 Waters公司);MS205DU电子天平(Mettler Toledo公司);ACQUITY UPLC BEH Shield RP18色谱柱(100 mm×2.1 mm,1.7 μm)购自沃特世科技(上海)有限公司。
1.2 试药
诺氟沙星杂质A(批号111869-201704,质量分数为97.2%)、诺氟沙星杂质E(批号110734-201914,质量分数为96.0%)、诺氟沙星杂质K(批号110714-201809,质量分数为96.2%)、诺氟沙星(批号110714-201809,质量分数为96.2%)均购自中国食品药品检定研究院;诺氟沙星胶囊(市售30批);乙腈(批号171060405001,LC-MS Grade,OMNI CHEM公司);甲酸(批号M185-500,Mreda Technology Inc公司);纯化水(用Milli-Q自制)。
2 方法与结果
2.1 方法
2.1.1混合溶剂的制备 取20 mL乙腈和0.2 mL甲酸,加水至100 mL,即得。
2.1.2对照品储备液的制备 精密称取诺氟沙星、诺氟沙星杂质A、杂质E、杂质K对照品各20 mg,分别置于100 mL量瓶中,加乙腈20 mL使溶解,加2 mL·L-1甲酸溶解,并稀释至刻度,摇匀,即得对照品储备液。
2.1.3混合对照品储备液的制备 分别精密量取2.1.2项下制备的4种对照品储备液各1 mL,置于同一50 mL量瓶中,加混合溶剂至刻度,摇匀,即得混合对照品储备液。
2.1.4标准曲线溶液制备 精密量取2.1.3项下制备的混合对照品储备液适量,制成质量浓度分别为4、20、40、80、160、400 ng·mL-1的对照品系列溶液,备用。
2.1.5供试品溶液的制备 精密称取诺氟沙星胶囊内容物10 mg,置于100 mL量瓶中,加混合溶剂超声10 min使溶解,并稀释至刻度,摇匀,即得。
2.1.6色谱条件 用ACQUITY UPLC BEH Shield RP18色谱柱(100 mm×2.1 mm,1.7 μm),以乙腈(A)-2 mL·L-1甲酸(B)为流动相进行梯度洗脱,流速为0.3 mL·min-1,柱温为40 ℃,进样量为0.5 μL;质谱离子化方式为 ESI,正离子模式。梯度洗脱:0~6 min,7%~4% A;6~7 min,4%~12% A;7~10 min,12%~50% A;10~10.5 min,50%~7% A;10.5~14 min,7% A,用分段模式检测[18],避免高质量浓度的诺氟沙星母核进入质谱。杂质A检测离子对为m/z270.223→288.352/224.227,杂质E检测离子对为m/z336.323 →318.327/247.220,杂质K检测离子对为m/z306.332→262.346/288.346,诺氟沙星检测离子对为m/z320.272→276.356/302.351。
2.2 结果
2.2.1线性与范围 精密吸取标准曲线溶液注入液相色谱-质谱仪,按照2.1.6项下色谱条件进行检测,以溶液质量浓度(ng·mL-1)为横坐标(x)、峰面积为纵坐标(y)进行线性回归,得各对照品回归方程:诺氟沙星杂质Ay1=1 377.35x1+4 926(r=0.999 4)、杂质Ey2=1 372.18x2+1 053.33(r=0.998 4)、杂质Ky3=362.50x3+824.04(r=0.998 7)。杂质A、杂质E和杂质K质量浓度分别在4.11~410.78、4.12~412.00、3.98~398.40 ng·mL-1范围内与其峰面积线性关系良好。
2.2.2专属性实验 分别精密量取混合对照品溶液、空白溶液各0.5 μL注入液相色谱-质谱仪,按照2.1.6 项下色谱条件测定,记录质谱图和色谱图,见图2、图3。结果表明各色谱峰保留时间分别为诺氟沙星5.84 min、杂质A 9.36 min、杂质E 4.83 min、杂质K 3.00 min,各色谱峰之间互不干扰,表明该方法的专属性较好。

注:A.空白溶液;B.对照品溶液。
2.2.3精密度实验 精密吸取标准曲线40 ng·mL-1的溶液0.5 μL,按照2.1.6项下色谱条件,连续进样6次,记录峰面积。结果显示,对照品诺氟沙星杂质A、杂质E和杂质K峰面积的RSD值分别为1.78%、0.95%、2.06%(n=6),表明仪器的精密度良好。
2.2.4重复性实验 取样品细粉6份,分别按照2.1.8项下方法制备供试品溶液,按照2.1.6项下色谱条件进样测定,诺氟沙星杂质A、杂质E和杂质K峰面积的RSD值分别为1.19%、2.04%、2.29%(n=6),结果表明该方法的重复性良好。
2.2.5稳定性实验 取同一份供试品溶液,分别于0、1、2、4、12 h进样测定。计算得诺氟沙星杂质A、杂质E和杂质K峰面积的RSD值分别为5.88%、4.76%、4.84%,结果表明供试品在12 h内稳定性较好。
2.2.6回收率实验 精密量取2.1.3项下混合对照品储备液0.9、1.0、1.1 mL,分别置于100 mL量瓶中,各质量浓度平行3份,共9个量瓶,每个量瓶中精密加入空白辅料10 mg,用混合溶剂溶解并稀释至刻度,摇匀,精密量取0.5 μL,按照2.1.6项下色谱条件进样测定,各杂质回收率结果见表1。回收率限度在80%~115%之间,符合要求。

表1 各杂质回收率实验结果
2.2.7批量样品实验 用本研究新建的液相色谱与串联质谱联用(liquid chromatograph tandem mass spectrometry,LC-MS/MS)法测定30批诺氟沙星胶囊(样品信息见表2)中3个杂质,按照2.1.5项下供试品溶液制备方法对样品进行处理,按照2.1.6项下色谱条件进样测定,含量分布见图4。检测结果表明,30批诺氟沙星胶囊中杂质A、杂质E、杂质K普遍存在,其中1批杂质E和4批杂质K含量超过0.15%(USP、EP限度),存在安全风险。而按照国内法定标准检测,杂质E完全包含在诺氟沙星主峰内,不能检出,见图5,新建的LC-MS/MS法可有效分离、检测杂质A、杂质E、杂质K。
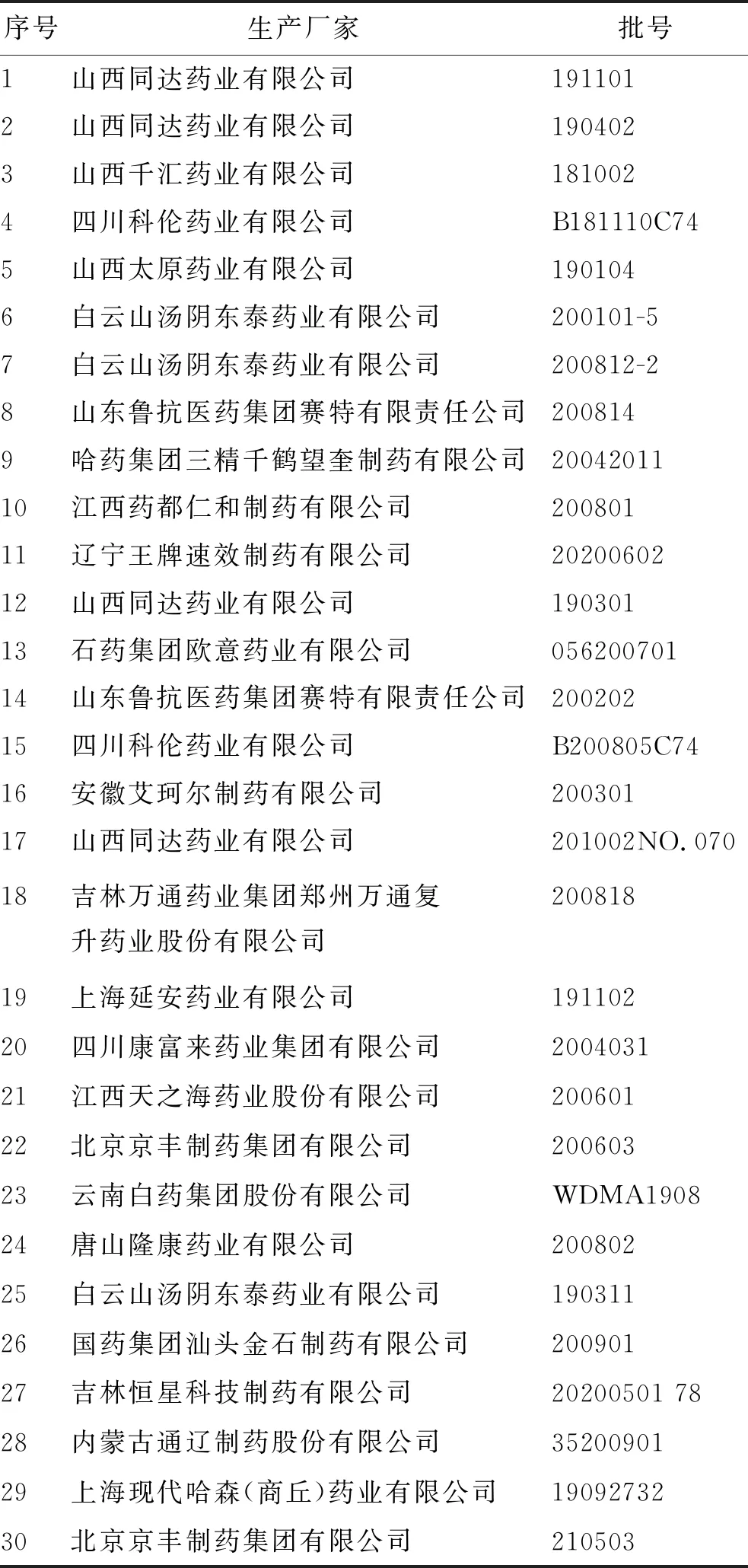
表2 30批诺氟沙星胶囊信息

图4 各杂质含量分布图

注:A.杂质E、杂质K色谱图;B.诺氟沙星样品色谱图;1.杂质K;2.诺氟沙星;3.杂质E。
3 讨论
供试品溶液中溶质的主要成分为诺氟沙星,因为高质量浓度诺氟沙星进入液质联用仪会污染质谱检测器,所以须采取分段模式检测,把诺氟沙星保留时间段的液体切换至废液,避免高质量浓度诺氟沙星母核进入质谱检测器。诺氟沙星峰和其他杂质峰的保留时间差在0.5 min以上才能保证分段模式检测,这就要对色谱柱和流动相进行选择和优化。
3.1 色谱柱的选择
分别考察了ACQUITY UPLC HSS T3 色谱柱(100 mm×2.1 mm,1.8 μm)、ACQUITY UPLC HSS C18色谱柱(100 mm×2.1 mm,1.8 μm)、ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm)、ACQUITY UPLC CHS C18色谱柱(100 mm×2.1 mm,1.7 μm)和ACQUITY UPLC BEH Shield RP18 色谱柱(100 mm×2.1 mm,1.7 μm)。结果表明用ACQUITY UPLC BEH Shield RP18 色谱柱(100 mm×2.1 mm,1.7 μm)检测时诺氟沙星和杂质E保留时间的差值为0.5~0.6 min,各杂质有较佳的峰形,且各峰分离度良好。这可能是因为该色谱柱在C18链上镶嵌了一个极性官能团氨基甲酸酯,对不同极性的化合物有不同的选择性,使诺氟沙星和杂质E有较好的分离度。
3.2 流动相的选择和优化
对新建检测方法进行重现性验证时,选择了其他药品检测实验室进行验证,各实验室的试剂、液相-质谱联用仪不同,影响各杂质峰的保留时间。因此,对流动相进行了优化。先后用2 mL·L-1甲酸溶液(用甲酸铵调节pH值至3.0)-乙腈体系、2 mL·L-1甲酸5 mmol·L-1乙酸铵溶液-乙腈体系和2 mL·L-1甲酸-乙腈体系进行梯度洗脱,结果显示,用2 mL·L-1甲酸-乙腈体系为流动相时,诺氟沙星和杂质E保留时间的差值可以达到0.9~1.0 min。这足以排除不同仪器、试剂对各杂质峰保留时间带来的影响,确保了色谱条件的适用性。
3.3 小结
2020年版《中华药典》用HPLC法进行有关物质检测,灵敏度和分离度不能满足要求。本研究新建的LC-MS/MS法可同时测定诺氟沙星胶囊中3个杂质,方法灵敏度高、专属性好、简便快捷,线性、精密度、稳定性满足测定要求。该方法可用于诺氟沙星及其制剂各杂质的检测,从而保证临床用药的安全性。所测30批次诺氟沙星胶囊中杂质A、杂质E、杂质K普遍存在,因此应加强诺氟沙星及其制剂中杂质的监测。
