影响肝叶切除术治疗的原发性肝癌患者长期生存的因素分析*
2023-09-12蓝春雨范丽琴王小龙朱加猛
蓝春雨,范丽琴,颜 状,王小龙,朱加猛
原发性肝癌(PLC)是起源于肝细胞或肝内胆管细胞的恶性肿瘤,在肝炎病毒感染、过度饮酒和遗传等因素共同作用下,发生细胞恶变[1]。目前,临床常用的治疗方法为肝叶切除术(hepatectomy,HT)和肝移植等根治性治疗手段,但PLC起病较为隐匿且发展迅速,部分患者确诊时已出现癌细胞转移,因此根治术后仍有较高的复发风险。部分肝癌患者存在微血管侵犯(microvascular invasion,MVI),进一步增加了手术难度,影响治疗效果,对患者的生命健康造成严重威胁[2,3]。MVI与肝癌患者肿瘤直径、数量、包膜完整性存在一定的关联,是导致根治术后预后不良的主要危险因素[4-6]。本研究分析了影响HT治疗的PLC患者长期生存的因素,现将结果报道如下。
1 资料与方法
1.1 病例来源 2018年1月~2020年1月我院诊治的PLC患者81例,男53例,女性28例;年龄为35~69岁,平均年龄为(58.3±8.4)岁。符合《原发性肝癌诊疗规范》[7]的标准,其中AdmensonⅠ期32例,Ⅱ期26例,Ⅲa期23例;单发肿瘤33例,多发肿瘤48例。MVI的诊断标准为:显微镜下可见明显的内皮细胞衬覆的血管腔存在癌细胞巢团。排除标准:合并其他恶性肿瘤、手术不耐受、术前采用放化疗等抗肿瘤治疗、凝血功能障碍、预计生存期不足3个月。患者及其家属签署知情同意书,本研究经我院医学伦理委员会审核、批准。
1.2 手术方法 所有患者均由同一手术小组行解剖性HT术治疗。术前,常规消毒铺巾,连接监护仪,监测各项生命体征。选择右侧肋弓下作人字形切口,逐层切开皮肤后依次分离皮下组织,打开腹膜,沿肝周围韧带游离,充分暴露病灶,根据病灶部位及其大小情况,确定肝叶切除的范围。随后,解剖病灶周围组织,明确第一肝门部位,沿血管方向截断血流,继续对肝实质进行解剖,完整切除肿瘤,逐层缝合切口。将引流管留置于肝脏切断面,关闭腹膜,缝合皮肤。根据切除病灶外的肝组织宽度,将其分为宽切缘组(≥1 cm)41例和窄切缘组(<1 cm)40例。
1.3 血清指标检测 采用ELISA法检测血清甲胎蛋白(alpha fetoprotein,AFP)水平(上海信帆生物科技有限公司)。
1.4 术后随访 采用门诊复诊、电话或病历系统查询等方式随访3年,记录肿瘤复发和患者生存情况,随访截止至患者死亡或至2023年1月。
2 结果
2.1 影响HT术后PLC患者1a肿瘤复发的单因素和多因素分析 本组81例PLC患者在HT术后1年内肿瘤未复发29例(35.8%),肿瘤复发52例(64.2%);复发组窄切缘、肿瘤Ⅲa期、多发肿瘤、伴有MVI和包膜不完整比率及血清AFP水平均显著高于未复发组(P<0.05,表1);多因素分析显示,以上因素均是影响肿瘤复发的独立危险因素(P<0.05,表2)。
表1 PLC根治术后1年复发的单因素分析比较
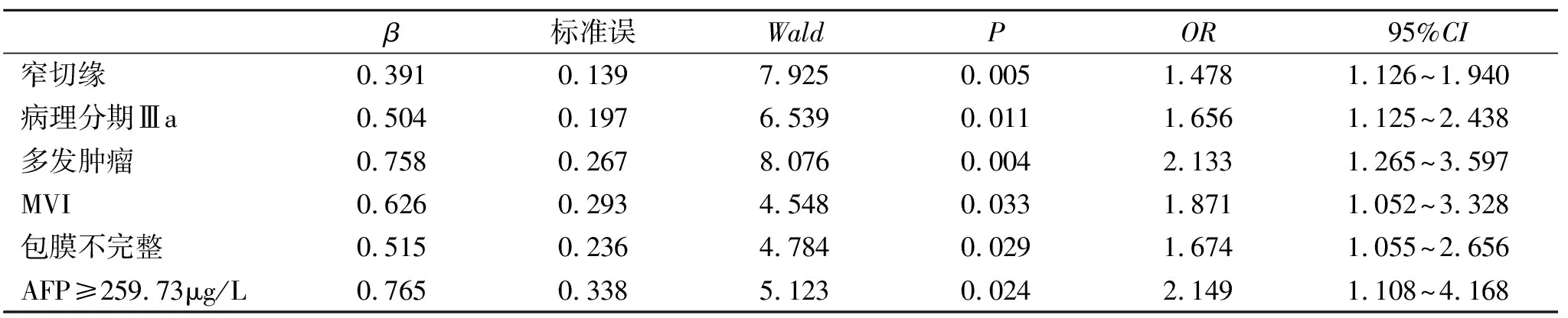
表2 影响HT术后1 a复发的多因素Logistic回归分析
2.2 血清AFP水平预测HT术后PLC患者肿瘤复发的效能分析 经ROC分析发现,血清AFP水平预测术后PLC患者肿瘤复发的最佳截断点为259.7μg/L,其曲线下面积为0.806(P<0.05,95%CI:0.709~0.902),敏感度为0.769,特异度为0.750(图1)。

图1 血清AFP水平预测HT术后PLC患者肿瘤复发的ROC曲线
2.3 两组患者3 a生存率比较 在HT术后,81例患者均获得3年院外随访,无失访患者;宽切缘组死亡13例(31.7%),生存28例(68.3%),窄切缘组死亡24例(60.0%),生存16例(40.0%);Kaplan-Meier生存分析显示,宽切缘组与窄切缘组PLC患者3 a生存率比较有显著性差异(Log-Rank=6.159,P=0.013,图2)。
3 讨论
PLC早期缺乏特异性症状,难以引起患者注意。当出现肝区疼痛、腹水、黄疸等明显临床症状时,肿瘤往往已处于中、晚期或存在癌细胞远处转移,导致错失最佳治疗时机而影响预后。因此,尽早诊断并给予干预措施对于提高患者生存质量具有重要的意义[8]。目前,根治性HT术是临床治疗PLC患者的主要手段。在尽可能多地保留正常肝组织的同时,将肿瘤完整切除,减少复发,以期延长生存期。受肿瘤大小、部位和包膜完整性等因素的影响,术后仍有较大的可能肿瘤复发。大量研究表明伴MVI的PLC患者术后预后显著差于无MVI的患者。因此,进一步明确影响术后肿瘤复发和预后的危险因素,以期延缓病情发展仍为国内外学者的研究重点[9,10]。部分学者认为手术切除边缘宽度与手术疗效存在一定的关联。肿瘤病灶与肿瘤旁肝脏组织的界面即为肿瘤边缘。肿瘤组织新生血管的生成和生长与其形态特点密切相关,因此正确选择手术切缘,将直接影响病灶组织的清除程度,进而影响手术效果[11,12]。故本研究将深入探讨接受根治术治疗的PLC患者预后的影响因素,为临床治疗提供参考。
本研究结果显示,采取宽切缘组患者术后3 a生存率显著高于采取窄切缘组,提示根治术时采取宽切缘切除肿瘤的疗效和预后可能更好,有关研究也有类似的发现[13]。一般认为,采取宽切缘可最大程度地切除肿瘤及其周围肝组织中分布的MVI,进一步降低肝癌复发的风险。另部分肿瘤生长位置复杂,影像学检查难以明确其形态及其大小,采取扩大的切缘手术将有助于医师进一步清除癌组织,提高术后生存率[14]。本研究结果显示81例PLC患者在根治术后1 a复发率为64.2%,而复发组采取了窄切缘手术、病理分期Ⅲa期、多发肿瘤、伴有MVI和包膜不完整占比及血清AFP水平均显著高于未复发组,提示以上因素均为影响PLC患者预后的重要因素,支持有关报道的结果[15]。手术切缘过窄将造成MVI和病灶切除不彻底,进而增加预后不良风险。肿瘤Ⅲa期的出现表明肿瘤直径过大,可能存在癌细胞转移或扩散。随着肿瘤持续生长,其与周围组织粘连,引发其他器官病变,威胁患者生命,加重死亡风险。另肿瘤数量与其增殖速度呈正相关。肿瘤数量多,加速侵犯周围组织,也影响患者预后[16,17]。包膜作为肿瘤组织浸润的屏障,主要受肿瘤大小及形态的影响。随着肿瘤扩大进一步压迫肝脏及其周围组织,破坏包膜的完整性,加重MVI危险程度。肿瘤包膜被破坏将导致肿瘤边界模糊,进一步加大手术难度[18,19]。AFP是目前临床诊断并评估治疗PLC患者疗效的重要指标,其水平与肿瘤数量和病情严重程度等呈正相关。当其水平异常升高需引起临床医师的重视,结合其他检查进一步明确病变情况[20]。
为进一步明确影响根治术后PLC患者肿瘤复发的危险因素,我们应用多因素Logistic回归分析,发现采取窄切缘手术、肿瘤Ⅲa期、多发肿瘤、伴有MVI、包膜不完整及血清AFP水平高是术后1年肿瘤复发的危险因素,这些都将直接影响术后患者预后。
综上所述,采取根治HT术治疗PLC患者术后肿瘤复发率较高。采用宽切缘手术患者预后可能较好。另影响患者预后的危险因素较多,包括窄切缘手术、肿瘤分期晚、多发肿瘤、伴有MVI、包膜不完整及术后血清AFP水平下降缓慢等,都将影响肿瘤复发和患者预后。当患者存在以上危险因素时,应给予高度重视,认真监测,对发现的复发病灶及时采取相应的干预措施,以改善患者预后。本研究存在一些不足之处,如如何确定合适的手术切缘就是一个比较难操作的问题。如果不切实际地扩大切除范围,是否会导致术后肝衰竭的发生,也需要认真加以研究。
