利奈唑胺治疗重症结核性脑膜炎疗效及对脑脊液生化指标的影响
2023-09-01李钦张嵩李消张舒江西省上饶市人民医院江西上饶334000江西省上饶市疾控中心江西上饶334000
李钦,张嵩,李消,张舒(.江西省上饶市人民医院,江西 上饶 334000;.江西省上饶市疾控中心,江西 上饶 334000)
结核性脑膜炎(Tuberculous meningitis,TBM)作为严重的肺外结核感染性疾病,其约占神经系统结核的70%,容易引起发热、头痛、意识障碍等症状,若不及时治疗,会导致脑实质受损,从而威胁患者生命安全[1]。目前,TBM的治疗主要以药物为主,其中经典四联抗痨疗法可有效抑制结核分枝杆菌增殖,缓解临床症状,但研究发现,该疗法疗效常常不达预期,且容易出现耐药性,应用存有局限[2]。利奈唑胺作为新型抗革兰阳性菌感染药物,其为恶唑烷酮类抗生素,能够与细菌核糖体50S亚基单位相结合,从而阻碍细菌70S初始复合物生成,阻止细菌蛋白质复制,起到有效杀菌作用[3]。目前,利奈唑胺已被临床广泛用于治疗各类感染性疾病,且研究证实该药物具有较好治疗效果,且与其他抗菌药物无交叉耐药性[4]。鉴于此,本研究旨在观察利奈唑胺治疗重症TBM疗效及对脑脊液生化指标的影响,为未来临床治疗重症TBM提供参考依据。现报告如下。
1 资料与方法
1.1 一般资料 选取我院2021年2月-2023年1月收治的80例重症TBM患者,用随机数字表法分为对照组、试验组,每组40例。纳入标准:重症TBM符合相关诊断标准[5],且结合临床表现、头颅CT或MRI、实验室指标等检查确诊;年龄≥18岁;患者及家属知情同意研究。排除标准:合并心、肝、肾等重要脏器器质性病变;合并其他传染性、感染性疾病;合并中枢神经系统病变;格拉斯哥昏迷指数(Glasgow Coma Scale,GCS)评分<8分;合并严重心脑血管疾病;合并肿瘤;合并脑外伤;哺乳或妊娠期患者;入组前1个月接受相关治疗;对本研究药物过敏。两组性别、年龄、结核病程、结核类型对比,差异不显著(P>0.05),有可比性,见表1。本研究经医学伦理委员会批准。
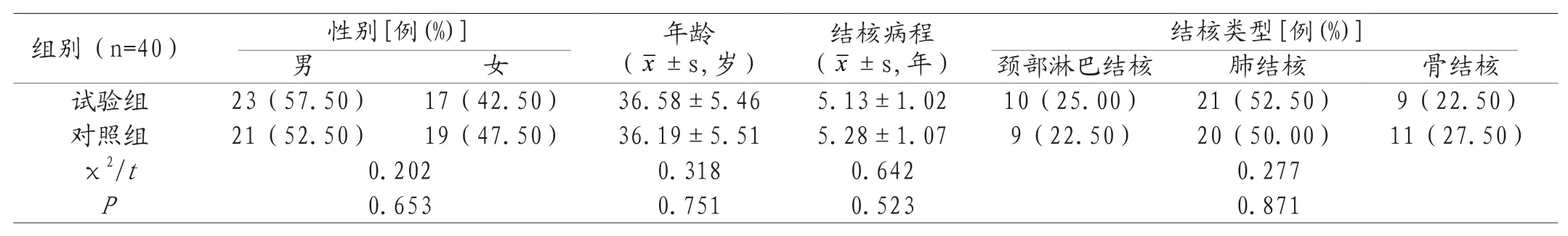
表1 两组一般资料对比
1.2 方法 对照组采用经典四联抗痨治疗,予以利福平胶囊(规格:0.15g)口服,0.45g/次,qd,于早晨顿服;异烟肼片(规格:0.3g)口服,0.3g/次,qd;吡嗪酰胺片(规格:0.5g)口服,1.5g/次,qd;盐酸乙胺丁醇片(规格:0.25g)口服,0.75g/次,qd,于早晨顿服。试验组在对照组基础上加用利奈唑胺片(规格:0.6g)口服治疗,0.6g/次,每12h一次。两组均以4周为1个疗程,均观察1个疗程。
1.3 观察指标 ①疗效:发热、抽搐等症状消失,GCS评分[6]恢复至15分,脑脊液各项指标恢复正常为显效;发热、抽搐等症状减轻,GCS评分较治疗前升高,脑脊液各项指标改善为有效;各项临床体征无变化或加重,GCS评分、脑脊液各项指标未改善为无效;总有效率为显效率与有效率之和。②脑脊液生化指标:分别于治疗前、1个疗程行腰椎穿刺,取脑脊液3ml,用酶联免疫吸附试验法测定脑脊液葡萄糖含量、白细胞计数、蛋白定量浓度,并计算脑脊液糖/同步血糖比值,检测试剂盒购自上海科澄维生物科技有限公司,严格按照试剂盒说明书规范检验流程。③不良反应:记录两组治疗期间胃肠道反应、皮疹、周围神经炎、血细胞减少等发生情况。
1.4 统计学方法 数据采用SPSS23.0软件处理,计量资料以±s表示,用t检验;计数资料用百分比表示,用χ2检验;P<0.05表示差异具有统计学意义。
2 结果
2.1 两组疗效对比 试验组总有效率较对照组高,差异有统计学意义(P<0.05)。见表2。

表2 两组疗效对比[n(%)]
2.2 两组脑脊液生化指标水平对比 两组治疗1个疗程后的脑脊液糖/同步血糖比值较治疗前升高,白细胞计数、蛋白定量浓度较治疗前降低,且试验组各指标水平变化显著,差异有统计学意义(P<0.05)。见表3。
表3 两组脑脊液生化指标水平对比(±s)

表3 两组脑脊液生化指标水平对比(±s)
注:相比治疗前,*P<0.05。
组别(n=40)脑脊液糖/同步血糖比值白细胞计数(×106/L)蛋白定量浓度(g/L)治疗前治疗1个疗程治疗前治疗1个疗程治疗前治疗1个疗程试验组0.21±0.050.46±0.12*113.26±12.6243.61±5.82*1.95±0.460.97±0.26*对照组0.23±0.070.35±0.10*112.85±12.4278.95±7.40*1.90±0.521.08±0.34*t 1.4704.4540.14623.7410.4563.103 P 0.146<0.0010.884<0.0010.6500.003
2.3 两组不良反应对比 两组不良反应总发生率对比,差异无统计学意义(P>0.05)。见表4。

表4 两组不良反应对比[n(%)]
3 讨论
调查显示,约10%的结核患者会发生TBM,且近年来随着结核发病率的升高,TBM发生率随之增长[7]。TBM确切病理机制尚未明确,加之尚无敏感诊断方式、结核分枝杆菌耐药等,容易错失最佳治疗时机,导致患者病情加重,研究发现,重症TBM远期致残、致死率高达20%-50%[8]。因此,寻求重症TBM患者有效治疗方案,对改善患者预后有积极意义。
目前,临床多采用经典四联抗痨疗法治疗TBM,以清除结核分枝杆菌,遏制疾病进展,但临床研究发现,TBM阳性菌株对异烟肼耐药率高达64.2%,对利福平耐药率达39.2%,因而整体治疗效果有限[9-10]。近年来,WHO指南推荐,应在抗结核经典四联疗法基础上,增加第五组药物应用,以提高抑菌效果[11]。利奈唑胺作为新型恶唑烷酮类抗菌药,其通过结合细菌50S亚基单位的23S核糖体RNA,可阻碍细菌70S初始复合物生成,从而阻止细菌DNA复制[12]。同时,利奈唑胺可作用于细菌L22、whiB7调节蛋白、核糖体L4等多靶点,且其独特作用机制与其他蛋白质抑制剂存在显著差异,因为不会出现交叉耐药情况,抗菌效果较好[13-14]。本研究结果显示,试验组总有效率较对照组高,说明重症TBM患者采用利奈唑胺治疗效果较好。分析原因在于,在四联抗痨疗法基础上增加利奈唑胺,可提高对结核分枝杆菌抑菌效果,从而有效杀灭细菌,减轻临床症状,提高患者整体获益。本研究还发现,试验组治疗1个疗程后的脑脊液糖/同步血糖比值较对照组高,白细胞计数、蛋白定量浓度较对照组低,说明重症TBM患者采用利奈唑胺治疗利于改善脑脊液生化指标。分析原因在于,利奈唑胺亲脂性好,且对脑脊液屏障穿透率达80%以上,血药浓度高,可快速控制细菌感染情况,同时细菌耐药率低,从而可提升整体治疗效果,有效改善脑脊液生化指标水平[15]。安全性方面,两组间不良反应总发生率对比无差异,说明利奈唑胺治疗安全性较好,不会增加不良反应发生,这一结果可能与观察周期短有关,因此未来临床用药期间,应密切监测患者的不良反应情况,若证实是该药物引起的反应,需立即停止用药,并积极对症处理。此外,本研究并未观察两组后遗症发生情况,研究结果存有局限,为明确利奈唑胺的远期疗效,未来仍需进一步研究探讨。
综上所述,重症TBM患者采用利奈唑胺治疗效果较好,可改善脑脊液生化指标,且药物安全性好。