蒺藜果实化学成分及其抗氧化活性研究
2023-08-03刘晓敏赵佳敏兰嘉豪程子芥曹金凤刘世巍赵江源李铭刚丁建海
刘晓敏,赵佳敏,兰嘉豪,魏 婕,程子芥,梅 瀚,曹金凤,刘世巍,赵江源,李铭刚,丁建海*
蒺藜果实化学成分及其抗氧化活性研究
刘晓敏1,赵佳敏1,兰嘉豪1,魏 婕1,程子芥1,梅 瀚1,曹金凤1,刘世巍1,赵江源2,李铭刚2,丁建海1*
1. 宁夏师范学院化学化工学院,宁夏 固原 756000 2. 云南大学生命科学学院,云南 昆明 650091
研究蒺藜果实的化学成分及其抗氧化活性。综合利用硅胶柱色谱、Sephadex LH-20凝胶柱色谱等分离手段进行分离纯化;结合NMR、MS、IR、UV等波谱学技术来鉴定化合物的结构;通过DPPH法、ABTS法以及羟基自由基清除方法测定化合物的抗氧化活性。从蒺藜果实75%甲醇提取物中分离鉴定了10个化合物,分别为()-4-hydroxy-N-(3-(4-hydroxy-3-methoxyphenyl)acryloyl)benzamide(1)、蒺藜酰胺(2)、海柯皂苷元(3)、25-螺甾-4-烯-3,12-二酮(4)、槲皮素(5)、3,4-二羟基-3-甲氧基苯丙酮(6)、对羟基苯甲酸(7)、(9,11)-13-hydroxy-9,11-octadecadienoic acid(8)、(8,12)-10-hydroxy-8,12-octadecadienoic acid(9)、肉豆蔻酸(10),其中化合物1~6对DPPH、ABTS自由基以及羟基自由基均有较显著的活性,并且化合物5清除ABTS自由基和羟基自由基半数抑制浓度(half maximal inhibitory concentration,IC50)分别为0.011、0.320 mmol/L,与VC阳性对照组的IC50值非常接近。化合物1为新化合物,命名为蒺藜酰亚胺D,化合物6~10均为首次从蒺藜属植物中分离得到。化合物1~6清除自由基能力较强,具有较好的抗氧化活性。
蒺藜;蒺藜酰胺;蒺藜酰亚胺D;海柯皂苷元;槲皮素;抗氧化活性
蒺藜L为蒺藜科(Zygophyllaceae)蒺藜属L草本植物[1]。《中国药典》记载,蒺藜是一味临床上广泛应用的中药,以其干燥成熟果实入药,有平肝解郁、活血祛风、明目、止痒的功效[2]。在国外,蒺藜提取物早已被开发成为增强性功能的“Tribustan”和“Vitanone”及软化血管的“Tribusaponin”等制剂。国内现代中药提取分离和药理学研究也表明,从蒺藜中分离到的甾体皂苷具有很好的改善心脑血管的作用,并且以蒺藜总皂苷为主要成分的制剂心脑舒通已在临床取得了较好的疗效[3]。
为进一步揭示其药理活性的化学物质基础,本课题组对蒺藜果实的甲醇提取物进行了化学成分研究,从中分离并鉴定出10个化合物,分别为()-4-hydroxy--(3-(4-hydroxy-3-methoxyphenyl)acryloyl) benzamide(1)、蒺藜酰胺(terrestriamide,2)、海柯皂苷元(hecogenin,3)、25-螺甾-4-烯-3,12-二酮(25-spirostan-4-ene-3,12-dione,4)、槲皮素(quercetin,5)、3,4-二羟基-3-甲氧基苯丙酮(3,4- dihydroxy-3-methoxyphenylacetone,6)、对羟基苯甲酸(-hydroxybenzoic,7)、(911)-13-hydroxy- 9,11-octadecadienoic acid(8)、(8,12)-10-hydroxy- 8,12-octadecadienoic acid(9)、肉豆蔻酸(myristic acid 10)。化合物1为新的酰胺类化合物,命名为蒺藜酰亚胺D,化合物6~10均为首次从蒺藜果实中分离得到。其中化合物1~6有较好的抗氧化活性效果。
1 仪器与材料
Bruker DRX-500 MHz超导核磁共振仪(德国Bruker公司);ZF-20D型暗箱式紫外分析仪(上海光豪分析仪器有限公司);RE-2000A旋转蒸发器(上海亚荣生化仪器厂);API QSTAR Pulsari质谱仪(加拿大Applied Biosystem公司);PT-3502B型酶标分析仪(北京普天新桥技术有限公司);Agilent Cary 3500紫外可见分光光度计(美国安捷伦公司);Thermo Scientific Nicolet iS5 FTIR傅里叶红外光谱仪(KBr压片,美国赛默飞公司)。Sephadex LH-20凝胶(瑞典Amersham Biosciences公司);柱色谱硅胶(80~100、200~300目)和薄层色谱GF254TLC预制板(青岛海洋化工厂);甲醇、石油醚、二氯甲烷、-抗坏血酸(Vc)、2,2-联苯基-1-苦基肼基(2,2-diphenyl-1-picrylhydrazyl,DPPH)、2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐 [2,2-azinobis- (3-ethylbenzthiazoline-6-sulphonate),ABTS]、过氧化氢、硫酸亚铁(分析纯)均由上海麦克林生化科技有限公司;醋酸乙酯、乙醇、浓硫酸、氯化钠、香草醛(分析纯)均由国药集团化学试剂有限公司。
实验用干燥蒺藜药材于2022年5月购自安徽毫州皖草堂药店,药材经宁夏师范学院丁建海教授鉴定为蒺藜科植物蒺藜L果实,样品标本(20220506)现保存于宁夏师范学院天然产物研究与开发实验室。
2 提取与分离
蒺藜果实10 kg粉碎,用等倍量75%甲醇浸渍提取3次,减压浓缩,回收溶剂,得到甲醇提取物浸膏,将提取物浸膏用水分散均匀,依次用醋酸乙酯、正丁醇萃取,浓缩得各溶剂萃取部位。取醋酸乙酯萃取部分115 g,用80~100目的硅胶拌样,200~300目正相硅胶装柱,以二氯甲烷-甲醇梯度洗脱(1∶0~0∶1),薄层色谱检识合并相同组分,得到7个精细组分(Fra. 1~7)。Fra.3通过正相硅胶柱色谱,二氯甲烷为洗脱剂得到3个亚组分(Fra. 3-1~3-3),Fra. 3-1经过重结晶得到化合物2(12.1 mg),Fra. 3-2经过Sephadex LH-20凝胶柱色谱(二氯甲烷-甲醇1∶1)纯化得到化合物9(10.5 mg)、10(10.1 mg)。Fra. 4经正相硅胶柱色谱,二氯甲烷-甲醇(100∶1)洗脱得到4个亚组分(Fra. 4-1~4-4),Fra. 4-3经过Sephadex LH-20凝胶柱色谱(二氯甲烷-甲醇1∶1)纯化,得到化合物8(5.6 mg)、11(3.2 mg),Fra. 4-4经过重结晶得到3(12.1 mg)。Fra. 5经正相硅胶柱色谱,二氯甲烷-甲醇(80∶1~40∶1)洗脱得到3个亚组分(Fra. 5-1~5-3),Fra. 5-2经Sephadex LH-20凝胶柱色谱(甲醇)分离纯化,得到化合物1(10.8 mg),Fra. 5-3再经Sephadex LH-20凝胶柱色谱(二氯甲烷-甲醇1∶1)分离纯化,得到化合物4(12.7 mg)。Fra. 6经Sephadex LH-20凝胶柱色谱(甲醇)纯化,得到化合物5(6.3 mg)、6(8.8 mg)。
3 结构鉴定
化合物1:白色无定形粉末,分子式C17H15NO5。HR-ESI-MS给出分子离子峰336.123 7 [M+Na]+,确定分子式为C17H15NO5,计算不饱和度为11。IR谱图显示出明显的吸收峰(3379、1655和1580 cm−1),暗示该化合物结构中应该含有酚羟基和酰胺基团,UV谱图显示出2个明显得吸收峰(240、320)nm,暗示该化合物结构中应该含有双键和胺基。1H-NMR (400 MHz, CD3OD) 数据H7.89 (1H, d,= 8.7 Hz), 6.84 (2H, d,= 8.7 Hz), 6.82 (1H, d,= 8.7 Hz),表明结构中存在2个对位取代的苯环;H7.50 (1H, d,= 15.8 Hz), 6.47 (1H, d,= 15.8 Hz) 表明结构中存在1个反式双键。13C-NMR (100 MHz, CD3OD) 数据中显示有15个碳信号,结合DEPT谱和HSQC谱,归属为1个甲氧基,9个次甲基,5个季碳。其中2个与氮或氧相连的羰基碳信号C170.2 (C-9), 168.7 (C-1) 占有2个不饱和度,2个双键碳信号C141.8 (C-7), 116.7 (C-8) 占1个不饱和度,剩下的8个不饱和度为2个苯环,故推测该化合物具有蒺藜酰胺骨架。1H-1H COSY谱中,H7.07 (dd,= 8.2, 1.9 Hz, H-2) 与6.82 (d,= 8.2 Hz, H-3);H7.50 (d,= 15.8 Hz, H-7)与6.47 (d,= 15.8 Hz, H-8);H7.89 (d,= 8.7 Hz, H-3) 与6.82 (d,= 8.7 Hz, H-4) 有相关,可连接成3个小片段。在HMBC谱中,H6.47 (1H, d,= 15.8 Hz, H-8) 与C126.7 (C-1), 170.2 (C-9) 相关,H7.50 (d,= 15.8 Hz, H-7) 与C122.0 (C-2), 116.7 (C-8), 170.2 (C-9) 相关,表明双键既与苯环相连又和羰基相连。H7.89 (2H, d,= 8.7 Hz, H-3') 与C168.7 (C-1') 相关,表明羰基和另一个苯环相连。在ROESY谱中,H3.89 (s, OCH3) 甲氧基质子与H7.14 (d,= 1.9 Hz, H-6) 存在相关,表明甲氧基位于C-6相邻位,即甲氧基位于C-5位且与羟基相邻(图1-1a)。结合ESI-MS (+): 336.123 7 [M+Na]+,可以推出片段1a和2a由NH连接(图1-3a)。

图1 化合物1的结构片段
综合1H-NMR、13C-NMR、HSQC、HMBC、1H-1H COSY、ROESY等信息,推得化合物1的结构为()-4-hydroxy--(3-(4-hydroxy-3-methoxyphenyl) acryloyl) benzamide,如图2所示,具体NMR信息见表1。经SciFinder Scholar网络检索,该化合物为未见文献报道的新化合物,命名为蒺藜酰亚胺D。

图2 化合物1的结构及重要HMBC、1H-1H COSY相关
化合物2:针状结晶(二氯甲烷-甲醇),分子式为C18H17NO5。HR-ESI-MS/350.141 9。1H-NMR (400 MHz, DMSO-6): 7.90 (2H, d,= 8.8 Hz, H-4′, 8′), 7.35 (1H, t,= 8.8 Hz, H-7), 7.17 (1H, t,= 2.9 Hz, H-2), 7.02 (2H, dd,= 5.2, 3.2 Hz, H-5′, 7′), 6.70 (1H, m, H-8), 4.66 (2H, d,= 5.5 Hz, H-1′), 3.82 (3H, s, H-OCH3);13C-NMR (100 MHz, DMSO-6): 193.4 (C-2′), 165.8 (C-9), 162.4 (C-6′), 148.4 (C-4), 147.9 (C-3), 139.5 (C-7), 130.4 (C-4′, 8′), 126.6 (C-1), 126.4 (C-3′), 121.7 (C-6), 118.7 (C-8), 115.7 (C-5), 115.4 (C-5′), 115.1 (C-7′), 110.9 (C-2), 55.6 (OCH3), 45.6 (C-1′)。以上数据与文献报道一致[4],故鉴定化合物2为蒺藜酰胺。

表1 化合物1的核磁数据(400/100 MHz, CD3OD)
化合物3:片状结晶(二氯甲烷-甲醇),分子式为C27H42O4。HR-ESI-MS/431.318 4。1H-NMR (400 MHz, CDCl3): 3.65~3.54 (1H, m, H-3), 3.48 (1H, dd,= 10.5, 2.1 Hz, H-26a), 3.34 (1H, t,= 10.9 Hz, H-26b), 1.05 (6H, d,= 9.5 Hz, H-21), 0.89 (3H, s, H-19), 0.78 (3H, d,= 6.3 Hz, H-27);13C-NMR (100 MHz, CDCl3): 213.7 (C-12), 109.3 (C-22), 79.3 (C-16), 71.0 (C-3), 67.0 (C-26), 55.9 (C-14), 55.6 (C-9), 55.2 (C-13), 53.6 (C-17), 44.7 (C-5), 42.2 (C-20), 38.0 (C-4), 37.9 (C-11), 36.6 (C-1), 36.2 (C-10), 34.4 (C-8), 31.6 (C-15), 31.5 (C-7), 31.3 (C-23), 31.2 (C-2), 30.3 (C-25), 28.8 (C-24), 28.4 (C-6), 17.2 (C-27), 16.1 (C-18), 13.4 (C-21), 12.0 (C-19)。以上数据与文献报道一致[5],故鉴定化合物3为海柯皂苷元。
化合物4:针状结晶(甲醇),分子式为C27H38O4。HR-ESI-MS/427.288 3。1H-NMR (400 MHz, CDCl3): 5.78 (1H, s, H-4), 3.55 (1H, m, H-26a), 3.35 (1H, t,= 10.9 Hz, H-26b), 1.28 (3H, s, H-18), 1.12 (3H, s, H-19), 1.08 (3H, d,= 7.0 Hz, H-21), 0.80 (3H, d,= 6.3 Hz, H-27);13C-NMR (100 MHz, CDCl3): 212.1 (C-12), 198.9 (C-3), 168.6 (C-5), 124.7 (C-4), 109.3 (C-22), 79.0 (C-16), 66.9 (C-26), 54.8 (C-14), 54.8 (C-9), 54.5 (C-13), 53.5 (C-17), 42.2 (C-20), 38.8 (C-10), 37.1 (C-11), 35.3 (C-1), 34.4 (C-8), 33.7 (C-6), 32.4 (C-2), 31.4 (C-15), 31.2 (C-23), 31.1 (C-7), 30.2 (C-25), 28.8 (C-24), 17.1 (C-27), 16.9 (C-19), 16.0 (C-18), 13.3 (C-21)。以上数据与文献报道一致[6],故鉴定化合物4为25-螺甾4-烯-3,12-二酮。
化合物5:黄色粉末,分子式为C15H10O7。HR-ESI-MS/301.136 7。1H-NMR (400 MHz, CD3OD): 7.75 (1H, d,= 2.1 Hz, H-2'), 7.65 (1H, dd,= 8.5, 2.1 Hz, H-6'), 6.90 (1H, d,= 8.5 Hz, H-5'), 6.41 (1H, d,= 2.0 Hz, H-8), 6.20 (1H, d,= 2.0 Hz, H-6);13C-NMR (100 MHz, CD3OD): 161.1 (C-5), 97.8 (C-6), 164.2 (C-7), 93.0 (C-8), 156.8 (C-9), 103.1 (C-10), 122.7 (C-1), 114.6 (C-2), 144.8 (C-3), 147.4 (C-4), 114.8 (C-5), 120.3 (C-6), 146.6 (C-2), 135.8 (C-3), 175.9 (C-4)。以上数据与文献报道一致[7],故鉴定化合物5为槲皮素。
化合物6:淡黄色油状物,分子式为C10H12O4。HR-ESI-MS/195.066 9。1H-NMR (400 MHz, CDCl3): 7.55 (1H, t,= 3.2 Hz, H-6), 7.53 (1H, s, H-2), 6.95 (1H, d,= 8.0 Hz, H-5), 4.01 (2H, d,= 4.2 Hz, H-9), 3.95 (3H, d,= 6.2 Hz, -OCH3), 3.18 (2H, t,= 5.3 Hz, H-8);13C-NMR (100 MHz, CDCl3): 199.3 (C-1), 150.9 (C-4), 146.8 (C-3), 129.8 (C-1), 123.8 (C-6), 114.1 (C-5), 109.7 (C-2), 58.4 (C-3), 56.2 (OCH3), 39.9 (C-2)。以上数据与文献报道一致[8],故鉴定化合物6为3,4-二羟基-3-甲氧基苯丙酮。
化合物7:黄色粉末,分子式为C7H6O3。HR-ESI-MS/137.024 7。1H-NMR (400 MHz, CD3OD): 8.03 (2H, 2H, d,= 8.2 Hz, H-2, 6), 6.90 (2H, d,= 8.2 Hz, H-3, 5);13C-NMR (100 MHz, CD3OD): 168.6 (C-1), 163.7 (C-1), 132.8 (C-2, 6), 115.2 (C-3, 5)。以上数据与文献报道一致[9],故鉴定化合物7为对羟基苯甲酸。
化合物8:黄色油状,分子式为C18H32O3。HR-ESI-MS/350.141 9。1H-NMR (400 MHz, CDCl3): 6.50 (1H, m, H-12), 5.99 (1H, m, H-10), 5.65 (1H, m, H-11), 5.46 (1H, m, H-9), 4.16 (1H, dd,= 13.9, 6.9 Hz, H-13), 0.90 (3H, t,= 6.2 Hz, H-18);13C-NMR (100 MHz, CDCl3): 179.3 (C-1), 135.7 (C-12), 133.2 (C-9), 127.7 (C-11), 126.0 (C-10), 73.0 (C-13), 37.3 (C-14), 34.0 (C-2), 31.8 (C-16), 29.3 (C-7), 29.3 (C-6), 29.2 (C-5), 29.0 (C-4), 27.8 (C-8), 25.3 (C-15), 24.7 (C-3), 22.6 (C-17), 14.1 (C-18)。以上数据与文献报道一致[11],故鉴定化合物8为 (9,11)-13-hydroxy-9,11-octadecadienoic acid。
化合物9:黄色油状物,分子式为C18H32O3。HR-ESI-MS/313.273 4。1H-NMR (400 MHz, CDCl3): 6.03 (1H, m, H-12), 6.00 (1H, m, H-9), 5.68 (1H, m, H-10), 5.46 (1H, m, H-8), 4.19 (1H, dd,= 13.9, 6.9 Hz, H-13), 0.90 (3H, t,= 6.2 Hz, H-18);13C-NMR (100 MHz, CDCl3): 179.3 (C-1), 133.1 (C-8), 132.4 (C-9), 132.1 (C-13), 124.7 (C-12), 72.6 (C-10), 35.4 (C-11), 33.9 (C-7), 31.9 (C-2), 31.3 (C-16), 29.4 (C-15), 29.3 (C-4), 29.0 (C-6), 29.0 (C-5), 27.4 (C-14), 24.6 (C-3), 22.2 (C-17), 13.9 (C-18)。以上数据与文献报道一致[12],故鉴定化合物9为 (8,12)-10-hydroxy-8,12-octadecadienoic acid。
化合物10:白色固体,分子式为C14H28O2。HR-ESI-MS/229.063 4。1H-NMR (400 MHz, CDCl3): 2.36 (2H, t,= 7.5 Hz, H-2), 1.64 (2H, m, H-3), 1.29 (20H, brs, H-4~13), 0.89 (3H, t,= 6.8 Hz, H-14);13C-NMR (100 MHz, CDCl3): 180.3 (C-1), 34.1 (C-2), 32.0 (C-12), 29.7~29.1 (C-4~11), 24.7 (C-3), 22.7 (C-13), 14.2 (C-14)。以上数据与文献报道一致[13],故鉴定化合物10为肉豆蔻酸。
4 抗氧化活性测定与评价
4.1 DPPH法抗氧化活性的测定
将不同质量浓度的样品溶液(0.5、0.4、0.3、0.2、0.1 mg/mL)100 μL与0.5 mmol/L的DPPH母液100 μL加入96孔酶标板中,避光保存30 min后测定在517 nm下的吸光度值(1),并用无水乙醇代替DPPH设置待测样品空白对照组,吸光度值为2,以及DPPH空白对照组,吸光度值为0。VC作为阳性对照,重复3次,根据公式计算DPPH自由基清除率[14]。
DPPH自由基清除率=1-(1-2)/0
4.2 ABTS法抗氧化活性的测定
将7 mmol/L的ABTS与2.45 mmol/L的过硫酸钾等体积混合,室温条件黑暗处反应12~16 h。第2天用无水乙醇稀释40~60倍(在734 nm处为0.70左右),摇匀,静置5 min,制成ABTS自由基工作液。将不同质量浓度的样品溶液(0.5、0.4、0.3、0.2、0.1 mg/mL)100 μL与制得的ABTS溶液100 μL加入96孔酶标板中,避光保存30 min后测定在734 nm下的吸光度值(1′),并用无水乙醇代替ABTS设置待测样品空白对照组吸光度值为2′,以及ABTS空白对照组,吸光度值为0′。VC作为阳性对照,重复3次,根据公式计算ABTS自由基清除率[14]。
ABTS自由基清除率=1-(1′-2′)/0′
4.3 羟基自由基清除法抗氧化活性的测定
将不同质量浓度的样品(0.33、0.20、0.14、0.11、0.01 mg/mL)、2.50 mmol/L的水杨酸、5.00 mmol/L 的FeSO4·7H2O、1%过氧化氢(1∶1∶1∶1)混合于96孔酶标板中,37 ℃恒温水浴30 min后,在510 nm下测定吸光度值(1′′),并用蒸馏水代替过氧化氢设置待测样品空白对照组,吸光度值为2′′,以及蒸馏水、水杨酸、FeSO4·7H2O、过氧化氢(1∶1∶1∶1混合)为空白对照,吸光度值为0′′。VC作为阳性对照,重复3次,根据公式计算羟基自由基清除率[15]。
羟基自由基清除率=1-(1-2)/0
4.4 抗氧化活性评价
抗氧化活性的测试结果显示,化合物7~10无抗氧化活性(IC50>50 mmol/L),化合物1~6的抗氧化活性检测结果如表1所示,其中酰胺类对DPPH、ABTS、OH自由基3种抗氧化测试均具有较好的活性;甾体皂苷类对DPPH、ABTS 2种抗氧化活性测试效果不明显,但是对OH自由基却具有较好的效果;黄酮类和苯丙素类对3种抗氧化测试均具有较好的活性。在一定范围内,这6个化合物对3种抗氧化活性的清除能力,随着物质的量浓度的增加而增加,呈明显量效关系。
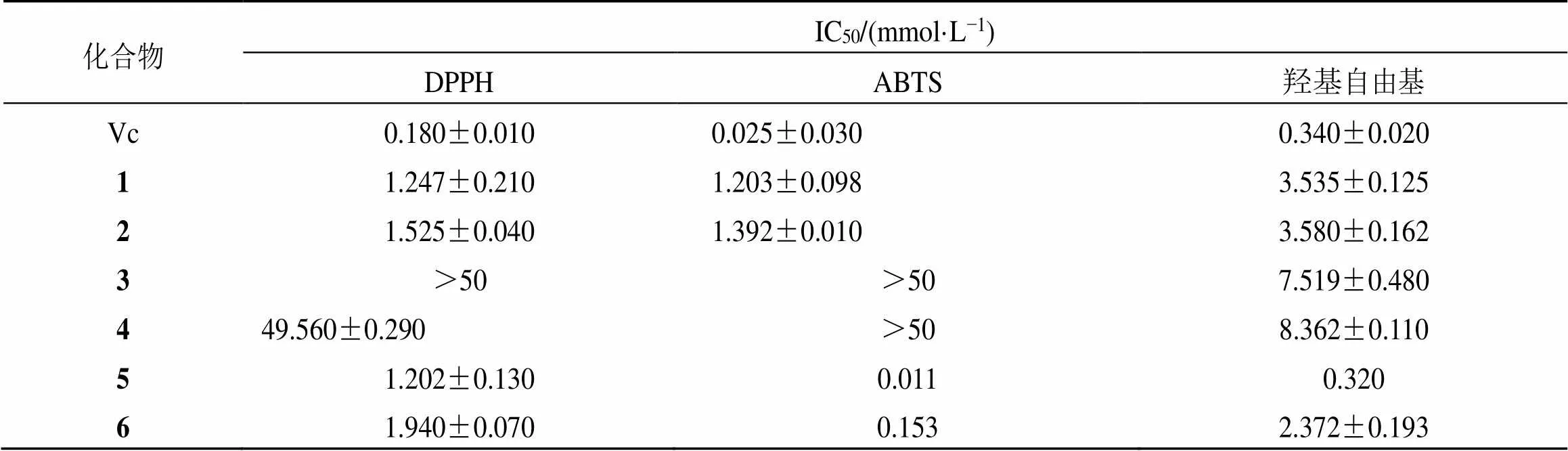
表1 化合物1~6的体外清除自由基能力结果(n = 3)
5 讨论
近年来,我国关于蒺藜化学成分的研究报道较多,已经从蒺藜全草、果实、地上部分等得到了多种单体化合物,蒺藜根、茎、叶、花、果实均可入药,《中国药典》收载了蒺藜果实作为药材,其具有抗衰老、抗菌、镇痛、调节血脂、降血糖、抑癌、利尿、性强壮、抑制酪氨酸酶等药理作用,通过文献检索发现,对分离得到的化合物抗氧化活性研究却很少有报道。因此,寻找单体化合物的抗氧化方面的活性成分,和研究活性成分的作用机制将对蒺藜药材的进一步应用与开发具有着非常重的要意义。
本研究从蒺藜果实中分离并鉴定出2个酰胺类、2个甾体皂苷类、1个黄酮类、1个苯丙素类。还有脂肪酸等10个化合物。化合物1为新的酰胺类化合物,命名为蒺藜酰亚胺D,化合物6~10均为首次从蒺藜果实中分离得到。进一步,本实验对化合物进行了抗氧化活性评估,结果显示化合物1~6具有较好的抗氧化活性效果,其中槲皮素对ABTS和OH自由基抗氧化活性的效果最好,IC50分别为0.011、0.32 mmol/L,与VC阳性对照组的IC50值几乎一致;而甾体皂苷类化合物对DPPH、ABTS两种抗氧化活性测试效果一般IC50>50 mmol/L,但是对OH自由基具有较好的效果IC50为(7.519±0.480)、(8.362±0.110)mmol/L。本研究的结果丰富了蒺藜的化学成分以及抗氧化活性研究,为蒺藜抗氧化的药效物质基础及开发奠定了基础。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典 [S]. 一部. 2020: 367.
[2] 肖培根. 新编中药志[M]. 北京: 化学工业出版社, 2001: 83.
[3] 李宝龙, 王康, 曾炜, 等. 蒺藜药理作用研究进展 [J]. 吉林医药学院学报, 2011, 32(4): 223-225.
[4] 吕阿丽, 张囡, 马宏宇, 等. 蒺藜果实的化学成分研究 [J]. 中国药物化学杂志, 2007, 17(3): 170-172.
[5] Eggert H, Djerassi C.13C NMR spectra of sapogenins [J]., 1975, 16(42): 3635-3638.
[6] Wu T S, Shi L S, Kuo S C. Alkaloids and other constituents from[J]., 1999, 50(8): 1411-1415.
[7] 娜黑芽, 张晓玲, 陈怡璇, 等. 药用沙棘果汁中1个新的黄酮苷类化合物 [J]. 中草药, 2022, 53(3): 659-666.
[8] Okuyama E, Suzumura K, Yamazaki M. Pharmacologically active components of(Fagraea racemosa), a medicinal plant from Borneo [J]., 1995, 43(12): 2200-2204.
[9] 王鹏程, 周先丽, 罗琴, 等. 青钱柳叶乙酸乙酯部位化学成分的研究 [J]. 中国药学杂志, 2018, 53(6): 418-420.
[10] 莫青胡, 周先丽, 周云, 等. 桃金娘叶的化学成分研究 [J]. 中药材, 2020, 43(3): 587-590.
[11] Dong M, Oda Y, Hirota M. (10,12,15)-9-hydroxy-10, 12,15-octadecatrienoic acid methyl ester as an anti-inflammatory compound from[J]., 2000, 64(4): 882-886.
[12] 韩清华, 谢兴林, 田晓清, 等. 两株南海真菌1-P1和1-I2的次级代谢产物研究 [J]. 海洋渔业, 2020, 42(4): 454-465.
[13] 邓赟, 陆崇玉, 郭大乐, 等. 细罗伞化学成分研究 [J]. 中药材, 2011, 34(3): 380-383.
[14] 和英, 顾婷, 杨永寿, 等. 美洲大蠊提取物抗氧化活性研究 [J]. 大理大学学报, 2021, 6(2): 10-14.
[15] 那吉, 马娇, 张海芬, 等. 三种云南产鲜花醇提液对ABTS自由基的清除作用 [J]. 化学与生物工程, 2019, 36(1): 47-50.
Chemical constituents from fruits ofand their antioxidant activity
LIU Xiao-min1, ZHAO Jia-min1, LAN Jia-hao1, WEI Jie1, CHENG Zi-jie1, MEI Han1, CAO Jin-feng1, LIU Shi-wei1, ZHAO Jiang-yuan2, LI Ming-gang2, DING Jian-hai1
1. College of Chemistry and Chemical Engineering, Ningxia Normal University, Guyuan 756000, China 2. School of Life Sciences, Yunnan University, Kunming650091, China
To investigate the chemical constituents from fruits ofand their antioxidant activity.The compounds were isolated and purified by silica gels column chromatography and Sephadex LH-20 column chromatography. Their structures were identified based on NMR, MS, IR, UV and other spectroscopic techniques. Their antioxidant activity were evaluated by scavenging capacity on DPPH, ABTS and ·OH radicals.Ten compounds were isolated from 75% methanol extract of the fruits ofand identified as ()-4-hydroxy--(3-(4-hydroxy-3-methoxyphenyl) acryloyl)benzamide (1), tribulusamide (2), hecogenin (3), 25-spirostan-4-ene-3,12-dione (4), quercetin (5), 3,4-dihydroxy- 3-methoxyphenylacetone (6),-hydroxybenzoic acid (7), (9,11)-13-hydroxy-9,11-octadecadienoic acid (8), (8,12)-10-hydroxy- 8,12-octadecadienoic acid (9), and myristic acid (10). Compounds 1—6 had the stronger DPPH, ABTS and OH radicals scavenging abilities and compound 5 showed significant abilities with IC50values of 0.011 and 0.320 mmol/L. The IC50values were almost consistent with that of the VCpositive control group.Compound 1 is a new compound, named tribulusimide D. Compounds 6—10 are isolated from fruits offor the first time and also from the fruit offor the first time. The antioxidant activity experiment showed that compounds 1—6 exhibited significant scavenging capacity.
L.; tribulus amide; tribulusimide D;hecogenin;quercetin; antioxidant activity
R284.1
A
0253 - 2670(2023)15 - 4774 - 06
10.7501/j.issn.0253-2670.2023.15.002
2023-04-02
宁夏自然科学基金项目(2022AAC02049);宁夏自然科学基金项目(2022AAC03297);宁夏高等学校科学研究项目(NGY2022073);宁夏师范学院2022年度大学生科技创新基金项目(自然科学类Z202202)
刘晓敏(1997—),女,硕士研究生,主要从事天然药物化学研究。E-mail: 849064934@qq.com
通信作者:丁建海,教授。E-mail: dingjh_nx@126.com Tel: 18809544664
[责任编辑 王文倩]
