青黛表面改性对口腔溃疡双层膜质量与药效的影响
2023-07-06黄胜杰钟婧娉贺亚男郭治平刘雪梅张定堃
黄胜杰,钟婧娉,谢 锦,贺亚男,郭治平,刘雪梅,杨 明,张定堃*,韩 丽*
·药剂与工艺·
青黛表面改性对口腔溃疡双层膜质量与药效的影响
黄胜杰1,钟婧娉1,谢 锦1,贺亚男1,郭治平2,刘雪梅1,杨 明3,张定堃1*,韩 丽1*
1. 成都中医药大学 西南特色中药资源省部共建国家重点实验室,四川 成都 611137 2. 四川厚德医药科技有限公司,四川 成都 610041 3. 江西中医药大学 现代中药制剂教育部重点实验室,江西 南昌 330004
采用溶剂浇铸法制备口腔溃疡双层膜剂,研究青黛表面改性前后对膜剂质量与药效的影响。通过单因素实验设计和响应面优化法优选膜剂最佳处方,并对膜剂表面形貌、黏附时间、抗拉强度、含量测定以及体外药物释放等性能进行评估。进一步采用化学灼烧法建立大鼠口腔溃疡模型,考察膜剂对溃疡组织肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-1β(interleukin-1β,IL-1β)、IL-6以及口腔溃疡组织形态的影响。空白隔离层确定为25 mg/mL的乙基纤维素乙醇溶液,载药膜最佳处方为63 mg/mL PVA17-88、55 mg/mL PVP K30、3.0 mg/mL明胶与0.047 mL/mL甘油。青黛表面改性后,双层膜剂比未改性双层膜剂具有更加光滑均一的外观、更高的含量均匀性和有效成分靛蓝释放率。药效学结果表明,与模型组相比,阳性组与青黛改性膜剂组显著降低了溃疡组织TNF-α、IL-1β、IL-6的含量(<0.05),并减少了炎症细胞的浸润,溃疡组织愈合程度较高。青黛改性之后的口腔溃疡双层膜剂具有更好的质量与更佳的疗效,具有较好的应用前景。
青黛;粉体表面改性;口腔溃疡散;双层膜剂;药效评价;靛蓝;靛玉红
口腔溃疡是一种发生于舌头、牙龈、嘴唇内部等部位的溃疡性损伤,其发病机制和促炎因子与抗炎因子的失衡以及维生素与铁元素的缺乏有关[1-2]。目前常通过减轻患者疼痛、抗炎以及免疫调节等方面进行治疗。口腔溃疡散是中医五官科治疗口腔溃疡的基础方,被收载入《中国药典》2015年版一部。口腔溃疡散由青黛、白矾、冰片按照10∶10∶1配伍而成,可用于火热内蕴所致的口舌生疮、黏膜破溃、红肿止痛[3]。由于口腔生理结构的特殊性以及散剂用药特点,口腔溃疡散易被唾液冲散,进入消化道,难以在溃疡患处固定并保持药物有效浓度[4]。
膜剂是常见的用于口腔疾病的剂型,可通过颊黏膜局部给药直接作用于病灶部位[5]。与散剂相比,膜剂具有免被唾液冲散、剂量准确、提高药物局部浓度以及保护创面等优点[6-7],因此,将口腔溃疡散制备成口腔溃疡膜剂可增加其临床适用性。膜剂常用的制备方法为溶剂浇铸法,该法要求药物在成膜材料溶液中溶解或分散均匀,否则难以制备含量均匀且外观良好的膜状制剂[8]。口腔溃疡散中的青黛表面由靛蓝、靛玉红等疏水性有机物组成[9],该结构决定了青黛亲水性差的宏观物理性质。在膜剂制备过程中,青黛常呈自聚集状态,不能均匀分散于成膜材料溶液中,且在静置脱气泡过程中容易沉降,导致铺膜不均。因青黛在口腔溃疡散中占比较大(47.6%),其疏水性及沉降性明显影响了膜剂的制备与质量。
粉体改性技术可有目的地改善粉末物理化学性质[10],课题组前期采用粉体表面改性技术研究了亲水性青黛的制备工艺,以无水乳糖(与青黛比例为1∶1)为辅料制备出了亲水性与沉降性均佳的改性青黛粉末[11]。因此,本研究选用改性青黛为口腔溃疡散原料之一,采用溶剂浇铸法制备由含药膜和空白保护膜组成的单向释药口腔溃疡双层膜剂,旨在通过改性青黛改善膜剂的均一性;采用保护膜维持药物局部浓度、控制药物单向释放,保证疗效的发挥,同时防止青黛对口腔着色,提高使用的顺应性。本课题组还以普通口腔溃疡散、物理混合物口腔溃疡散(处方见“药品与试剂”)为原料制备膜剂,将其与青黛改性之后的膜剂进行系统比较,考察青黛改性前后膜剂之间的差异。本研究为口腔溃疡新制剂的开发提供了参考。
1 仪器与试药
1.1 仪器
UPH-II-10T型优普超纯水制造系统,成都超纯科技有限公司;KQ-500DE型数控超声波清洗器,昆山市超声仪器有限公司;Quintix 35-1CN型赛多利斯电子分析天平,赛多利斯科学仪器(北京)有限公司;ZEISS Gemini SEM 300扫描电子显微镜(SEM),德国卡尔·蔡司股份公司;RYJ-6B型药物透皮扩散试验仪,上海黄海药检仪器有限公司;KQ-500DE型电热恒温鼓风干燥箱,上海凯朗仪器设备厂;Shimadzu LC-20AT型液相色谱仪,日本岛津公司。
1.2 药品与试剂
青黛,雅安迅康药业有限公司,批号20210228;乳糖,山西锦洋药用辅料有限公司,批号20210303;改性青黛,自制,乳糖与青黛以1∶1的比例于振动磨中共研6 min);白矾,安徽惠丰国药有限公司,批号200901;冰片,康美药业股份有限公司,批号210101841;口腔溃疡散,自制,青黛-白矾-冰片(10∶10∶1);改性口腔溃疡散,自制,改性青黛、白矾与冰片以20∶10∶1混合;物混溃疡散,自制,乳糖青黛简单轻研混合后,与白矾、冰片以20∶10∶1比例混合;聚乙烯醇17-88(PVA 17-88)、聚乙烯吡咯烷酮K30(PVP K30)、丙三醇、壳聚糖、阿拉伯胶、,-二甲基甲酰胺、乌来糖,成都市科隆化学品有限公司,批号分别为2021090301、2021030901、2021110201、2020120101、2020091801、2022092301、2021050601;HPMC,上海易恩化学技术有限公司,批号R011806;明胶,上海麦克林生化科技有限公司,批号2991975;肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-1β(interleukin-1β,IL-1β)、IL-6酶联免疫试剂盒(ELISA),杭州联科生物技术股份有限公司,批号分别为A38220642、A301B20921、A30620757。
1.3 动物
SPF级雄性SD大鼠,体质量180~220 g,购自斯贝福(北京)生物技术有限公司,许可证号SCXK(京)2019-0010。所有动物实验于成都中医药大学药学院动物房的SPF级屏蔽环境内,许可证号:SYXK(川)2019-049,动物实验遵循3R原则并获得成都中医药大学伦理委员会同意,动物处理符合伦理委员会及动物保护法相关规定。
2 方法与结果
2.1 评价标准
空白膜以外观、成膜性、韧性为考察指标,载药膜以外观、成膜性能、柔韧性、黏附性为考察指标,评价标准见表1。

表1 综合评价标准
2.2 空白隔离层制备工艺筛选
空白隔离层可保护药膜层不受口腔唾液的影响,从而保证药物单向释放,增加药物疗效。分别配制15、20、25、30、35 mg/mL的乙基纤维素乙醇溶液,采用流延成膜法铺于涂有液体石蜡的光滑玻璃板上,制备空白隔离层。结果表明,当乙基纤维素质量浓度过低时,难以顺利成膜,且在脱膜过程中难以揭膜。当质量浓度过高时,干燥后表面不平,且厚度增加。由实验可知,当乙基纤维素乙醇溶液质量浓度为25 mg/mL时,制得的空白隔离层性能较优良,故选择隔离层为25 mg/mL的乙基纤维素乙醇溶液。
2.3 载药膜成膜材料考察与处方初筛
常用的成膜材料有PVA 17-88、HPMC、PVP、阿拉伯胶、明胶、壳聚糖等,课题组前期对成膜材料种类进行了大量的初筛,优选出PVA 17-88为主要的成膜材料,同时为了改进外观以及黏附性,将PVA 17-88与其他成膜材料混合,最终确定PVA 17-88、PVP K30、明胶为复合膜材,所制备的膜剂外观、成膜性、韧性、黏附性较好。
2.4 单因素实验设计
选择PVA 17-88、PVP K30、明胶以及甘油为膜材进行单因素实验,参数分别选择:PVA 17-88用量(20、40、60、80、100 mg/mL)、PVP K30用量(10、20、40、60、100 mg/mL)、明胶用量(1.0、2.5、4.0 mg/mL)、甘油用量(0.01、0.02、0.05、0.08 mL/mL)。PVA 17-88单因素实验结果表明,当PVA 17-88质量浓度过低时,膜剂外观、韧性以及黏附性均较差;当PVA 17-88质量浓度过高时,虽韧性和黏附性较好,然外观形态不佳,表面不平整,PVA 17-88质量浓度为60 mg/mL时综合评分最高,为(96.3±2.9)分,故选择初步筛选PVA 17-88质量浓度为60 mg/mL;PVP K30单因素实验结果表明,当PVP K30质量浓度过低时,膜剂外观与黏附性稍差,当质量浓度过高时,膜剂外观形态差,当PVP K30质量浓度为60 mg/mL时,综合评分最高(96.0±2.6)分,故选择PVP K30质量浓度为60 mg/mL;明胶以及甘油单因素实验表明,当明胶用量为2.5 mg/mL,甘油用量为0.05 mL/mL时,膜剂的外观与韧性最佳,因此选择2.5 mg/mL为明胶用量,0.05 mL/mL为甘油用量。
2.5 响应面优化法优选载药膜最优处方
2.5.1 响应面实验设计及结果 根据单因素实验结果,分析PVA 17-88用量(1)、PVP K30用量(2)、明胶用量(3)、甘油用量(4)对膜剂质量的影响。以综合评价()为响应值,采用Box-Behnken设计-响应面法(Box-Behnken design-response surface method,BBD-RSM)优化口腔溃疡膜剂处方,各因素水平、实验方案及结果见表2。
2.5.2 响应面法回归方程及方差分析 对实验数据进行多元回归拟合,得到以综合评分结果为响应值的二次回归方程:=97.200+1.5801-0.8332+0.916 73-0.5004-0.25012-0.75013+0.75014+0.25024-8.31012-3.18022-1.06032-2.68042。回归模型的方差分析及显著性结果见表3。由表3可知,1、2、3、12、22、42为显著影响因素,失拟项=0.144 6,差异不显著,说明实验误差小,模型拟合程度好。
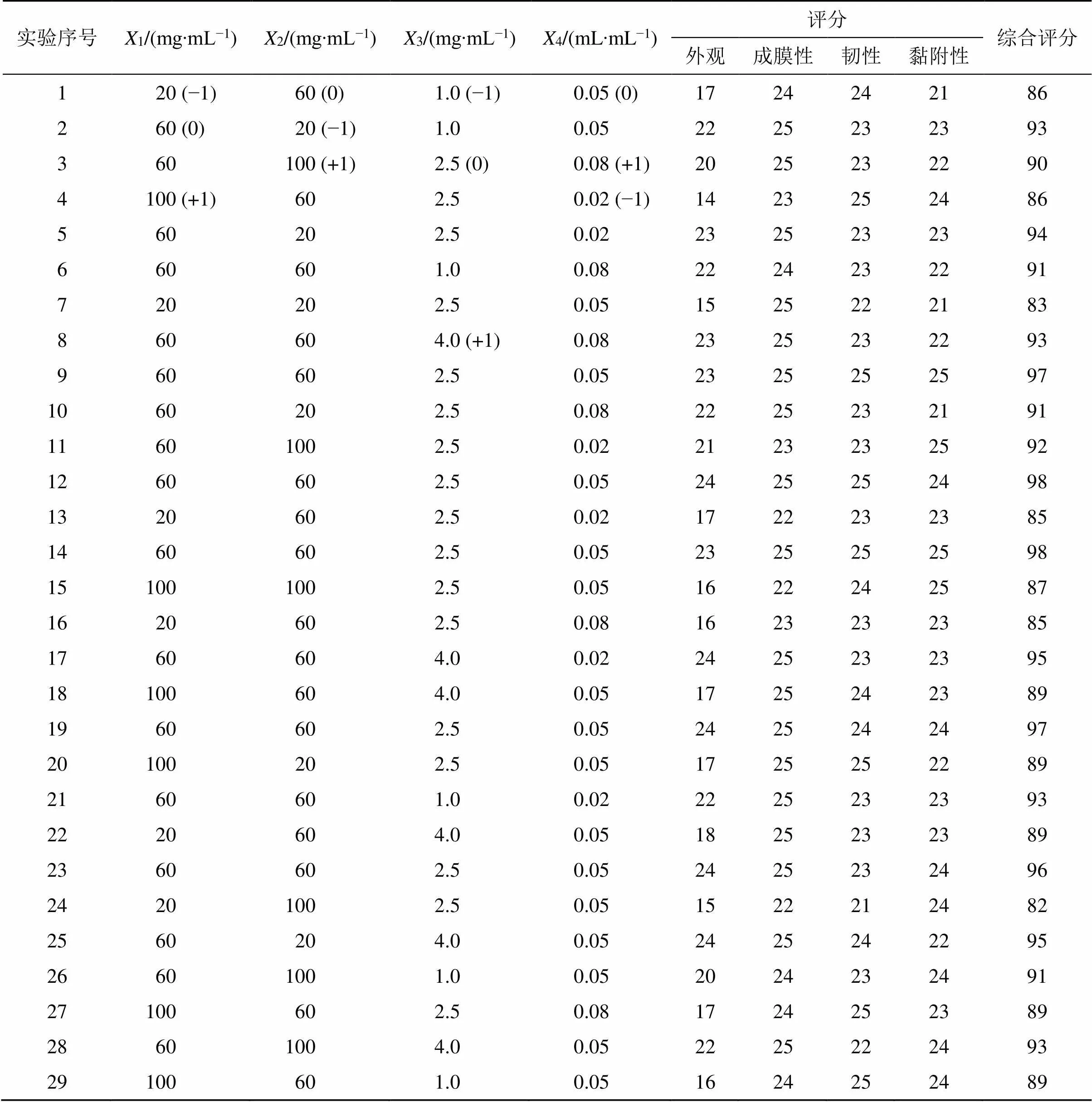
表2 响应面实验方案及实验结果
2.5.3 响应曲面分析 响应面图直观体现了响应值受各因素和交互作用的影响。响应面图曲线弯曲程度越大,表明因素对响应值的影响越大。结果如图1所示,各等高线图均呈椭圆形,表明因素间相互作用显著。利用Design Expert 11软件得到最优条件为63 mg/mL PVA 17-88、55 mg/mL PVP K30、3.0 mg/mL明胶、0.047 mL/mL甘油。在该条件下制备膜剂,得到的膜剂综合评分结果为96.7,与预测值接近,表明由该响应面设计所得的膜剂处方工艺具有一定的可行性。
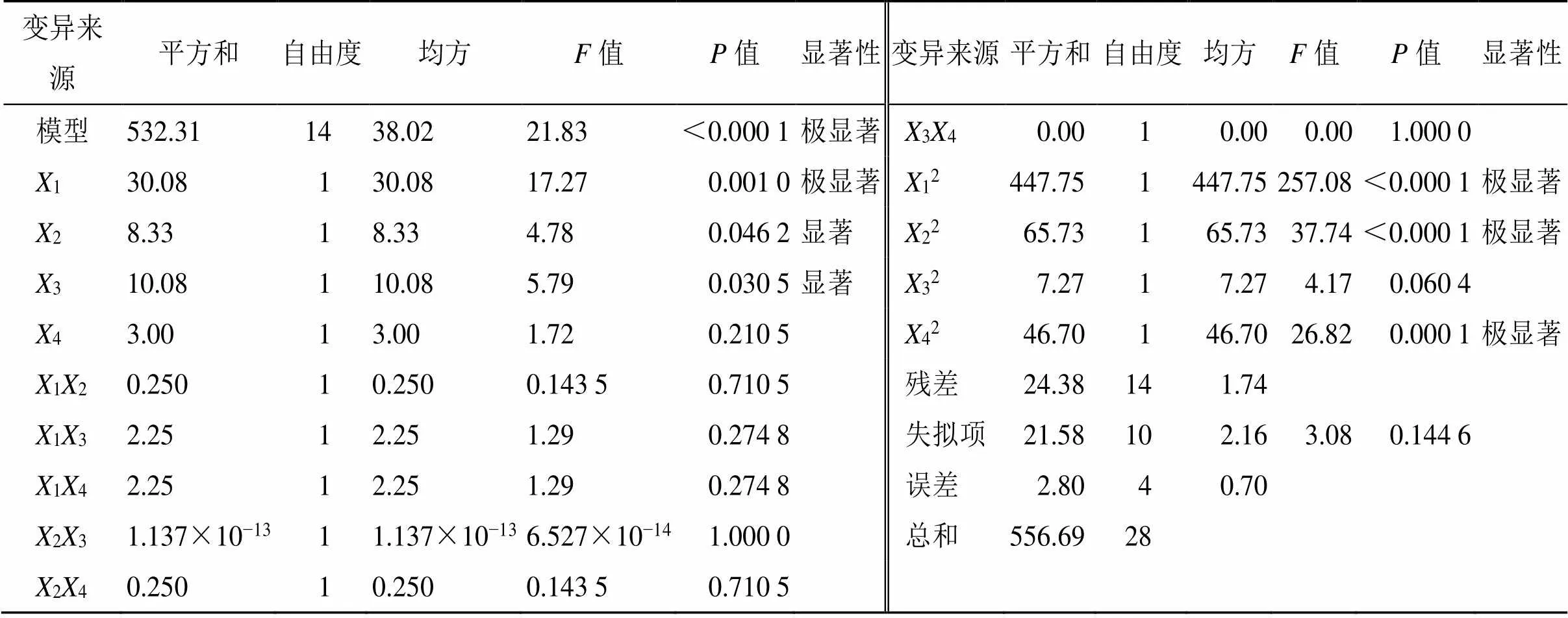
表3 回归模型方差分析结果

图1 各因素对膜剂综合评分影响的响应面图
2.6 3种口腔溃疡膜剂的制备
配制3份25 mg/mL乙基纤维素乙醇溶液,取12 mL铺于预先涂有液体石蜡的光滑玻璃板上(10 cm×10 cm)上,制成空白隔离层。取3份63 mg/mL PVA 17-88、55 mg/mL PVP K30、3.0 mg/mL明胶和0.047 mL/mL甘油溶解于20 mL蒸馏水中,后分别加入6 g改性口腔溃疡散(改性青黛∶白矾∶冰片20∶10∶1)、6 g物混溃疡散(青黛-乳糖物理混合物∶白矾∶冰片20∶10∶1)、4 g普通口腔溃疡散(青黛∶白矾∶冰片10∶10∶1),混匀后静置脱气泡。将脱气泡后的溶液铺于预先制备的空白隔离层上,于40 ℃下烘干得到药膜,将药膜裁剪为1 cm×1 cm,即得对应的膜剂。
2.7 口腔溃疡膜剂质量评价
2.7.1 表面形貌观察 3种膜剂药物层见图2-A,可见3种膜剂均呈现深蓝色,其中普通口腔溃疡膜剂表面十分不平整,凹凸不平;物理混合物口腔溃疡膜剂(下称物混膜剂)表面平整程度较普通膜剂好,但表面浮有少量药物颗粒;改性口腔溃疡膜剂表面光滑,有光泽。膜剂隔离层见图2-B,可见3种膜剂的隔离层相似,光泽感强。3种膜剂药物层SEM图见图2-C,可见普通膜剂表面凹凸不平,厚薄不均一;物混膜剂表面稍有不平,而青黛改性之后的膜剂表面光滑,较平整。这可能是因为普通口腔溃疡膜剂含有疏水性的青黛,使得药物难以在基质中分散均匀。且青黛的不溶性与重力因素使其在静置脱气泡时沉降至底部,涂膜不均。青黛改性后亲水性增加,且粒度降低,在基质中分散均匀且减缓了静置脱气泡时的沉降速度,故制成的膜剂表面均一,外观形态较好。

图2 双层膜剂的药物层(A)、空白隔离层(B)和SEM图(C)
2.7.2 pH值测定 膜剂的pH值对口腔黏膜的刺激性有重要影响。取膜剂置于装有5 mL pH值为6.8的磷酸盐缓冲液(PBS)的离心管中,后将pH计置于膜剂表面,读数稳定后测定pH值。平行3次实验。由表4可知,3种膜剂pH值在6.93~7.02,无刺激性,接近于口腔中的pH值。3种膜剂的表面pH值无显著性差异。
2.7.3 黏附性能 剪下大鼠颊黏膜,将其固定于烧杯内侧,取润湿后的膜剂粘贴于黏膜组织上,烧杯中加入生理盐水,用磁力搅拌器在37 ℃下以150 r/min转速搅拌,记录膜剂从黏膜组织上脱落的时间。结果如表4所示,普通口腔溃疡膜剂的平均黏附时间为142.67 min左右,改性口腔溃疡膜剂的平均黏附时间在149.33 min左右,物混口腔溃疡膜剂平均黏附时间在146.67 min左右,3者黏附时间相差不大。
表4 普通膜剂、改性膜剂和物混膜剂的表面pH值、黏附时间、抗拉强度(, n = 3)
与物混膜剂比较:*<0.05
*< 0.05physical mixed film
2.7.4 抗张强度 采用质构仪对不同膜剂的机械性能进行测定,质构仪选择拉伸模式,探头距离30 mm,测试速度为1 mm/s,记录抗拉力和拉伸长度,计算3种膜剂的抗拉强度,结果如表4所示。改性膜剂和普通膜剂抗拉强度接近,为1.06 MPa左右,而物混膜剂抗张强度最低,为0.93 MPa左右。
2.7.5 含量测定
(1)色谱条件:色谱柱为Welchrom-C18柱(250 mm×4.6 mm,5 mm);流动相为甲醇-水(70∶30);体积流量为1 mL/min;柱温30 ℃;进样量10 μL;检测波长289 nm。
(2)对照品溶液的制备:精密称取靛蓝对照品、靛玉红对照品适量,分别置于25 mL棕色量瓶中,加入,-二甲基甲酰胺(DMF)超声30 min并定容,制得155.6 μg/mL靛蓝对照品溶液和126.4 μg/mL靛玉红对照品溶液,作为储备液。
(3)供试品溶液制备:取青黛改性之后的膜剂于10 mL量瓶中,加入DMF超声30 min,过0.22 μm微孔滤膜后,即得。
(4)线性关系考察:将上述靛蓝、靛玉红对照品储备液稀释制成6个不同质量浓度的对照品溶液,以峰面积为纵坐标(),质量浓度为横坐标()进行线性回归,结果表明靛蓝、靛玉红回归方程分别为=6×107-678.83(=0.999 9),=5×107+905.05(=0.999 6),靛蓝在31.12~38 900.00 ng/mL、靛玉红在50.56~3 160.00 ng/mL线性关系良好。
(5)精密度考察:取靛蓝、靛玉红对照品溶液,按“色谱条件”项下方法连续进样6次,结果表明靛蓝峰面积RSD为0.24%,靛玉红峰面积RSD为0.60%,表明仪器精密度良好。
(6)重复性考察:取6份改性膜剂按“供试品溶液的制备”项下方法制备样品,测定靛蓝、靛玉红质量分数,结果表明靛蓝RSD为2.82%,靛玉红RSD为2.49%,表明方法重复性良好。
(7)稳定性考察:取1份改性膜剂按“供试品溶液的制备”项下方法制备样品,于0、2、4、8、12、24 h后测定靛蓝、靛玉红峰面积,计算靛蓝RSD为1.06%、靛玉红RSD为0.44%,表明供试品溶液稳定性良好。
(8)加样回收率考察:取已测定靛蓝和靛玉红含量的供试品按1∶1加入靛蓝、靛玉红对照品溶液,测定含量,结果表明靛蓝、靛玉红的平均加样回收率分别为100.31%、93.72%。
(9)含量均匀性测定:分别取3种口腔溃疡膜剂置于10 mL棕色量瓶中,加入DMF超声30 min并定容,过0.22 μm微孔滤膜后进样测定,每种膜剂平行测量10次。结果如表5所示,普通口腔溃疡膜剂靛蓝和靛玉红质量分数分别为0.429%、0.043%;改性口腔溃疡膜剂靛蓝和靛玉红质量分数分别为0.335%、0.030%;物混口腔溃疡膜剂靛蓝、靛玉红质量分数分别为0.247%、0.022%。改性口腔溃疡膜剂中靛蓝和靛玉红的RSD(分别为3.18%、2.38%)均小于普通膜剂(分别为0.429%、0.043%)和物混膜剂(8.76%、9.54%),表明改性口腔溃疡膜剂含量均匀性高于普通膜剂和物混膜剂。
表5 普通、改性、物混口腔溃疡膜剂含量均匀性(, n = 10)
2.7.6 体外药物释放 采用Franz扩散池研究口腔溃疡膜剂的体外药物释放。将0.22 μm的醋酸纤维素膜在pH值为6的PBS缓冲液中水化12 h,然后将其固定于扩散池,将1 cm×1 cm的双层膜剂固定在醋酸纤维素膜上,以pH值为7.4的PBS为接受介质,37 ℃恒温水浴加热,接收池内的磁力搅拌子转速为300 r/min。分别于0.5、1.0、1.5、2.0、2.5、3.0 h的时间点取样(同时加入同体积的空白接收介质),采用HPLC法测定接收液中的靛蓝含量。结果如图3所示,仅改性口腔溃疡双层膜剂测出了靛蓝含量,其余膜剂未测出。改性口腔溃疡膜剂靛蓝溶出量随时间的增加而增加。体外药物释放证明了改性双层膜剂有效成分渗透量高于未改性膜剂,这可能是因为青黛经改性后,粒度的降低使有效成分渗透量增多[11]。
2.8 口腔溃疡膜剂药效学评价
2.8.1 口腔溃疡模型的建立、动物分组与给药 56只SD雄性大鼠适应性喂养1周,用20%乌来糖(1 g/kg)ip麻醉,暴露大鼠下唇黏膜,将浸润50%冰醋酸的脱脂棉球置于大鼠下唇黏膜上烧灼60 s,24 h后观察溃疡面形成情况。溃疡表面呈白色类椭圆形,水肿,边缘充血。将大鼠分为7组,空白组、模型组、阳性组(蜂胶口腔膜)、口腔溃疡散剂组,普通口腔溃疡膜剂组、改性口腔溃疡膜剂组、物混口腔溃疡膜剂组。每天给药3次,1次1片(普通口腔溃疡膜给药剂量为40 mg/片,改性口腔溃疡膜与物混口腔溃疡膜给药剂量为60 mg/片,三者含药量相同,均为40 mg/片),间隔4 h。
2.8.2 各组大鼠溃疡形态比较 大鼠第1、3、5、7天的口腔溃疡图像如图4所示,溃疡面积用黄色线条勾勒出。从图中可看出,50%冰醋酸处理第1天后各组大鼠均表现出口腔溃疡,即黏膜周围红肿,表面覆盖白色假膜。各给药组在7 d后的口腔溃疡严重程度均有所减轻,溃疡面积逐渐减小,其中阳性药组与改性膜剂给药组愈合过程更快,表现出最佳的治疗效果。
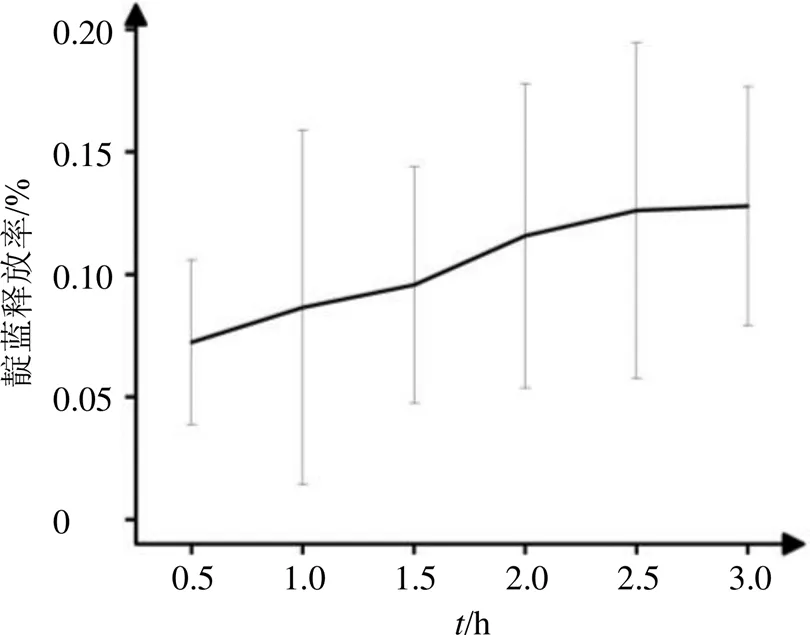
图3 改性口腔溃疡膜剂体外靛蓝释放度(, n = 3)

图4 各组大鼠口腔溃疡形态
2.8.3 溃疡组织病理学考察 组织病理学HE染色结果如图5所示,空白组大鼠口腔黏膜结构正常,黏膜上皮、固有层以及黏膜下层结构完整,较少炎症细胞浸润;模型组大鼠口腔黏膜组织上皮破损并脱落严重,有较多炎症细胞浸润;口腔溃疡散剂组大鼠稍有黏膜组织上皮层破损;普通膜剂组与物混膜剂组黏膜结构完整,然普通膜剂组黏膜角化层稍有脱落现象,物混膜剂组棘层松散;改性膜剂组、阳性药组与模型组相比,结构完整,减少了炎症细胞的浸润。
2.8.4 溃疡组织中TNF-α、IL-β、IL-6水平 溃疡组织炎症指标检测结果如表6所示。结果表明,模型组溃疡组织中TNF-α、IL-1β、IL-6含量显著增加(<0.01),表明造模成功。与模型组相比,阳性给药组显著减少了口腔溃疡组织中TNF-α、IL-1β的含量(<0.05)、显著减少了IL-6的含量(<0.01);改性膜剂组的TNF-α、IL-1β、IL-6的含量低于模型组,差异有统计学意义(<0.05);普通膜剂组较模型组显著减少了IL-1β的含量(<0.05)。
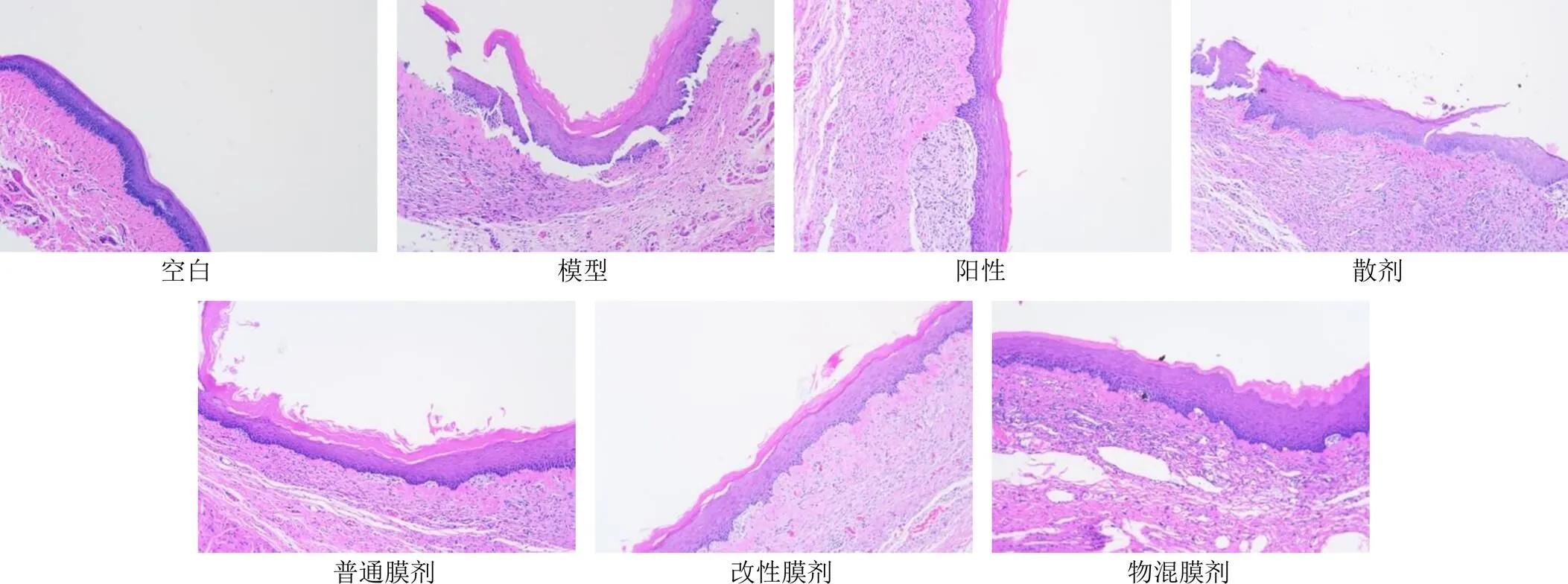
图5 各组大鼠口腔溃疡组织病理切片
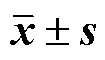
表6 各组大鼠口腔溃疡组织中TNF-α、IL-1β、IL-6含量(, n = 8)
与模型组比较:*<0.05**<0.01
*< 0.05**< 0.01model group
3 讨论
青黛具有抗炎、调节免疫、抗菌和抗病毒作用[14];冰片可抗菌、镇痛抗炎[15];白矾能收敛消炎、止血抗菌[16]。3者合用,可有效缓解溃疡病灶处的痛感,促进创面的愈合[17]。因此,本研究选择口腔溃疡散作为模型药物制备口腔溃疡膜剂。课题组前期将口腔溃疡散制成单层膜剂,发现由于膜剂中有青黛的存在,手指在取用以及口腔在贴膜时易被染色,因此课题组设计制备双层膜剂,空白隔离层不仅避免手指和口腔染色,提高了患者用药的依从性,还控制了药物单向释放,提高疗效。
本课题组在前期成膜材料处方筛选预实验中发现,阿拉伯胶成膜性和韧性差,CMC-Na不能与改性青黛混合均匀,HPMC虽成膜性较好,然而韧性欠佳。通过处方筛选与优化,最终选择PVA 17-88、PVP K30、明胶、甘油为膜剂处方。对比青黛改性前后所制备的膜剂,从肉眼观察以及SEM结果可看出,青黛改性之后的膜剂具有更光滑均一的外观,这是因为青黛经改性后,一方面亲水性增加,均匀分散在成膜材料溶液中,另一方面粒径降低,减缓了药物在静置脱气泡时的沉降速率,从而在铺膜过程中均匀分布,这也使改性膜剂具有更高的含量均匀性。本课题组在膜剂体外药物释放度实验中发现,青黛改性之后的膜剂靛蓝渗透量低且标准差较大,这可能与靛蓝性质有关。靛蓝是一种结构对称的非极性平面分子,表面自由能非极性分量高,疏水性强[18],在接受液中不能形成均匀分散体系,故取样时难以保证均一性。然而青黛未改性膜剂未检测出靛蓝,说明青黛改性之后的膜剂有效成分释放量增加,这与课题组前期在改性青黛工艺研究中的发现较为一致,即乳糖增加了靛蓝的释放率,这可能是由于青黛改性之后粒度减小,比表面积增加,导致有效成分释放更多。
综上,本研究制备的口腔溃疡双层膜剂,表面光滑平整,色泽均一,药物含量均匀,对口腔溃疡有较好的治疗效果,克服了口腔溃疡散给药量不准确,难以保持有效浓度等问题,为提高口腔溃疡散的临床适用性提供了依据。
利益冲突 所有作者均声明不存在利益冲突
[1] Gu Y H, Huang Y X, Qiu Z Y,. Vitamin B2functionalized iron oxide nanozymes for mouth ulcer healing [J]., 2020, 63(1): 68-79.
[2] 龚琴琴, 王倩, 郭玲, 等. 雷公藤红素口腔溃疡膜剂的制备及其质量初步评价 [J]. 中国药房, 2020, 31(21): 2574-2578.
[3] 张定堃, 秦春凤, 韩丽, 等. 粒子设计对口腔溃疡散粉体学性质的影响 [J]. 中国中药杂志, 2013, 38(3): 334-340.
[4] 刘博洋. 口腔溃疡含片与口腔溃疡散治疗III期复发性阿弗他溃疡疗效对比 [J]. 中国烧伤创疡杂志, 2022, 34(1): 9-11.
[5] 黄月英, 唐晓萌, 王志君, 等. 盐酸利多卡因双层颊黏膜黏附膜剂的研制及表征 [J]. 中国医药工业杂志, 2022, 53(9): 1292-1297.
[6] 杜娟, 夏晓彤, 马皖婷, 等. 中药药膜治疗复发性口腔溃疡的临床研究进展 [J]. 全科口腔医学电子杂志, 2019, 6(13): 3-5.
[7] Li W, He W X, Gao P,. Preparation,andevaluations of compoundand ornidazole film [J]., 2016, 39(10): 1588-1595.
[8] Alves T F R, Rios A C, da Silva Pontes K,. Bilayer mucoadhesive buccal film for mucosal ulcers treatment: Development, characterization, and single study case [J]., 2020, 12(7): 657.
[9] 杨明, 张定堃, 贺亚男, 等. 青黛产业高质量发展的挑战与策略 [J]. 中国中药杂志, 2021, 46(13): 3171-3179.
[10] 韩丽, 张定堃, 林俊芝, 等. 适宜中药特性的粉体改性技术方法研究 [J]. 中草药, 2013, 44(23): 3253-3259.
[11] 韩丽, 张定堃, 黄胜杰, 等.一种青黛干混悬剂及其制备方法: 中国, CN 202211538601.9 [P]. 2022-12-02.
[12] 张强, 王倩倩, 陆剑锋, 等. 水产动物明胶的研究进展 [J]. 明胶科学与技术, 2013, 33(3): 147-153.
[13] 李文娜, 欧水平, 王玉和. 皮肤用成膜制剂研究进展 [J]. 遵义医科大学学报, 2021, 44(3): 389-395.
[14] 高凤洋, 张大方, 李超英. 中药青黛炮制及药理作用的研究进展 [J]. 长春中医药大学学报, 2020, 36(1): 180-183.
[15] 魏楚蓉, 伍赶球. 冰片的药理作用及其机制研究进展 [J]. 国际病理科学与临床杂志, 2010, 30(5): 447-451.
[16] 尤淑霞, 吴德康, 刘圣金, 等. 白矾的基原考证及药理作用 [J]. 中国中医药信息杂志, 2010, 17(7): 111-112.
[17] 闫春霞, 王常建. 甲硝唑口腔粘贴片联合口腔溃疡散治疗复发性口疮患者的疗效分析 [J]. 现代诊断与治疗, 2021, 32(6): 892-893.
[18] 王鑫, 刘剑云, 张定堃, 等. 青黛饮片亲水性改性工艺的优选研究 [J]. 中草药, 2016, 47(3): 401-406.
Effects of surface modification ofon quality and drug efficacy of oral ulcer bilayer film
HUANG Sheng-jie1, ZHONG Jing-ping1, XIE Jin1, HE Ya-nan1, GUO Zhi-ping2, LIU Xue-mei1, YANG Ming3, ZHANG Ding-kun1, HAN Li1
1. State Key Laboratory of Southwestern Chinese Medicine Resources, Chengdu University of Traditional Chinese Medicine, Chengdu 611137, China 2. Sichuan Houde Pharmaceutical Technology Co., Ltd., Chengdu 610041, China 3. State Key Laboratory of Modern Chinese Medicine Preparations, Ministry of Education, Jiangxi University of Chinese Medicine, Nanchang 330004, China
To prepare the bilayer film for oral ulcer by solvent casting method, and study the effect of surface modification on film quality and efficacy of Qingdai ().The optimal formulation of the film was optimized by single-factor experimental design and response surface optimization method, and the properties of the film such as surface morphology, adhesion time, tensile strength, content determination and drug releasewere evaluated. A rat oral ulcer model was further established by the chemical burning method, and the effects of film preparations on tumor necrosis factor-α (TNF-α), interleukin-1β (IL-1β), IL-6 and oral ulcer tissue morphology were investigated.The blank isolation layer was determined to be 25 mg/mL ethyl cellulose ethanol solution, and the best formulation of the drug-loaded film was as follow: 63 mg/mL PVA17-88, 55 mg/mL PVP K30, 3.0 mg/mL gelatin and 0.047 mL/mL glycerin. After the surface modification of, the double-layer film preparation had a smoother and more uniform appearance, higher content uniformity and release rate of active ingredient indigo than the unmodifieddouble-layer film preparation. The pharmacodynamic results showed that compared with the model group, the contents of TNF-α, IL-1β, and IL-6 (< 0.05) were significantly reduced in the positive group and the modified film group and the infiltration of inflammatory cells was reduced, and the healing degree of ulcer tissue was higher.The double-layer film for oral ulcers of modifiedhas better quality and curative effect, and has a better application prospect.
; powder surface modification; mouth ulcer powder; double-layer film formulation; evaluation of drug efficacy; indigo; indirubin
R283.6
A
0253 - 2670(2023)13 - 4118 - 10
10.7501/j.issn.0253-2670.2023.13.005
2022-12-21
国家自然科学基金面上项目(82173976);国家自然科学基金面上项目(81773918)
黄胜杰,女,硕士研究生,研究方向为中药新制剂、新技术、新剂型。E-mail: 2398931073@qq.com
通信作者:韩 丽,女,教授,博士生导师,研究方向为中药制剂工艺原理与品质优化。E-mail: hanliyx@163.com
张定堃,男,博士,副教授,硕士生导师,研究方向为中药制剂与品质评价新技术。E-mail: zhangdingkun@cdutcm.edu.cn
[责任编辑 郑礼胜]
