超声心动图在经导管二尖瓣缘对缘修复术中的应用进展
2023-06-12罗丽唐莹
罗 丽 唐 莹
(广西壮族自治区人民医院, 1 超声科,2 麻醉科,广西南宁市 530021)
【提要】 经导管二尖瓣缘对缘修复术(TEER)已成为治疗严重二尖瓣反流(MR)的成熟介入技术。该手术被推荐用于经最佳药物治疗仍有症状的心力衰竭合并重度MR患者。在TEER治疗MR中,超声心动图在术前诊断和筛选患者、术中实时监测指导夹合器置入、术后评估手术效果中发挥着极其重要的作用,尤其是经食管超声心动图已成为术中必不可少的影像学监测手段。
二尖瓣反流(mitral regurgitation,MR)是最常见的心脏瓣膜疾病,也是心力衰竭的常见原因[1-2]。目前,外科瓣膜修复或置换是治疗严重MR的主要方法,但50%以上的患者由于高龄、基础病多、心功能差等因素影响,手术风险太大而不能接受外科手术治疗[3]。对于手术耐受性差的患者迫切需要一种创伤较小的替代治疗方案,因此,具有微创、安全、恢复快等优点的经皮二尖瓣介入技术应运而生。经导管二尖瓣介入方法主要包括经导管二尖瓣缘对缘修复术(transcatheter edge-to-edge repair,TEER)、经导管瓣环成形术及经导管人工腱索修复术[4],其中TEER最为成熟。TEER是一种高度依赖超声引导的介入手术,本文就超声心动图在TEER中的应用进展综述如下。
1 TEER概述
TEER是一项基于外科二尖瓣缘对缘修复术的经导管介入技术,其通过夹合二尖瓣的前后瓣叶,使二尖瓣变为双孔,从而减少二尖瓣反流[5]。TEER的相应器械包括 MitraClip(雅培)、PASCAL(爱德华)和国产的 ValveClip(纽脉医疗)、Dragonfly(德晋医疗)、ValveClamp(捍宇医疗)[6]等。其中,MitraClip系统运用最早、最经典,是TEER的代表性器械。2003年委内瑞拉成功开展了第1 例使用MitraClip系统的TEER[7]。2012年,我国葛均波院士等[8]成功运用MitraClip系统完成国内首例TEER,术后随访显示该技术治疗MR具有较好的疗效[9]。Foster等[10]研究认为,对于高龄、外科手术耐受性差的患者,TEER是一种理想的手术方式。TEER高度依赖超声引导,超声在TEER术前筛选、术中监测引导及术后评价方面起着极其重要的作用。
2 超声心动图在TEER术前的应用
超声心动图可以评价MR的分型、病因,精准判断二尖瓣病变部位及病变程度,对于TEER术前诊断和筛选患者非常重要。
2.1 MR的分型 根据Carpentier分型,MR可分为3种类型。Ⅰ型:瓣叶活动正常,反流原因为瓣环扩张(Ⅰa型)或瓣叶穿孔(Ⅰb型);Ⅱ型:瓣叶活动过度,反流原因为瓣膜脱垂(Ⅱa型)或腱索断裂延长、乳头肌断裂(Ⅱb型);Ⅲ型:瓣叶活动受限,反流原因为瓣叶开放和关闭时均受限制(Ⅲa型)或瓣叶关闭时受限(Ⅲb型)[11]。目前指南推荐使用二尖瓣夹合手术的患者,主要针对Ⅱ型MR[12]。而Stone等[13]研究显示Ⅰa型患者行TEER能明显获益,这类人群也可能是二尖瓣夹合术的适合人群。
2.2 MR的病因 根据病因,可将MR分为退行性MR(degenerative MR, DMR)和功能性MR(functional MR, FMR)[14]。DMR也称原发性MR,是由二尖瓣自身病变如退行性病变、感染、炎症等因素引起,表现为瓣叶脱垂、腱索断裂等。FMR也称为继发性MR,其二尖瓣瓣膜结构完整,反流是由于左心室重构或功能障碍导致二尖瓣瓣环扩张、乳头肌移位或瓣叶栓系,常发生于缺血性或扩张型心肌病患者中。其中,FMR占MR罹患人群的70%以上[15]。FMR又分为房性FMR和室性FMR。房性FMR指左心室射血分数(left ventricular ejection fraction, LVEF)≥50%且无左心室壁活动异常的MR,室性FMR指LVEF<50%或左心室壁活动异常的MR。其中,室性FMR又可分为缺血性MR和非缺血性MR,外科治疗对于FMR,尤其是缺血性MR的效果较差。TEER治疗的获益人群仍存在争议[16-17]。Nagaura等[18]在一项使用TEER分别治疗38例房性FMR患者和49例室性FMR 患者的研究中发现:TEER治疗与MR的改善相关,房性FMR患者与室性FMR患者相比,其瓣叶对合更佳,二尖瓣瓣环缩小更明显,二尖瓣环面积减少也更多。由此可见,明确MR的病因非常重要,不同病因的MR选择药物治疗或手术治疗方案的疗效均有所不同。
2.3 定量评估MR 根据《二尖瓣反流介入治疗的超声心动图评价中国专家共识》[11],MR反流程度可分为无(0+)、轻度(1+)、中度(2+)、中重度(3+)、重度(4+)、极重度(5+)。其评价指标包括反流颈宽度(vena contracta width,VCW)、有效反流口面积(effective regurgitant orifice area, EROA)、反流容积(regurgitant volume, RVol)和反流面积分数(regurgitation fraction, RF)。(1)VCW<3 mm为轻度反流。(2)VCW为3~7 mm,MR程度需结合以下参数进行评估:①轻度MR,EROA<0.20 cm2,RVol<30 mL,RF<30%;②中度MR,EROA为 0.20~0.29 cm2,RVol为 30~44 mL,RF为30%~39%;③中重度MR,EROA为0.30~0.39 cm2,RVol为45~59 mL,RF为40%~49%;④重度MR,EROA≥0.4 cm2,RVol≥60 mL,RF≥50%。(3)VCW>7 mm为重度、极重度反流。对于LVEF≥60%,经胸二维超声心动图提示反流束冲击房顶部并且折返,为重度MR;如果折返的血流束超过左心房中段,且RF≥75%,RVol≥80 mL为极重度MR。
2.4 MR的解剖情况 经食道超声心动图(trans esophageal echocardiography, TEE)与经胸超声心动图(trans thoracic echocardiography,TTE)相比,TEE探头更靠近二尖瓣,分辨率更高,瓣叶结构及VCW显示更清晰,病变部位定位更准确[14]。亚太心脏病学会专家组[19]推荐应用TTE对患者进行初步筛查,评估MR严重程度;而TEE可以对二尖瓣解剖结构做出详细评估,明确MR病因及是否适合行TEER手术。TTE探查二尖瓣:(1)胸骨旁长轴切面显示A2、P2区(图1A);(2)二尖瓣水平短轴切面显示A1、A2、A3、P1、P2、P3区(图1B);(3)心尖四腔心切面显示A2、P2区(图1C);(4)心尖二腔心切面显示A1、P3区(图1D)。TEE探查二尖瓣:(1)食管中段的四腔心切面显示P1和A2、A3区(图2A);(2)食管中段的二尖瓣联合交界处切面显示P1、A2和P3区(图2B);(3)食管中段的二腔心切面显示A1、A2和P3区(图2C);(4)食管中段的左室长轴切面显示A2和P2区(图2D)。经食管三维超声心动图(three-dimensional TEE,3D-TEE)有两个非常重要的切面,一个为X-plane正交切面,包括食管中段的二尖瓣联合交界切面及左室长轴切面,可同时显示二尖瓣的内中外侧及前后侧关系;另一个为二尖瓣的“三维外科切面”,可以立体显示二尖瓣的整体观,在术中更好地观察二尖瓣夹合器与周边的空间关系,方便调整夹合器的位置,减少穿刺并发症,缩短操作时间。在3D-TEE中,Philips TrueVue心腔镜成像新技术是一种新型3D超声技术[20]:TrueVue Light光源心腔镜,光影变化,可透过表面看本质,真实还原心脏立体结构;TrueVue Color彩色心腔镜,血流溯源,更准确地显示心脏血流动力学形态,使图像更形象、直观。
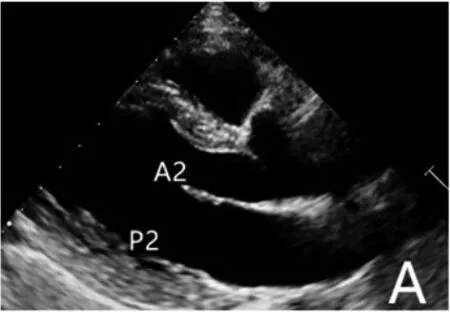
图1A胸骨旁长轴切面显示A2、P2区;
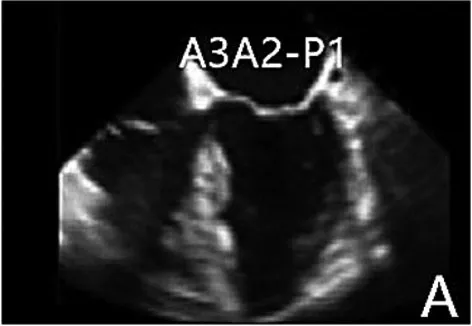
图2A四腔心切面显示P1和A2、A3区;
2.5 TEER的适应证 目前对于具有较高外科手术风险的DMR及大部分FMR患者,传统的外科手术已无法进行有效治疗。2020 年美国心脏病学会(American College of Cardiology,ACC)和美国心脏协会(American Heart Association,AHA)联合发布的《心脏瓣膜病管理指南》及《二尖瓣反流决策路径ACC专家共识》均将最佳药物治疗仍有症状的心力衰竭合并重度MR列为TEER适应证[21-22]。欧洲心脏病学会指南[23]亦指出,对于FMR患者,优化药物治疗后如仍有持续症状,推荐选用手术(Ⅱa型)或导管介入治疗(Ⅱb型)。TEE评估二尖瓣解剖符合TEER的指标包括:中重度(3+)或重度(4+)MR,房间隔高度>4 cm、二尖瓣瓣口面积>4 cm2、平均跨瓣压差<4 mmHg、返流区无明显钙化、穿孔或瓣中裂等;另外,DMR需满足瓣叶脱垂宽度<15 mm,连枷间隙<10 mm,活动瓣叶长≥10 mm;FMR需满足左室舒末内径<65 mm、非栓系瓣叶长≥10 mm、对合深度<11 mm、对合高度>2 mm[24]。Estévez-Loureiro等[25]研究发现MitraClip系统治疗偏心反流(A1、P1 或A3、P3区)与治疗中心性反流(A2、P2区)的手术成功率和手术相关并发症发生率相近,术后两组的心功能恢复差异无统计学意义。
3 超声心动图在TEER术中术后的应用
TEE在TEER术中可指导选择夹合器、清晰显示夹合器与周围组织的空间关系,实时监控夹合器输送、捕获及释放瓣叶的情况。
3.1 术中TEE指导选择夹合器型号 Feldman等[26]发现实时3D-TEE在TEER术中能准确测量二尖瓣脱垂部位或瓣叶脱垂高度以及容积等,为手术方案提供重要指导意义。根据TEE测量的二尖瓣脱垂宽度和瓣叶长度,选择合适型号的夹合器。MitraClip G4是目前最新产品,其包括4 种不同长度和尺寸的夹合器(NTR、NTW、XTR、XTW), 并具有单独捕获二尖瓣瓣叶及监测心房压力的功能,可实时监测手术效果[27]。
3.2 术中TEE实时监测和引导夹合器置入
3.2.1 TEE引导房间隔穿刺 TEE可清楚地显示房间隔的形态,通过双房上下腔切面确定穿刺点上下的位置,大动脉短轴切面确定穿刺点前后的位置,再通过四腔心切面测量穿刺点高度,确定穿刺点位置后在大动脉短轴切面直视下进行穿刺。一般选择房间隔后上部位为穿刺点,穿刺点高度为房间隔穿刺点与二尖瓣环的距离。DMR 穿刺点高度为:A1-P1区3.5 cm、A2-P2区4.0 cm、A3-P3区4.5 cm;FMR穿刺点高度为4.0 cm。潘翠珍等[28]研究发现实时3D-TEE能够通过准确定位房间隔穿刺点以及术中监测夹合器的位置等引导TEER术的顺利进行。
3.2.2 TEE引导输送系统进入左心房 用二维TEE在大动脉短轴切面跟踪器械头端,注意避免与左房壁及左心耳壁接触,必要时用3D-TEE追踪,注意将鞘管放于二尖瓣的“三维外科切面”的3~4点位置。
3.2.3 TEE引导夹合器在二尖瓣上方定位 为避免损伤二尖瓣叶、腱索、乳头肌等结构,选择空间相对大的左房对夹合器轴向进行调整。通常采用3D-TEE的X-plane切面(二尖瓣联合交界切面+左室长轴切面)及二尖瓣的“三维外科切面”引导。打开钳夹器的两个臂,调整夹合器,使其能够垂直于二尖瓣平面。在二尖瓣联合交界切面可调整夹合器位置更靠前或后,在左室长轴切面可调整夹合器位置更靠近内交界或外交界。另外通过二尖瓣的“三维外科切面”,可以实时整体观察夹合器的位置。
3.2.4 TEE引导夹合器进入左心室 当调整好夹合器方向后,保持鞘管方位不变,舒张期进入左心室。同样采用3D-TEE的X-plane切面及二尖瓣的“三维外科切面”,引导夹合器定位至二尖瓣前后叶的病变区。捕获瓣膜前,夹合器在左心室长轴切面显示为V字形,在二尖瓣交界切面显示为直线形。
3.2.5 TEE引导夹合器捕获和夹合瓣膜 通过左室长轴切面引导夹合器捕获二尖瓣叶,将夹合器放置于反流束最多处,此时应注意放大图像、调窄扇角以提高时间分辨率使图像更清晰。完成二尖瓣叶捕获后,判断夹合器是否已抓取足够的瓣叶组织。当瓣叶抓取成功后,在二尖瓣的“三维外科切面”可显示典型的双口二尖瓣图像,同时可见MR显著减少,肺静脉血流频谱改变及左房自发显影。随后应用TEE引导鞘管退出,并观察房间隔穿刺点分流情况。
3.3 术中TEE评估TEER效果 夹合器释放后,用TEE评估夹合器的稳定性、MR的残余程度及起源位置,判断是否需要置入第2枚夹合器。另外,还需评估二尖瓣前后瓣叶夹合量是否为6~9 mm,二尖瓣平均压差应<5 mmHg。理想效果是MR至少减少到轻度(1+),若术中二尖瓣反流减少程度不理想,则可能需要放置第2枚甚至更多的夹合器。余蕾等[29]研究指出TEE对于术中引导2枚夹合器的置入具有重要的意义。
3.4 在TEER术后的应用 超声心动图可对TEER治疗后进行近期、远期随访:再次评估夹合器是否稳定,评估有无二尖瓣残余反流及程度、二尖瓣结构损伤、二尖瓣狭窄、心功能变化、心包积液、心律失常等并发症[30]。
4 小 结
综上所述,在TEER治疗MR中,超声心动图在术前诊断和筛选患者、术中引导房间隔穿刺、实时监测指导夹合器置入、术后评估手术效果等方面发挥着极其重要的作用。与其他影像学检查不同的是TEE探头位于食管内,具有不干扰手术视野的优点。3D-TEE使图像更形象、直观,有利于超声科医生与临床介入医师的协作与沟通。相信随着TEER手术的不断进步,超声心动图也将发挥更大的作用。
