Sc、Zn、B等元素对Ag-4Cu-0.5Ni合金抗硫化性能的影响
2023-06-11王洪凯王春新李斌川
王洪凯, 王春新, 韩 庆, 李斌川
(1.辽宁新都黄金有限责任公司, 辽宁 朝阳 122000; 2.东北大学 冶金学院, 辽宁 沈阳 110819;3.沈阳市有色金属资源循环利用重点实验室, 辽宁 沈阳 110819)
0 引言
电触点是连接器、断路器、继电器等各种电气和电子设备的关键部件[1-2],广泛应用于汽车、家用电器、航空航天、工业仪器[3],而设备性能的优劣很大程度上取决于电触点材料的可靠性和稳定性;其中,接触材料应具有优良的导电性、机械性能和抗电弧侵蚀性能[4]。银(Ag)具有优良的导热性、较低的接触电阻、优异的化学稳定性、较高的塑性变形能力、良好的抗电弧侵蚀和抗熔焊性等优点,广泛用于电触点材料的制备[5-6]。
虽然Ag在纯净的大气中较为稳定,但是在含工业污染物(如H2S、SO2、Cl2和HCl等)的大气中易腐蚀变色。Ag与含还原硫的无机硫化物、有机硫化物相互作用,表面易形成黑色的Ag2S薄膜[7];其中,H2S对Ag的腐蚀能力最强[8],而Ag2S的形成将导致触点面积的减小和接触电阻的增大,加速触点损坏。
合金化法是常见的改善Ag合金抗硫化性的方法[9-10],尤其加入稀土元素RE(Rare Earth)时,可使Ag-RE固溶体晶内与晶界的电极电位差下降,可减缓腐蚀反应速率,相应使Ag合金抗硫化能力增强[11-13]。除此之外,Zn元素可以改善Ag合金制备过程中熔体的流动性,B可减少Ag熔体的表面张力,使熔体混合均匀[6];与此同时,两种元素的加入均对Ag合金的抗硫化性有一定的提高作用。本文通过在Ag-4Cu-0.5Ni合金中添加Sc、Zn、B等元素,采用静态浸渍试验、动电位扫描等手段,探讨合金成分对电接触银在0.1 mol/L的Na2S溶液中的腐蚀行为的影响规律。采用静态气氛暴露试验探讨合金成分对电接触银在室温H2S气氛中的腐蚀行为的影响规律,并用扫面电镜分析合金的硫化机理。
1 实验
1.1 实验原料及合金成分
实验用原材料Ag和Cu的质量分数均高于99.99%(辽宁新都黄金有限责任公司)。Ni、Sc、B元素均以含铜中间合金形式加入;其中,Ni、B中间合金分别为CuNi50和CuB4,采购于锦州市金属材料研究所,CuSc中间合金为自制的CuSc8.5。Zn采用化学纯锌粒,由天津市申泰化学额试剂有限公司提供。实验合金设计成分为Ag-4Cu-0.5Ni、Ag-4Cu-0.5Ni-0.3Sc、Ag-4Cu-0.5Ni-0.3Sc-1Zn和Ag-4Cu-0.5Ni-0.3Sc-1Zn-0.03B,分别命名为S1、S2、S3和S4。
1.2 合金制备过程
合金按设计成分进行配料,在30 kW高真空中频感应炉(锦州远腾电炉厂)中进行熔炼。先将感应炉抽真空至真空度达10-2Pa以下,其次通入高纯氩气并往复2次,在高纯氩气气氛下熔炼,且熔炼温度为1 200 ℃;合金熔化后在炉内保温0.5 h,浇铸得到厚度为9 mm的合金锭;铣去上下两个表面各1 mm的表面层,720 ℃均匀化退火4 h,热轧至3 mm;600 ℃中间退火0.5 h,终冷轧至1 mm。最后对样本进行热处理,热处理工艺为700 ℃固溶0.5 h,250 ℃时效处理4 h,将经过热处理后得到的银合金用冲片器进行冲片,得到直径10 mm样品若干。
1.3 性能测试及表征
将样品磨抛后进行静态浸渍实验和动电位扫描测试。静态浸渍实验分别将样品浸泡在0.1 mol/L的Na2S溶液中和H2S气氛的密闭容器中。H2S气氛的制备:先将60 g试剂纯Na2S·9H2O加入200 mL水中,并充分溶解;其次,称取7 g试剂纯KH2PO4加入200 mL水中,并充分溶解,随后将预配置的两种溶液混合后获得H2S气氛。采用扫描电镜(SEM,Ultra Plus,ZEISS Group)和能谱分析(EDS,Ultim Extreme,Oxford Instruments),观测H2S静态浸渍后的试样形貌和元素组成。动电位扫描测试采用经典三电极体系,合金片经封装后作为工作电极,铂片为辅助电极,采用饱和甘汞电极为参比电极,在科斯特CS 350电化学工作站上进行测试,电位扫描速度为0.5 mV/s。
2 结果与讨论
2.1 H2S静态浸渍实验
图1为样品S1~S4在H2S中静态浸渍的照片。可以看出,Ag-4Cu-0.5Ni合金在10 h时开始出现硫化斑,24 h出现彩色硫化层,48 h硫化层开始黑化。添加Sc、Zn、B后10 h均未见硫化斑,24 h同样出现硫化层,48 h有向黑色硫化层转化的迹象。加入Sc、Zn后样品24 h和48 h硫化程度减弱,加入B后效果不明显。

图1 S1~S4在H2S中静态浸渍的照片(其中1、2、3、4 分别为未浸渍、浸渍10 h、24 h、48 h)
2.2 0.1 mol/L Na2S溶液静态浸渍实验
0.1 mol/L Na2S浸泡5天的S1~S4合金表面硫化状态如图2所示。可以看出,Ag-4Cu-0.5Ni在0.1 mol/L Na2S浸泡5天合金表面出现较为严重的硫化腐蚀,而加入Sc、Zn、B后Ag-4Cu-0.5Ni合金的表面状态并未变化,表明加入Sc、Zn、B后可以显著提高Ag-4Cu-0.5Ni合金的抗硫化性能。

图2 S1~S4在0.1 mol/L Na2S溶液中静态浸渍照片
2.3 0.1 mol/L Na2S溶液的动电位扫描实验
S1~S4合金试样在0.1 mol/L Na2S溶液中腐蚀自腐蚀电位、腐蚀电流和年腐蚀速率如表2所示。可以看出,试样S1~S4的自腐蚀电位相近,腐蚀电流和腐蚀速率呈现降低趋势。Sc加入后自腐蚀电流降低55%左右,加入Zn后自腐蚀电流显著降低,B的加入使合金的自腐蚀电流略有上升,腐蚀速率也呈现对应的变化规律。
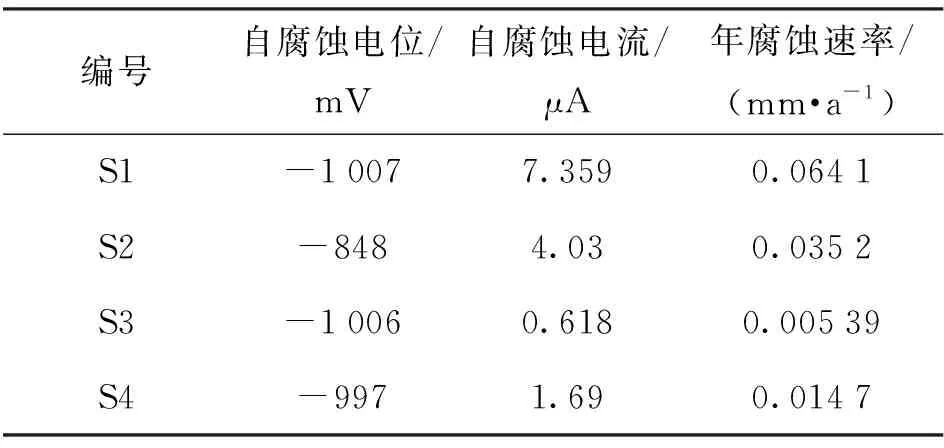
表1 S1~S4合金试样在0.1 mol/L Na2S溶液中腐蚀自腐蚀电位、腐蚀电流和年腐蚀速率
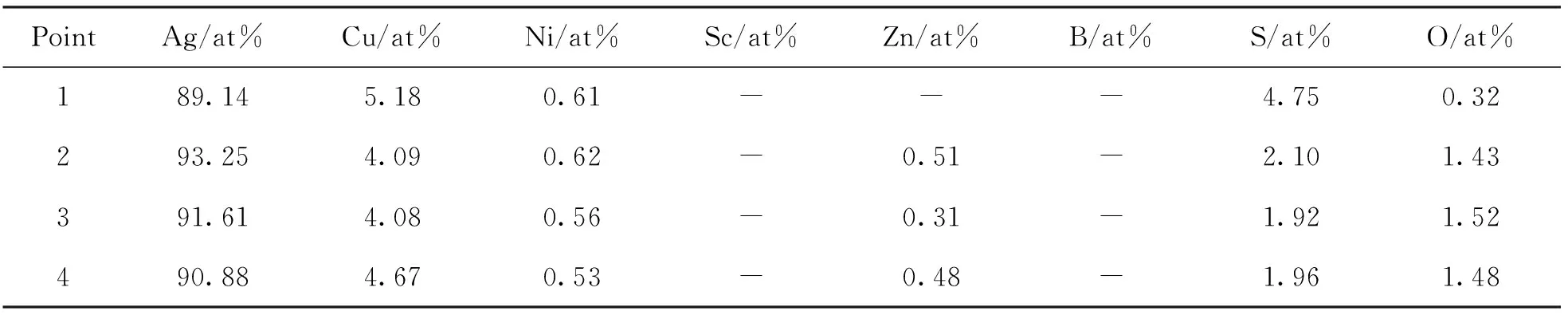
表2 S1~S4合金试样的元素定量分析结果
2.4 H2S静态浸渍的扫描电镜和能谱分析
图3为S1~S4合金试样的扫描电镜照片,对应图中各点的能谱分析结果如表2所示。

图3 S1~S4合金试样的扫描电镜照片
Sc与B元素在元素能谱分析过程中并未检出,可能由于添加量较少,并未达到对应元素的检测限。加入Sc、Zn、B可以看出H2S静态浸渍的合金表面S元素含量显著降低,而氧含量有所提高。由于Ag合金两相间的成分不同和显微缩松的存在,容易发生电化学腐蚀。添加Sc可使Ag合金组织更加致密,缩孔减少,抗腐蚀性能增强;Sc的电极电位较Ag、Cu的电极电位低,在Ag合金表面自发形成钝化膜,阻止了基体金属与腐蚀介质的接触,从而减缓电化学腐蚀。Zn与S的反应优先与Ag、Cu先发生,可以阻碍Ag和Cu的硫化腐蚀。同时Zn可以改善熔体的流动性,B可减少Ag熔体的表面张力,使熔体混合均匀,使合金的显微缩孔减少,增强合金的抗硫化性。
3 结论
本文利用高真空感应炉制备了Ag-4Cu-0.5Ni合金,探究了Sc、Zn、B等元素的加入对合金抗硫化性能的影响,主要结论如下:
(1)Ag-4Cu-0.5Ni合金中添加Sc、Zn、B等元素可提高合金在H2S气氛和Na2S溶液中的抗硫化能力;
(2)Ag-4Cu-0.5Ni合金中添加Sc、Zn、B等元素后合金的自腐蚀电位基本不变,自腐蚀电流和腐蚀速率降低;
(3)Ag-4Cu-0.5Ni合金抗硫化性的提高与合金显微缩孔的减少、Zn与S的优先反应和Sc生成的钝化膜有关。
