聚乙二醇洛塞那肽联合二甲双胍治疗新诊断肥胖2型糖尿病
2023-03-09周英旎石敏赖敬波李晓苗刘向阳
周英旎 石敏 赖敬波 李晓苗 刘向阳
空军军医大学西京医院内分泌代谢科(西安 710032)
随着经济快速发展、人口老龄化和生活方式改变等多种因素,近30年来我国糖尿病患病率快速增长。2015—2017年相关流行病学调查显示,我国成人糖尿病患病率已经高达11.2%,且肥胖和超重人群糖尿病患病率显著增加[1]。对于肥胖的2 型糖尿病患者治疗方案的选择,除了考虑降糖疗效外,同时需要兼顾减重、改善胰岛素抵抗等多方面因素。尽管随着医学的发展与进步,降糖药物种类越来越多,但是存在每日需多次服用或者有增加体质量等问题,胰高血糖素样肽1(GLP-1)及其类似物具有葡萄糖浓度依赖的刺激胰岛素分泌、延缓胃排空、减重、促进胰岛β 细胞增殖、保护心肾功能等作用[2-3],近年来在糖尿病治疗领域中的地位越发突出。聚乙二醇洛塞那肽(PEX168)是我国自主研发的长效GLP-1 受体激动剂,其作用机制与已批准上市的艾塞那肽一致,但作用时间更长,可每周给药1 次,且有明显减轻体质量、改善胰岛素抵抗等作用,极大提高了治疗效果及依从性。目前关于PEX168 在新诊断肥胖2 型糖尿病患者中的疗效与安全性报道较少,本研究通过在上述人群中使用PEX168,旨在探讨PEX168 治疗新诊断肥胖2 型糖尿病患者的有效性及安全性,为肥胖糖尿病患者治疗提供新思路。
1 资料与方法
1.1 一般资料选取空军军医大学西京医院内分泌代谢科门诊2021年10月至2022年4月共80 例新诊断的肥胖2 型糖尿病患者。采用随机数字表法将其分为治疗组和对照组。 其中对照组40 例(男21例,女19例),平均年龄为(47.2±12.1)岁。治疗组40 例(男20 例,女20 例),平均年龄为(46.8 ±11.3)岁。两组患者在年龄、体质指数(BMI)、血糖、血压、血脂等一般资料比较方面差异均无统计学意义。本研究获得医院医学伦理委员会批准(编号:KY20182008-1 号),所有患者入组前均签署知情同意书。
1.2 纳入和排除标准纳入标准:(1)符合《中国2 型糖尿病防治指南(2020 版)》中2 型糖尿病诊断标准;(2)新诊断或者已经确诊但未使用降糖药超过3 个月以上;(3)性别不限,年龄18 ~65 岁(含),BMI 24.0 ~32.0 kg/m2,空腹血糖(FBG)<11.0 mmol/L,7.5% ≤糖化血红蛋白(HbA1c)≤11.0%,甘油三酯(TG)<5.6 mmol/L。排除标准:(1)对PEX168过敏;(2)1 型糖尿病;(3)有糖尿病严重并发症的患者;(4)既往多次发生胰腺炎或者重度高脂血症患者;(5)甲状腺癌病史患者;(6)合并中重度心、肝、肺、肾疾病或任何可能影响研究结果的疾病;(7)备孕、孕期及哺乳期女性。
1.3 方法所有患者入组时均进行糖尿病知识教育,指导其合理饮食及运动管理,同时培训患者进行正规的自我血糖监测。对照组给予二甲双胍(中美上海施贵宝制药有限公司,国药准字:H20023370)500 mg,口服,每天3 次。治疗组给予二甲双胍(用法用量同对照组)联合PEX168(江苏豪森药业集团有限公司,规格0.5 mL:200 μg,批号:512200203)0.2 mg,皮下注射,1 次/周。两组患者均治疗12 周。
1.4 观察指标治疗前和治疗后检测所有患者的血糖、血脂、血压、体质量、尿酸等一般指标的变化。采用VARIANTⅡ型高压液相仪(美国伯乐公司)检测HbA1c;MAGLUMI 4000 型全自动化学发光免疫分析仪(厦门海菲生物技术有限公司)检测空腹胰岛素(FINS)。采用CKD-EPI 公式计算肾小球滤过率(eGFR),HOMA-IR,HOMA-β 计算公式分别为HOMA-IR=FBG × FINS/22.5,HOMA-β=20 ×FINS/(FBG-3.5)。
1.5 统计学方法采用SPSS 22.0 统计学软件进行数据分析。所有符合正态分布的计量资料以均数±标准差表示,非正态分布数据采用M(P25,P75)表示。两两比较采用t检验;计数资料比较采用χ2检验。P<0.05 代表差异有统计学意义。
2 结果
2.1 按照研究方案治疗12 周后,治疗组有2 例退出研究,对照组有4 例退出。以上患者均因为个人原因未能完成研究。
2.2 血糖及胰岛细胞功能变化两组患者治疗后FBG、PBG、HbA1c、HOMA-IR 均较治疗前下降,且治疗组上述指标改善程度优于对照组(P<0.05)。虽两组患者经治疗12 周后HOMA-β 差异无统计学意义,但均较基线水平有所改善。见表1。
表1 两组患者治疗前后血糖及胰岛细胞功能比较Tab.1 Blood glucose and islet cell function between the two groups±s
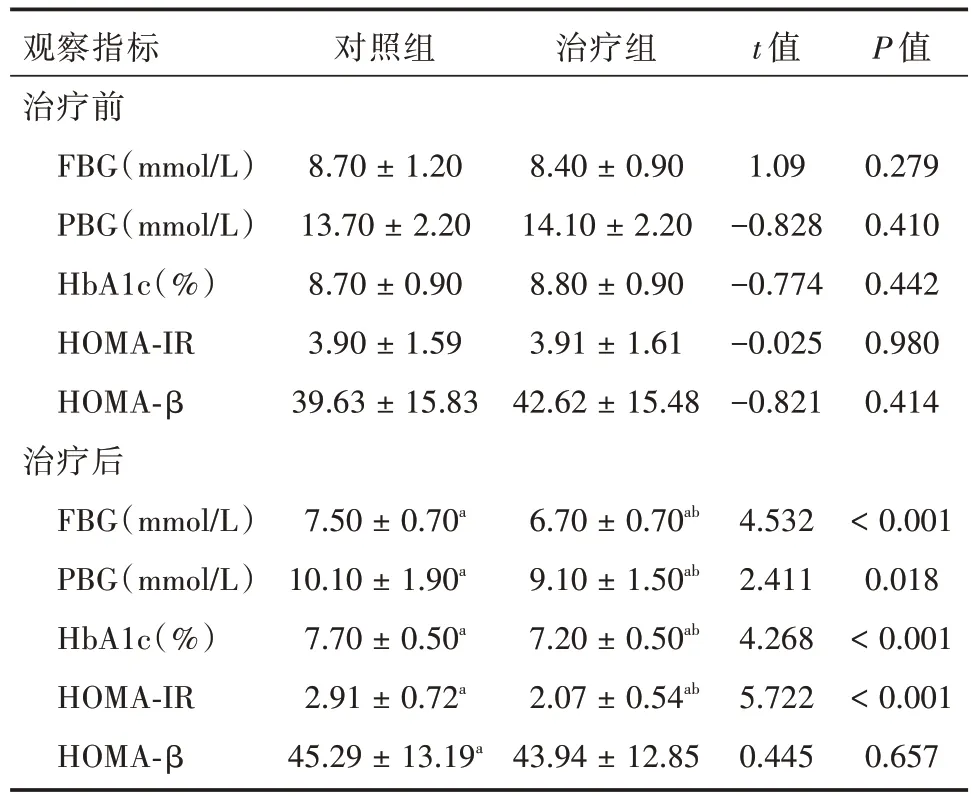
表1 两组患者治疗前后血糖及胰岛细胞功能比较Tab.1 Blood glucose and islet cell function between the two groups±s
注:与同组治疗前比较,aP <0.05;与同期对照组比较,bP <0.05
观察指标治疗前FBG(mmol/L)PBG(mmol/L)HbA1c(%)HOMA-IR HOMA-β治疗后FBG(mmol/L)PBG(mmol/L)HbA1c(%)HOMA-IR HOMA-β对照组治疗组t 值P 值8.70 ± 1.20 13.70 ± 2.20 8.70 ± 0.90 3.90 ± 1.59 39.63 ± 15.83 8.40 ± 0.90 14.10 ± 2.20 8.80 ± 0.90 3.91 ± 1.61 42.62 ± 15.48 1.09-0.828-0.774-0.025-0.821 0.279 0.410 0.442 0.980 0.414 7.50 ± 0.70a 10.10 ± 1.90a 7.70 ± 0.50a 2.91 ± 0.72a 45.29 ± 13.19a 6.70 ± 0.70ab 9.10 ± 1.50ab 7.20 ± 0.50ab 2.07 ± 0.54ab 43.94 ± 12.85 4.532 2.411 4.268 5.722 0.445<0.001 0.018<0.001<0.001 0.657
2.3 BMI、血压及生化指标变化治疗后两组患者BMI、SBP、DBP、TG、TC、UA 均较前下降,且治疗组下降幅度明显优于对照组,差异有统计学意义(P<0.05);而对照组LDL-C 较前无明显降低,治疗组LDL-C 较前下降明显(P<0.05)。两组患者在治疗后eGFR 均较治疗前改善,治疗组上升到(88.7 ± 17.60)mL/(min·173 m2),对照组上升到(84.76 ± 21.40)mL/(min·173 m2),其中治疗组用药前后eGFR改善差异有统计学意义(P<0.05)(表2)。
表2 两组患者治疗前后生化指标比较Tab.2 Biochemical indexes of patients in each group ±s

表2 两组患者治疗前后生化指标比较Tab.2 Biochemical indexes of patients in each group ±s
注:与同组治疗前比较,aP <0.05;与同期对照组比较,bP <0.05
观察指标治疗前BMI(kg/m2)SBP(mmHg)DBP(mmHg)TC(mmol/L)TG(mmol/L)HDL-C(mmol/L)LDL-C(mmol/L)eGFR[mL/(min·173 m2)]UA(μmol/L)治疗后BMI(kg/m2)SBP(mmHg)DBP(mmHg)TC(mmol/L)TG(mmol/L)HDL-C(mmol/L)LDL-C(mmol/L)eGFR[mL/(min·173 m2)]UA(μmol/L)对照组治疗组t值P值27.30±1.60 137.00±7.00 86.00±5.00 4.84±1.07 3.04±1.03 1.07±0.24 3.43±0.96 80.80±19.80 397.00±73.00 27.90±2.50 139.00±9.00 85.00±4.00 4.55±0.74 3.00±0.80 1.09±0.30 3.81±0.91 79.00±18.50 382.00±91.00-1.256-0.900 1.115 1.389 0.181-0.213-1.767 0.398 0.786 0.213 0.371 0.268 0.169 0.857 0.832 0.081 0.692 0.435 26.60±1.50a 136.00±7.00a 83.00±3.00a 2.28±0.39a 4.36±0.74a 1.18±0.26a 3.33±0.82 84.76±21.40 373.00±49.00a 25.80±2.00ab 132.00±6.00ab 79.00±3.00ab 1.73±0.47ab 3.85±0.65ab 1.38±0.29ab 2.93±0.74ab 88.70±17.60a 347.00±36.00ab 2.122 2.392 6.830 5.480 3.127-3.179 2.240-1.867 2.695 0.037 0.019<0.001 0.003<0.001 0.002 0.028 0.066 0.009
2.4 不良反应发生情况两组中均有患者出现轻度胃肠道反应,其中治疗组恶心3 例,腹泻1 例,心悸1 例,不良反应发生率13.1%。对照组腹泻2 例,恶心2 例,不良反应发生率11.1%,两组不良反应发生率差异无统计学意义。且胃肠道不良反应均为轻度,可耐受,坚持治疗2 ~4 周后自行缓解。治疗过程中所有患者未发生低血糖、肝、肾功能异常等。
3 讨论
随着城市化进程的加快及静态生活方式的流行,近年来我国糖尿病患病率逐年增加,且肥胖及超重人群糖尿病患病率显著增加[1],2017年数据发现,25 kg/m2≤BMI ≤30 kg/m2糖尿病患病率为13.8%,BMI ≥30 kg/m2者糖尿病患病率高达20.1%[4]。而肥胖可加重患者的胰岛素抵抗,使2 型糖尿病的心血管、肾病等各类并发症的风险、进展速度及危害显著增加[5-6]。因此,对于肥胖的2 型糖尿病治疗策略的选择除了着眼于其优秀的降糖效果外,还需关注其在减重、改善胰岛素抵抗,减少糖尿病并发症等方面的表现[7]。
GLP-1 是人体重要的肠道激素,主要由回肠和结肠中的L 细胞分泌,在维持机体血糖稳态中起到双向调节的作用:在高血糖状态下,GLP-1 与胰岛β 细胞特异性受体结合后,使细胞内环磷酸腺(cAMP)合成增加,通过Ca2+内流刺激胰岛素分泌,同时还可有效抑制胰高血糖素的分泌。而当机体血糖降低时,GLP-1 对血糖的抑制作用消失,可减少低血糖风险。此外因其受体广泛分布于胰腺外、肝脏、肾脏、中枢神经系统等多个部位,GLP-1还有增加肌肉和脂肪组织葡萄糖摄取,抑制肝脏葡萄糖的生成,促进胰岛β 细胞复制和再生,并抑制其凋亡,抑制胃排空及食欲、心血管保护等作用[8-11]。而研究[12]发现在2型糖尿病患者中,GLP-1的分泌存在明显缺陷,且肥胖2 型糖尿病患者GLP-1水平低于正常体质量患者。因此,本研究在肥胖的T2DM 患者中使用长效GLP-1 受体激动剂PEX168联合二甲双胍治疗,结果发现,12 周后两组患者的FBG、PBG、HbA1c 均较基线水平下降,在对照组基础上增加PEX168 治疗可以使HbA1c 在终点时下降幅度达1.6%,HbA1c <7%比例占36.8%,这与GAO 等[13]研究结果一致。良好的血糖控制,灵活的注射方式及较长时间的用药间隔使得患者依从性大大增加,可以进一步提高血糖达标率。此外,治疗组患者BMI 较对照组明显下降,经12 周治疗后平均减重约3.3 kg,提示PEX168 在肥胖的2 型患者中有良好的降糖及减重效果。在GAO 等[13-14]研究中显示,不同剂量PEX168 联合二甲双胍治疗后患者血脂、血压等指标较对照组比无明显改善,但本研究发现治疗组12 周后血脂、血压水平较对治疗前显著降低,且上述指标较对照组改善明显。提示PEX168 可有效调节肥胖糖尿病患者的血脂谱,对血压也具有一定调控作用。上述结果的不一致性可能与入组人群BMI 不同有关,本试验入组患者BMI 为24.0 ~32.0 kg/m2,而在GAO 等相关研究中入组患者BMI 跨度较大(20.0 ~40.0 kg/m2),此外该研究的主要终点是HbA1c 从基线到24 周的变化。由于整个研究的设计都集中在这一主要终点上,因此可能不利于观察洛塞那肽对体质量的影响。陶娅等[15]研究发现GLP-1 受体激动剂利拉鲁肽可以明显改善糖尿病患者肾脏功能,本研究发现使用PEX168 治疗12 周后,eGFR治疗较治疗前明显升高,与陶娅等研究结果一致,提示PEX168 有肾脏保护作用。其可能机制除了血糖、血压、体质量的良好控制外,还可能通过保护血管内皮、抑制缩血管因子释放、血小板活化等途径减轻糖尿病肾病患者的微血管并发症[16-18]。同时其对RASS 系统的影响以及抑制促炎信号通路和活性氧的形成对于糖尿病肾病改善亦起到一定作用[19]。本研究中,两组患者的HOMA-IR 均较前改善,且治疗组明显优于对照组,虽经12 周治疗后两组患者HOMA-β 差异无统计学意义,但均较基线水平有所改善,提示PEX168能够调节胰岛素分泌和改善胰岛素抵抗。此外,超重、肥胖可引起高尿酸血症[20],而糖尿病患者多数合并尿酸代谢障碍,高尿酸血症是胰岛素抵抗的独立危险因素,而胰岛素抵抗通过调节尿酸代谢相关蛋白来增加尿酸重吸收,减少尿酸排泄[21]。目前的降糖药物绝大部分只是针对性的降糖,而对尿酸无明显改善。本研究发现治疗组在12 周后尿酸水平较用药前明显下降,且降尿酸效果优于对照组,这可能与用药后脂联素水平升高及GLP-1 改善肾小球系膜增生、减少足细胞损伤等作用相关[22-24]。
关于GLP-1 受体激动剂,最常见不良反应为胃肠道反应,另外亦可能使急性胰腺炎发生风险增加,但较为少见[25]。有研究[26]显示GLP-1 受体激动剂胃肠道反应多为轻、中度,可自行缓解。本研究发现两组中均有部分患者在用药初期出现恶心、腹泻等症状,但两组不良反应发生率无差异,均未经特殊处理自行缓解,且在治疗过程中无低血糖、胰腺炎等事件发生,提示PEX168 在治疗糖尿病患者中有较好的耐受性。
综上所述,PEX168 联合二甲双胍在肥胖的T2DM 患者中,除了有可靠的降糖疗效外,还能够改善胰岛β 细胞功能,调节血脂、血压、减轻体质量,具有心血管及肾脏获益,且无明显不良反应,具有良好的安全性和耐受性。但本研究存在不足之处在于观察时间较短,且样本量小,缺乏对不同BMI 人群的分层分析,因此在下一步的工作中将会扩大样本,延长观察时间,同时对不同BMI 人群进行分层研究,争取获得更多的关于GLP-1 受体激动剂在糖尿病患者中的临床证据。
【Author contributions】ZHOU Yingni and SHI Min analyzed the data and contributed to the article,which was revised by LAI Jingbo and LI Xiaomiao. LIU Xiangyang designed the study and reviewed the paper. All authors read and approved the final manuscript submitted.
