基于LC-MS/MS和比较基因组学技术解析海洋源解淀粉芽孢杆菌CMT-9产抗菌脂肽的分子机理
2023-02-21花梅芳李东迅邓旗孙力军钟赛意廖建萌
花梅芳,李东迅,邓旗*,孙力军*,钟赛意,廖建萌
1(广东海洋大学 食品科技学院,广东省水产品加工与安全重点实验室,广东省海洋食品工程技术研究中心,广东省海洋生物制品工程实验室,水产品深加工广东普通高等学校重点实验室,广东 湛江,524088) 2(海洋食品精深加工关键技术省部共建协同创新中心(大连工业大学),辽宁 大连,116034) 3(湛江市食品药品检验所,广东 湛江,524022)
抗菌脂肽是芽孢杆菌中的非核糖体多肽合成酶催化合成的小分子脂肽,主要包括表面活性素(surfactin)、伊枯草菌素(iturin)和芬荠素(fengycin)3大家族化合物[1-2]。抗菌脂肽抗菌谱广,对大多数细菌和真菌都有抑制作用,且具有绿色、高效、低毒、无污染等优点[3-5]。因此,在食品、医药、农业等领域具有广泛的发展前景[6-9]。
芽孢杆菌种类繁多,枯草芽孢杆菌、解淀粉芽孢杆菌和贝莱斯芽孢杆菌等均能产生抗菌脂肽[10-12]。不同芽孢杆菌的脂肽谱有所差异,主要与其合成酶及关键基因的数量和结构相关[13-14]。DENG等[15]对B.velezensisCMT-6进行高通量测序发现,合成酶基因srfA、ituA、fenA的完整性分别是菌株合成脂肽(surfactin、iturin和fengycin)的前提条件,而核心基因发生的InDels和SNP情况是造成脂肽种类和产量差异的主要原因。此外,脂肽是由前体物质氨基酸残基和脂肪酸链组成的大环内酯类物质[16-17],但目前关于前体物质合成途径中功能基因和代谢通路中关键基因的表达情况及其对脂肽谱的影响鲜有报道。
本课题组从海洋红树林生境中筛选到一株芽孢杆菌B.amyloliquefaciensCMT-9,该菌株具有生长速度快、营养需求简单且抗逆性强、抗菌谱广泛等特点,展现出良好的应用潜力。为探明海洋源CMT-9产脂肽的组分及其分子机理,本研究拟以高效液相色谱串联质谱(liquid chromatography tandem mass spectrometry,LC-MS/MS)技术鉴定CMT-9的发酵液组分,采用全基因组测序技术探明CMT-9基因组中合成脂肽的代谢通路和关键基因,同时通过比较基因组学分析其与不同种属的陆地源芽孢杆菌B.velezensisCMT-6(可合成surfactin、iturin和fengycin)、B.velezensisFZB42(可合成surfactin、fengycin)、B.amyloliquefaciensDSM7T(可合成surfactin、iturin)和B.subtilis168(无脂肽合成能力)之间的脂肽谱差异性,为解析CMT-9产脂肽的调控机制和指导其实际生产提供理论参考。
1 材料与方法
1.1 实验材料
1.1.1 实验菌株
BacillusamyloliquefaciensCMT-9,广东海洋大学食品科技学院水产品绿色控制实验室保藏。
1.1.2 培养基
改良Landy培养基(g/L):葡萄糖20.0,L-谷氨酸氢钠5.0,MgSO4·7H2O 0.5,KCl 0.5,KH2PO4·3H2O 1.0,FeSO4·7H2O 0.001 5,MnSO·5H2O 0.05,CuSO4·5H2O 0.001 6,pH 7.0。
LB培养基(g/L):蛋白胨10.0,酵母粉5.0,NaCl 5.0,pH 7.0。
1.2 仪器与设备
HHS恒温水浴锅、SPX-250B-Z生化培养箱,上海博迅实业有限公司;PHS-3E型pH计,上海雷磁仪器有限公司;DC-12H氮吹仪,上海安谱科学仪器有限公司;Invitrogen Qubit 4荧光定量仪,美国赛默飞世尔公司。
1.3 实验方法
1.3.1 脂肽发酵条件
挑取菌株CMT-9在50 mL LB培养基中37 ℃、150 r/min培养14 h进行活化复壮。按体积分数为5%的接种量加入100 mL改良Landy培养基中,30 ℃、160 r/min发酵培养36 h。
1.3.2 脂肽组分检测
将发酵液置于4 ℃,8 000 r/min离心30 min,获得上清液。加入甲酸调节pH至2.0,静置沉淀8 h。8 000 r/min、4 ℃离心20 min,向沉淀物加入少量的无菌水,用氨水调pH至7.0,甲醇萃取2~6 h,然后10 000 r/min、4 ℃离心20 min,取上清液。同样步骤萃取2次,合并上清液并经旋转蒸发仪浓缩至近干,加入无菌水稀释,用无菌0.22 μm滤膜过滤。采用LC-MS/MS技术测定发酵液主要成分,参照DENG等[18]进行参数设置。
1.3.3 RNA提取和检测
采用DNeasy plantMini kit试剂盒提取CMT-9的基因组RNA,通过1%琼脂糖凝胶电泳检测技术和荧光定量仪检测样品基因组RNA的完整性、总量和浓度。
1.3.4 基因组测序与基因功能注释
将合格的RNA样品送到深圳华大基因研究院进行富集纯化、反转录文库的构建及测序。将通过高通量测序获得的每个样品的转录组文库转化为原始测序序列数据,对其进行CASAVA碱基序列鉴定分析。通过软件HTseq(版本:0.12.4)来处理高通量测序所产生的数据,将这些reads高效、准确地比对到基因上去,使不同基因、不同实验间估计的基因表达水平具有可比性。用DESeq 2R软件分析和比较差异表达基因。采用Benjamini & Hochberg方法调整P值,将P<0.05和∣log2fold change∣≥2设置为差异表达基因。利用GO数据库(http://geneontology.org/)和KEGG数据库(https://www.kegg.jp/kegg/pathway.html)分别对差异表达基因进行分析;利用COG数据库(https://www.ncbi.nlm.nih.gov/research/cog-project/)、CAZy数据库(http://www.cazy.org/)分别对差异表达基因的代谢途径、碳水化合物酶类进行注释。
1.3.5 比较基因组学分析
将B.amyloliquefaciensCMT-9与B.velezensisCMT-6、B.amyloliquefaciensDSM7T、B.velezensisFZB42和B.subtilis168进行比较基因组学分析。
2 结果与分析
2.1 CMT-9发酵产物的LC-MS/MS分析
CMT-9发酵产物的LC-MS/MS离子流图如图1所示。
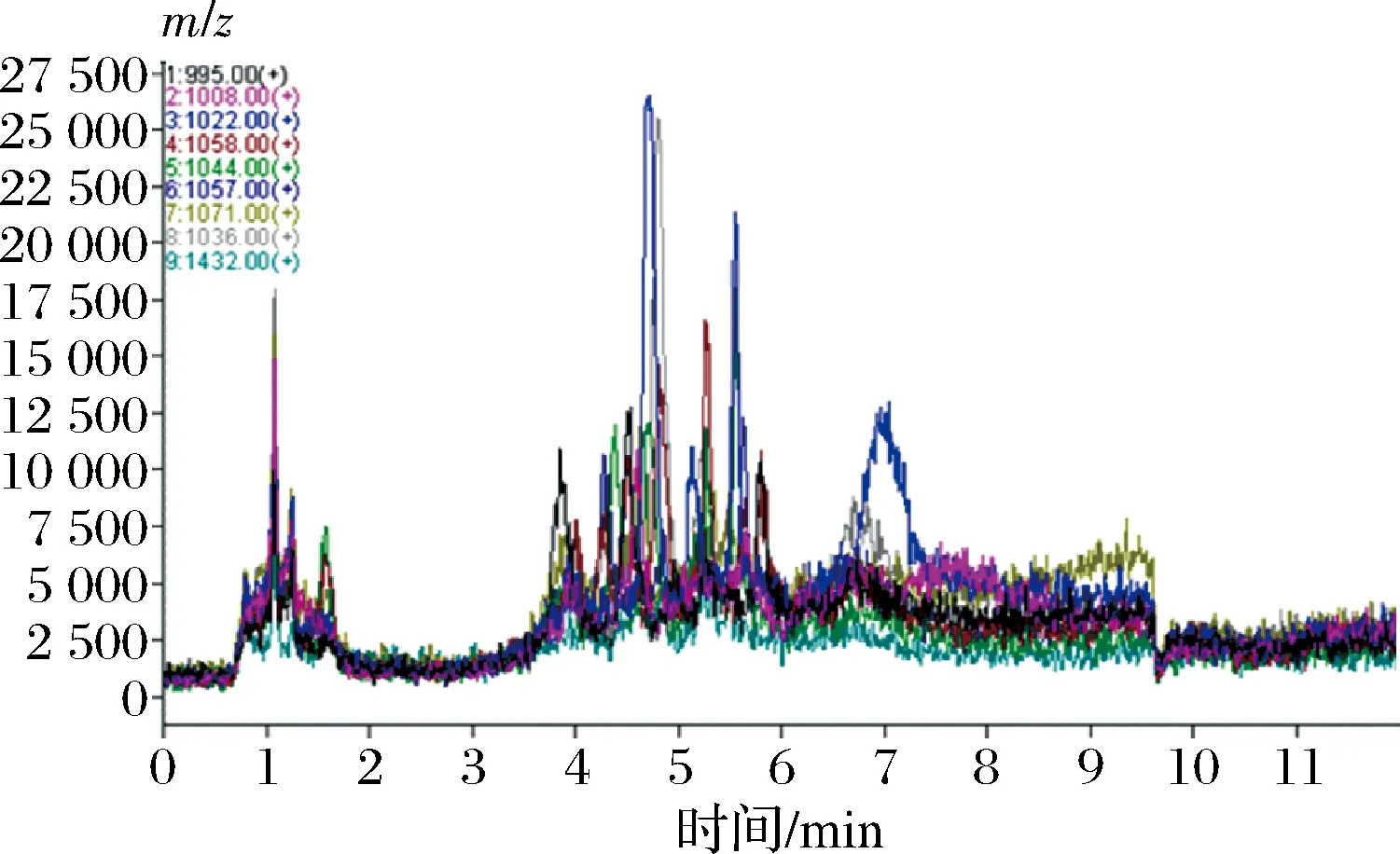
图1 CMT-9发酵产物的总离子流色谱图Fig.1 Total ion chromatogram of CMT-9 fermentation products
CMT-9菌株发酵产物的主要质荷比为995、1 008、1 022、1 058、1 044、1 057、1 071、1 036、1 432,共9种组分。这些组分的质荷比与文献报道的在相同发酵工艺和纯化条件下检测到的surfactin(m/z为995、1 008、1 022、1 036、1 058、1 044)和iturin(m/z为1 057、1 071)的分子质量相一致[18]。由此初步判定CMT-9菌株所产生的抗菌物质为surfactin和iturin[18]。此外,邓旗等[19]研究发现fengycin A的质荷比在1 431~1 492,由此推测质荷比为1 432的组分可能是fengycin A的一种。
2.2 CMT-9差异表达基因的功能富集分析
由图2可得,将菌株CMT-9的基因序列与GO数据库进行比对共注释到9 763个基因,其中与分子功能相关的基因数量为4 617个,主要富集在催化活性(catalytical activity),转运能力(transport activity);与细胞组成相关的基因数量为2 189个,主要富集在高分子聚乳酸(macromolecular complex);与生物过程相关的基因数量为2 957个,主要富集在代谢过程(metabolic process),细胞过程(cellular process),生物调节(biological regulation)。
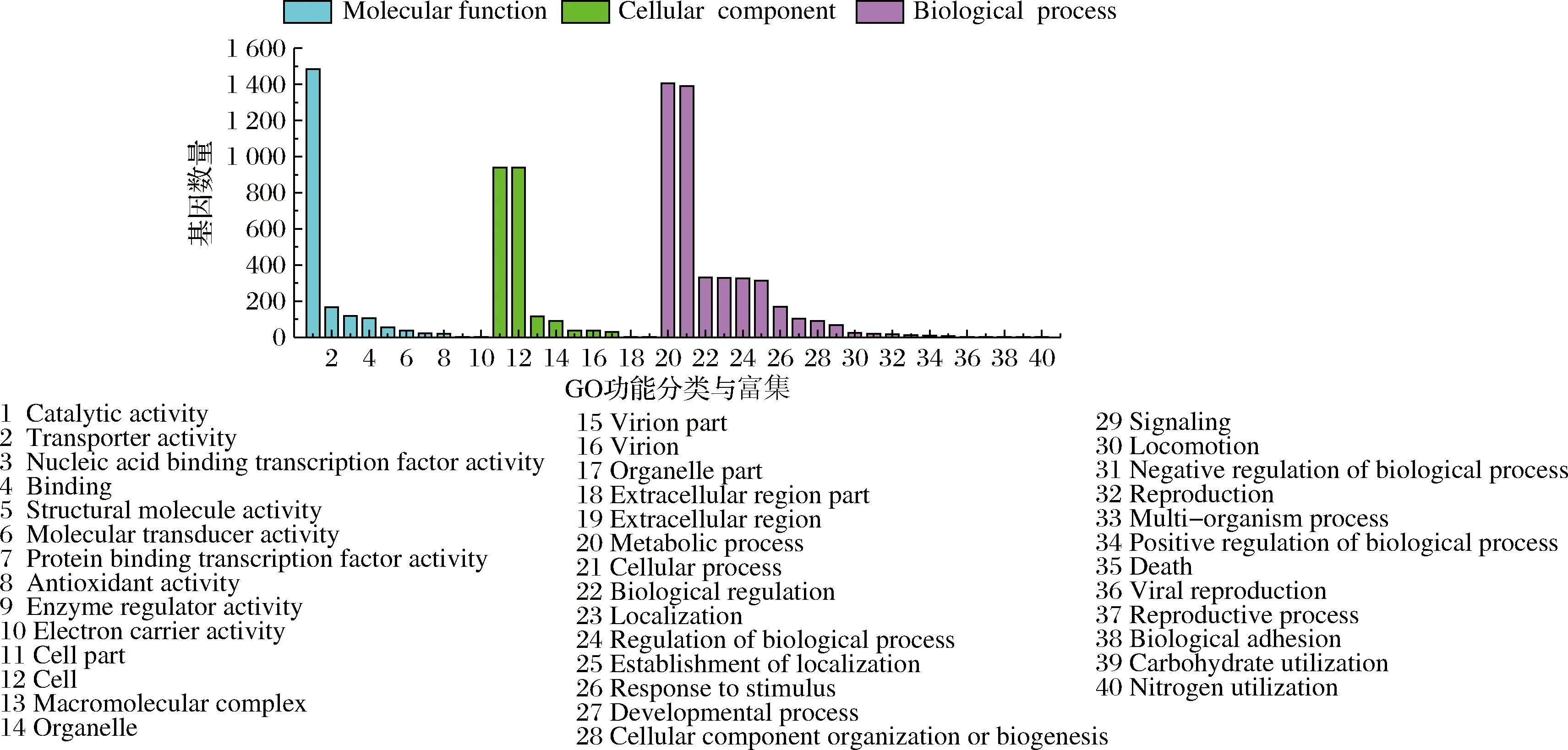
图2 CMT-9差异基因的GO功能分类与富集Fig.2 GO functional classification and enrichment of CMT-9 differential genes
由图3可得,KEGG分析表明CMT-9发酵培养后的差异基因在代谢(metabolism)、环境信息过程(environmental information processing)和基因信息过程(genetic information processing)通路显著富集,其中最丰富的路径为代谢过程中的碳水化合物代谢(carbohydrate metabolism)和氨基酸代谢(amino acid metabolism),它们的差异基因个数分别为506和411。
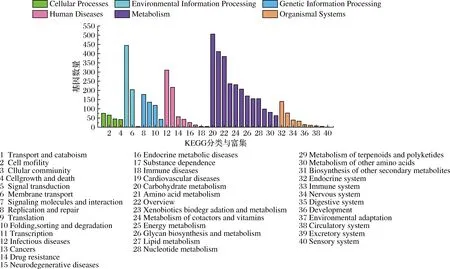
图3 CMT-9差异基因的KEGG通路分类与富集Fig.3 KEGG pathway classification and enrichment of CMT-9 differential genes
由图4可得,通过COG功能分析发现差异基因主要富集在一般功能预测(general function prediction only)、氨基酸运输与代谢(amino acid transport and metabolism)、碳水化合物运输与代谢(carbohydrate transport and metabolism)。其中,参与氨基酸运输与代谢(amino acid transport and metabolism)的基因个数为333个;参与碳水化合物运输与代谢(carbohydrate transport and metabolism)的基因个数为230个;参与次级代谢物的生物合成、转运和分解代谢(secondary metabolites biosynthesis, transport and catabolism)的基因个数为97个。

图4 CMT-9差异基因的COG功能分类与富集Fig.4 COG functional classification and enrichment of CMT-9 differential genes
2.3 CMT-9碳水化合物活性酶(carbohydrate-active enzymes,CAZymes)分析
碳水化合物活性酶主要由5类催化酶和一类非催化模块组成,催化酶包括糖苷水解酶(glycoside hydrolases, GHs)、多糖裂解酶(polysaccharidelyases, PLs)、碳水化合物酯酶(carbohydrate esterases, CEs)、糖基转移酶(glycosyltransferases, GTs)以及辅助氧化还原酶(auxiliary activities, AAs),非催化模块即碳水化合物结合模块(carbohydrate-binding modules, CBMs)[20]。由图5可得,菌株CMT-9中含有138个碳水化合物活性酶,其中尤以GH最多,数量为46个,所占比例为33.33%;其次是GT,数量为36,所占比例为26.09%,CBM、CE、AA、PL的数量分别为31、17、5、3,所占比例分别为22.46%、12.32%、3.62%、2.17%。

图5 CMT-9碳水化合物活性酶(CAZymes)的分布情况Fig.5 Distribution of CMT-9 CAZymes
2.4 基因组组分分析
由表1可知,CMT-9的基因组大小为3 928 149 bp,G+C含量为46.39%,蛋白质编码序列长度为4 080,tRNA的数量为83,rRNA的数量为9。CMT-9的基因组大小、G+C含量与CMT-6、FZB42和DSM7T的相似度较高;蛋白质编码序列长度与CMT-6相似度较高;tRNA的数量与CMT-6、FZB42和168的相似度较高。因此,CMT-9与4株菌株的基因组组分的相似度从高到低依次为CMT-6、FZB42、DSM7T、168。
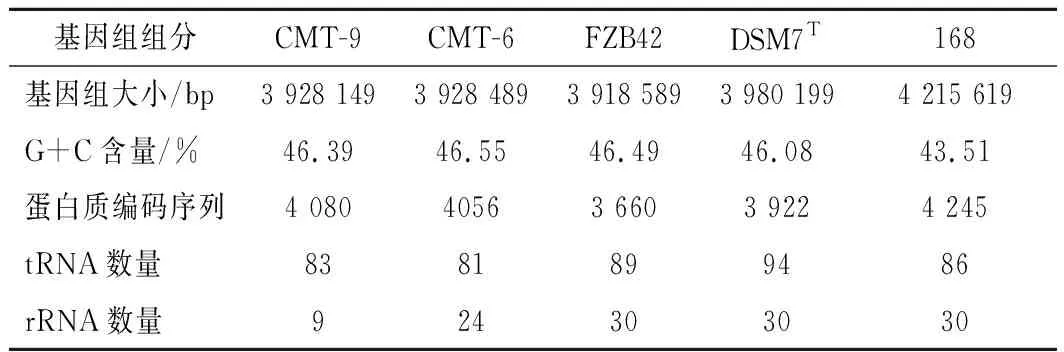
表1 基因组组分比较Table 1 Genome component comparison
2.5 共线性分析
2个物种之间的共线性关系可以作为衡量物种之间进化距离的尺度,进而判断其亲缘关系[21]。由图6可知,CMT-9与CMT-6、FZB42均表现出高度的共线性;与DSM7T的共线性较差,在1~1.75 Mb片段出现较明显的缺失和易位;与168的共线性最差,存在显著的插入、易位、倒位和等基因重排现象,在1.3~1.4、1.85~1.95和2.65~2.8 Mb片段最为明显。
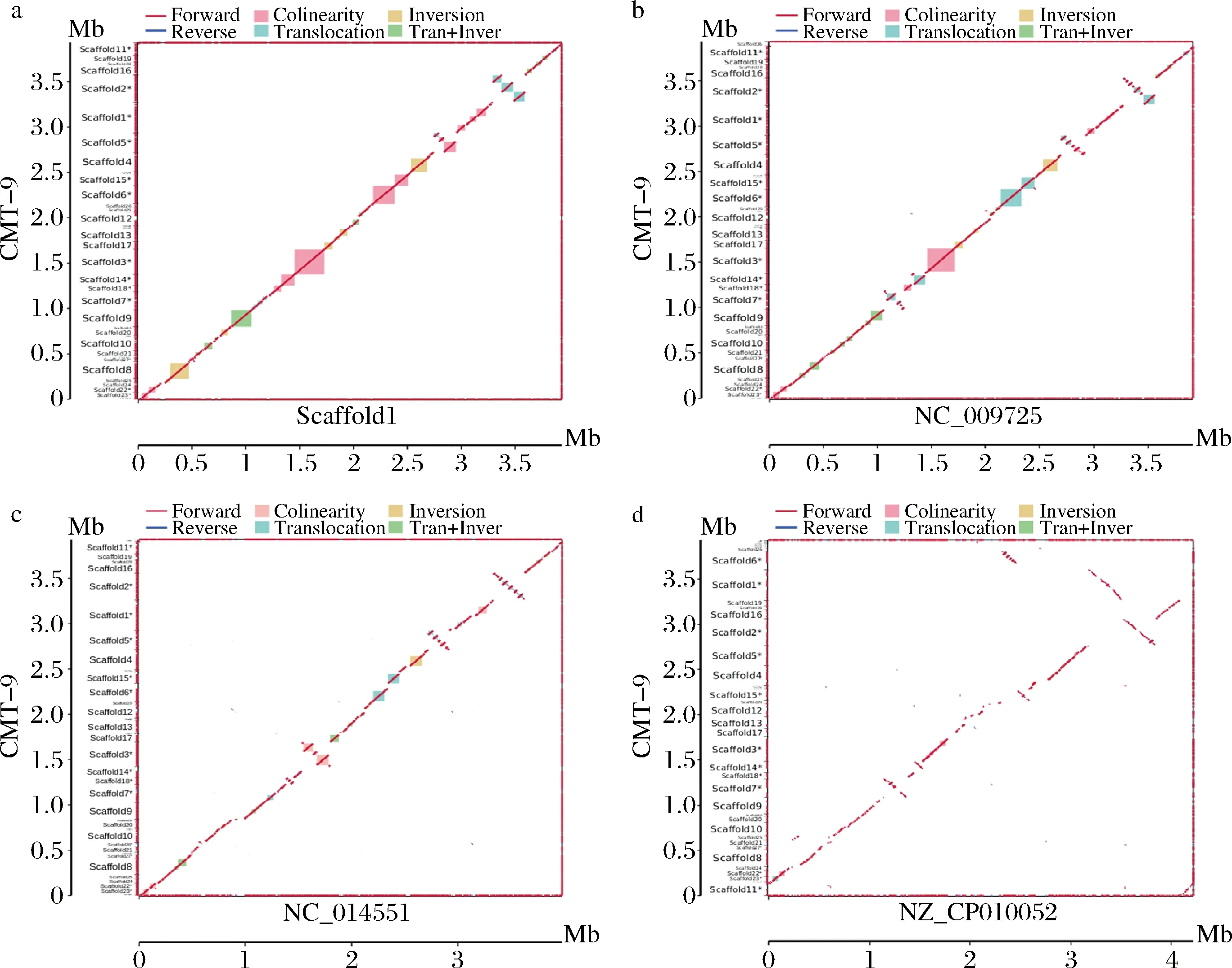
a-CMT-6;b-FZB42;c-DSM7T;d-168图6 全基因组二维共线性比较Fig.6 Two-dimensional collinearity comparison of genomes
2.6 同源性分析
将CMT-9的Reads比对到4株芽孢杆菌的基因组序列上,其中与CMT-6的覆盖率最高,覆盖区域总长度为3 724 736 bp,占CMT-6基因组的94.81%;其次是FZB42,覆盖区域总长度为3 918 589 bp,占FZB42基因组的90.68%;而CMT-9与DSM7T、168的覆盖率较低,覆盖区域总长度分别为2 036 571、104 859 bp,各占其基因组的51.17%和2.49%(表2)。
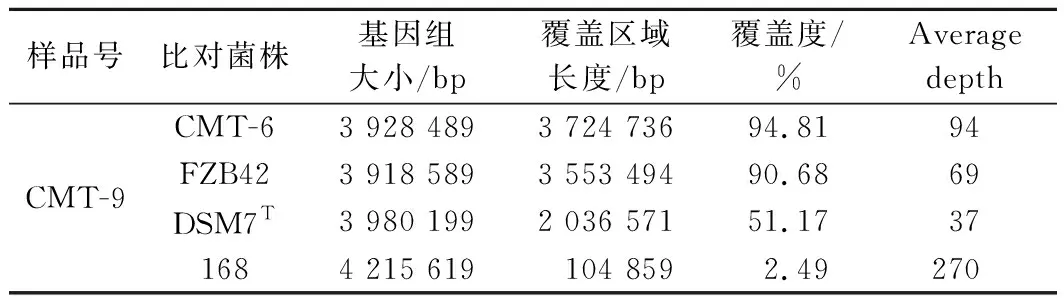
表2 测序长度和覆盖度比较Table 2 Comparison of sequencing length and coincidence
同时,将菌株CMT-9与CMT-6、168、DSM7T、FZB42基因组的蛋白序列进行比较,构建基因组间的Core-Pan基因集。将5株菌株的基因进行同源性分析,5株菌株的共有基因为2 675个,CMT-9与CMT-6的共有基因数量最多(3 545个),与FZB42、DSM7T、168的共有基因数量分别为3 166、3 090、2 882(图7)。
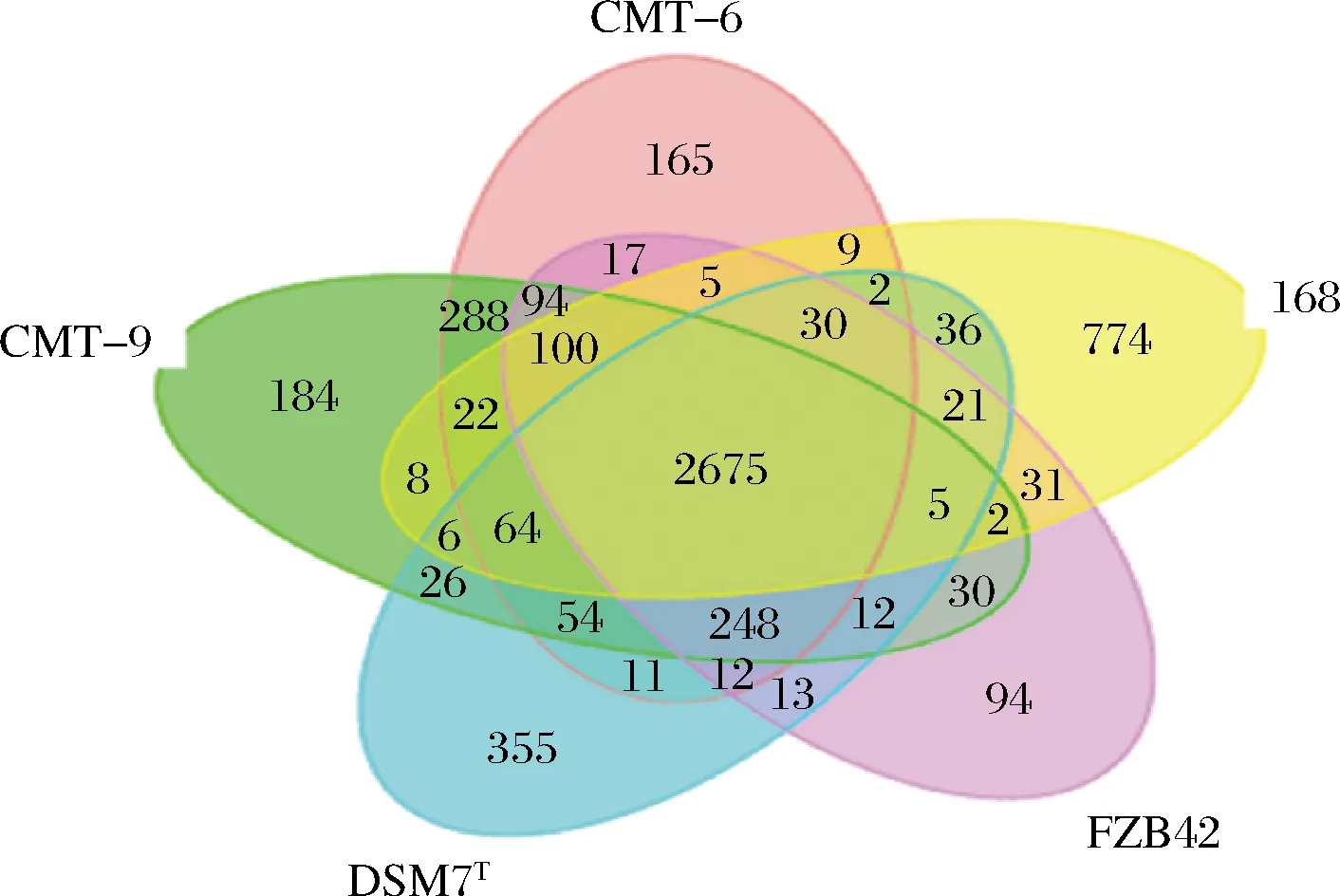
图7 基因组的Core-Pan基因数目维恩图Fig.7 Venn diagram of the number of Core-Pan genes in the genome
3 结论
本研究采用LC-MS/MS方法检测菌株CMT-9的发酵产物组分,发现其质荷比与张宁等[22]的研究中的surfactin和iturin相一致,说明CMT-9可以发酵产生抗菌脂肽。同时还检测到一个质荷比为1 432的组分,该值在fengycin质荷比(1 431~1 492)范围内,因此推测其可能为fengycin[23],但具体结构仍需进一步的探索和验证。
全基因组测序技术可从基因层面挖掘活性菌株次级代谢产物的合成潜力。本研究对菌株CMT-9进行全基因组测序和通路分析,发现其差异表达基因主要富集在碳水化合物代谢、氨基酸代谢通路。碳水化合物代谢过程中产生的丙酮酸会影响乙酰CoA的合成,乙酰CoA可进一步合成脂肪酸[24-25]。因此,这2条通路可为脂肽的合成提供脂肪酸和氨基酸等重要前体物质,前体物质的含量是菌株高效合成脂肽的关键。WU等[26]研究发现添加复合氨基酸可显著提高解淀粉芽胞杆菌Ba-BPD1的iturin产量。LU等[27]研究碳水化合物对解淀粉芽胞杆菌合成抗菌脂肽的影响,发现果糖通过提升氨基酸的浓度,进而增加抗菌脂肽相关合成酶基因的表达,最终提高抗菌脂肽的产量。因此,脂肽前体物质合成通路中基因的数量和表达水平与脂肽产量呈正相关性。
前期研究发现,菌株CMT-6具备合成surfactin、iturin和fengycin 3大类脂肽的合成酶基因,且数量较多,可合成高水平的抗菌脂肽[15]。根据已公布的CMT-6菌株的全基因组序列,通过比较基因组学发现CMT-9与CMT-6菌株的基因组大小、G+C含量、蛋白质编码序列和tRNA数量均表现高度的一致性。此外,在共线性分析中,发现菌株CMT-9与CMT-6具有高度共线性,与FZB42、DSM7T和168相比存在不同程度的差异,甚至出现线性缺失现象。同源性分析中CMT-9与CMT-6菌株的同源性较FZB42、DSM7T、168最高,达到94.81%。因此,芽孢杆菌基因组组分、共线性和同源性决定了其脂肽谱的相似度。
本研究采用LC-MS/MS技术发现CMT-9的发酵液中含有surfactin、iturin和fengycin 3种脂肽组分,进一步的全基因组测序和比较基因组学分析发现,前体物质合成基因数量与脂肽产量密切相关,基因组组分、共线性和同源性的差异是脂肽谱多样化的重要原因。研究结果为脂肽产生菌的筛选及脂肽定向合成工程菌株的改造提供理论依据。
