乌骨鸡中沙拉沙星残留消除规律研究
2023-02-18静岳琴李丽徐俊胡易容冯波李云赵立军
张 静岳 琴李 丽徐 俊胡易容冯 波李 云赵立军
(1.农业农村部畜禽产品质量安全风险评估实验室(成都),成都 610041;2.江西省农业科学院农产品质量安全与标准研究所,南昌 330200;3.乐山市饲草饲料工作站;四川乐山 614000)
乌骨鸡,又称乌鸡、绒毛鸡、泰和鸡、黑脚鸡等,属雉科动物,为我国特有的地方鸡种,其以乌皮、乌肉、乌骨而著称。现代医学研究表明,乌骨鸡的药用价值主要在于其体内的黑色素物质,有滋阴益气、强身健体、抗衰老等功效和作用[1~2]。因此,乌骨鸡成为消费者非常喜欢的药食两用食物,同时乌骨鸡产业也成为了我国乡村振兴和精准扶贫的重要产业之一。然而,乌骨鸡产品中抗菌药物残留超标情况时有发生,国家市场监督管理总局2018-2019年共发布了63批次食品不合格情况的通告,涉及鸡肉的为19批次,其中乌骨鸡肉11批次,占鸡肉通告的58%;氟喹诺酮类药物残留超标导致乌骨鸡肉不合格的为5批次,占乌骨鸡肉不合格总数的45%。
氟喹诺酮类药物属化学合成广谱抗菌药,是禽病防治中的常用药物,滥用或不合理使用会使其在动物体内残留,引发食品安全和耐药性等问题,严重威胁消费者健康[3]。目前,我国肉鸡养殖过程中执行的休药期多以白羽肉鸡为对象获得,不适合乌骨鸡生产情况。氟喹诺酮类药物在乌骨鸡中代谢、消除与其他品种有所不同,其在乌骨鸡中的半衰期要比在其他种类鸡中时间要长[4]。因未设定合理的抗菌药物休药期带来的乌骨鸡产品质量安全问题,已成为影响乌骨鸡产业健康发展的重要阻碍。
经资料调研和实地考察,选取四川特优品种山地乌骨鸡为试验对象,开展氟喹诺酮类药物残留相关研究试验。GB 31650—2019《食品安全国家标准 食品中兽药最大残留限量》规定了沙拉沙星在家禽产蛋期禁用,在家禽肌肉中的最大残留限量(MRL)为10μg/kg,在脂肪中的MRL为20μg/kg,在肝脏和肾脏中的残留量不得超过80μg/kg[5]。本研究以沙拉沙星为对象,力求探明其在乌骨鸡体内的残留消除规律,为其在乌骨鸡养殖中的安全使用和合理休药期制定提供科学依据,为行业监管和相关标准制修订提供技术支撑。
一、材料和方法
(一)试剂与仪器盐酸沙拉沙星片:10 mg/片、80 mg/片,由四川省畜牧科学研究院兽药研究所提供。标准品:盐酸沙拉沙星(北京曼哈格生物科技有限公司)。内标:D8-盐酸沙拉沙星(德国Witega Laboratorien Berlin-Adlershof GmbH公司)。乙腈、甲醇为色谱纯[西格玛奥德里奇(上海)贸易有限公司]。
液相色谱-质谱联用仪(1290/6460,美国Agilent公司)。
(二)饲喂试验设计选取320日龄、体重1.9±0.2 kg四川山地乌骨鸡(四川省乐山市沐川县黑凤凰乌骨鸡业有限公司提供)300只,分为空白组(60只)和实验组(240只),实验组按每日给药剂量5、10、40、80 mg/kg bw分为A、B、C、D 4组,其中A、B为正常治疗剂量组,C、D为超治疗剂量组,每组60只。采用不含任何抗生素的基础日粮预饲5 d后进入正饲期,正饲期共计10 d(给药期5 d、休药期5 d)。给药方式为片剂灌喂,每日给药1次,连续给药5 d。自由饮水,试验期均饲喂不含抗生素的基础日粮。
(三)样品采集分别在休药后第2、4、6、8、12、48 h进行采样,每个时间点屠宰10只鸡,采集肌肉、肝脏、皮脂,置于-20℃条件下保存备用。并于休药后第4、5 d采集鸡蛋,休药后第5 d采集血液。
(四)测定方法
1.提取。(1)肌肉、肝脏、皮脂、血液:称取均质试样2.0 g,置于50 mL聚丙烯离心管中,加入150 ng/mL D8-沙拉沙星内标溶液100μL,加入20 mL 0.1 mol/L EDTA-Mcllvaine缓冲液,振荡提取10 min,超声提取10 min,以10 000 r/min低温离心5 min,提取2次,合并上清液,用滤纸过滤,备用。(2)鸡蛋:称取均质试样2.0 g,置于50 mL聚丙烯离心管中,加入150 ng/mL D8-沙拉沙星内标溶液100μL,加入30 mL 0.1 mol/L EDTAMcllvaine缓冲液,振荡提取10 min,超声提取10 min,以10 000 r/min低温离心5 min,量取15 mL上清液,用0.1 mol/L EDTA-Mcllvaine缓冲液稀释1倍,用滤纸过滤,备用。
2.净化。HLB固相萃取柱(200 mg,6 mL),使用时用6 mL甲醇、6 mL水活化。将提取的滤液以2~3 mL/min的速度过柱,弃去滤液,用2 mL 5%甲醇水溶液淋洗,将小柱抽干,再用6 mL甲醇洗脱并收集洗脱液。洗脱液用40℃氮气吹干,用1 mL 0.2%甲酸水溶液复溶,过0.22μm微孔滤膜后上机测定。
3.液相色谱-串联质谱条件。(1)色谱条件:Agilent Eclipse Plus C18柱 (50 mm×3.0 mm,1.8 μm);流动相为乙腈(A相)-0.2%甲酸水溶液(B相);柱温为30℃;流速为0.3 mL/min;进样体积为5μL。液相色谱梯度洗脱程序为0~1.00 min,90%B;1.01~3.00 min,90%B→10%B;3.01~5.00 min,10%B;5.01~7.00 min,10%B→90%B。(2)质谱条件:离子源为电喷雾离子源(ESI);正离子扫描;检测方式为多反应监测(MRM);雾化气、辅助加热气、碰撞气为高纯氮气;雾化气温度为300℃。沙拉沙星定性定量离子对(m/z)为386.1/299.1、386.1/368.1,D8-沙拉沙星定量离子对(m/z)为394.0/375.9。
二、结果与分析
(一)方法学验证 目前,对动物体内氟喹诺酮类药物残留的检测方法主要有免疫学检测方法[6]、高效液相色 谱法[7~9]、 液相 色 谱-质谱法[10~12]等。本研究在参考GB/T 21312-2007《动物源性食品中14种喹诺酮药物残留检测方法 液相色谱-质谱/质谱法》[13]的基础上,建立了检测乌骨鸡组织(肌肉、肝脏、皮脂、血液)和鸡蛋中沙拉沙星残留的液相色谱-串联质谱法。本法采用同位素内标法测定,有效消除了质谱基质效应,定量更准确。
1.线性范围、检出限和定量限。精密称取适量盐酸沙拉沙星标准品,用甲醇配制成浓度为1 mg/mL的沙拉沙星储备液,再逐级稀释成浓度分别为5、25、50、100、200、500 ng/mL的沙拉沙星标准系列工作液(含内标溶液15 ng/mL),供液相色谱-串联质谱测定。以沙拉沙星定量离子峰面积与内标峰面积之比为纵坐标,样品浓度为横坐标作标准曲线,结果见图1。结果表明,沙拉沙星标准工作液在5~500 ng/mL浓度范围内呈良好的线性关系。
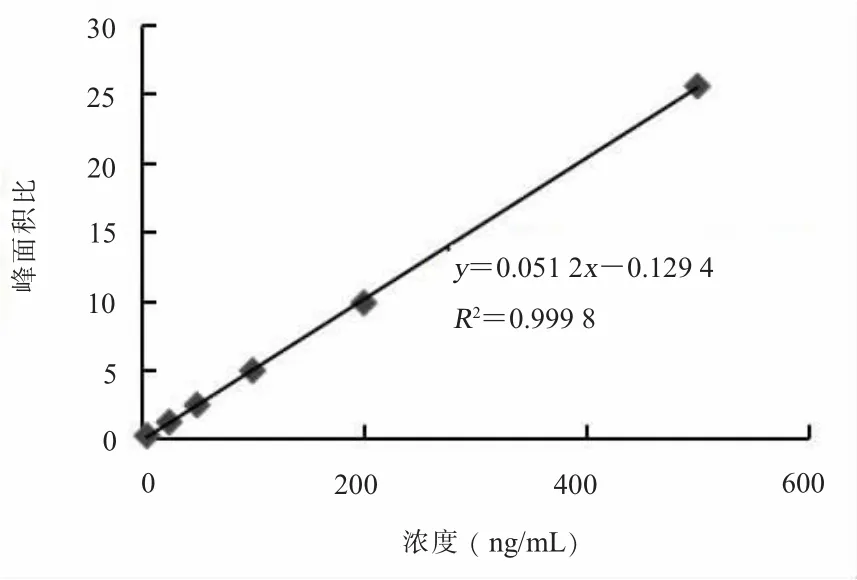
图1 沙拉沙星定量标准曲线
在空白基质中添加不同浓度的沙拉沙星标准溶液,经前处理、测定,根据信噪比(S/N)=3的峰响应值和样品前处理的稀释倍数,得出沙拉沙星在肌肉、肝脏、皮脂、血液的检出限(LOD)为1 μg/kg,在鸡蛋中的检出限为2μg/kg;根据信噪比(S/N)=10的峰响应值和样品前处理的稀释倍数,得出沙拉沙星在肌肉、肝脏、皮脂、血液的定量限(LOQ)为2.5μg/kg,在鸡蛋中的定量限为5μg/kg。
2.回收率及精密度试验。选取空白肌肉、肝脏、皮脂、血液样品在2.5、50、200μg/kg水平下进行加标回收试验;选取空白鸡蛋样品在5、100、500μg/kg水平下进行加标回收试验,每个添加浓度测定5个平行样品,结果见表1。结果显示,在空白肌肉、肝脏、皮脂、血液、鸡蛋样品中,沙拉沙星的平均回收率在82.9%~106.0%之间,相对标准偏差(RSD)小于10%。本方法准确度和精密度良好,符合实验室质量控制规范要求,适用于乌骨鸡各组织和鸡蛋中沙拉沙星的定性和定量检测。

表1 方法回收率和精密度试验结果 (n=5)
(二)沙拉沙星在乌骨鸡各组织和鸡蛋中的残留情况
1.沙拉沙星在乌骨鸡肌肉中的残留消除规律。由测定数据可知,各剂量组中沙拉沙星在肌肉中的残留量随休药时间的增加呈现出先升高再降低的规律,且均在休药后第4 h达到残留量峰值(见图2)。正常治疗剂量组(5、10 mg/kg bw),在休药后第48 h采集的肌肉中仍检出沙拉沙星,含量分别为17.3、39.8μg/kg;超治疗剂量组 (40、80 mg/kg bw),在休药后第48 h采集的肌肉中也检出沙拉沙星,含量更高,分别为72.0、161.5μg/kg。

图2 沙拉沙星在乌骨鸡肌肉中的残留消除规律
GB 31650-2019标准规定沙拉沙星在鸡(或火鸡)肌肉中的MRL为10μg/kg,此外最新《兽药质量标准》(2017年版)[14]中规定沙拉沙星的休药期为0 d。本研究数据证明了在乌骨鸡养殖中使用正常治疗剂量的沙拉沙星,在休药48 h后,肌肉中沙拉沙星残留量仍然超标,若超剂量使用,则残留量更高。
2.沙拉沙星在乌骨鸡肝脏中的残留消除规律。由测定数据可知,由于肝脏对药物的持续累积作用,各剂量组沙拉沙星在乌骨鸡肝脏中的残留量随休药时间的增加呈现出逐渐降低的规律,且残留量峰值均为休药后第2 h(见图3)。正常治疗剂量组(5、10 mg/kg bw)休药后第6 h采集的肝脏中能检出沙拉沙星,含量分别为103.8、188.1μg/kg,超过国家规定的MRL(80μg/kg);超治疗剂量组(40、80 mg/kg bw)休药后第12 h采集的肝脏中能检出沙拉沙星,含量分别为274.4、354.1μg/kg,超过国家规定的MRL(80μg/kg)。

图3 沙拉沙星在乌骨鸡肝脏中的残留消除规律
3.沙拉沙星在乌骨鸡皮脂中的残留消除规律。由测定数据可知,由于乌骨鸡皮脂对药物的持续累积作用,各剂量组沙拉沙星在皮脂中的残留量随休药时间的增加呈现出逐渐降低的规律,且均在休药后2 h达到残留峰值(见图4)。正常治疗剂量组(5、10 mg/kg bw)直到休药后第48 h,在皮脂中仍能检出沙拉沙星,且含量分别为23.8、51.2μg/kg,均高于GB 31650-2019标准规定的脂肪中沙拉沙星MRL(20μg/kg);超治疗剂量组 (40、80 mg/kg bw)在休药后第48 h采集的皮脂中也检出沙拉沙星,含量分别为125.7、356.0μg/kg,远远高于国家规定的MRL(20μg/kg)。
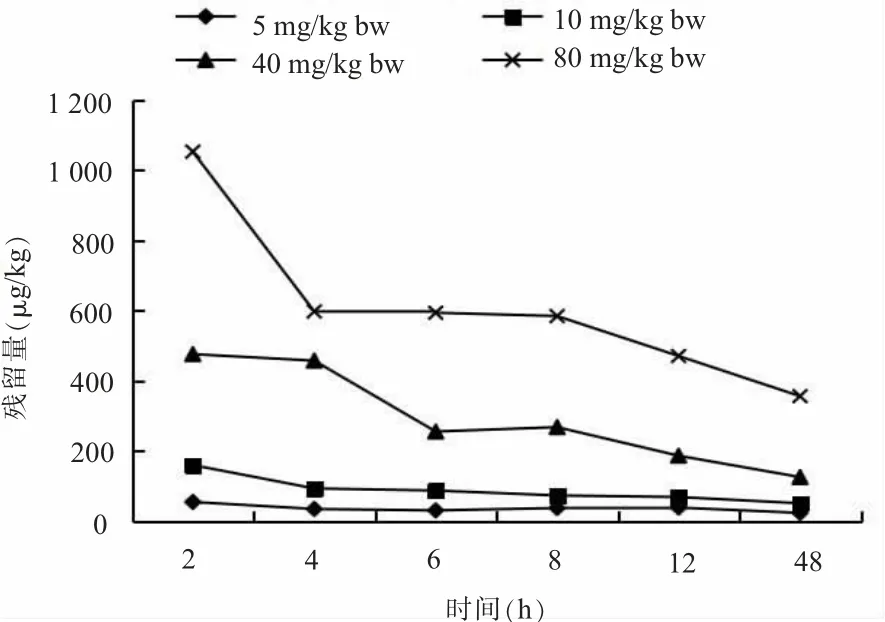
图4 沙拉沙星在乌骨鸡皮脂中的残留消除规律
4.沙拉沙星在乌骨鸡鸡蛋中的残留量。由测定数据可知,正常治疗剂量组(5、10 mg/kg bw)在休药后第5 d,在乌骨鸡鸡蛋中仍检出沙拉沙星,含量分别为21.3、40.3μg/kg,而超治疗剂量组(40、80 mg/kg bw)在休药后第5 d,检出鸡蛋中沙拉沙星的含量分别高达117.7、230.6μg/kg(见图5)。
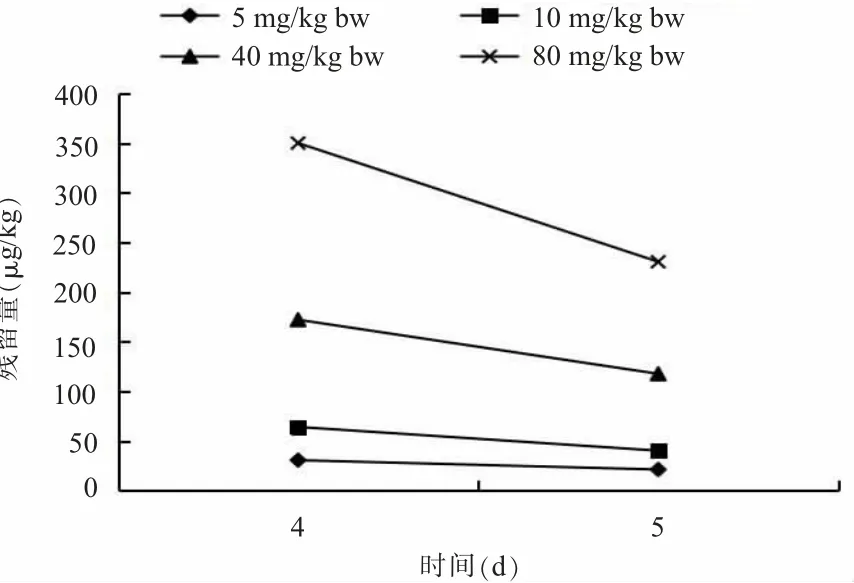
图5 沙拉沙星在乌骨鸡鸡蛋中的残留量
GB 31650-2019标准中规定产蛋鸡禁用沙拉沙星,即鸡蛋中不得检出沙拉沙星。按此规定,正常治疗剂量组和超治疗剂量组在使用沙拉沙星休药5 d后,仍在乌骨鸡鸡蛋中检出沙拉沙星,均属于不合格产品。
5.沙拉沙星在乌骨鸡血液中的残留量。由测定数据可知,正常治疗剂量组(5、10 mg/kg bw)直到休药后第5 d,在乌骨鸡血液中仍检出沙拉沙星,含量分别为3.3、8.5μg/kg,而超治疗剂量组(40、80 mg/kg bw)检出的沙拉沙星含量则分别高达20.8、22.5μg/kg。
三、结论及建议
(一)结论本研究建立了一种检测乌骨鸡组织(肌肉、肝脏、皮脂、血液)和鸡蛋中沙拉沙星残留的液相色谱-串联质谱法。该方法可最大程度消除基质效应,其检测限、定量限、准确度和精密度均满足动物源食品中低含量药物残留检测的要求。
基于所建立的方法开展了乌骨鸡摄入不同剂量(5、10、40、80 mg/kg bw)沙拉沙星后,各组织和鸡蛋中沙拉沙星残留水平和消除规律的研究。结果显示,乌骨鸡各组织部位中药物残留量水平不同,由高到低依次为肝脏、肌肉、皮脂。正常治疗剂量组(5、10 mg/kg bw)中,休药后第6 h采集的肝脏中仍能检出沙拉沙星,且超过国家规定的MRL(80μg/kg);休药后第48 h采集的肌肉和皮脂中仍能检出沙拉沙星,且含量均超过国家规定的MRL(10μg/kg和20μg/kg)。超治疗剂量组(40、80 mg/kg bw)中,在各个休药时间,沙拉沙星在肝脏、肌肉、皮脂中的残留量均远高于正常剂量组。休药后第5 d,在乌骨鸡鸡蛋中仍能检出沙拉沙星残留,不符合禽蛋质量安全要求;同时,在乌骨鸡血液中也能检出沙拉沙星残留,因对血液中沙拉沙星无残留限量要求,故无法作出判定。
同时,研究发现,各组织部位药物残留量达到峰值的时间和低于MRL的时间不同。在正常治疗剂量组和超治疗剂量组中,沙拉沙星在肌肉中的残留量随休药时间的增加呈先升高再降低的趋势,且各剂量组均在休药后第4 h达到残留量峰值。在正常治疗剂量组中,沙拉沙星在肝脏和皮脂中的残留量均随休药时间的增加呈逐渐降低的趋势,且各剂量组均在休药后第2 h达到残留量峰值。在休药12 h后,肝脏中沙拉沙星残留量才低于MRL,而在肌肉、皮脂中,即使休药时间达到48 h,残留量仍超过MRL。在超治疗剂量组中,沙拉沙星的残留消除趋势与正常治疗剂量组一致。
(二)建议从上述研究结果来看,乌骨鸡对沙拉沙星的消除代谢过程与普通品种鸡存在差异,因此提出3点建议。
1.乌骨鸡养殖中减少氟喹诺酮类药物的使用。沙拉沙星作为一种高效廉价的氟喹诺酮类抗菌药,已广泛用于治疗家禽细菌和支原体感染[15]。国家最新《兽药质量标准》(2017年版)中规定了鸡使用沙拉沙星的休药期为0 d,但从本研究数据来看,此规定不适用于乌骨鸡品种。因此,在国家出台针对乌骨鸡的新休药期规定之前,建议养殖中使用其他药物替代沙拉沙星。
2.制定科学合理的休药期。据报道,达氟沙星、恩诺沙星等氟喹诺酮类药物在乌骨鸡体内代谢慢、消除时间长,这可能是造成近年来乌骨鸡药物残留超标问题的重要原因。本研究同时证明,沙拉沙星在乌骨鸡各组织部位中药物残留代谢情况不同,因此建议国家相关部门针对乌骨鸡品种进一步深入研究其残留代谢情况,重新评估制定休药期。
3.加强养殖规范用药的宣传。走访调研中发现,部分养殖者受利益驱使,在治疗家禽疾病中往往超剂量使用药物。本研究证明,超治疗剂量组中沙拉沙星在乌骨鸡不同组织部位的残留量均远高于正常治疗剂量组。因此建议相关部门加强对养殖端科学合理用药的宣传和监督,从源头上保障人民群众“舌尖上的安全”。
