程序性死亡受体1抑制剂卡瑞利珠单抗联合化疗治疗晚期食管鳞状细胞癌的临床疗效△
2023-01-14张殿宝康议心米优嘉
张殿宝,康议心,米优嘉
河南科技大学第一附属医院肿瘤内科,河南 洛阳 471003
食管癌是临床常见的恶性肿瘤之一,典型临床症状为食管管腔狭窄导致吞咽困难,逐渐引起营养不良、消瘦、脱水[1-2]。食管鳞状细胞癌是食管癌最常见的病理类型,占食管癌的95%。近年来,随着中国人口老龄化加剧,食管癌的发病率逐渐升高,且多数患者确诊时已进展为晚期,失去了最佳的手术时机[3]。晚期食管鳞状细胞癌的治疗以化疗为主,多西他赛为常用的化疗药物,可缓解患者的临床症状,但部分患者的耐药性较差,对复发转移性肿瘤的治疗效果有限[4]。程序性死亡受体1(programmed cell death 1,PDCD1,也称PD-1)是一种重要的免疫抑制分子,常用于免疫治疗,有研究表明,PD-1抑制剂用于肺癌、肾癌等肿瘤的治疗效果显著[5-6]。因此,本研究旨在探讨PD-1抑制剂卡瑞利珠单抗联合化疗治疗晚期食管鳞状细胞癌的临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年3月至2021年7月河南科技大学第一附属医院收治的晚期食管鳞状细胞癌患者。纳入标准:①符合《食管癌规范化诊治指南》[7]中关于食管癌的诊断标准;②经病理学检查证实为晚期食管鳞状细胞癌;③年龄>18岁。排除标准:①合并肝肾等器官功能不全;②近期有放化疗史;③合并严重高血压、糖尿病等基础疾病;④不耐受化疗。依据纳入和排除标准,本研究共纳入102例晚期食管癌患者,根据治疗方式的不同分为对照组和观察组,每组51例,对照组患者给予多西他赛化疗,观察组患者给予多西他赛联合卡瑞利珠单抗治疗。对照组中,男29例,女22例;年龄46~73岁,平均(56.74±4.38)岁;临床分期:Ⅲ期24例,Ⅳ期27例。观察组中,男28例,女23例;年龄45~73岁,平均(56.72±4.31)岁;临床分期:Ⅲ期25例,Ⅳ期26例。两组患者性别、年龄、临床分期比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准通过,所有患者均知情同意并签署知情同意书。
1.2 治疗方法
对照组患者给予多西他赛75 mg/m2静脉滴注,使用前口服地塞米松0.75 g。观察组患者在对照组基础上给予多西他赛联合卡瑞利珠单抗治疗,多西他赛治疗方法同对照组,卡瑞利珠单抗200 mg静脉滴注。两组患者均每3周治疗1次,持续治疗至出现疾病进展或不耐受,化疗期间针对患者出现的不良反应及时处理。
1.3 观察指标和评价标准
①采用实体瘤疗效评价标准[8]评估两组患者的临床疗效:完全缓解,目标病灶完全消失,至少持续4周;部分缓解,目标病灶长径总和缩小≥30%,至少持续4周;疾病稳定,目标病灶长径总和缩小<30%或增加<20%;疾病进展,目标病灶长径总和增加≥20%或出现新病灶。客观缓解率=(完全缓解+部分缓解)例数/总例数×100%,疾病控制率=(完全缓解+部分缓解+疾病稳定)例数/总例数×100%。②治疗前后,采用欧洲癌症研究与治疗组织生命质量测定量表(European Organization for Research and Treatment of Cancer quality of life questionnaire core-30,EORTC QLQ-C30)[9]评估两组患者的生活质量,包括躯体功能、情绪功能、社会功能、认知功能、角色功能等,每个维度总分为100分,评分越高表示生活质量越好。③参考国际肿瘤化疗药物不良反应评价系统——通用不良反应术语标准4.0版[10]评估两组患者的不良反应发生情况,包括甲状腺功能减退、发热、胃肠道反应、贫血、乏力、高脂血症、肝功能损伤、皮肤不良反应、心脏毒性。④采用微信、电话等方法对两组患者进行随访,随访时间截至2022年7月,记录两组患者的无进展生存期(progression-free survival,PFS),PFS指第一次治疗时至首次肿瘤进展时间。
1.4 统计学方法
采用SPSS 21.0软件对所有数据进行统计分析,计数资料以例数和率(%)表示,组间比较采用χ2检验;正态分布计量资料以均数±标准差(±s)表示,组间比较采用t检验;采用Kaplan-Meier法绘制生存曲线,组间比较采用Log-rank检验。以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
治疗后,观察组患者的客观缓解率为17.65%(9/51),与对照组患者的13.73%(7/51)比较,差异无统计学意义(χ2=0.267,P=0.586);观察组患者的疾病控制率为88.24%(45/51),明显高于对照组患者的58.82%(30/51),差异有统计学意(χ2=11.333,P=0.001)。(表1)

表1 两组患者的临床疗效[n(%)]*
2.2 生活质量的比较
治疗前,两组患者EORTC QLQ-C30量表各维度评分比较,差异均无统计学意义(P>0.05)。治疗后,两组患者EORTC QLQ-C30量表各维度评分均高于本组治疗前,且观察组患者EORTC QLQC30量表各维度评分均高于对照组,差异均有统计学意义(P<0.05)。(表2)
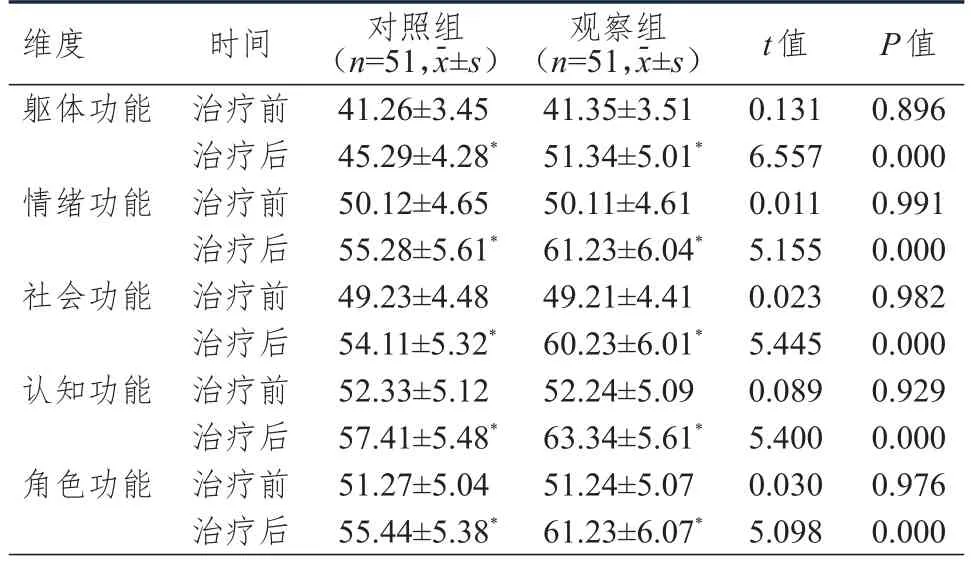
表2 治疗前后两组患者EORTC QLQ-C30量表评分的比较
2.3 不良反应发生情况的比较
两组患者甲状腺功能减退、发热、胃肠道反应、贫血、乏力、高脂血症、肝功能损伤、皮肤不良反应、心脏毒性发生率比较,差异均无统计学意义(P>0.05)。(表3)

表3 两组患者的不良反应发生情况[n(%)]
2.4 预后情况的比较
对照组患者的中位PFS为4.9个月(95%CI:2.4~7.8),明显短于观察组患者的7.1个月(95%CI:4.3~9.9),差异有统计学意义(χ2=9.560,P<0.01)。
3 讨论
食管癌的发生与生活环境、饮食生活习惯、遗传等因素有关,虽然食管癌的治疗手段不断更新发展,但有研究显示,晚期食管癌患者的5年生存率仅为10%[11]。晚期食管癌患者体质较差,且多数患者对化疗药物的敏感性较差,影响了化疗效果,因此,寻找积极有效的治疗方法相当重要[12]。
多西他赛能够抑制细胞有丝分裂,作用于细胞周期的G2/M期,可诱导肿瘤细胞凋亡[13-14]。但部分患者对铂类药物和紫杉醇类药物的耐药性较强,影响了治疗效果,且化疗药物的不良反应明显,易产生骨髓抑制、血小板减少、肝肾功能损伤等不良反应[15]。随着医学研究的不断发展,免疫治疗方案逐渐成熟,与手术、化疗、放疗等合称为肿瘤治疗的“四大支柱”;免疫治疗方案中免疫抑制剂特别是PD-1抑制剂一直是临床研究的热点之一[16-17]。PD-1能够促进淋巴结中抗原特异性T细胞凋亡,通过降低T细胞的抗氧化能力、阻止T细胞的正常代谢、抑制T细胞炎症活动以及调节免疫系统来促进机体自身耐受,但也限制了免疫系统对肿瘤细胞的杀伤作用[18]。PD-1抑制剂是阻断PD-1的一类新药,能够激活免疫系统攻击肿瘤细胞;PD-1人源化单克隆抗体包括纳武利尤单抗、派姆单抗、帕博利珠单抗、国产的特瑞普利单抗、信迪利单抗及卡瑞利珠单抗等[19]。PD-1抑制剂已应用于临床多种肿瘤的治疗中,且取得了一定的疗效,在晚期食管癌的治疗中也有大量研究。
ATTRACTION-3研究显示,纳武利尤单抗治疗化疗后进展食管鳞状细胞癌患者的中位PFS为1.7个月,客观缓解率和疾病控制率分别为19%和37%[20],表明PD-1抑制剂纳武利尤单抗治疗晚期食管癌患者的效果显著。PD-1抑制剂卡瑞利珠单抗在晚期食管癌中的应用也在逐步探索中,ESCORT研究显示,卡瑞利珠单抗单药治疗标准治疗失败的食管鳞状细胞癌患者的中位PFS为1.9个月,客观缓解率和疾病控制率分别为20.2%和44.7%[21];卡瑞利珠单抗在晚期食管鳞状细胞癌患者中的临床疗效是值得肯定的。本研究结果显示,观察组患者的客观缓解率为17.65%,与对照组患者的13.73%无明显差异;观察组患者的疾病控制率为88.24%,高于对照组患者的58.82%;但两组患者的不良反应发生率均无明显差异(P>0.05);治疗后,两组患者EORTC QLQC30量表各维度评分均高于本组治疗前,且观察组患者EORTC QLQ-C30量表各维度评分均高于对照组;表明PD-1抑制剂卡瑞利珠单抗联合化疗治疗晚期食管鳞状细胞癌有一定的临床疗效,特别是对疾病的控制有积极意义,且不会加重患者的不良反应,有助于提高患者的生活质量,与Chambers等[22]报道的结果一致。综上所述,PD-1抑制剂卡瑞利珠单抗联合化疗治疗晚期食管鳞状细胞癌有一定的临床疗效,特别是对疾病控制有积极意义,且不会加重患者的不良反应,有助于提高患者的生活质量。
