甲状腺次全切、全切治疗对甲状腺功能亢进症患者临床疗效、心脏功能及复发率的影响
2023-01-12程洁夏京辉
程洁 夏京辉
(驻马店市中心医院甲状腺外科,河南 驻马店 463000)
甲状腺功能亢进症属于内分泌科疾病,原因是甲状腺过度合成,造成甲状腺激素释放过度,引起代谢亢进、交感神经兴奋的一组症候群[1]。甲状腺功能亢进症可导致外周血液循环造成影响,从而累及其他脏器,若影响心血管系统,可能出现心律失常、心衰等情况,甚至危及生命[2]。因此,如何减少心功能损伤是治疗该病的重心。
目前临床针对甲状腺功能亢进症主要治疗方案为手术治疗,包括甲状腺次全切、甲状腺全切术,其目的是通过大部分或近完全切除甲状腺组织,降低甲状腺激素的释放,从而控制其临床症状。研究发现,甲状腺次全切、甲状腺全切术均具有一定疗效,但由于腺体周围神经、血管丰富,对于腺体切除范围临床未得出统一答案[3]。甲状腺次全切术虽可避免术后甲状腺素治疗,但难以评估应保留的甲状腺腺体,具有复发风险[4]。
基于此,本文旨在分析甲状腺次全切、全切治疗对甲状腺功能亢进症患者临床疗效、心脏功能及复发率的影响,从而为临床术式的合理选择,提高临床疗效提供参考。
1 资料与方法
1.1 一般资料
选取2019年4月-2021年5月本院收治甲状腺功能亢进症患者106例为研究对象,根据治疗方案不同分为对照组(甲状腺次全切术)51例和研究组(甲状腺全切术)55例。
其中对照组男26例,女25例,年龄26-49岁,平均年龄36.83±5.27岁,病程4-34 m,平均病程24.79±5.86 m,平均术前甲状腺体积24.93±3.18 cm3;观察组男28例,女27例,年龄27-49岁,平均年龄37.53±5.41岁,病程4-32 m,平均病程23.94±5.81 m,平均术前甲状腺体积24.42±3.09 cm3。
两组一般资料无显著差异(P>0.05),具有可比性。本研究经本院伦理委员会同意,且患者及家属知情签署《知情同意书》。
纳入标准:经超声检查确诊双侧甲状腺弥漫性肿大但无异常结节,且符合《甲状腺功能亢进症基层诊疗指南(2019年版)》[5]相关标准;符合手术指征;临床资料完整。排除标准:肝肾功能不全者;凝血功能及免疫功能异常者;存在精神障碍和心理疾病,无法正常沟通者。
1.2 方法
两组均行气管插管麻醉,体位平卧,垫肩,使头后仰,暴露颈部。切口选于胸骨上切迹上方两横指处沿皮纹,依次切开皮肤、皮下组织及颈阔肌,用组织钳拉起上下皮瓣,用刀分离颈阔肌后面的松散组织,上至甲状软骨下缘,下达胸骨柄切迹。沿胸锁肌前缘切开筋膜,切断颈前肌并结扎止血。
1.2.1 对照组
对照组采用甲状腺次全切术。分离结扎甲状腺内缘血管和甲状腺外侧缘悬韧带,分别结扎上、中静脉,保留后囊。分支远离甲状腺下极,尽可能贴近腺体,引导甲状腺下动静脉分离结扎,防止显露喉返神经,分离甲状腺,切除峡部和大部分双侧腺叶,两侧保留腺体(大小似拇指末端),中断缝合,消毒冲洗创面,然后放置引流管。
1.2.2 观察组
观察组采用甲状腺全切术。采用“精细化被膜解剖”。靠近腺体,对甲状腺上极行处理,切断结扎甲状腺上动静脉,然后靠近腺体,对下极行处理,保留甲状腺下动脉主干,结扎甲状腺下动脉进入甲状腺。将甲状腺拉向中线,将甲状腺背侧显露,为识别甲状旁腺需推开周围组织,解剖喉返神经。贴近腺体后部,甲状腺上极位置至甲状软骨上方;游离甲状腺上极,切除峡部和所有对侧腺叶。清洗伤口,引流管置于气管旁,依次缝合伤口。
1.3 观察指标
1.3.1 术后恢复情况
通过观察两组治疗后甲状腺功能减退、术中失血量、手术时间、术后引流量、总住院天数等,反映术后恢复情况。
1.3.2 心脏功能
采用彩色多普勒超声诊断仪检测左心室射血分数(Left ventricular ejection fraction,LVEF)、高峰射血率(Peak Ejection Rate,PER)、高峰充盈率(Peak filling rate,PFR)[4]。
1.3.3 并发症发生率及复发率
通过电话、上门等方式进行6个月随访,观察两组并发症(切口出血、喉返神经损伤、暂时性低钙血)及复发率。
1.4 统计学方法
2 结果
2.1 治疗效果
研究组短暂性甲状腺功能减退发生率高于对照组,术中失血量、术后引流量少于对照组,手术时间、总住院的时间短于对照组( P<0.05 )。见表1。
表1 两组治疗效果比较[n(%),±SD]
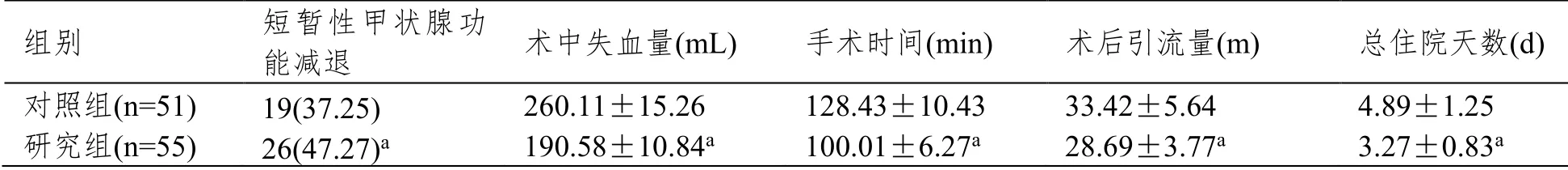
表1 两组治疗效果比较[n(%),±SD]
注:两组间比较,aP<0.05。
组别 短暂性甲状腺功能减退 术中失血量(mL) 手术时间(min) 术后引流量(m) 总住院天数(d) 对照组(n=51) 19(37.25) 260.11±15.26 128.43±10.43 33.42±5.64 4.89±1.25 研究组(n=55) 26(47.27)a 190.58±10.84a 100.01±6.27a 28.69±3.77a 3.27±0.83a
2.2 心脏功能指标
两组治疗后LVEF、PER及PFR水平均下降,且观察组LVEF、PER及PFR水平均低于对照组(P<0.05)。见表2。
表2 两组治疗前后LVEF、PER及PFR水平比较(±SD)

表2 两组治疗前后LVEF、PER及PFR水平比较(±SD)
注:两组间比较,aP<0.05;同组间比较,bP<0.05。
组别 LVEF(%) PER(L·S-1) PFR(L·S-1) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组(n=51) 70.36±13.28 67.16±10.52a 4.86±1.63 4.09±0.85a 5.46±2.03 4.31±1.37a 研究组(n=55) 69.81±13.11 62.48±9.14ab 4.99±1.59 3.37±0.66ab 5.23±2.01 3.28±0.89ab
2.3 并发症发生率及复发率
研究组并发症发生率及复发率分别为3.62%、1.81%,对照组并发症发生率及复发率分别为13.72%、15.68%;观察组并发症发生率及复发率均低于对照组(P<0.05)。见表3。

表3 两组并发症及复发率比较[n(%)]
3 讨论
甲状腺功能亢进症可导致外周血液循环造成影响,从而累及其他脏器,若影响心血管系统,可能出现心律失常、心衰等情况,甚至危及生命[1,2]。因此,如何减少心功能损伤是治疗该病的重心。目前临床针对该病主要治疗方案为手术治疗,包括甲状腺次全切、甲状腺全切术,其目的是通过大部分或近完全切除甲状腺组织,降低甲状腺激素的释放,从而控制其临床症状。但由于腺体周围神经、血管丰富,对于腺体切除范围临床未得出统一答案[3,4]。
本研究显示,研究组短暂性甲状腺功能减退发生率高于对照组,术后恢复情况优于对照组,其中研究组短暂性甲状腺功能减退发生率更高是由于甲状腺全切术切除全部腺体,术后需应用甲状腺激素进行替代治疗。但其剂量未调整适宜,随着时间增长,甲状腺激素若得到调整,甲减症状会随之消失;观察组术后恢复情况更优,可能是因为甲状腺全切术依靠“精细化被膜解剖法”,操作更为精细。另外,甲状腺功能亢进时,甲状腺激素可直接作用心肌收缩蛋白,增加心肌收缩力,会释放过多的甲状腺激素对心肌β受体产生刺激,导致对儿茶酚胺的敏感性增加,从而增加心输血量代偿性[6]。另外,甲状腺功能亢进症亦对肝功能造成一定损伤,其高代谢状态可导致肝脏能量状态发生障碍[6]。因此,甲状腺功能亢进症的主要治疗原则为控制过多的甲状腺激素分泌,从而减低对身体各器官带来的损害[2,3,7]。
本研究应用LVEF、PER及PFR评估心功能,其水平上升代表心功能受到损伤,结果显示两组治疗后LVEF、PER及PFR水平均下降,且观察组LVEF、PER及PFR水平均低于对照组,提示甲状腺全切术更能有效改善心功能,原因在于该术切除腺体完全,能更有效缓解临床症状。有文献报道,甲状腺次全切除术与甲状腺全切除术术后发生低钙血症并发症发生率相似,但后者复发概率低于前者,前提条件是熟知解剖结构,操作熟悉[7]。本次研究显示研究组复发率低于对照组,与以往研究结果类似,原因可能是甲状腺次全切除术未完全切除腺体,为彻底清除病源,故复发率更高。
综上所述,甲状腺功能亢进症患者应用甲状腺次全切、全切术治疗均具有一定临床疗效,但后者可更有效改善心脏功能,且复发率更低。
