参花外用颗粒皮肤用药安全性评价
2023-01-10朱聪聪连天雁陈中建朱全刚
喻 琴,侯 岩,朱聪聪,陈 亚,连天雁,陈中建,朱全刚
(上海市皮肤病医院/上海中药外用制剂创新工程技术研究中心,上海 200443)
银屑病是一种以鳞屑性红斑为特征的慢性炎症性皮肤病,主要分为寻常型、关节病型、脓疱型和红皮病型,其中寻常型约占银屑病的97.98%[1]。银屑病病因复杂,发病机制尚不明确,全球发病率可高达2%,且有逐年增高的趋势[2]。该病常伴瘙痒,迁延不愈,严重影响患者的生活质量。目前,尚无彻底根治的药物及方法,主要是减轻皮损及瘙痒等症状,控制及稳定病情,减少银屑病相关的并发症,提高患者生活质量[3-4]。中医辨证论治银屑病越来越受到关注,大量研究认为中西医结合治疗能显著降低该病复发率,整体治疗效果更好,且不良反应少[5-6]。参花外用颗粒原名中浴1号,由苦参、花椒、野菊花、生侧柏叶组成,具有清热解毒、除湿止痒的功效,主要用于寻常型银屑病等多种炎症性皮肤病的治疗。该方在上海市皮肤病医院临床应用已逾10年,效果显著,目前该院对该方进行剂型优化,由传统洗剂开发为使用携带方便、稳定性更好的颗粒剂即参花外用颗粒,但尚未对其进行系统的安全性评价。故本实验参考国家食品药品监督管理总局颁发的《中药、天然药物局部刺激性和溶血性研究的技术指导原则》和《中药天然药物免疫毒性(过敏性、光过敏反应)研究的技术指导原则》等,对参花外用颗粒外用的安全性进行了评价,以为其开发应用提供实验依据。
1 实验材料与方法
1.1实验动物 7~8周龄健康豚鼠,雌雄各半,体重250~300 g,购自上海杰思捷实验动物有限公司,动物许可证号:SCXK(沪)2018-0004。动物饲养于上海市皮肤病医院动物房,温度22~26 ℃,相对湿度40%~65%,噪声≤50 dB。本实验经上海市皮肤病医院伦理委员会批准[2021-108(动)预],并按照机构指南进行。
1.2药物与试剂 参花外用颗粒,由上海市皮肤病医院委托上海宝龙药业有限公司生产,批号:2108001。制备方法:取处方量苦参、野菊花、生侧柏叶、花椒,每次加6倍量水,煎煮2次,第1次2 h,第2次1 h,煎液滤过、合并,静置24 h,取上清液,浓缩至相对密度为1.25(70~90 ℃)的清膏,加入适量糊精,混匀,制粒,干燥,制成颗粒即得。参花外用颗粒临床药浴使用浓度的生药比为0.5%,即临床使用浓度,药液配置方法:称取适量颗粒,加蒸馏水配置成生药比为0.5%的药液;最大浓度即400倍临床使用浓度,药液配置方法:称取适量颗粒,加蒸馏水配置成生药比为200%的药液。2,4-二硝基氯苯购自美国Sigma公司。
1.3实验方法
1.3.1参花外用颗粒的皮肤刺激性试验 将20只豚鼠随机分为临床使用浓度完整皮肤组、临床使用浓度破损皮肤组、最大浓度完整皮肤组、最大浓度破损皮肤组及空白对照组,每组4只,雌雄各半。
1.3.1.1单次给药皮肤刺激性试验 采用自体背部左右侧对比方法进行:实验前24 h在豚鼠背部脊柱两侧建立范围为3 cm×3 cm的脱毛区,分别作为给药区和对照区。破损皮肤组用无菌针头于脱毛区划“#”字,以表皮出血丝、不伤及皮下组织为度。除空白对照组外,其他各组豚鼠给药区均涂抹参花外用颗粒药液200 μL,对照区涂抹等量蒸馏水,涂抹面积为2 cm×2 cm,覆盖消毒纱布后用无刺激性胶布固定。单次给药24 h后,用温水清洗去除残留药液。观察给药后1 h、24 h、48 h、72 h给药部位皮肤有无红斑、水肿等情况,并参照文献[7]中“皮肤刺激反应评分及刺激强度评价标准”进行评分。
1.3.1.2多次给药皮肤刺激性试验 操作方法与单次给药皮肤刺激性试验相同,每天于同一部位给药1次,每次6 h,连续14 d。从第2天开始,每次给药前剪毛,用温水清洗去除残留药物,1 h后观察结果,并进行皮肤刺激反应评分及皮肤刺激强度评价。末次给药停药后1 h、24 h、48 h、72 h观察给药部位皮肤有无红斑、水肿、溃烂等现象,并进行皮肤刺激反应评分及皮肤刺激强度评价。
1.3.2参花外用颗粒的急性毒性反应 多次给药皮肤刺激性试验期间,每日称豚鼠体重,记录体重增长情况。试验结束后取豚鼠腹主动脉血液、受试部位皮肤及主要脏器组织。称量心、肝、肺、肾、脾组织重量,计算各脏器系数,脏器系数=脏器重量/体重×100;对受试部位皮肤及脏器组织进行石蜡切片,HE染色观察;对腹主动脉血样离心取血清,用深圳雷杜生命科技(Chemray 240)全自动生化分析仪测定肝功能指标[谷丙转氨酶(ALT)、谷草转氨酶(AST)]及肾功能指标[血尿素氮(BUN)、肌酐(Cr)、尿酸(UA)]水平。
1.3.3参花外用颗粒的皮肤过敏试验 将16只豚鼠随机分为蒸馏水组、参花外用颗粒临床使用浓度组、参花外用颗粒最大浓度组、2,4-二硝基氯苯组(致敏浓度为1%,激发浓度为0.1%),每组4只,雌雄各半。考虑到2,4-二硝基氯苯的毒性,故未进行破损皮肤过敏性试验。致敏接触:试验前24 h于豚鼠背部左侧去毛3 cm×3 cm。将受试液均匀涂抹于脱毛区,涂抹面积为2 cm×2 cm,以消毒纱布覆盖,用无刺激性胶布加以固定,6 h后用温水洗去残留药液。第7天、第14天用同样方法给药诱导。激发接触:第28天于豚鼠右侧脱毛区再次涂抹各受试液进行激发,6 h后用温水清洁给药部位除去残留药液。即刻(0 h)、24 h、48 h、72 h观察豚鼠背部皮肤的过敏情况。记录各时间点所有豚鼠局部皮肤变态反应发生情况,同时注意有无全身变态反应(哮喘、站立不稳或休克等)。致敏率=出现皮肤红斑、水肿或全身变态反应的所有动物例数(不论程度轻重)/受试动物总数。参照文献[8]中“皮肤过敏反应评分标准”进行评分,计算平均分值,积分≥2分判为该动物出现皮肤变态反应。各组皮肤过敏评分(红斑或水肿项)总分表述为:皮肤该项过敏评分×动物数量分。

2 结 果
2.1参花外用颗粒的皮肤刺激性 参花外用颗粒在临床使用浓度及最大使用浓度下单次外用对豚鼠完整及破损皮肤的刺激反应评分和刺激强度评分均为0,无刺激性。连续外用14 d,临床使用浓度下对豚鼠完整皮肤组及破损皮肤组的皮肤刺激反应评分和刺激强度评分为0分,无刺激性。最大浓度下连续外用6 d后,完整皮肤组及破损皮肤组皮肤均出现轻微红斑,无水肿反应;连续外用14 d后,完整皮肤组皮肤刺激性评分均值为1.25分,破损皮肤组评分均值为1.75分,均小于2分,且在末次给药后72 h内红斑均消失。试验结束后受试部位皮肤病理学显示,临床使用浓度下,完整皮肤组及破损皮肤组皮肤组织完整,无结构紊乱,表皮无增厚、水肿,与空白对照组皮肤相比无明显差异;最大浓度下,完整皮肤组及破损皮肤组表皮增厚约为空白对照组的2倍,无结构紊乱、出血及水肿反应。见图1。

图1 空白对照组和参花外用颗粒各组豚鼠受试部位皮肤病理表现(HE,×100)
2.2参花外用颗粒的急性毒性反应
2.2.1体重及脏器系数比较 各组豚鼠在给药期间大小便正常,无反应差、抓痕及死亡等情况。给药前、给药第3天、给药第7天、给药第14天,参花外用颗粒临床使用浓度完整皮肤组、临床使用浓度破损皮肤组及最大浓度完整皮肤组、最大浓度破损皮肤组豚鼠体重与空白对照组比较差异均无统计学意义(P均>0.05),见表1。参花外用颗粒临床使用浓度完整皮肤组、临床使用浓度破损皮肤组、最大浓度完整皮肤组豚鼠的主要脏器系数与空白对照组比较差异均无统计学意义(P均>0.05);最大浓度皮肤破损组豚鼠脾脏系数明显高于空白对照组(P<0.05),其他脏器系数与空白对照组比较差异均无统计学意义(P均>0.05)。见表2。
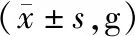
表1 空白对照组和参花外用颗粒各组豚鼠体重比较

表2 空白对照组和参花外用颗粒各组豚鼠脏器系数比较
2.2.2主要脏器病理学表现 临床使用浓度完整皮肤组和临床使用浓度破损皮肤组豚鼠心脏、肝脏、肺脏、肾脏、脾脏细胞染色均匀,结构正常,与空白对照组相比无明显差异,未发现病理性改变;最大浓度完整皮肤组和最大浓度破损皮肤组豚鼠的肝脏局部均有炎症反应(箭头位置),出现病理组织学改变,其他脏器未发现病理改变。见图2。
2.2.3肝肾功能指标比较 参花外用颗粒连续外用14 d后,临床使用浓度完整皮肤组、临床使用浓度破损皮肤组及最大浓度完整皮肤组、最大浓度破损皮肤组豚鼠的血清ALT、AST、BUN、Cr、UA水平与空白对照组比较差异均无统计学意义(P均>0.05),在正常范围内波动。见表3。

图2 空白对照组和参花外用颗粒各组豚鼠主要脏器组织病理表现(HE,×200)
2.3参花外用颗粒的皮肤致敏性 蒸馏水组激发6 h后,即刻至72 h脱毛区皮肤均未出现红斑及水肿,致敏率为0。2,4-二硝基氯苯组自激发给药6 h后,即刻观察到2只出现严重红斑(3×2分) [1只伴勉强水肿(1×1分),1只伴明显水肿(2×1分)],2只出现明显红斑(2×2分)[均伴勉强水肿(2×1分)],平均积分为3.75分,致敏率为100%;24 h开始消退,平均积分为2.75分,致敏率为75%(3/4);48 h平均积分为1.0分,致敏率为25%(1/4);72 h后仅1只可见微弱红斑,无水肿,平均积分为0.25分, 致敏率为0。参花外用颗粒临床使用浓度组激发给药6 h后,即刻至72 h脱毛区皮肤均未出现红斑及水肿,致敏率为0;参花外用颗粒最大浓度组激发给药6 h后,即刻观察到3只豚鼠出现轻微红斑,均无水肿现象,平均积分为0.75分(<2分),24 h已完全消退,致敏率为0。

表3 空白对照组和参花外用颗粒各组豚鼠肝肾功能指标水平比较
3 讨 论
目前银屑病仍以西医治疗为主。西医治疗主要分为系统用药、局部用药以及物理疗法,或多种治疗方法联用[9]。系统用药主要有糖皮质激素、维A酸类药、抗生素、维生素类、免疫疗法以及生物制剂等;局部用药主要有焦油制剂、地蒽酚、糖皮质激素、维A酸类药、维生素D3类似物等;物理治疗主要有紫外线治疗、水疗、日光浴等[10]。西医治疗,尤其是激素治疗,存在易复发、不良反应严重的特点,联合中药治疗有增效减毒作用[11]。中药外用为传统中医药治疗疾病尤其是皮肤疾病的重要手段[12],如中药洗剂治疗银屑病具有疗效确切、不良反应小、使用简便、复发率低的优势[13-15]。
参花外用颗粒方剂中苦参清热燥湿、祛风消炎为君药,野菊花清热解毒、疏风凉肝为臣药,以生侧柏叶凉血止血、除内湿、散肿毒为佐药,花椒祛风除湿、杀虫止痒为使药。全方针对银屑病血“热”的主要病因病机。宋勋等[16]报道该方药浴联合NB-UVB照射治疗寻常型银屑病效果优于单用NB-UVB照射治疗,能够明显改善患者生活质量。徐爽等[17]观察该方熏洗联合走罐治疗斑块状银屑病的临床疗效与NB-UVB联合外用中效糖皮质激素的长期疗效差异无统计学意义,且不良反应小。鉴于参花外用颗粒的传统制剂效果显著,故进行新剂型的皮肤安全性研究,对于安全用药及临床转化至关重要。
本实验结果显示,参花外用颗粒在临床使用浓度下无论外用于豚鼠完整皮肤还是破损皮肤,单次及多次刺激均显示无刺激性;当浓度增大至临床使用浓度的400倍时,单次外用于完整及破损皮肤无刺激性,连续多次使用出现轻度红斑,在末次给药72 h内可自行消失,皮肤病理学检查发现表皮增厚约为空白对照组的2倍,表现为轻度表皮增厚,对皮肤有轻度刺激性。急性毒性评价显示,临床使用浓度下对豚鼠体重、主要脏器及肝肾功能无影响,无毒性;最大浓度下对豚鼠存在潜在肝毒性。上述结果说明参花外用颗粒临床使用浓度下对皮肤无刺激性、致敏性及毒性;最大浓度下对皮肤有轻度刺激性,存在潜在肝毒性,无致敏性。总体而言,参花外用颗粒是安全的外用制剂,值得临床推广应用及开发新产品。
利益冲突:所有作者均声明不存在利益冲突。
