基于氧化石墨烯在大黄中有机氯的含量测定*
2022-12-27魏江存杨正腾马家宝王成龙江先再陆景荣崔健陈圣斌
魏江存,杨正腾,马家宝△,王成龙,江先再,陆景荣,崔健,陈圣斌
1广西中医药大学附属国际壮医医院,广西 南宁 530201;2广西中医药大学第一附属医院
曼彻斯特大学Geims教授在2004年使用胶带剥离石墨晶体首次获得了石墨烯[1],从此石墨烯的研究进入了一个快速发展的时代。其结构为紧密堆积成的二维蜂窝状晶体,以单层碳原子sp2杂化连接,属于新型碳纳米材料[2]。制备氧化石墨烯最经典的方法是Hummers法,近几年的研究多见于对其的改进[3-5]。因为氧化石墨烯的制备较为简单,产量大,价格低,合成的原料石墨资源也丰富,且能与金属、无机非金属、聚合物等材料合成性能更加优越的复合材料[6-7],因此,氧化石墨烯已成为最具广泛应用前景的吸附材料之一,多次被应用到农残分析中。氧化石墨烯在农残前处理中,主要被用作固相萃取和固相微萃取的吸附剂。多见于以氧化石墨烯为填料,制备固相萃取柱净化水果中有机磷的报道中,其净化富集有机磷回收率可达69.8%~106.2%[8],对6种氨基甲酸酯类农药的提取回收率也高达81.1%~111.0%[9]。
石墨烯在传统中药方面的研究中并不常见,重金属和残留农药的检测方面,也不常用[10-11]。传统的药材农残的前处理方法有索氏提取法、溶剂萃取法和超声波提取法等,存在分析周期长、溶剂消耗量大、操作过程繁琐且回收率低等缺点。而农药的残留一般为痕量级别,对分析方法的要求很高,如果提取分离不够纯化,富集不够彻底,很容易导致含有一定农药残留的药材未被检测出,势必影响药效和患者的健康。
中药大黄在种植过程中,由于虫害的原因,偶尔使用有机氯农药消除虫害,农药或除草剂中含有有机氯类成分,如2,4-滴丙酸和2,4,5-三氯苯氧乙酸残留。本实验采用正交试验,利用氧化石墨烯进行中药有机氯萃取方法的研究,从洗脱时间、氧化石墨烯用量和丙酮洗剂浓度方面进行正交试验,并采用HPLC高效液相色谱法对有机氯的成分进行含量测定,旨在寻找新型材料氧化石墨烯在中药大黄有机氯检测中的应用,为氧化石墨烯在传统中药中的应用提供科学依据,也为中药大黄农残前处理的研究提供实验数据。
1 材料与方法
1.1 仪器2695型高效液相色谱仪(美国Waters公司);Simplicity超纯水系统(密理博中国有限公司);Practum224-1CN分析天平[赛多利斯科学仪器(北京)有限公司];SHB-III循环水式多用真空泵(郑州长城科工贸有限公司);DHG-9203A型电热恒温鼓风干燥箱(上海齐欣科学仪器有限公司);TGL-16G高速台式离心机(上海安亭科学仪器厂);HWS-26电热恒温水浴锅(上海齐欣科学仪器有限公司)。
1.2 试药与药材2,4-滴丙酸(美国AccuStandard®,Inc,批号:217031400,纯度:>98.0%);2,4,5-三氯苯氧乙酸(美国AccuStandard®,Inc,批号:217081073,纯度:>98.0%);石墨粉(天津市大茂化学试剂厂,批号:20180118);甲醇和乙腈为色谱纯(Fisher,4L);浓硫酸、丙酮、乙醇、磷酸、醋酸和其他试剂为分析纯,实验用水为超纯水;大黄药材(广东康美药业有限公司,批号:180307002)购于老百姓大药房,药材样品经广西中医药大学药用植物教研室梁子宁教授鉴定为豆科植物大黄Glycyrrhiza uralensisFisch.、胀 果 大 黄Glycyrrhiza inflataBat.或光果大黄Glycyrrhiza glabraL.的干燥根和根茎。本实验所有样品执行标准均采用《中华人民共和国药典》2020年版一部。
1.3 方法
1.3.1 氧化石墨烯的制备由天然石墨粉反应生成氧化石墨,大致分为3个阶段,低温反应:在冰水浴中放入大烧杯,加入适量的浓硫酸(H2SO4),在磁力搅拌器上搅拌,放入温度计,测定其温度使之降至4℃左右。加入精密称定的100目鳞片状石墨粉,再加入硝酸钠(NaNO3),然后缓慢加入高锰酸钾(KMnO4),加完后记时,在磁力搅拌器上搅拌反应90 min。中温反应:将冰水浴换成温水浴,在磁力搅拌器搅拌下将烧杯里的温度控制在30~40℃,让其反应30 min。高温反应:中温反应结束之后,缓慢加入一定量的去离子水,加热保持温度70~100℃,缓慢加入一定双氧水(5%)进行高温反应,反应后的溶液在离心机中多次离心洗涤,直至BaCl2检测无白色沉淀生成(说明没有SO42-的存在)或洗涤至中性溶液,样品在40~50℃温度下烘干,即得氧化石墨烯。
1.3.2 供试品溶液和对照品溶液的制备取常用中药大黄25 g,将其粉碎,加入50 mL超纯水,用榨汁机加工成糊状。加入适量的氧化石墨烯粉振荡摇匀,每次用不同浓度的丙醇进行洗脱,控制洗脱时间。将洗脱液用氮气吹干,后加入适量的50%甲醇溶解定容到50 mL的容量瓶中,作为供试品溶液,取适量容量瓶中的溶液,以离心半径10 cm,13 000 r/min离心15 min,取上清液,0.45 μm微孔滤膜滤过,即得。2,4-滴丙酸(100 μg/mL);2,4,5-三氯苯氧乙酸(100 μg/mL);分别精密量取上述对照品溶液为1、0.5 mL,置5 mL量瓶中,摇匀即得混合对照品溶液(2,4-滴丙酸20 μg/mL,2,4,5-三氯苯氧乙酸10 μg/mL)。
1.3.3 单因素考察
1.3.3.1 氧化石墨烯加入量固定有机氯萃取时间为20 min,萃取溶剂丙酮浓度为25%,以氧化石墨烯的加入量对大黄中机氯萃得率做单因素试验,设计氧化石墨烯的加入量分别为10、30、50、80、100、120 mg,在合理使用资源的情况下,发现氧化石墨烯的加入量为50 mg时,有机氯得率较高。见图1。
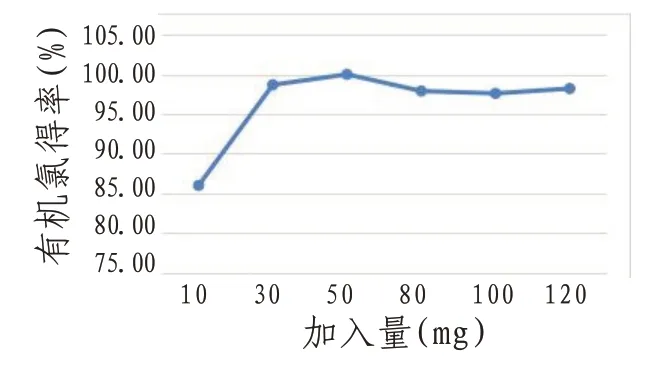
图1 氧化石墨烯加入量考察
1.3.3.2 萃取时间以有机氯萃取时氧化石墨烯加入量50 mg和丙酮浓度35%,萃取时间对大黄中有机氯的得率做单因素试验,设萃取时间为10、20、30、40、50 min,发现萃取时间为30 min时,有机氯得率较高。见图2。
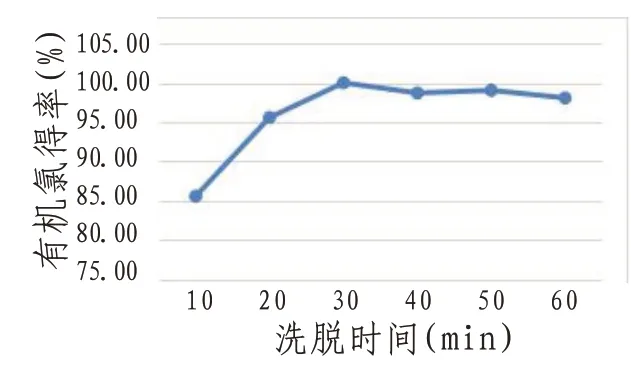
图2 萃取时间考察
1.3.3.3 萃取溶剂丙酮浓度考察以有机氯萃取时氧化石墨烯加入量50 mg和萃取时间20 min,以萃取溶剂丙酮浓度对大黄中有机氯得率做单因素试验,萃取溶剂丙酮浓度为20%、25%、30%、35%、40%、45%、50%,结果显示丙酮浓度为35%时,有机氯得率较高。见图3。

图3 萃取溶剂丙酮浓度考察
1.3.4 有机氯萃取方法优选正交试验设计[12],采用L9(34)正交表。考察氧化石墨烯用量,分别为20、50、800 mg,考察萃取时间,分别为20、30、40 min三个水平,考察洗脱溶剂,浓度分别为30%丙酮、35%丙酮、40%丙酮三个水平。精密吸取10 μL注入液相色谱仪,记录峰面积值,计算各指标成分含量,结果见表1。
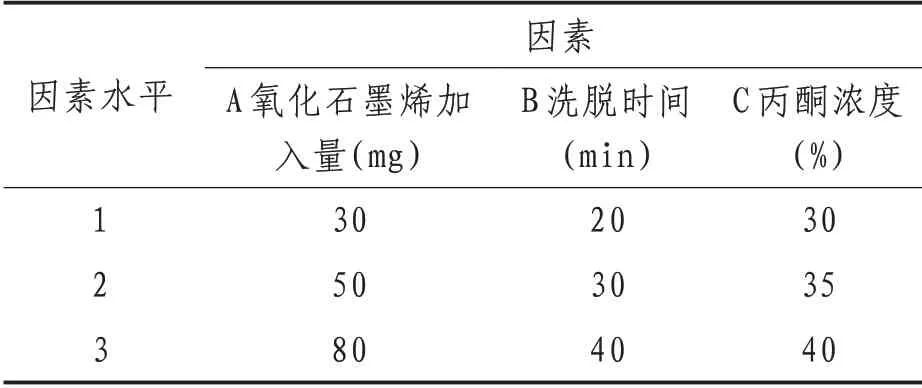
表1 正交试验因素与水平
1.3.5 正交试验取大黄药材粉末25.0g,精密称定,按照上述“2.2”项下的提取方法进行提取,再依供试品溶液的制备方法操作,按L9(34)正交设计方案进行试验,使用高效液相色谱法对中药大黄中2,4-滴丙酸、2,4,5-三氯苯氧乙酸成分进行含量测定。见表2—3。
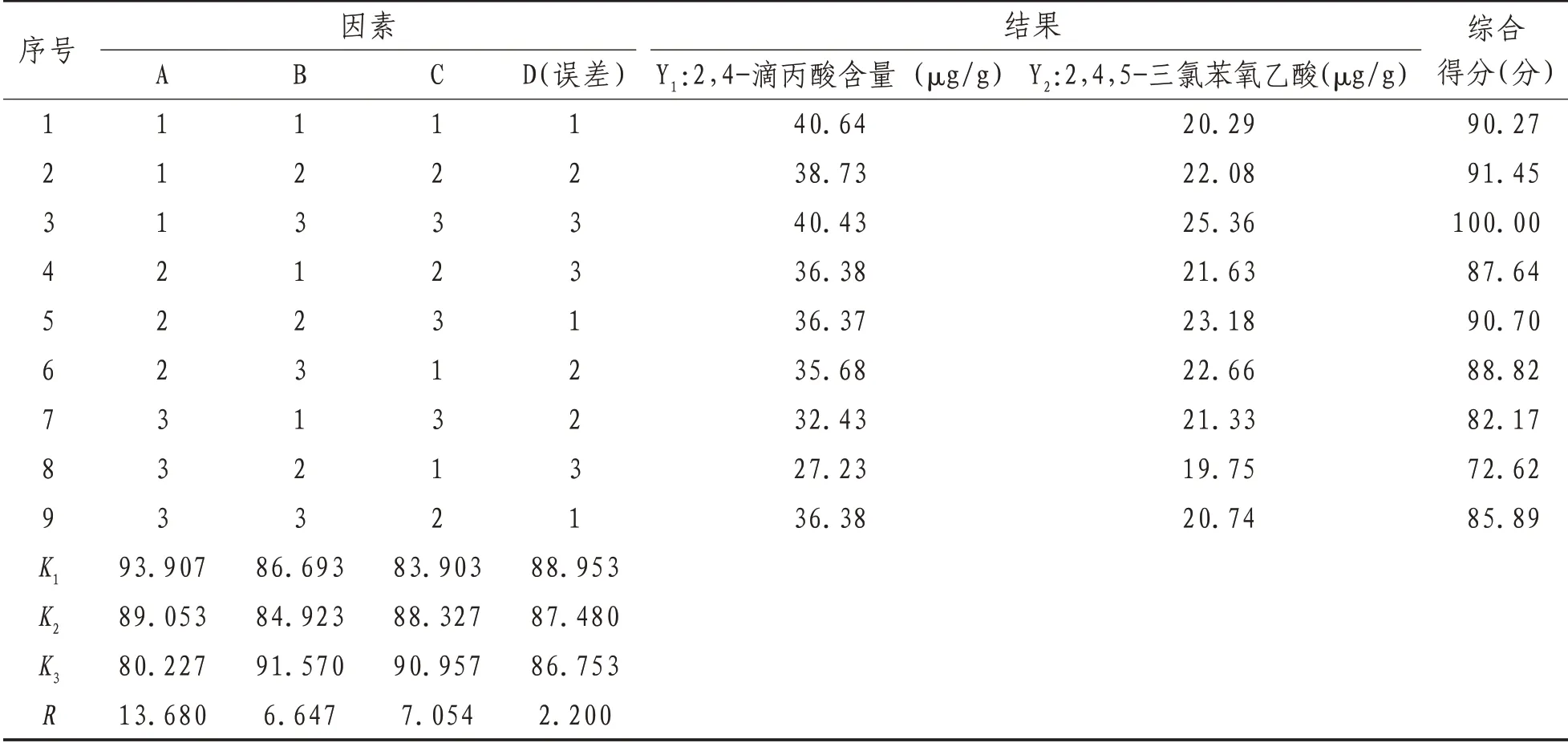
表2 正交试验设计与结果
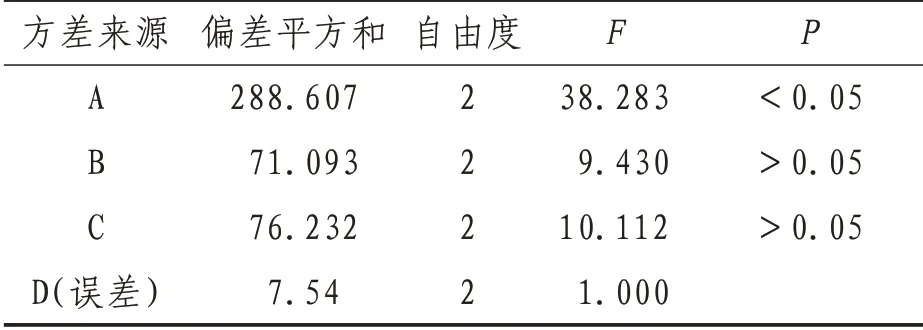
表3 方差分析结果
1.3.6 色谱条件色谱柱为Agilent Zorbax SB-C18(5μm,4.6mmX250mm),流动相为甲醇(A)-0.1%磷酸水溶液(B),梯度洗脱程序见表4,流速1 mL/min,柱温为30℃,进样量10 μL,检测波长为230 nm。理论塔板数以2,4-滴丙酸峰计算应不低于3000,以2,4,5-三氯苯氧乙酸峰计算不低于4000。2个成分都能达到较好分离,样品中其他成分对测定成分无干扰。见图4—5、表4。
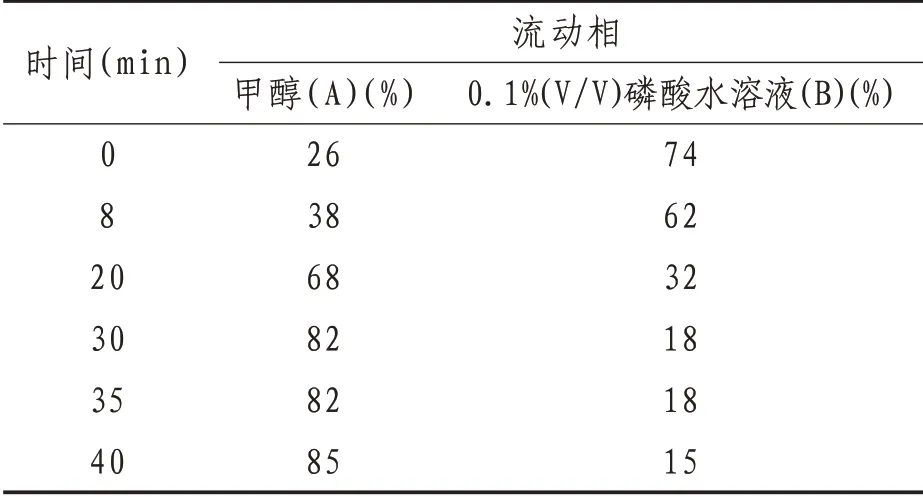
表4 梯度洗脱程序表
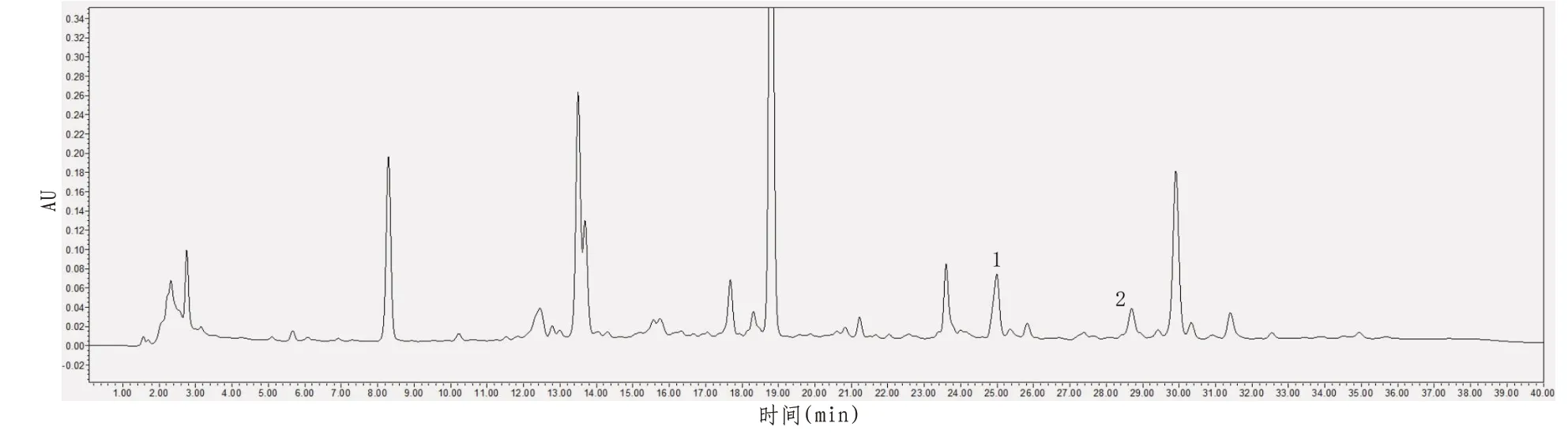
图4 大黄样品HPLC色谱图
1.3.7 标准曲线的制备精密吸取上述混合对照品溶液(2,4-滴丙酸20 μg/mL,2,4,5-三氯苯氧乙酸10 μg/mL)2、5、8、10、12、15、20 μL注入液相色谱仪,以峰面积和进样量(μg)分别为纵坐标和横坐标,绘制标准曲线并计算回归方程。测定其信号(以峰高计)与噪声比值,将S/N=3时的浓度定为检测限(LOD),将S/N=10时的浓度定为定量限(LOQ)。2,4-滴丙酸Y=4.0×106X+37327(R2=0.9998),检测限(ng)为2.4,定量限(ng)为18.6;2,4,5-三氯苯氧乙酸Y=4.0×106X+12495(R2=0.9993),检测限(ng)为3.1,定量限(ng)为25.3。结果,2,4-滴丙酸进样量在0.04~0.40 μg范围和2,4,5-三氯苯氧乙酸进样量在0.02~0.20 μg范围都呈良好的线性关系。见图6—7。
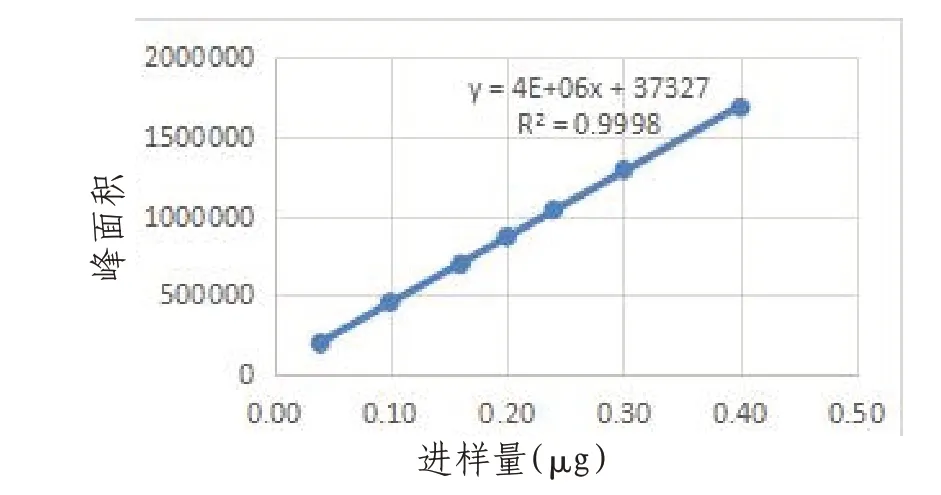
图6 2,4-滴丙酸线性方程图
1.3.8 方法学考察
1.3.8.1 精密度试验精密量取混合对照品溶液适量(2,4-滴丙酸20 μg/mL,2,4,5-三氯苯氧乙酸10 μg/mL),按“1.3.6”项下条件连续进样6次,计算2,4-滴丙酸和2,4,5-三氯苯氧乙酸峰面积的RSD分别为1.22%和1.15,均小于3%,说明仪器精密度良好。
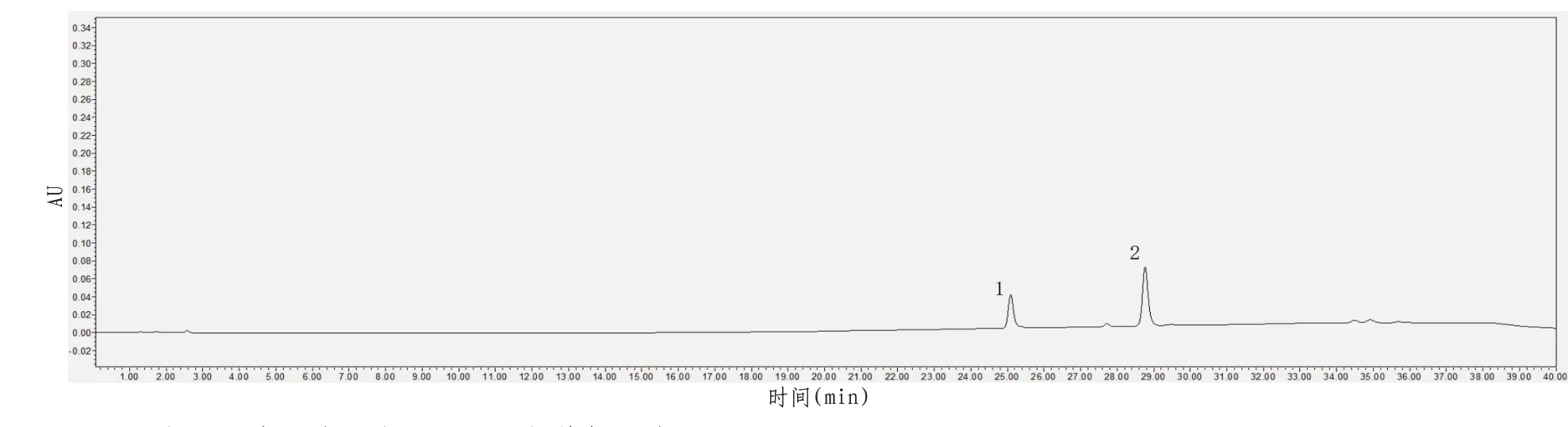
图5 2,4-滴丙酸和2,4,5-三氯苯氧乙酸混合对照品HPLC色谱图
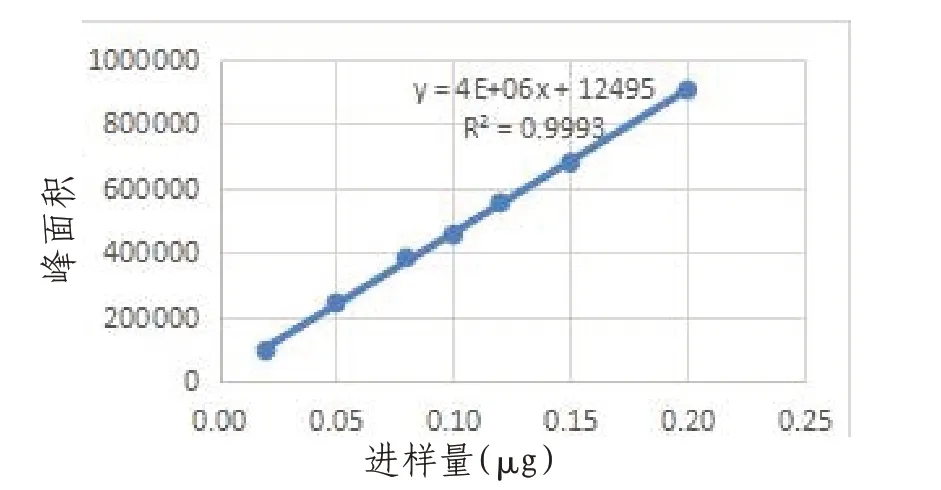
图7 2,4,5-三氯苯氧乙酸线性方程图
1.3.8.2 稳定性试验取同一批大黄药材粉末25.0 g,精密称定,按“1.3.2”项下的方法,加入氧化石墨烯粉30 mg振荡摇匀,洗脱时间30 min,40%丙醇进行洗脱,制备成供试品溶液,分别在供试品溶液制备后0、2、4、8、12、24 h按“1.3.2”项下条件测定,计算大黄中2,4-滴丙酸和2,4,5-三氯苯氧乙酸峰面积的RSD分别为1.84%和2.33%,均小于3%,说明24 h内供试品溶液稳定性良好。1.3.8.3重复性试验精密称取同一批大黄药材粉末25.0 g,精密称定,共6份,按“1.3.2”项下的方法,加入氧化石墨烯粉30 mg振荡摇匀,洗脱时间30 min,40%丙醇进行洗脱,制备成供试品溶液,按“1.3.2”项下条件测定,计算大黄中2,4-滴丙酸和2,4,5-三氯苯氧乙酸的平均含量分别为39.56、22.61 μg/g,其供试品溶液的浓度分别为19.78、11.30 μg/mL,其RSD分别为1.39%、1.96%,均小于3%,表明该方法重复性良好。
1.3.8.4 加样回收率试验精密量取已知浓度的6份供试品溶液1 mL,加入适量对照品溶液,用50%甲醇定容至2 mL的容量瓶,即得进样溶液,按照“1.3.2”项下的方法,加入氧化石墨烯粉20 mg振荡摇匀,洗脱时间30 min,40%丙醇进行洗脱,制备供试品溶液,按“1.3.6”项色谱条件进样,记录色谱峰面积,计算2,4-滴丙酸和2,4,5-三氯苯氧乙酸含量及RSD,计算加样回收率,平均回收率分别为99.78%、99.65%,RSD为2.27%、2.78%,结果见表2—3。以上结果表明,该方法准确性良好。结果见表5—6。
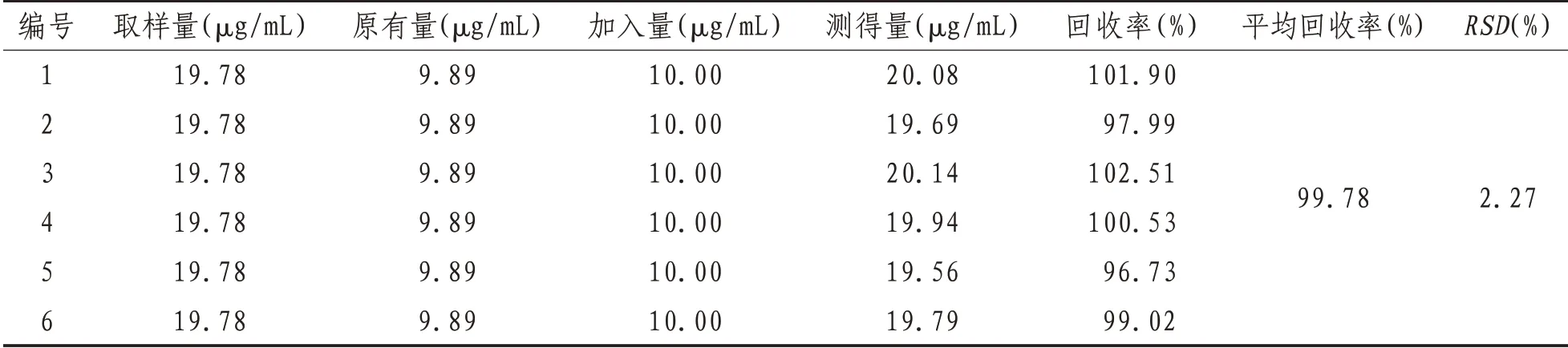
表5 大黄中2,4-滴丙酸的加样回收率结果(n=6)
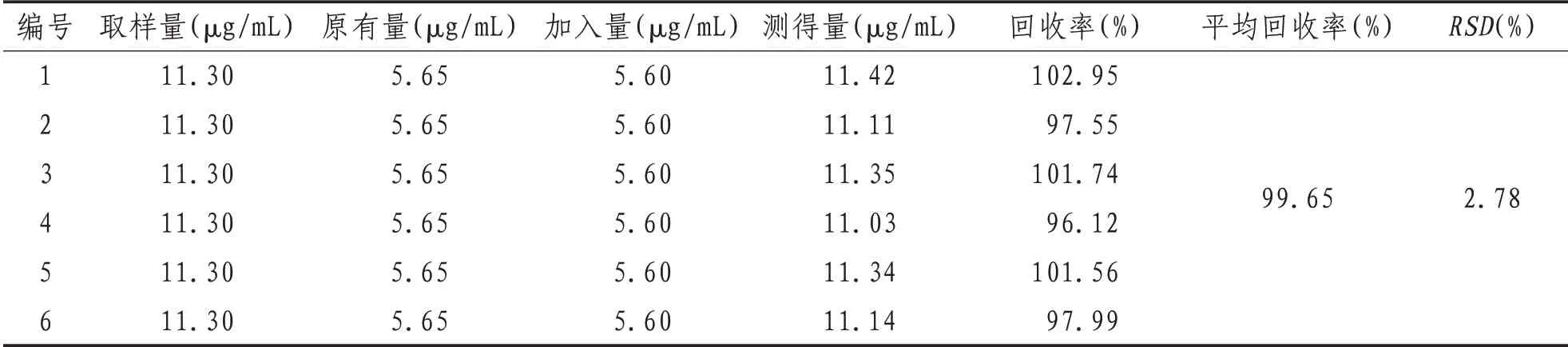
表6 大黄中2,4,5-三氯苯氧乙酸的加样回收率结果(n=6)
2 结果与分析
2.1 结果分析由于本次实验同时对大黄中的2个有效成分进行分析,采用综合加权评分法[13-15],2,4-滴丙酸的权重系数为0.5,2,4,5-三氯苯氧乙酸的权重系数为0.5,分别把2个成分项下最好的指标定为100分,其他各实验项按下式评分:综合得分=Yl/50.83×100×0.5+Y2/32.03×100×0.5。根据正交设计软件,实验方差分析结果显示,以大黄中2,4-滴丙酸和2,4,5-三氯苯氧乙酸的含量为实验指标,由于各实验因素对大黄提取效果的影响程度不同,从结果可以看出,各因素的主次顺序是A>C>B。因素氧化石墨烯加入量对实验结果有显著影响,因素洗脱时间和丙酮浓度对实验结果无显著性影响,经过综合分析,确定大黄的最佳提取工艺为A1B3C3,即在取25 g中药大黄的条件下,氧化石墨烯加入量为30 mg,洗脱时间为40 min,丙酮浓度为40%,此提取效果最佳。
2.2 工艺验证试验以优选出的2,4-滴丙酸和2,4,5-三氯苯氧乙酸提取条件对大黄中残留的2,4-滴丙酸和2,4,5-三氯苯氧乙酸含量进行验证试验,平行进行3次测定。计算大黄中残留的2,4-滴丙酸和2,4,5-三氯苯氧乙酸平均含量分别为41.08、25.32 μg/g,RSD分别为1.82%和2.39%(n=3)。验证试验表明,优化后的2,4-滴丙酸和2,4,5-三氯苯氧乙酸提取条件较好,工艺可行。
2.3 含量测定取同一批次的大黄药材粉末3份,每份25 g,按照“1.3.2”项方法制备供试品溶液,按“1.3.6”项色谱条件进样,记录色谱峰面积,计算2,4-滴丙酸和2,4,5-三氯苯氧乙酸含量,结果见表7。

表7 中药大黄中2,4-滴丙酸和2,4,5-三氯苯氧乙酸的含量(n=3) μg/g
3 讨论
3.1 流动相的选择考察了不同甲醇-酸水系统和乙腈-酸水系统(0.05%磷酸、0.1%磷酸、0.2%磷酸、0.1%冰醋酸、0.2%冰醋酸、0.1%甲酸、0.2%甲酸和纯水),结果表明,甲醇-0.1%磷酸溶液作为流动相时,分离度相对较好,基线较平稳,出峰时间适当,故流动相确定为甲醇-0.1%磷酸水溶液。
3.2 波长的选择采用二极管阵列检测器,在200~400 nm波长下对大黄提取液与2,4-滴丙酸和2,4,5-三氯苯氧乙酸混合对照品溶液进行全波长扫描,2,4-滴丙酸和2,4,5-三氯苯氧乙酸在230、282 nm下有最大吸收。在230、282 nm检测波长时,282基线漂移以及杂峰较多,而用230 nm时,基线相对平稳,杂峰较少,溶剂峰小,2,4-滴丙酸和2,4,5-三氯苯氧乙酸响应值较大,故最终采用230 nm作为本实验的检测波长。
本实验在对氧化石墨烯萃取大黄中有机氯的方法进行优化筛选的基础上,排除了其他杂质的干扰及影响,对实验的操作步骤进一步优化,检测常见中药大黄中的2,4-滴丙酸和2,4,5-三氯苯氧乙酸残留量变得简便与快速。本方法的建立对于中药大黄中2,4-滴丙酸和2,4,5-三氯苯氧乙酸残留的快速监测有着重要的意义。
目前,中药材的来源基本上都是人工种植,种植中药所喷洒的农药己成为影响中药品质的主要指标。本文利用氧化石墨烯萃取大黄药材中2,4-滴丙酸和2,4,5-三氯苯氧乙酸,经提取离心过滤后用高效液相色谱仪测定。该方法操作简单、快捷,在所用试验条件下,检测限适宜,具有良好的精密度、稳定性、重复性和加样回收率,能满足2,4-滴丙酸和2,4,5-三氯苯氧乙酸残留量的检测要求。
