吉西他滨联合顺铂治疗耐药性晚期乳腺癌的临床疗效及对患者预后的影响
2022-12-24李航刘晓敏王小龙
李航,刘晓敏,王小龙
西安国际医学中心医院甲乳外科,西安 710100
随着生活方式的改变和人口老龄化,乳腺癌的发病率逐渐上升,居女性全部恶性肿瘤首位,其病死率居女性全部恶性肿瘤第二位[1]。乳腺癌是由于乳腺细胞生长失去控制引起的恶性肿瘤,可导致人体自身免疫系统被破坏,乳腺细胞失去正常特性,严重危害患者的生命健康[2-3]。目前临床中治疗乳腺癌的常用方法包括手术治疗和化疗等,手术主要针对早中期乳腺癌患者,而对于无法行手术治疗的晚期患者常采取化疗。临床中治疗乳腺癌的常用药物包括蒽环类、紫杉类药物,但部分患者出现耐药情况,严重影响临床疗效及预后[4]。因此,寻找有效的治疗方法对改善蒽环类与紫杉类耐药的晚期乳腺癌患者预后具有重要意义。基于此,本研究探讨吉西他滨联合顺铂治疗耐药性晚期乳腺癌的临床疗效及对患者预后的影响,现报道如下。
1 资料与方法
1.1 一般资料
收集2019年1月至2021年1月西安国际医学中心医院收治的耐药性晚期乳腺癌患者的病历资料。纳入标准:①符合乳腺癌的诊断标准[5],经病理检查确诊为乳腺癌;②临床资料及实验室检查资料完整;③对蒽环类药物耐药;④TNM分期为Ⅳ期。排除标准:①合并重要脏器严重病变;②合并其他恶性肿瘤;③合并精神障碍。依据纳入和排除标准,本研究共纳入87例患者。根据治疗方法的不同将患者分为观察组(n=46,吉西他滨联合顺铂治疗)和对照组(n=41,吉西他滨联合卡培他滨治疗)。观察组患者年龄32~50岁,平均(39.91±8.68)岁;病变部位:左侧20例,右侧26例;病程4~16个月,平均(10.05±5.62)个月。对照组患者年龄34~51岁,平均(40.12±8.39)岁;病变部位:左侧21例,右侧20例;病程5~16个月,平均(10.21±5.59)个月。两组患者的年龄、病变部位及病程比较,差异均无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者均知情同意并签署知情同意书。
1.2 治疗方法
对照组患者采用吉西他滨联合卡培他滨治疗。将1000 mg/m2吉西他滨加入150 ml生理盐水中,静脉滴注,第1、8天;卡培他滨口服,一天2次,每次1000 mg/m2,连续服用两周,停药一周,3周为1个疗程。
观察组患者采用吉西他滨联合顺铂治疗。吉西他滨使用方法与对照组相同。将25 mg/m2顺铂加入200 ml生理盐水中,静脉滴注,第1~3天,3周为1个疗程。
1.3 观察指标及评价标准
1.3.1 临床疗效 采用世界卫生组织(WHO)实体瘤疗效评价标准[6]评价两组患者的临床疗效。完全缓解:临床症状、病灶完全消失;部分缓解:临床症状消失,病灶体积缩小50%及以上;疾病稳定:临床症状减轻,病灶体积缩小50%以下或增大不超过25%;疾病进展:病灶体积增大25%以上或出现新病灶。疾病控制率=(完全缓解+部分缓解+疾病稳定)例数/总例数×100%。
1.3.2 炎性因子 治疗前后采集两组患者的空腹静脉血5 ml,3000 r/min离心10 min,取上层血清于-20℃冰箱保存。采用酶联免疫吸附试验检测C反应蛋白(C-reactive protein,CRP)、白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平,严格按照说明书进行操作。
1.3.3 不良反应 记录并比较两组患者治疗期间的不良反应发生情况,包括肝功能不全、胃肠道反应、血小板减少等。
1.3.4 预后 出院后采用电话、微信、回院复查等方式对两组患者随访1年,记录并比较两组患者的生存率和复发率。
1.4 统计学方法
采用SPSS 22.0软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验;以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的疾病控制率为93.48%(43/46),高于对照组患者的78.05%(32/41),差异有统计学意义(χ2=4.340,P=0.037)。(表1)

表1 两组患者的临床疗效[n(%)]
2.2 炎性因子水平的比较
治疗前,两组患者的CRP、IL-6、TNF-α水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者的CRP、IL-6、TNF-α水平均低于本组治疗前,观察组患者的CRP、IL-6、TNF-α水平均低于对照组,差异均有统计学意义(P<0.05)。(表2)

表2 治疗前后两组患者炎性因子水平的比较
2.3 不良反应发生情况的比较
观察组患者的不良反应总发生率为21.74%(10/46),与对照组患者的14.63%(6/41)比较,差异无统计学意义(χ2=0.729,P=0.393)。(表3)

表3 两组患者的不良反应发生情况[n(%)]
2.4 预后的比较
治疗后,两组患者的3、6个月生存率比较,差异均无统计学意义(P>0.05);观察组患者的1年生存率高于对照组,1年复发率低于对照组,差异均有统计学意义(P<0.05)。(表4)
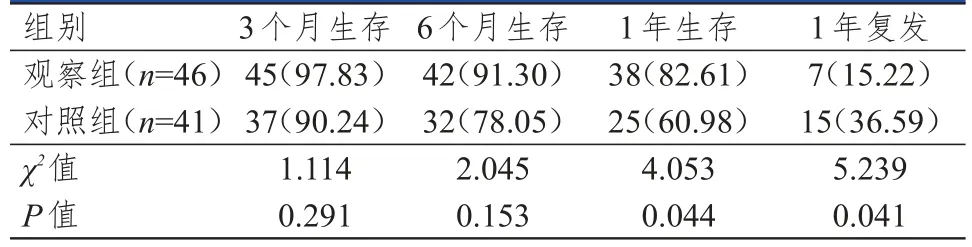
表4 两组患者预后的比较[n(%)]
3 讨论
乳腺癌作为女性常见的恶性肿瘤,严重威胁着女性的身心健康。乳腺癌的发病率较高,据统计,其在全部恶性肿瘤中的比例达7%~10%[7-8]。乳腺癌发病初期病情较为隐匿,且无典型症状,发展至中晚期才可触及肿块,出现乳头溢液、橘皮样变以及淋巴结肿大等,多数患者此时进行手术治疗意义已不大[9]。对于不能进行手术治疗的晚期乳腺癌患者,临床常予以化疗,以延缓疾病发展,延长患者的生存时间。蒽环类、紫杉类等化疗药物是临床治疗乳腺癌的一线药物,研究发现,长期应用此类药物会导致患者出现耐药情况,从而导致化疗失败[10]。因此,临床需要采取新的化疗方案继续进行治疗。单一药物化疗的临床效果欠佳,临床中虽然存在多种辅助化疗方案,但对于蒽环类、紫杉类化疗药物耐药的晚期乳腺癌的化疗方案尚未达成共识,还需进一步研究。
研究发现,吉西他滨与顺铂具有不同于蒽环类、紫杉类药物的独特作用机制,这两种药物与蒽环类、紫杉类药物无交叉耐药性,且两药联合又有协同作用。其中吉西他滨为新型嘧啶类抗代谢剂,能够被胃肠道迅速吸收,再通过三步酶促反应转化成氟尿嘧啶,通过细胞内的代谢作用抑制DNA的合成和核糖核苷酸还原酶的活性,有效杀死S期细胞,抑制肿瘤细胞转移[11]。顺铂是中心以二价铂同两个氯原子和两个氨分子结合的重金属络合物,与双功能生物烷化剂相似,能抑制DNA复制,具有抗肿瘤范围广、作用力强的优点,同时可与多种抗肿瘤药物联用,不易使机体产生交叉耐药性,是目前化疗联合用药中最为常用的一种药物[12]。本研究结果显示,观察组患者的疾病控制率高于对照组(P<0.05);治疗后,两组患者的CRP、IL-6、TNF-α水平均低于本组治疗前,观察组患者的CRP、IL-6、TNF-α水平均低于对照组,差异均有统计学意义(P<0.05)。说明吉西他滨与顺铂联合治疗耐药性晚期乳腺癌患者可有效提高临床疗效。可能是由于吉西他滨与顺铂的药物机制不同,具有协同作用[13]。此外,观察组患者的1年生存率高于对照组,1年复发率低于对照组,差异均有统计学意义(P<0.05)。说明吉西他滨联合顺铂治疗耐药性晚期乳腺癌可提高患者生存率,降低患者复发率。本研究结果还显示,两组患者的不良反应总发生率比较,差异无统计学意义(P>0.05)。本研究中,两组患者在化疗前后均应用粒细胞集落刺激因子(granulocyte colony stimulating factor,GCSF)、血小板生成素(thrombopoietin,TPO)、5-羟色胺受体拮抗剂等药物,因此治疗期间患者肝功能不全、胃肠道反应、血小板减少及其他不良反应均较少,未影响化疗的正常进行,由此提示吉西他滨联合顺铂治疗方案导致的不良反应可提前预防,具有一定的可控性,安全性高。
综上所述,吉西他滨联合顺铂治疗耐药性晚期乳腺癌的临床疗效较好,可提高患者生存率,降低患者复发率,且具有较好的安全性,临床可考虑将其推广应用。
