异位促肾上腺皮质激素综合征行双侧肾上腺切除术发生肾上腺危象1例报道
2022-11-23徐浩卫超许盛飞吴磊袁晓奕杨为民
徐浩 卫超 许盛飞 吴磊 袁晓奕 杨为民
异位促肾上腺皮质激素综合征(ectopic adrenocorticotropic hormone syndrome, EAS)是一类由垂体以外的组织分泌过量的促肾上腺皮质激素(adrenocorticotropic hormone, ACTH)而导致的一种特殊类型的库欣综合征(cushing’s syndrome, CS),占所有CS患者的5%~15%[1]。EAS的病因为分泌ACTH的各种肿瘤[1-2],约30%~56%的EAS患者因异位ACTH分泌不能通过手术切除原发病控制,需行双侧肾上腺切除术,术后需长期使用激素替代治疗,肾上腺危象是其术后严重并发症[1,3]。
肾上腺危象是一类高死亡率的临床急症,对患者进行即刻识别与治疗是避免患者死亡的关键。本文拟报道1例因EAS行双侧肾上腺切除术、术后住院期间并发肾上腺危象病例的诊治经过,以供临床参考。
患者,女,59岁,因“发现血糖升高5月余,双下肢、颜面浮肿1个月”收治于华中科技大学同济医学院附属同济医院内分泌科。患者于2年前体检时发现肝脏占位,经进一步行肝脏占位穿刺活检及肿瘤PET/CT等检查,最终确诊为胰腺神经内分泌肿瘤伴肝脏转移。经本院胆胰外科评估,认为患者胰腺及肝脏转移灶无法通过手术清除,因而先后接受依维莫司、化疗及索凡替尼等非手术治疗;同时患者伴有高血压病史4年。体格检查:身高160 cm,体重70 kg,BMI 27.34 kg/m2,血压135/95 mmHg,呈满月脸、水牛背体型,腹部皮肤可见紫纹。血生化检测提示血ACTH、皮质醇水平显著增高,血钾显著降低,血钠高。岩下窦静脉采血提示ACTH浓度与外周静脉相当,头部MRI未见垂体肿瘤性病变,排除垂体性ACTH分泌可能。胸腰椎MRI提示胸11椎体压缩性骨折。骨密度测定提示骨质疏松症。结合患者病史、体检、血生化及影像学检查结果,诊断为EAS、胰腺神经内分泌肿瘤伴肝脏转移、低钾血症、糖尿病、高血压2级(极高危组)、骨质疏松症伴病理性骨折、性腺功能减退症、甲状腺功能减退症。术前给予胰岛素泵控制血糖,钙离子拮抗剂联合螺内酯、α受体抑制剂控制血压,纠正低血钾等术前准备后,转入泌尿外科行经腹膜后途径腹腔镜双侧肾上腺切除术,手术顺利完成。术前腹部CT增强提示双侧肾上腺体积明显增大(图1),术后标本:左侧肾上腺大小约为4.5 cm×2.5 cm×1.5 cm,右侧肾上腺大小约为6.0 cm×3.0 cm×2.0 cm,切面灰黄、灰褐(图2)。术中给予氢化可的松200 mg静滴,输液3 500 ml,补氯化钾1 g,出血50 ml,尿量900 ml,胃管引流液700 ml。因患者基础疾病较多,病情重,手术时间较长,术后患者带气管插管转入ICU监护。转入ICU后当天未再给予糖皮质激素,输液量1 270 ml,尿量3 000 ml。术后第1天清晨一次性给予氢化可的松200 mg静滴,下午血压下降至80/40 mmHg,心率上升至140次/分,给予补液、升压药物维持血压。术后第2天清晨再次给予氢化可的松200 mg静滴,随后患者出现高热症状,心率继续上升至160~180次/分,需要大剂量升压药维持血压。经泌尿外科会诊后,考虑肾上腺危象可能,立刻追加甲强龙40 mg静滴,并将氢化可的松用法改为100 mg,每8 h 1次静滴。PICCO监测显示全心舒张末容积指数降低,前负荷不足,给予加强补液、抗感染、营养支持等处理,患者体温、血氧饱和度、血压、心率等逐渐好转。于术后第6天顺利拔除气管插管、停用呼吸机,随后转入泌尿外科普通病房。术后第8天转入内分泌科病房,继续补钾、控制血糖、减量使用氢化可的松等治疗,术后第15天出院,并改用口服氢化可的松片治疗。术后病理:肾上腺皮质结节状增生。
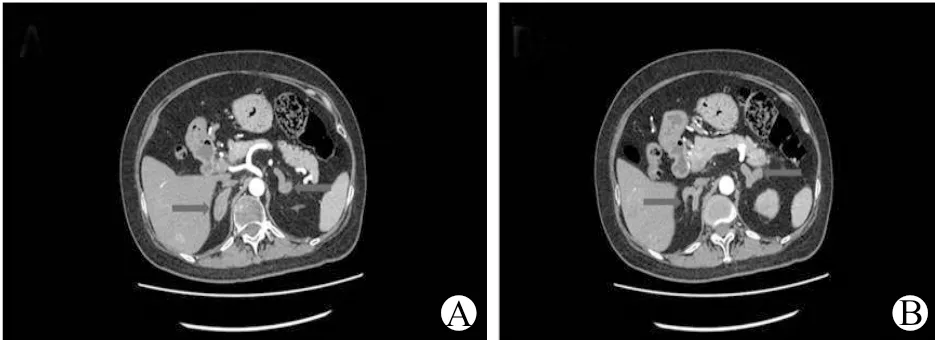
A:红色箭头指示肾上腺内、外支结合部肥厚;B:红色箭头指示肾上腺内支和外支均肥厚
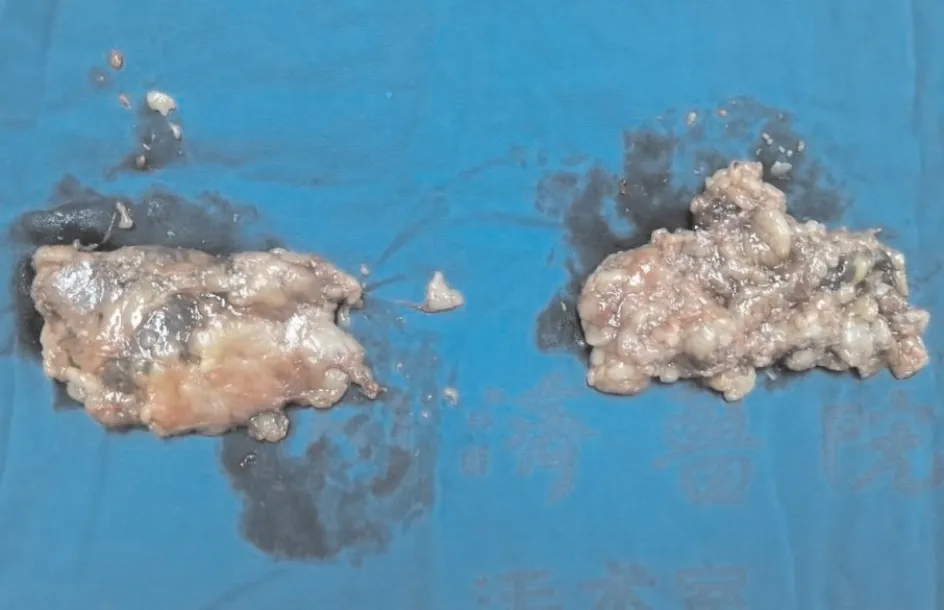
图2 双侧肾上腺全部切除标本
讨论EAS虽然是CS的一种少见类型,但近年来报道较多,国内外均有相关专家共识[3-4]。EAS具有和一般CS相同、因血皮质醇增高导致的临床症状和体征;通过MRI、CT等影像学检查定位肾上腺及垂体外的肿瘤,结合血生化及岩下窦静脉采血,是诊断EAS的关键,PET/CT可以作为有效的定位辅助诊断方法[5]。目前认为,EAS最有效的治疗方式是早期发现异位肿瘤来源并行根治性切除;在原发病灶无法切除的情况下,可选的治疗方法有药物治疗或靶腺切除(肾上腺切除)后糖皮质激素替代治疗[3,6]。接受药物治疗常导致无法耐受的副反应,靶腺切除成为治疗EAS的合理选择。值得注意的是,靶腺切除是指双侧肾上腺全切。因EAS患者体内存在过量的ACTH,不完全切除双侧肾上腺组织,可能导致残余的肾上腺组织在持续过量ACTH的刺激下,继续分泌过量皮质醇,影响手术效果。靶腺切除可以快速、有效地控制患者高皮质醇血症并改善相关症状,降低因高皮质醇血症而导致的死亡风险,还可避免药物治疗所致的不良反应,其已被证明是一种安全有效的治疗方法,被相关指南及专家共识所推荐[6-8]。目前尚未有采用一侧肾上腺切除、另一侧肾上腺次全切除治疗EAS的报道。双侧肾上腺切除术后并发症包括Nelson综合征、肾上腺危象、严重感染等,其中肾上腺危象最为紧急。目前缺少关于双侧肾上腺切除术后住院期间肾上腺危象发生率的报道;在术后长期随访过程中,肾上腺危象的发生率为4.1~9.3次/100人/年,相关死亡率为0.2人/100人/年,其发生率、死亡率与一般接受激素替代治疗的肾上腺皮质功能减退患者相当[7,9-12]。
目前,对肾上腺危象的诊断并无统一的标准[13]。Allolio[10]将肾上腺危象定义为患者出现恶心、呕吐、严重疲劳、发热、嗜睡、低钠血症或高钾血症、低血压等症状或体征中的两种或以上,健康状况急剧恶化的需要住院治疗,在接受糖皮质激素治疗后状况可迅速改善。研究认为,低血压并不是肾上腺危象发生所必须的特征,而休克可能是肾上腺危象的特异性表现[11,13]。肾上腺危象发生的原因既可以是糖皮质激素的绝对不足,也可以是体内糖皮质激素水平下降过快而导致的相对不足,不能维持机体稳态而发生的撤药反应[9]。因此,血皮质醇的绝对值水平不能作为肾上腺危象的诊断标准。本例患者因胰腺肿瘤已经出现肝脏转移,原发肿瘤无法通过手术切除控制,内分泌科行相关检查确诊为EAS,且患者合并非常严重的高血压、低血糖、低血钾,需要用大量药物维持生命体征及电解质稳定,且合并严重骨质疏松症伴病理性骨折,与患者及家属充分沟通后,选择了经腹膜后途径腹腔镜双侧肾上腺切除术。术中、术后均给予了一定量的氢化可的松治疗。术后患者转入ICU观察,处于镇静、气管插管、呼吸机辅助呼吸状况下,无主观不适症状,但出现血压下降、心率上升、血氧饱和度下降、高热、颜面部抽搐、脱水、休克等客观表现,经及时大剂量补充糖皮质激素,同时增加了其给药频次,并在此基础上给予大量补液等纠正脱水、抢救休克的措施,最终使患者各项生理指标迅速好转,证实了肾上腺危象诊断的同时,也及时纠正了低容量性休克,避免了因休克时间过长而导致的严重后果。
肾上腺危象的早期识别对于患者的治疗结局非常关键。本例患者肾上腺危象发生时处于镇静状态,无典型主观症状;而低血压、高热、休克等表现并不具有特异性,易与误感染性休克混淆。而肾上腺危象是以补充糖皮质激素为基础的对症支持治疗,而感染性休克则应在抗感染的基础上进行对症支持治疗,应避免大剂量使用糖皮质激素而导致免疫抑制。本例患者血常规白细胞、血降钙素原等感染指标始终处于可用外科手术操作来解释的轻度升高状态,并不符合严重感染导致感染性休克的特征;另外,感染性休克患者常因肾灌注不足而少尿,本例患者虽然血压显著下降,但每天尿量却维持在2 000~4 000 ml之间,与感染性休克的特征不符。
目前,双侧肾上腺切除术后需要适当补充糖皮质激素以预防肾上腺危象已成为共识,但具体的糖皮质激素补充方法并无公认的标准。氢化可的松由于同时具有糖皮质激素和盐皮质激素样作用,为首选用药。Howlett[14]的研究认为,CS患者术后使用氢化可的松每日3次的给药方案优于每日2次方案,具体剂量遵循个体化原则。Mishra等[15]在对肾上腺切除术后CS患者的研究中,术后糖皮质激素补充方案为术后24 h内,每小时给药1次(前6 h,每小时给予氢化可的松30 mg,后18 h每小时给予氢化可的松10 mg);术后第1天一次性给予氢化可的松200 mg;术后第2天一次性给予氢化可的松100 mg,并在此基础上每6 h一次给予口服制剂;术后第3天开始,仅给予口服制剂,并逐渐减量;双侧肾上腺切除术者从术后第3天开始每日加服氟氢可的松0.1 mg。氟氢可的松主要具有盐皮质激素样作用,而糖皮质激素样作用较弱,主要用以维持患者的水电解质平衡。Shen等[16]在研究中术前给予氢化可的松100 mg静滴,术后每8 h给予100 mg,3 d后减量。鉴于氢化可的松的半衰期为80~144 min,生物学作用半衰期约为8~12 h,因此,每日1次的给药方案对于双侧肾上腺切除术后的患者是不可取的;而以每8 h 1次给予氢化可的松是合理的给药方法,可能有助于预防并治疗肾上腺危象;此外,鉴于EAS患者一般术前皮质醇水平非常高,因此,每次给药剂量也应相应加大。总之,EAS患者行双侧肾上腺切除术后的糖皮质激素补充,应遵循个体化治疗原则,应尽量避免因给药频率不合理或虽按频次补充,但因补充剂量不足而导致术后皮质醇水平较术前断崖式下降,而导致皮质醇相对不足引发肾上腺危象。同时,对于双侧肾上腺切除术后,不管采用何种激素补充方案,患者一旦出现相关的临床表现,应首先考虑到糖皮质激素相对不足引起的肾上腺危象的可能,及时调整激素补充方案。值得注意的是,EAS患者行双侧肾上腺切除术后糖皮质激素补充剂量、频率的确定,尚缺乏大样本的临床研究证据,因此,有必要进一步进行大样本研究。
综上,我们报道了1例因EAS行双侧肾上腺切除术后于ICU监护期间发生肾上腺危象的患者。该病例提示EAS患者在行双侧肾上腺切除术后,合理的糖皮质激素补充方案是预防体内激素水平波动引发肾上腺危象的关键。在补充激素的条件下,如患者出现低血压、休克、高热、血氧饱和度下降等相关症状,应考虑糖皮质激素相对不足导致的肾上腺危象可能,应及时调整激素补充的剂量及频次。我们希望此病例能为今后临床工作提供宝贵的经验。