肝移植术后移植物抗宿主病诊治1 例
2022-11-21李君范铁艳陈虹徐光勋
李君,范铁艳,陈虹,徐光勋
(清华大学附属北京清华长庚医院肝胆胰中心,北京 102218)
移植物抗宿主病(graft versus host disease,GVHD)是肝移植术后的一个少见并发症,是指供者移植物中的T 淋巴细胞对受者的组织器官发动异常的细胞毒攻击,主要攻击皮肤、黏膜、消化道、造血组织,临床表现有发热、皮疹、腹泻等,其病死率极高,患者多死于败血症、多器官功能衰竭、消化道出血。现报道1 例肝移植术后诊断GVHD 并成功救治的患者。
1 临床资料
患者58 岁男性,主诉为“二次肝移植术后28 d,发热3 d”。患者28 d 前因移植肝肝癌复发行第二次肝移植手术,供体年龄44 岁。术中及术后第3 天巴利昔单抗20 mg 诱导,术中甲泼尼龙500 mg,后续逐渐减量,术后第2 日加用他克莫司2 mg,Q12 h、吗替麦考酚酯0.5 g,Q12 h 抗排斥反应治疗,监测他克莫司浓度4.4 ng/ml 左右,术后第8 日加用西罗莫司2 mg,Qd,雷帕霉素浓度3.5 ng/ml 左右。本次入院前糖皮质激素已停用,无新增可疑药物,无增强CT 或核磁检查史,抗排斥反应方案为:他克莫司2 mg,Q12 h,西罗莫司2 mg,Qd,吗替麦考酚酯0.5 g,Q12 h。入院前3 d(术后25 d)患者出现发热,最高38.2℃,伴有躯干部大量皮疹(图1),部分融合成片,无咽痛、咳嗽,无腹痛、腹泻、黑便、血便,无泌尿系症状。既往7 年前因乙肝肝硬化、肝癌行原位肝移植术,无丙肝、糖尿病病史。
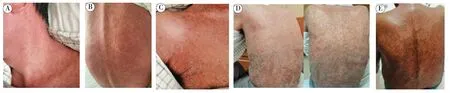
图1 皮疹改变
住院期间主要表现为高热、皮疹、意识模糊、记忆力、定向力下降,治疗过程中出现消化道出血。入院后主要检查结果:血常规提示三系降低(白细胞最低1.10×109/L、血红蛋白最低75 g/L、血小板最低13×109/L);肝肾功正常;巨细胞病毒-IgM(cytomegalovirus-IgM,CMV-IgM)、pp65、DNA 正常;EB 病 毒-IgM(Epstein Barr virus-IgM,EBVIgM)、DNA 正常,真菌G 试验、GM 试验及结核γ-干扰素(interferon-γ,IFN-γ)释放试验均为阴性。铁蛋白为2510.93 μg/L(正常:21.81 ~274.66)。他克莫司浓度为2.20 ng/ml,CD4 计数为252 cells/μl。CRP、PCT 不高。大小便常规正常。TH1/TH2 相关细胞因子白细胞介素(interleukin,IL)IL-2、IL-4、IL-6、IL-10、IFN-γ、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)正常。肝脏超声未见异常。胸部CT 未发现明显肺部感染改变。头颅MRI 提示:脑白质脱髓鞘改变,老年性脑改变。骨穿提示:骨髓早期造血增生减低(图2)。皮肤活检:少许皮肤组织,表皮角化过度,真皮内见个别淋巴细胞浸润(图3)。行肝穿刺活检组织与患者外周血STR 分析,结果提示患者移植后供者细胞占2.43%,表现为微嵌合状态。
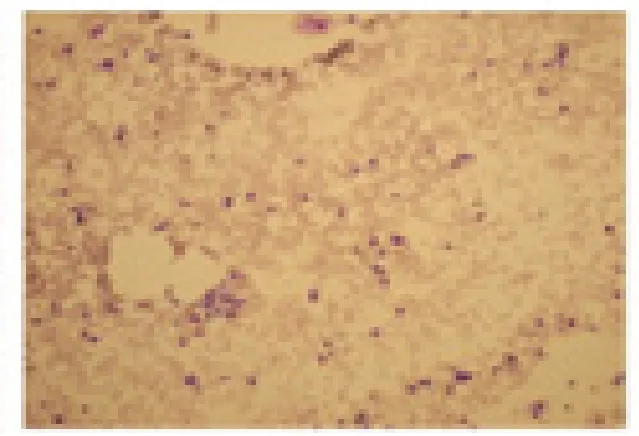
图2 发病1 个月时骨穿提示骨髓早期造血增生减低(Wright-Giemsa 染色,×100)
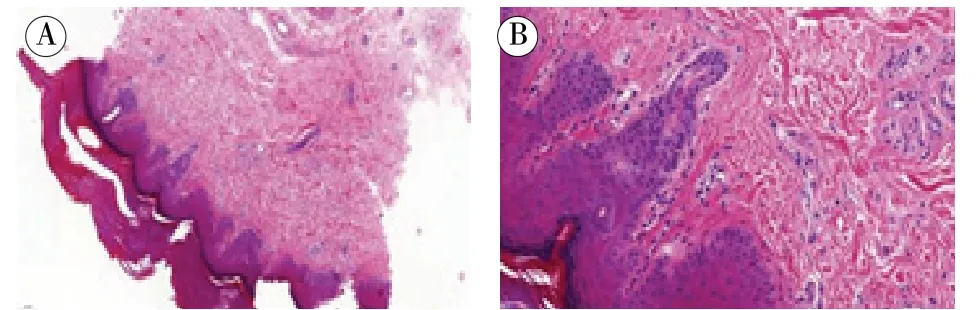
图3 第一次皮肤活检病理图
结合患者临床表现及嵌合体检查、皮肤活检,诊断考虑GVHD,停用抗排斥反应药物,给予丙球20 g/d 静滴,同时甲强龙60 mg/d 起始剂量,逐渐减量,并给予预防性抗细菌(G+球菌、G-杆菌)、抗真菌及抑酸、口服联合静脉用止血药物、输注红细胞及血小板、升血小板、升白细胞等治疗,患者皮疹逐渐好转,开始出现黑色素沉着,体温高峰下降,消化道出血好转。因经济原因在人免疫球蛋白减量过程中,患者皮疹较前增多,在黑色素沉着的皮肤上新出现点片状红色斑疹,伴有皮肤皲裂,再次行皮肤活检提示:皮肤组织,表皮角化过度,可见单个角化不良并坏死细胞,上皮脚下延融合,基底细胞液化变性,真皮浅层血管及附属器周围淋巴细胞浸润,多量嗜色素细胞沉积(图4)。考虑GVHD 未完全控制,丙球恢复原始剂量,暂缓激素减量,同时给予羟氯喹软膏和维生素E 乳膏交替外用,治疗15 d 后,患者体温正常,皮疹减退,皲裂改善,开始脱皮屑,无发热、新发皮疹,记忆力、定向力有所恢复,皮肤脱屑后留下大面积黑色素沉着(图1E)。距发病2 个半月时,患者肝功转氨酶开始轻度升高,考虑排斥反应可能,从他克莫司0.5 mg,Q12 h 起始,逐步恢复抗排斥反应药物,患者无不适症状,肝功能正常,好转出院,出院时他克莫司1 mg, Q12 h、麦考酚钠360 mg ,Q12 h、泼尼松5 mg ,Qd。
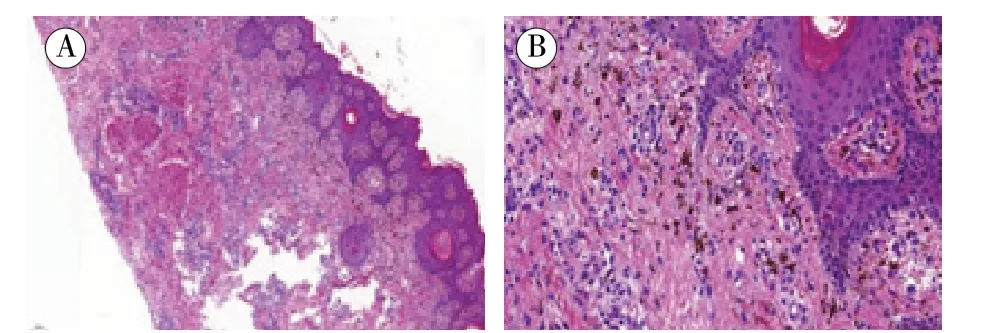
图4 第二次皮肤活检病理图
2 讨 论
GVHD 的发生是由于具有免疫功能的供体细胞识别受体细胞为外来细胞,导致供体T 淋巴细胞的活化、增殖和克隆性扩增,对受体组织和器官发起破坏性的免疫反应。GVHD 的发生需要以下3 个条件:① 具有免疫能力的淋巴细胞来源。② 供体与宿主之间的抗原相容性差异。③ 宿主不能排斥供体淋巴细胞[1]。在实体器官移植中,最常发生的是小肠移植,其次是肝移植,肺移植、肾脏移植比较少见[2]。根据发病时间不同,GVHD 分为急性(acute graft versus host disease,aGVHD)和慢性两类,aGVHD往往发生在移植后100 d 内。肝移植术后GVHD 的发生率为0.5% ~ 2%,病死率高达85%[3],主要死亡原因有败血症、多器官功能衰竭、消化道出血等[2]。
在肝移植受者中,GVHD 的发生往往与以下危险因素有关,如年龄、种族、人类白细胞抗原(human leukocyte antigen,HLA)配型、肝癌、再次移植、糖尿病、酒精性肝病、自身免疫性肝炎、供受者年龄差、丙型肝炎病毒(hepatitis C virus,HCV)感染、移植前输血、排斥反应史等[2,4-6]。皮肤、肠道、骨髓是最常受累的器官,临床主要表现为发热、皮疹、全血细胞降低、胃肠道症状(腹泻)等[6],少数有肾脏、中枢神经系统受累。GVHD 患者往往容易合并感染,出现发热时需要鉴别是感染导致的还是与GVHD 本病相关。其诊断比较困难,主要依赖于临床表现、嵌合体检查以及组织病理学证据[7-10]。本病例为再次肝移植患者,既往有乙肝、肝癌病史及输血史,供受体年龄差14 岁,免疫抑制剂浓度不高,但淋巴亚群计数明显低于正常范围,免疫力低,这些可能是其发生GVHD 的危险因素。患者临床主要表现为发热、皮疹和全血细胞降低,早期消化道症状不明显,根据临床症状入院时疑诊GVHD,进一步行嵌合体检查和皮肤病理活检后确诊,在感染方面进行了广泛排查,没有证据支持感染性发热。患者住院治疗近2 个月时出现消化道出血,因排斥反应药物已停用故不考虑排斥药物所致,因家属拒绝行胃肠镜检查,同时结合患者血小板低至13×109/L 的实际情况,给予PPI、止血药物、输血、升血小板等药物保守治疗后出血停止。
皮疹是GVHD 的最常见的表现之一,其与药疹很难鉴别,即使皮肤活检也很难得到理想的结果支持。急性移植物抗宿主病的皮肤表现为皮肤红斑、斑丘疹,通常开始于耳朵、手掌和脚底,早期也可累及颈部、面颊和背部,在晚期可进展为全身性麻疹样病变,伴有光滑或角化过度丘疹和色素沉着,在严重的GVHD 病例中,患者通常会出现全身性的、严重的红皮病、水疱或大量皮肤脱落[11-12]。病理改变主要是表皮交界处空泡样改变,表皮角质形成细胞凋亡,淋巴细胞外分泌等。本例患者发病前无可疑致敏药物史,刚开始皮疹比较轻,快速进展,不伴皮肤瘙痒,临床考虑药疹可能性小,第一次皮肤活检病理表现并不典型,皮疹反复后第二次皮肤病理与GVHD 的表现有一定吻合,通过全身治疗及局部用药后脱屑明显,随之皮疹消退,留下黑色素沉着。
神经系统症状方面,有文献报道了造血干细胞移植后表现为神经系统症状的GVHD,这些改变包括认知功能障碍、颅神经病变和癫痫发作,有些患者头部影像学检查正常,影像学异常的患者主要表现有出血或缺血、白质病变等[13]。另外,也有文献报道骨髓移植后GVHD 出现多发性肌炎、癫痫发作、意识改变、语言障碍等[13-15]。本例患者在住院期间有记忆力、定向力下降,MRI 提示脑白质脱髓鞘改变,我们不能确定是GVHD 引起的神经系统损害还是脑白质改变引起的症状,但患者病情好转出院后这些情况有明显改善。
在骨髓移植GVHD 受者中往往有肝脏受累,而肝移植物抗宿主病受者的肝功几乎都是正常的,这是因为移植物肝脏和导致GVHD 的免疫细胞都来源于供体,不会成为GVHD 的攻击目标[16-18]。本例患者停用抗排斥反应药物2 个月肝功一直正常,直到GVHD 症状完全缓解时,才出现转氨酶升高,加用排斥反应药物后恢复正常,原因考虑为GVHD 停用抗排斥反应药物后受者免疫力恢复,开始排斥移植物。
GVHD 在治疗方面也有争议,缺乏有效的标准治疗方案。糖皮质激素被认为是治疗GVHD 的主要方法[3]。 另外,也有文献报道联合使用ATG、IL-2 拮抗剂(巴利昔单抗、达克利单抗)、CD2 抑制剂(阿法西普)或者TNF-a 抑制剂(英夫利昔单抗)等药物也用于GVHD 的治疗[2,6]。Murali 等[2]总结的GVHD 个案系列中提到的治疗方案有:① 单用类固醇激素(未提及使用CNI 或增加CNI 剂量),类固醇激素联用IVIG 或硫唑嘌呤或CNI 剂量增加。② 单用胸腺球蛋白ATG,或者ATG 联用类固醇激素,或者ATG、类固醇激素、CNI 三联用药。③ IL-2 拮抗剂联合激素,或者加ATG/CNI 三联用药。④ 其他方案,包括阿法西普与激素、ATG 联用,TNF-α 抑制剂与激素、ATG 联用,或者利妥昔单抗±ATG±IL-2 拮抗剂等,在存活的37 例患者中有单用激素4 例,同时有CNI 剂量增加3 例,ATG联合激素4 例,IL-2 拮抗剂联合激素5 例,阿法西普联合激素及ATG 7 例,TNF-α 抑制剂联合激素、ATG 4 例,这都说明了激素为基础治疗GVHD的重要地位。而增加免疫抑制剂会导致败血症致死的风险增高[2],对HSCT 后GVHD 患者进行的一项研究表明,使用英夫利昔单抗显著增加非念珠菌侵袭性真菌感染的风险[19]。 也有文献报道使用糖皮质激素、他克莫司减量以及联合巴利昔单抗治疗过程中,患者出现了CMV 性视网膜炎等感染并发症[20]。部分学者认为,减少或停用免疫抑制可以帮助受者免疫系统自身重建恢复,有助于宿主对抗移植物来源淋巴细胞的免疫反应,同时也能减少感染风险[3,21-22]。在排斥反应风险方面,有文献报道,对于外周嵌合超过10%的患者,减少或停用免疫抑制剂并不会增加排异风险[23]。本例患者嵌合率不高,监测CD4 淋巴细胞计数远低于正常,提示患者免疫力低下明显,预估发生排斥反应的风险低,因此采取的治疗方案是在糖皮质激素治疗的基础上,停用CNI、西罗莫司和吗替麦考酚酯排斥反应药物,同时联合静脉用丙种球蛋白的方案,治疗过程中加强肝功和淋巴亚群计数监测,肝功在前2 个月内始终正常,免疫力低,GVHD 症状缓解后停用IVIG,糖皮质激素逐步减量,此后患者肝功转氨酶才出现升高趋势,及时恢复抗排斥反应药物,根据肝功及淋巴亚群情况,逐步恢复抗排斥反应药物。另外,在整个治疗过程中,即便没有明确感染,我们还是预防性使用了覆盖球菌、杆菌、真菌等抗感染药物,避免患者出现感染并发症。目前患者已出院1 年余,无发热、皮疹不适,皮肤色素沉着逐渐减退,肝功正常。
总之,GVHD 是肝移植术后的少见并发症,病死率高,临床表现不一,诊断困难,组织病理学检查非常必要,而嵌合体检测是诊断的重要依据,目前尚缺乏确切有效的治疗方案,早期诊断、及时治疗以及GVHD 病情的严重程度是影响预后的重要因素。
