西式快餐条件下煎炸油氧化稳定性及其不饱和脂肪酸氧化动力学研究
2022-11-11胡明明吴思纷张国文
胡明明,张 权,吴思纷,张国文
(1.江西师范大学国家淡水鱼加工技术研发专业中心,江西南昌 330022;2.江西师范大学生命科学院,江西南昌 330022;3.南昌大学食品科学与技术国家重点实验室,江西南昌 330047)
在煎炸过程中,食用油因长时间高温受热,加上周围水、氧气及食品组分的存在,会发生各种复杂的化学反应,产生大量有害物质,生成大量有害产物,包括非挥发性的游离脂肪酸、非皂化产物、环状化合物、三酰甘油氧化聚合物等以及挥发性的烃类、醛、酮、呋喃、羧酸等,从而使食用油的营养价值大大降低,影响了煎炸食品的品质和安全性,并危害消费者的健康[1-3]。影响煎炸油的稳定性因素很多,包括内在的和外在的,其中最主要的是煎炸油的脂肪酸组成。植物油通常由饱和脂肪酸(SFA,如硬脂酸、棕榈酸等)和不饱和脂肪酸(UFA,如亚麻酸、亚油酸及油酸等)组成。与SFA相比,UFA更容易氧化,这也是导致油脂品质劣变的主要原因[4-6]。UFA中双键的数量很大程度上决定了油脂的氧化速率。而亚麻酸、亚油酸及油酸等UFA双键数目及双键分布的位置不同,其氧化速率也各有差异[7-8]。据报道,纯的油酸、亚油酸及亚麻酸酯的氧化速率比值约为1:12:25[9]。在煎炸过程中,不同植物油的煎炸稳定性受其含有的亚麻酸、亚油酸及油酸影响较大。所以,探讨煎炸油中UFA的热氧化动力学规律对研究煎炸油的煎炸稳定性具有重要意义。
目前,关于食用油的氧化稳定性及动力学研究已有较多报道。张丽等[10]采用热重分析法评估了美藤果油和普洱茶籽油的热氧化稳定性,并对主要脂肪酸的氧化动力学进行了研究。刘姗姗等[11]研究不同储藏温度下猪油的氧化规律,并建立氧化指标和储藏时间及储藏温度间的氧化动力学模型。易醒等[12]研究了冷/热榨紫苏子油的氧化稳定性及其α-亚麻酸氧化动力学。李孟俊等[13]利用近红外光谱技术研究了四种植物油在常温条件下的氧化动力学规律。然而,在油炸过程中,通常将油温加热至150~190 ℃,相比常温储藏或低温热加工,高温油炸时食用油氧化更为剧烈。目前,关于煎炸条件下食用油的氧化动力学方面的研究鲜有报道。
本研究以5种常用煎炸油(棕榈油、大豆油、菜籽油、葵花籽油及稻米油)为研究对象,以薯条为煎炸原料,在模拟实际西式快餐煎炸条件下连续煎炸7 d,每天煎炸结束时取样,对5种煎炸油在煎炸过程中的氧化稳定性及其主要UFA(亚麻酸、亚油酸、油酸)的氧化动力学进行研究,以期为西式快餐条件下煎炸过程中煎炸油的氧化规律提供理论依据。
1 材料与方法
1.1 材料与仪器
大豆油、菜籽油、棕榈油、稻米油、葵花籽油当地商场;冷冻薯条 内蒙古蓝威斯顿薯业有限公司;甲醇、异辛烷 均为色谱纯,上海国药集团化学试剂有限公司;氢氧化钾、硫酸氢钠、乙醚、异丙醇、石油醚、甲基叔丁基醚、冰乙酸、硫代硫酸钠、三氯甲烷、p-茴香胺、无水硫酸钠 均为分析纯,上海国药集团化学试剂有限公司;脂肪酸甲酯混标(C8~C24)标准品 纯度>99%,美国 Sigma公司。
OFE-28A型电热炸炉 上海一喜食品机械有限公司;Agilent 6890气相色谱仪 美国Agilent公司;TU-1930紫外分光度计 北京普析公司;AL204-IC电子天平 梅特勒-托利多仪器(上海)有限公司;W201恒温水浴锅 上海申胜生物技术有限公司;DHG-9240A电热鼓风干燥箱 上海精宏实验设备有限公司;VORTEX-6涡流振荡器 海门其林贝仪器制造有限公司。
1.2 实验方法
1.2.1 煎炸过程 模拟实际快餐煎炸条件,将13 L煎炸油(大豆油、菜籽油、棕榈油、稻米油、葵花籽油)分别倒入煎炸锅中,加热并保持油温在170±5 ℃,称取市售冷冻薯条200 g,放入热油中炸3 min(中途1.5 min左右提起炸篮翻动一次)后捞起,每小时炸5批,每天炸12 h,连续煎炸7 d。每煎炸6 h后过滤一次,过滤时,停止加热,并清洁油炸锅内壁,向滤油槽加入60 g滤油粉(滤油2次后更换),搅拌5 min,抽回至油缸中,滤油后添加新鲜油至起始刻度线(13 L)处。每天煎炸完成后,待油冷却,用棕色瓶收集油样250 mL,存放于-20 ℃冰箱,供进一步分析。
1.2.2 脂肪酸组成(FAC)分析 煎炸油脂肪酸组成检测参照AOCS检测方法Ce 1f-96及文献[14]。将油样甲酯化后,用气相色谱仪分析脂肪酸组成。气相色谱条件:CP-Sil 88毛细管柱(100 m×0.25 mm,0.2 μm),检测器为氢火焰离子化检测器(FID);以高纯氮气为载气,流速1.3 mL/min,进口和检测器温度分别设置为160、250 ℃。程序升温:160 ℃柱温条件下保持5 min,并以10 ℃/min升温到220 ℃。氢气和空气流速35 mL/min、375 mL/min,分流比为50:1,进样量为1 μL。通过与脂肪酸甲酯标准品的色谱峰谱图对照定性,采用面积归一化法确定脂肪酸的相对含量(以峰面积的百分数表示)。
1.2.3 煎炸过程中煎炸油氧化指标分析 过氧化值(PV)的测定:参照GB 5009.227-2016中的滴定法;茴香胺值(p-AV)和碘值(IV)的测定分别参照GB/T 24304-2009、GB 5532-2008。
1.2.4 煎炸过程中煎炸油不饱和脂肪酸氧化动力学模型的研究
1.2.4.1 零级反应动力学模型 煎炸过程中,若脂肪酸的变化与初始含量没有关系,则其随煎炸时间的变化符合零级反应动力学模型,其相应的反应速率方程可表述为:

通过积分后,可得到:

因此,假设以Ct对t作图后的图形是直线,那么证明其氧化反应为零级反应[15]。
式中,C表示脂肪酸含量;t表示煎炸时间;C0、Ct分别表示脂肪酸的初始含量及在煎炸时间(t)时的含量;k0为氧化反应速率常数。
1.2.4.2 一级反应动力学模型 煎炸过程中,若脂肪酸随煎炸时间的变化符合一级反应动力学模型,则其相应的反应速率方程可表述为:

通过积分后,可得到:

因此,假设以ln[Ct]对t作图后的图形是直线,那么证明其氧化反应为一级反应[16]。
式中,C表示脂肪酸含量;t表示煎炸时间;C0、Ct分别表示脂肪酸的初始含量及在煎炸时间(t)时的含量;k为氧化反应速率常数。
1.2.4.3 二级反应动力学模型 煎炸过程中,若脂肪酸随煎炸时间的变化符合二级反应动力学模型,则其相应的反应速率方程可表述为:

通过积分后,可得到:

因此,假设以1/Ct对t作图后的图形是直线,那么证明其氧化反应为二级反应[16]。
式中,C表示脂肪酸含量;t表示煎炸时间;C0、Ct分别为脂肪酸的初始含量及在煎炸时间(t)时的含量;k为氧化反应速率常数。
1.3 数据处理
所有实验做3次平行,结果以均值±标准差(M±SD)表示。利用Excel2010对数据进行处理作图,采用IBM SPSS Statistics 20.0对数据进行单因素方差分析(ANOVA),P<0.05表示存在显著性差异。
2 结果与分析
2.1 煎炸前煎炸油的脂肪酸组成比较
表1为5种煎炸油煎炸前的脂肪酸组成,从表1可以看出,不同煎炸油的脂肪酸组成各有不同,棕榈油、大豆油和稻米油中的主要脂肪酸是棕榈酸(分别为46.83%、11.75%、16.73%)、油酸(分别为37.41%、24.34%、41.39%)和亚油酸(分别为9.70%、53.65%、37.51%)。然而,菜籽油和葵花籽油的主要脂肪酸是油酸(分别为 60.86%、29.22%)和亚油酸(分别为20.11%、60.36%)。整体而言,5种煎炸油的SFA含量范围为6.47%~52.54%,单不饱和脂肪酸(MUFA)含量范围为 24.34%~60.86%,多不饱和脂肪酸(PUFA)含量范围为9.77%~60.59%。其中,棕榈油中以 SFA(53.44%)为主,其次是 MUFA(37.49%)和PUFA(9.77%),而大豆油、菜籽油、葵花籽油和稻米油中以UFA为主,只含有少量的SFA(6.47%~18.18%)。通常,UFA氧化是引起油脂品质劣变主要原因之一,5种煎炸油中主要UFA均为十八碳UFA,即油酸、亚油酸、亚麻酸(C18:3)。因此,对煎炸油中主要UFA(油酸、亚油酸及亚麻酸)的氧化动力学研究具有重要意义。据研究报道,油脂在加工贮藏过程中,油脂的氧化一般都符合零级或者一级动力学模型[17]。
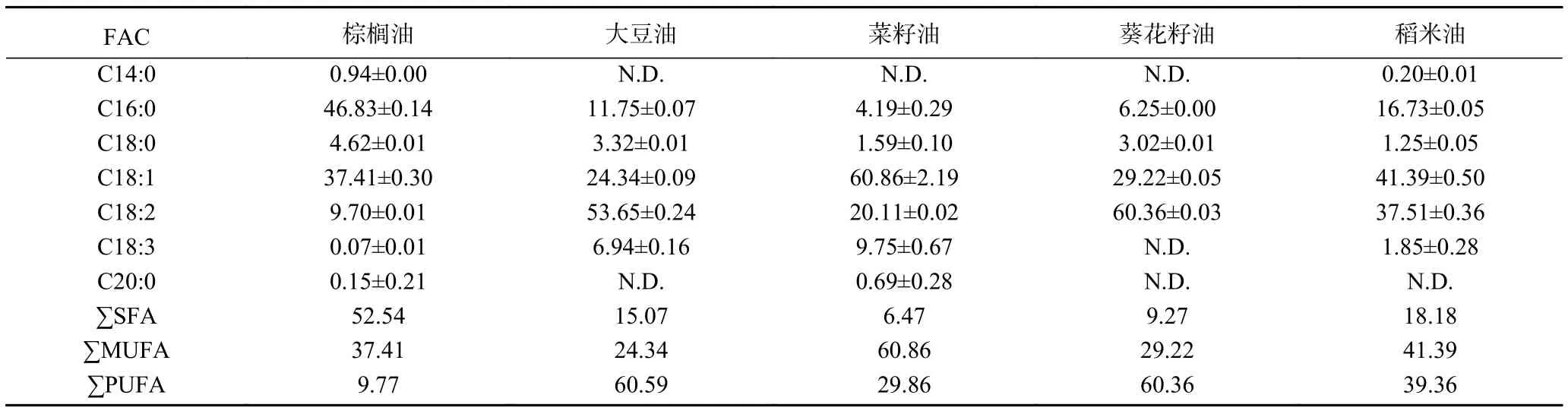
表1 5种煎炸油煎炸前主要脂肪酸组成及含量Table 1 Fatty acid composition of five frying oils before frying
2.2 煎炸过程中煎炸油的氧化指标分析
2.2.1 过氧化值(PV)的变化 PV是评价煎炸油在氧化早期阶段所含过氧化物或氢过氧化物最常用的方法。煎炸过程中PV的增加,说明煎炸过程中氢过氧化物的形成是早期氧化的结果。然而,氢过氧化物是不稳定的,在油炸条件下会自发地分解成其他次级产物。此外,随着煎炸油的继续氧化变质,氢过氧化物可能会分解,形成羰基和醛类化合物,这可能导致PV下降[18]。从图1可以看出,在整个煎炸过程中,5种煎炸油PV呈波动变化的趋势,没有明显的变化规律。有报道表明,在煎炸过程中,不同植物油PV的变化存在差异,Waghmare等[19]发现植物油在煎炸过程中PV随煎炸时间的延长呈明显上升的趋势,而更多研究发现在煎炸过程中PV呈波动变化的不规则趋势[20],本研究结果同后者相一致。在煎炸过程中,葵花籽油相对其他四种植物油PV较高,且波动幅度较大,这可能与葵花籽油为物理压榨工艺所制得有关,压榨法经过高温处理使得抗氧化物质受到较多的损失[21],导致油脂在煎炸时更容易氧化。刘玉兰等[22]比较了压榨和浸出工艺对油莎豆油品质影响的研究,结果也发现,压榨法制取的油莎豆油PV(平均值为2.97 mmol/kg)明显高于溶剂浸出法(平均值为0.39 mmol/kg)。

图1 五种煎炸油煎炸过程中过氧化值的变化Fig.1 Changes in PV of five frying oils during frying
2.2.2 茴香胺值(p-AV)的变化 煎炸过程中氢过氧化物的热分解会产生大量的次级氧化产物,p-AV反映的是这些降解产物形成的非挥发性不饱和醛类化合物的含量,常用来评价煎炸油氧化后的二次生成物醛类的含量,对监测煎炸油品质意义重大[23]。由图2可以看出,5种煎炸油的p-AV在煎炸的前2 d显著升高(P<0.05),且均在第4 d基本达到稳定,此后略有降低,较低的p-AV可能与煎炸过程中每天滤油并添加新鲜油有关,且煎炸过程中部分醛类物质高温条件下受热分解及被薯条吸附也会使p-AV降低。此外,还可以看出,在煎炸4 d后p-AV达到稳定时,五种煎炸油p-AV增加的幅度顺序依次是:大豆油(49.16 unit)>葵花籽油(44.22 unit)>菜籽油(42.64 unit)>稻米油(33.20 unit)>棕榈油(24.46 unit)。整个煎炸过程中,棕榈油的p-AV显著低于其他四种植物油(P<0.05),这可能是由于棕榈油中的脂肪酸绝大多数是相对稳定的SFA和MUFA,而更容易氧化的PUFA(9.07%)含量较少,这和 Przybylski等[24]发现改性后低PUFA的菜籽油和大豆油比常规菜籽油和大豆油p-AV更低的结果一致。而稻米油虽然含有较高含量的PUFA,但其p-AV相对大豆油、菜籽油、葵花籽油更低,这可能和稻米油中有较高含量的维生素E、谷维素和植物甾醇等抗氧化成分有关[25]。

图2 五种煎炸油煎炸过程中茴香胺值的变化Fig.2 Changes in p-AV of five frying oils during frying
2.2.3 全氧化值(TOTOX)的变化 在煎炸过程中,油脂氧化是一个复杂的动态变化过程,由于PV和p-AV分别只适合评估油脂的初级、次级氧化阶段。因此,油脂的氧化程度常用 TOTOX(即 TOTOX=2PV+p-AV)来综合评估[26]。5种煎炸油的TOTOX值如图3所示,与p-AV类似,在煎炸的前2 d,4种煎炸油的TOTOX都急剧增加,且在油炸第4 d后基本达到稳定,此后略有降低。从图中可以明显看出在煎炸4 d后,棕榈油的TOTOX值增加量(26.02 unit)显著低于稻米油(31.66 unit)、菜籽油(42.58 unit)、葵花籽油(47.15 unit)和大豆油(50.06 unit)(P<0.05),表明棕榈油的氧化稳定性较其他四种油好,这主要是因为其他四种油中含有相对较高的UFA含量,尤其是PUFA,如亚油酸和亚麻酸。相比之下,棕榈油含有大量的SFA(棕榈酸)和MUFA(油酸),研究表明PUFA(亚麻油酸和亚麻酸)的相对氧化速率至少高于 MUFA(油酸)十倍[8]。

图3 五种煎炸油煎炸过程中全氧化值的变化Fig.3 Changes in TOTOX of five frying oils during frying
2.2.4 碘值(IV)的变化 IV可以反映油脂的不饱和程度。不饱和度越高的油脂,IV越大。在煎炸过程中,煎炸油IV会因UFA不饱和键处发生氧化及聚合反应而下降[27]。如图4所示,棕榈油的IV在整个煎炸过程几乎保持不变,而其他4种煎炸油随煎炸时间的延长,IV均逐渐下降。煎炸结束后,棕榈油的 IV 变化量(2.22 g/100 g)显著(P<0.05)低于稻米油(7.99 g/100 g)、菜籽油(9.41 g/100 g)、大豆油(13.48 g/100 g)和葵花籽油(13.84 g/100 g),表明棕榈油相比其他四种植物油在煎炸过程中更不容易氧化,这可能和棕榈油不饱和度较低,具有更长的氧化诱导周期有关[18]。同样的是,Abdulkarim等[18]也发现高油酸辣木籽油、大豆油和菜籽油的IV在煎炸过程中也呈逐渐下降趋势,且高油酸辣木籽油下降速率更慢,这在很大程度上归因于高油酸辣木籽油中含有大量的MUFA和少量的PUFA。

图4 五种煎炸油煎炸过程中碘值的变化Fig.4 Changes in IV of five frying oils during frying
2.3 煎炸油在煎炸过程中不饱和脂肪酸的氧化动力学研究
2.3.1 亚麻酸的氧化动力学级数及速率常数的确定表2为五种煎炸油在煎炸过程中亚麻酸含量变化。由于棕榈油和葵花籽油中的亚麻酸含量较低或未被检出,故主要研究大豆油、菜籽油及稻米油在煎炸过程中亚麻酸的氧化动力学规律。从表2可以看出,三种煎炸油中的亚麻酸随煎炸时间的增加而逐渐降低,其中,菜籽油中的亚麻酸含量相对最高。煎炸7 d后,大豆油、菜籽油和稻米油中亚麻酸含量降低显著(P<0.05),分别减少了25.65%、15.69%、20.00%。曹君[28]在研究大豆油、菜籽油、紫苏油等8种植物油在加热过程中的氧化规律时,发现亚麻酸含量下降不明显(≤1.06%),这可能与其烘箱加热加速氧化试验所用温度较低(62 ℃)有关。

表2 煎炸过程中煎炸油中亚麻酸含量的变化(%)Table 2 Changes in linolenic acid percentages of frying oils during frying (%)
表3为大豆油、菜籽油及稻米油在煎炸过程中亚麻酸含量(y)随煎炸时间(x)变化拟合后的回归方程结果。从表3中可以看出,通过比较三种煎炸油0级、1级反应动力学模型预测值和实验值决定系数R2,大豆油中亚麻酸的 0级R2值(0.943)和 1级R2值(0.944),以及菜籽油中亚麻酸的 0级R2值(0.941)和 1 级R2值(0.949)均大于 0.85,表明菜籽油和大豆油中亚麻酸的变化与0级、1级模型均有较好的拟合度,即与0级、1级反应动力学规律均相符;此外,ANOVA方差分析显著性值均小于0.05,说明建立的回归模型具有统计学意义。稻米油中亚麻酸的 0 级R2值(0.685)和 1 级R2值(0.674)均小于0.85,表明稻米油中亚麻酸的变化与0级、1级模型均有较差的拟合度,与0级、1级反应动力学规律均不相符。

表3 亚麻酸反应动力学模型的参数及决定系数Table 3 Parameters and determination coefficient of reaction kinetic model of linolenic acid
比较0级和1级模型的R2值发现,大豆油和菜籽油中亚麻酸氧化的1级反应动力学方程决定系数相比0级反应动力学方程决定系数略大,说明其降解规律略贴近指数变化规律(1级反应动力学模型);稻米油中的亚麻酸预测值和实验值间的相关性不好(R2<0.85)。
2.3.2 亚油酸的氧化动力学级数及速率常数的确定相比亚麻酸,煎炸油中含有更丰富的亚油酸(9.70%~60.36%)。表4为5种煎炸油在煎炸过程中亚油酸的含量变化,从表4可以看出,随着煎炸时间的延长,5种煎炸油中的亚油酸逐渐降低,其中,葵花籽油中的亚油酸含量相对最高,且下降速率最快。煎炸7 d后,棕榈油、大豆油、菜籽油、葵花籽油及稻米油中亚油酸的含量降低显著(P<0.05),分别减少了8.56%、12.49%、3.23%、19.32%、15.44%。

表4 煎炸过程中煎炸油中亚油酸含量的变化(%)Table 4 Changes in linoleic acid percentages of frying oils during frying (%)
表5为棕榈油、大豆油、菜籽油、葵花籽油及稻米油在煎炸过程中亚油酸含量(y)随煎炸时间(x)变化拟合后的回归方程结果。从表5中可以看出,通过比较5种煎炸油0级、1级反应动力学模型预测值和实验值决定系数R2,棕榈油中亚油酸的0级R2值(0.955)和 1 级R2值(0.957),菜籽油中亚油酸的 0 级R2值(0.986)和 1 级R2值(0.987),葵花籽油中亚油酸的 0 级R2值(0.918)和 1 级R2值(0.935),以及稻米油中亚油酸的0级R2值(0.918)和1级R2值(0.929)均大于0.85,表明棕榈油、菜籽油、葵花籽油及稻米油中亚油酸的变化与0级、1级模型均有较好的拟合度,即与0级、1级反应动力学规律均相符;而大豆油中亚油酸的0级R2值(0.812)小于0.85,而 1 级R2值(0.916)大于 0.85,表明大豆油中亚油酸的变化与1级模型有较好的拟合度,即与1级反应动力学规律相符;此外,ANOVA方差分析显著性值均小于0.05,说明建立的回归模型具有统计学意义。
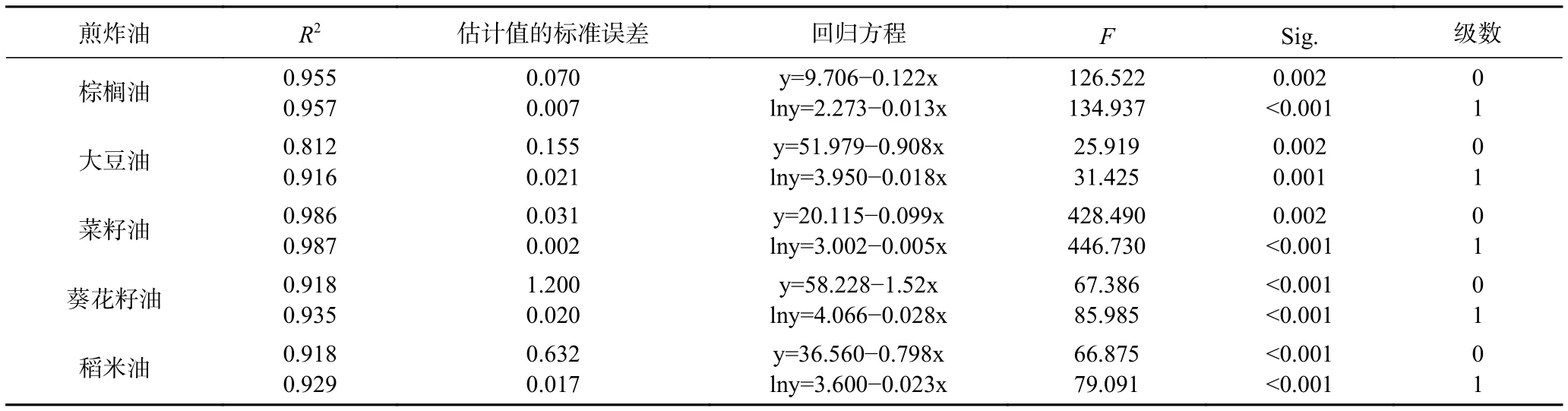
表5 亚油酸反应动力学模型的参数及决定系数Table 5 Parameters and determination coefficient of reaction kinetic model of linoleic acid
比较R2值,棕榈油、菜籽油、葵花籽油及稻米油中亚油酸氧化的1级反应动力学方程决定系数相比0级反应动力学方程决定系数略大,说明其降解规律略贴近指数变化规律(1级反应动力学模型)。
2.3.3 油酸的氧化动力学级数及速率常数的确定表6为5种煎炸油在煎炸过程中油酸的含量变化,从表6可以看出,随着煎炸时间的延长,棕榈油、大豆油及葵花籽油中的油酸逐渐增加,稻米油中的油酸先增加后减少,而菜籽油中的油酸则呈现逐渐减少的趋势。煎炸7 d后,棕榈油、大豆油、葵花籽油及稻米油中油酸含量增加显著(P<0.05),分别增加了7.30%、23.71%、13.52%、2.73%,菜籽油中油酸含量降低显著(P<0.05),减少了3.27%。通常,与亚油酸及亚麻酸相比,油酸的氧化速率远远要小。当煎炸油中同时存在MUFA和PUFA时,PUFA会先发生氧化降解反应。这是由于脂肪酸吸收氧原子的能力与其双键位置及数量有关。亚麻酸、亚油酸的吸收氧原子能力比油酸和SFA强很多[28]。根据5种煎炸油煎炸前的脂肪酸组成可知,大豆油和葵花籽油中的UFA以PUFA(亚油酸、亚麻酸)为主(约60%),PUFA不稳定而氧化使得油酸的增加幅度相对较大,煎炸7 d后油酸分别增加了23.71%、13.52%,而棕榈油中脂肪酸以SFA和MUFA为主(约90%),使得其比大豆油、葵花籽油更加稳定,煎炸7 d后油酸增加了7.30%,这和前人报道结果一致[29]。值得注意的是,煎炸过程中PUFA(亚油酸、亚麻酸)含量的减少并没有导致菜籽油和稻米油中的油酸增加,甚至反而呈现降低的趋势,这说明在煎炸薯条过程中,油酸本身作为反应底物与薯条中的其他成分反应,使得油酸含量随煎炸时间逐渐减少或呈波动变化趋势[30]。另外,预炸薯条中含有脂肪(油酸含量为38.82%)在煎炸过程中会不断进入煎炸油中,这可能也是菜籽油和稻米油中的油酸出现下降趋势的原因之一。此外,还注意到,菜籽油、稻米油中油酸含量基数相对较大,这可能使得其油酸的相对变化幅度较其他3种煎炸油小。
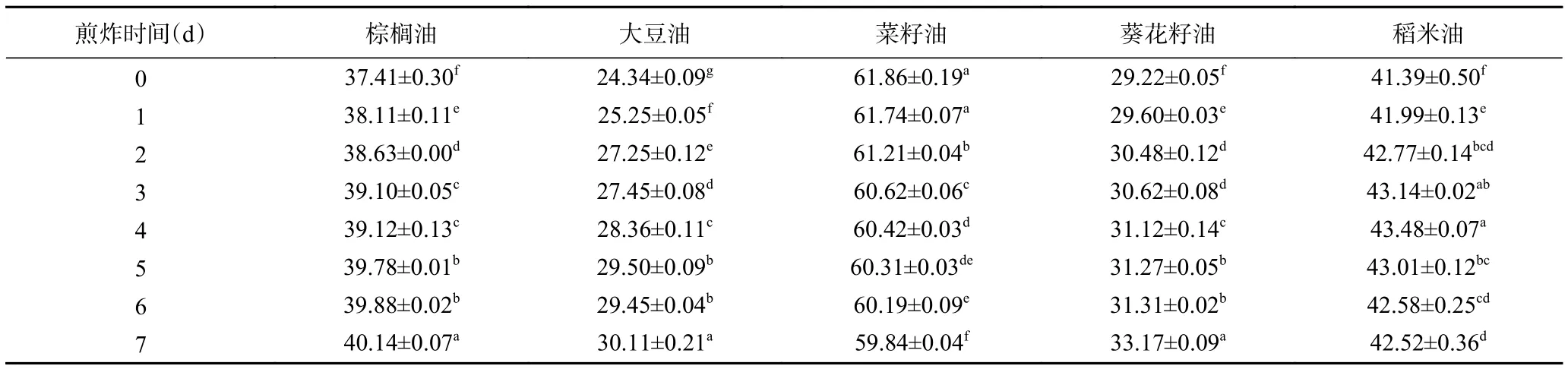
表6 煎炸过程中煎炸油中油酸含量的变化(%)Table 6 Changes in oleic acid percentagesof frying oils during frying (%)
表7为棕榈油、大豆油、菜籽油、葵花籽油及稻米油在煎炸过程中油酸含量(y)随煎炸时间(x)变化拟合后的回归方程结果。从表7中可以看出,通过比较5种煎炸油0级、1级反应动力学模型预测值和实验值决定系数R2,棕榈油中油酸的0级R2值(0.955)和 1 级R2值(0.951),大豆油中油酸的 0 级R2值(0.943)和 1 级R2值(0.920),菜籽油中油酸的0 级R2值(0.943)和 1 级R2值(0.944)以及葵花籽油中油酸的 0 级 R2值(0.886)和 1 级R2值(0.894)均大于0.85,表明棕榈油、大豆油、菜籽油及葵花籽油中油酸的0级、1级模型拟合程度均较好,同时符合0级、1级反应动力学规律;此外,ANOVA方差分析显著性值均小于0.05,说明建立的回归模型具有统计学意义。稻米油中油酸预测值同实验值间存在较低的相关性(R2<0.28),没有统计学意义。
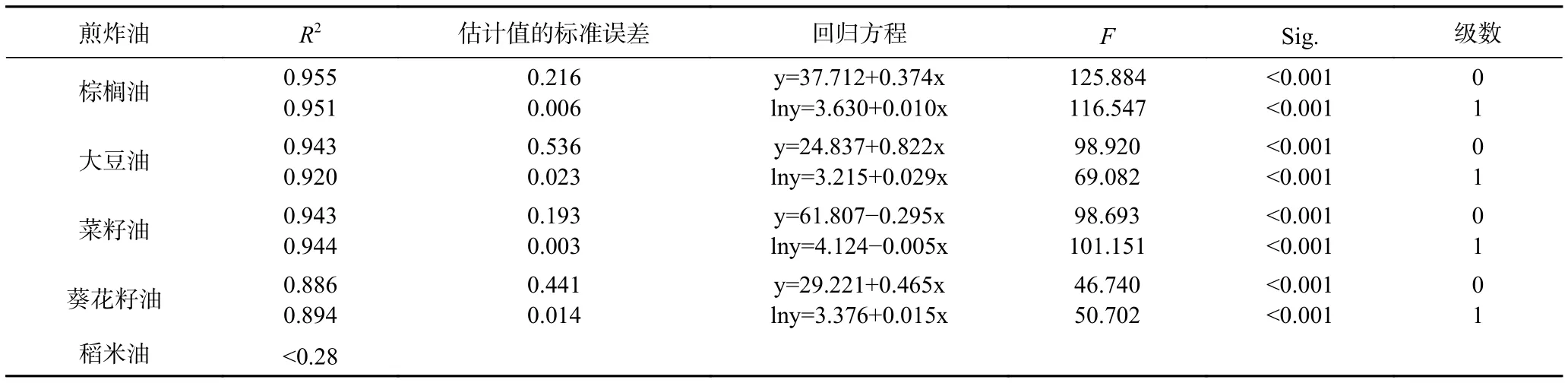
表7 油酸反应动力学模型的参数及决定系数Table 7 Parameters and determination coefficient of reaction kinetic model of oleic acid
比较R2值,棕榈油、大豆油中油酸氧化的0级反应动力学方程决定系数相比1级反应动力学方程决定系数略大,说明其氧化规律与线性变化规律(0级反应动力学模型)更为接近;同理,菜籽油、葵花籽油中油酸氧化规律与指数变化规律(1级反应动力学模型)更为接近。
通过研究煎炸油中主要UFA(亚麻酸、亚油酸、油酸)在煎炸过程中氧化速率常数,表明不同煎炸油中亚麻酸、亚油酸、油酸的氧化速率常数各有差异。当然,尽管理论上PUFA相对MUFA更容易氧化,但在实际的煎炸体系中,影响UFA氧化的因素除了脂肪酸本身的种类(双键数目及位置)外还有很多,比如脂肪酸在甘三酯中的位置、内源性抗氧化营养素(如维生素E、植物甾醇等)、煎炸食物的组分[31-32]。因此,还需要对煎炸油中的这些影响因素做进一步研究。
3 结论
本研究探讨了西式快餐煎炸条件下5种煎炸油在煎炸过程中的氧化稳定性及其主要UFA(亚麻酸、亚油酸及油酸)的氧化动力学模型。结果表明,相比其他4种煎炸油,棕榈油在煎炸过程中具有更好的氧化稳定性。菜籽油中亚麻酸、亚油酸、油酸,棕榈油和葵花籽油中亚油酸、油酸,大豆油中亚麻酸和油酸,稻米油中亚油酸的反应规律均同时符合0级和1级反应动力学模型,大豆油中亚油酸只符合1级反应动力学模型,且模型拟合程度均较好,可用来分析煎炸过程中亚麻酸、亚油酸、油酸的氧化反应动力学。此外,不同煎炸油中UFA的氧化分解速率各有差异,其受内源性抗氧化成分、脂肪酸组成、双键位置及数目等因素影响,因此,还需要对煎炸油中的这些影响因素做进一步研究。
