交互四元体系K+,NH4+//Cl-,H2PO4--H2O在313.15 K时相平衡研究
2022-10-18樊小娟邓文清李天祥
樊小娟,朱 静,邓文清,陈 艳,李天祥
(贵州大学化学与化工学院,贵州贵阳550025)
固-液相平衡是化工热力学的基础,对化学产品的生产、分离和纯化具有重要意义[1]。水溶肥的生产方式主要包括物理混合与化学合成两种方法[2-3]。其中,化学合成主要应用共结晶技术[4-5]。水溶肥相关组分的固-液相平衡数据和相图是研究其生产方式的基础。NH4H2PO4、KH2PO4、KCl、NH4Cl、(NH2)2CO 是生产水溶肥的主要原料,其多元固-液相平衡是结晶过程的基础,而共结晶过程的设计是基于精确溶解度数据和相图的分析。因此,要用共结晶法生产水溶肥,其固-液相平衡数据必不可少,而不同温度下多组分体系的固-液相平衡对多组分共结晶研究具有重要的指导意义。
本课题组已完成部分温度下相关体系的相平衡 研 究,胡 雪 等[6]研 究 了283.15 K 下 三 元 体 系(NH2)2CO-NH4H2PO4-H2O固液相平衡,结果表明该体系为简单共饱和型,有一个共饱和点、两条单变量曲线、3 个结晶区。黄林川等[7]研究了283.15 K下三元体系KH2PO4-CO(NH2)2-H2O 固液相平衡,结果表明,该体系有1 个共饱和点、2 条单变量曲线和3 个结晶区。杨家敏等[8]研究了283.15 K 下三元体 系KCl-NH4Cl-H2O 和KH2PO4-NH4H2PO4-H2O 固液相平衡,结果表明两个体系均有部分互溶的固溶体形成,相图均有一个共饱和点、两条单变量曲线和6 个相区。吴强等[9]研究了283.15 K 下三元体系KH2PO4-KCl-H2O、NH4H2PO4-NH4Cl-H2O 固液相平衡,结果表明两个三元体系均为简单共饱和型,无固溶体或加合物形成,每个相图包含1 个不变点、2条单变量曲线和3 个结晶区。王肖丽等[10]研究了298.15 K 下四元体系K+,NH4
+//H2PO4-,CO(NH2)2-H2O 固液相平衡,结果表明该体系中有1 个共饱和点、3 条单变量曲线、3 个结晶区。这些已完成的低温及常温下的固液相平衡研究为本文交互四元体系K+,NH4
+//Cl-,H2PO4--H2O研究提供了一定的基础。交互四元体系K+,NH4+//Cl-,H2PO4--H2O 在313.15 K 下的固-液相平衡的研究,包含了4 个三元 体 系,分 别 为KCl-KH2PO4-H2O[11]、NH4Cl-NH4H2PO4-H2O[12]、KH2PO4-NH4H2PO4-H2O[13]、KCl-NH4Cl-H2O。目前,该体系本课题已研究了283.15 K[14]和298.15 K[15]下的固-液相平衡。结果表明,该系统是一个含有固溶体的交互四元体系。然而,所研究的平衡数据只涵盖了低温、常温两个温度。温度范围不足以设计结晶过程。因此,本文研究了四元体系K+,NH4
+//Cl-,H2PO4--H2O 以及三元子体系KCl-NH4Cl-H2O 在313.15 K 下的固液平衡,并绘制了该体系的干盐相图和水图,为水溶肥的生产、相应的模型拟合提供必要基础数据。
1 实验部分
1.1 试剂及仪器
实验试剂:KH2PO4、NH4H2PO4、KCl、NH4Cl,均为分析纯;尿素,分析纯;实验过程中所用的水均为自制去离子水,电阻率为18.25 MΩ·cm。
实验仪器:BSM型电子天平(精度值为0.000 1 g);DC-4006 型低温恒温槽(精度值为±0.1 K);S10-3型恒温磁力搅拌器;TU-1810 型紫外可见分光光度计;X'Pert3 Powder 型X 射线衍射仪(XRD);GZX-9146MBE型电热鼓风干燥箱。
1.2 实验方法
实验采用等温溶解平衡法[16]。实验装置见文献[6],在整个实验过程中,系统温度由低温恒温槽保持在(313.15±0.1)K。根据次级体系溶解度数据,配制饱和溶液,加入一定量的另一种盐,并不断搅拌。体系恒温4 h 之后每隔1 h 取其上层清液进行分析,直到液相组成不再发生变化时,该体系达到溶解平衡。结果表明,该三元体系的平衡时间为8 h,四元体系为11 h。平衡后静置一定时间分别取上层清液和湿固相进行分析,得到液相和湿渣组成。
1.3 分析方法
采用甲醛法测定NH4+含量[17](相对偏差小于0.5%);采用钼锑抗比色法测定H2PO4-含量[18](相对偏差小于0.5%);采用铁铵矾指示剂法测定Cl-的含量[19](相对偏差小于0.5%);采用差减法计算K+的含量(相对偏差小于0.5%);采用湿渣法结合X 射线粉末衍射法测定平衡固相组成。实验中每个样本至少分析3次,并取平均值。
2 结果与讨论
2.1 三元体系KCl-NH4Cl-H2O 313.15K 相平衡研究
三元体系KCl-NH4Cl-H2O 在313.15 K 时的相平衡研究的实验结果见表1。根据表1 实验数据绘制了三元体系KCl-NH4Cl-H2O 等温溶解平衡相图,如图1 所示。为了对不同区域固相组成进一步鉴定,本文用X 射线衍射法对图1 中具有代表性的点,Ⅱ区的6 号、Ⅲ的8(D)和Ⅳ的9 号实验点固相进行了鉴定。其XRD谱图分别见图2~4。
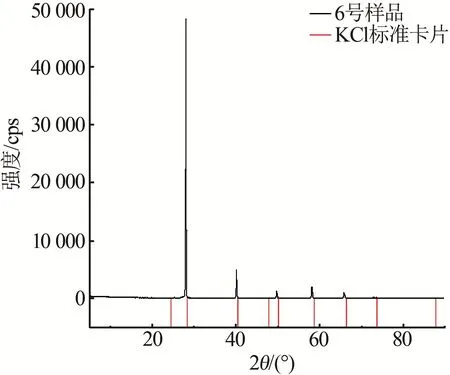
图2 表1中6号样品实验平衡固相X射线衍射图Fig.2 Experimental equilibrium solid-state X-ray diffraction pattern of sample 6 in table 1
由表1和图1可知,该体系有一个共饱和点、两条单变量曲线、6 个相区。相图中三角形的3 个顶点P、A、W分别表示纯KCl、纯NH4Cl 和纯H2O,点B表示KCl 在水中的溶解度,点C表示NH4Cl 在水中的溶解度,E、F表示KCl 与NH4Cl 开始形成两种固溶体(NH4,K)Cl 与(K,NH4)Cl 的点。曲线BD和曲线CD为两条单变量曲线,在单变量曲线CD上,NH4Cl 溶解度由45.80 g 下降到37.07 g,表明KCl 对NH4Cl 有较弱的盐析作用;在单变量曲线BD上,KCl由40.30 g下降到22.02 g,可见NH4Cl 对KCl 有较强的盐析作用;其中点D为共饱和点,D的液相组成为:w(KCl)=13.85%,w(NH4Cl)=23.30%,w(H2O)=62.85%,D的 湿 渣 组 成 为:w(KCl)=20.80%,w(NH4Cl)=40.00%,w(H2O)=39.20%。
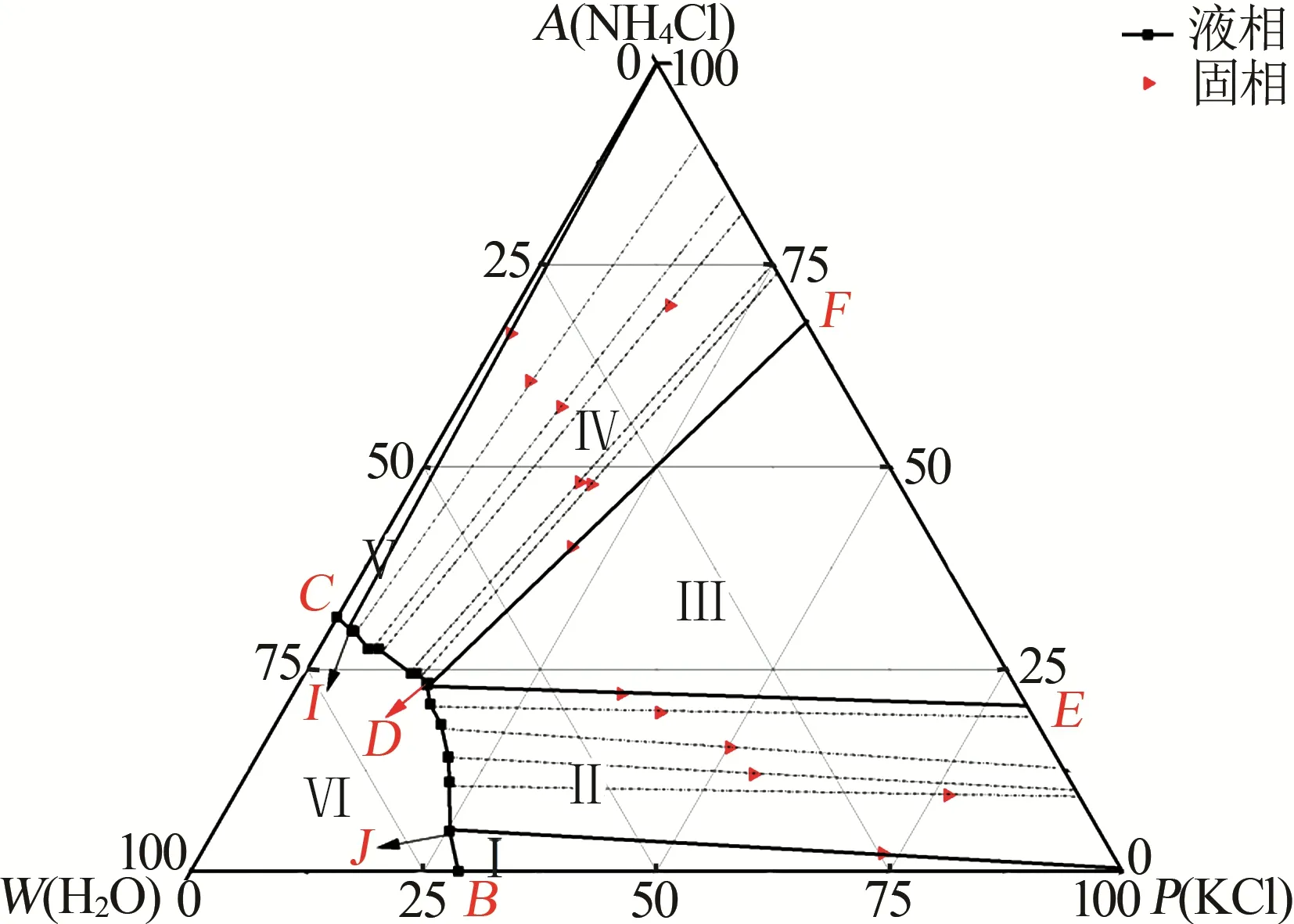
图1 313.15 K时KCI-NH4Cl-H2O三元体系等温溶解相图Fig.1 Isothermal dissolution phase diagram of ternary system of KCl-NH4Cl-H2O at 313.15 K
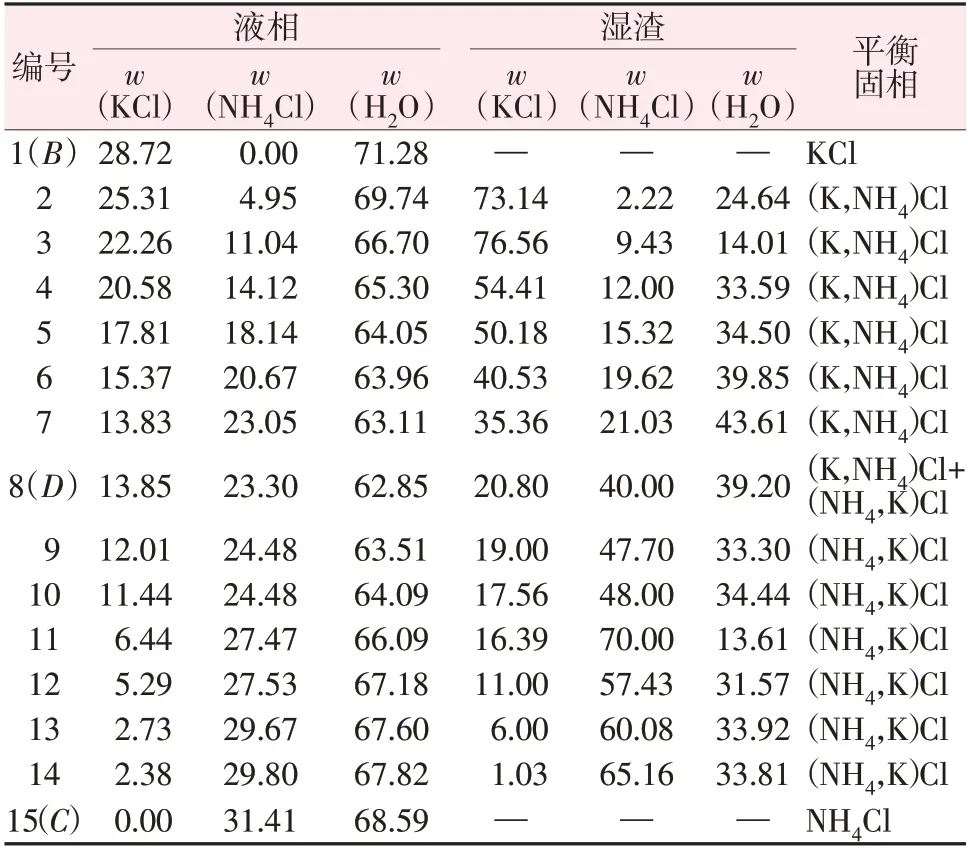
表1 三元体系KCl-NH4Cl-H2O在313.15 K时溶解度数据Table 1 Solubility data of ternary system of KCl-NH4Cl-H2O at 313.15 K %
图2 及图4 是该三元体系KCl-NH4Cl-H2O 在实验中6 号样品和9 号样品固相的XRD 谱图,图中特征峰的位置和标准卡片上的峰相对向左或向右偏移,是因为钾离子半径为138 pm,铵根离子半径为143 pm;当铵根离子取代钾离子时会使晶胞参数变大,从而导致XRD 谱图的出峰角度与主相的氯化钾发生左移,同理,当钾离子取代铵根离子时会使晶胞参数变小,从而导致XRD 谱图的出峰角度与主相的氯化铵发生右移。因此,区域Ⅱ是以KCl 为主的固溶体的结晶区、Ⅳ是以NH4Cl 为主的固溶体的结晶区。图3 是实验中共饱和点D(8 号样品)的XRD 谱图,由图3 可知,共饱和点的XRD 谱图与氯化钾、氯化铵的XRD 谱图都不一致。因此与298.15 K[20]、301.15 K[21]、308.15 K[22]、353.15 K[23]KCl-NH4Cl-H2O 结构变化对比规律可知,Ⅲ为两种固溶体(K,NH4)Cl、(NH4,K)Cl的共结晶区。
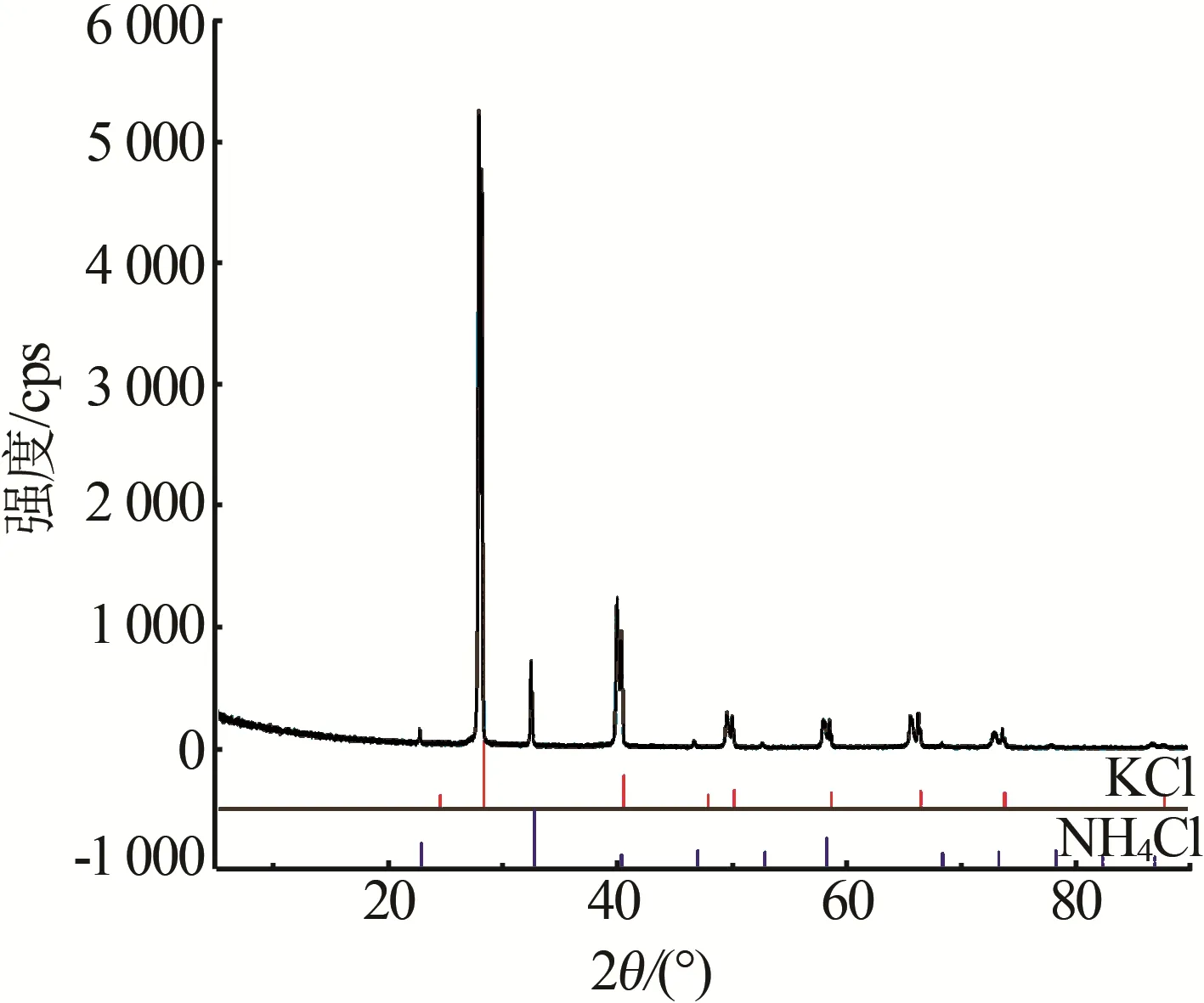
图3 表1中8号样品(共饱和点D)实验平衡固相X射线衍射图Fig.3 Experimental equilibrium solid-state X-ray diffraction pattern of sample 8(co-saturation point D)in table 1
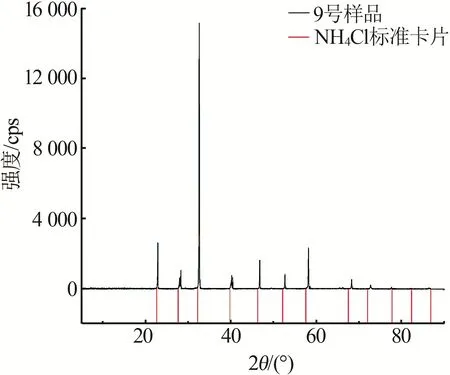
图4 表1中9号样品实验平衡固相X射线衍射图Fig.4 Experimental equilibrium solid-state X-ray diffraction pattern of sample 9 in table 1
通过以上分析可知,313.15K 时三元体系KCl-NH4Cl-H2O为部分互溶型,相图(图1)中共有6个相区,Ⅰ为纯的KCl 结晶区、Ⅴ为纯的NH4Cl 结晶区、Ⅱ是以KCl 为主的固溶体的结晶区、Ⅳ是以NH4Cl为主的固溶体的结晶区、Ⅲ为两种固溶体的共结晶区、Ⅵ为不饱和区。体系中有少量的NH4Cl 溶解到KCl 中形成了以KCl 为主的固溶体,少量的KCl 溶解到NH4Cl中形成了以NH4Cl为主的固溶体。
2.2 四元体系NH4+,K+//H2PO4-,Cl--H2O 313.15 K下相平衡研究
交互四元体系K+,NH4+//Cl-,H2PO4--H2O 实验数据如表2 所示,表中的w表示质量分数,J表示耶涅克指数[以n(H2PO4-)+n(Cl-)=100 mol(n为物质的量)为基准]。在此基础上绘制了该交互四元体系在313.15 K 时的干盐相图和水图,如图5 和图6所示,水图局部放大图见图7。并对表2 中共饱和点(E、F)处平衡固相进行了XRD 鉴定,如图8 和图9所示。
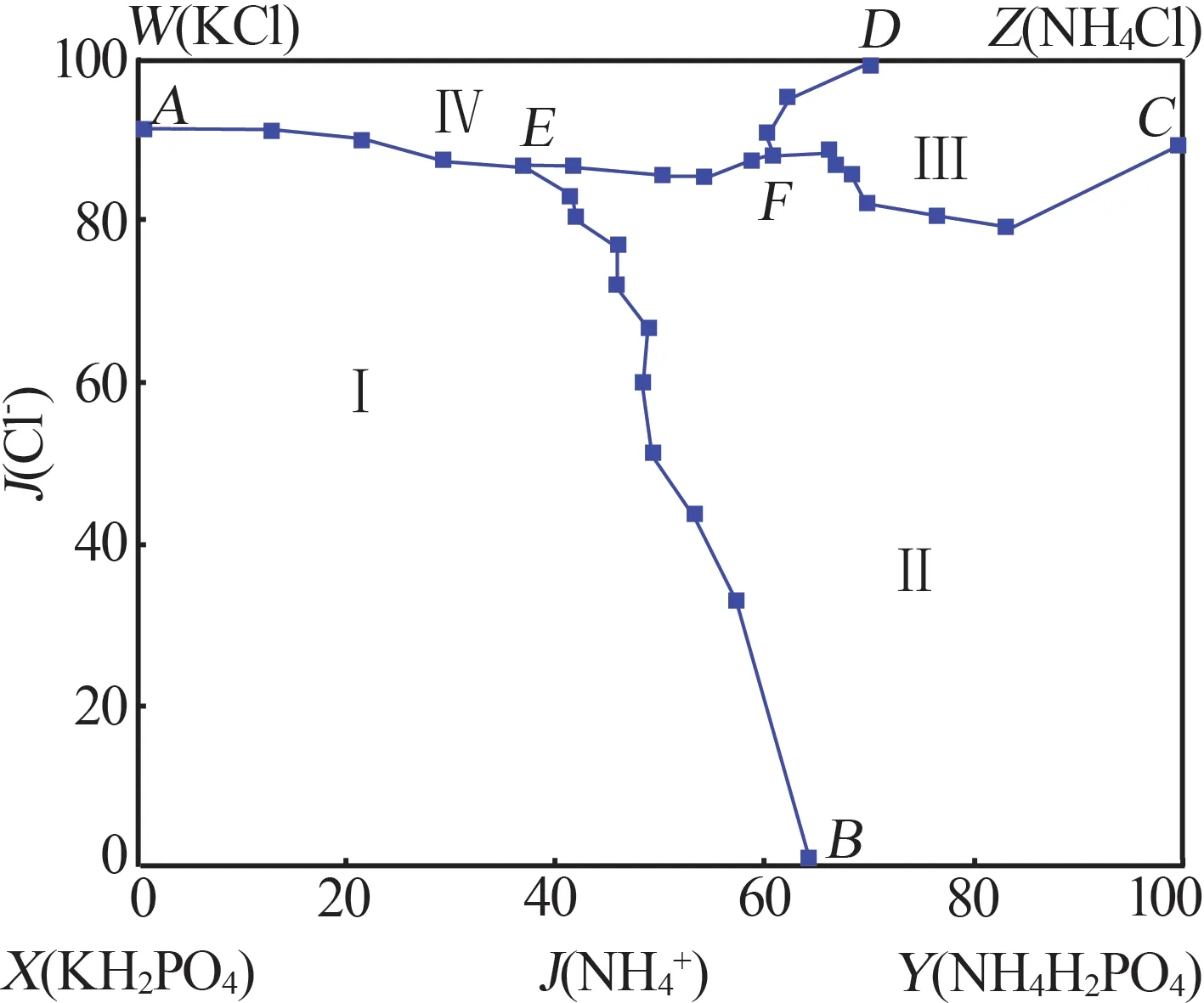
图5 313.15 K时交互四元体系K+,NH4+//Cl-,H2PO4--H2O等温溶解相图Fig.5 Isothermal dissolved phase diagram of reciprocal quaternary system of K+,NH4+//Cl-,H2PO4--H2O at 313.15 K
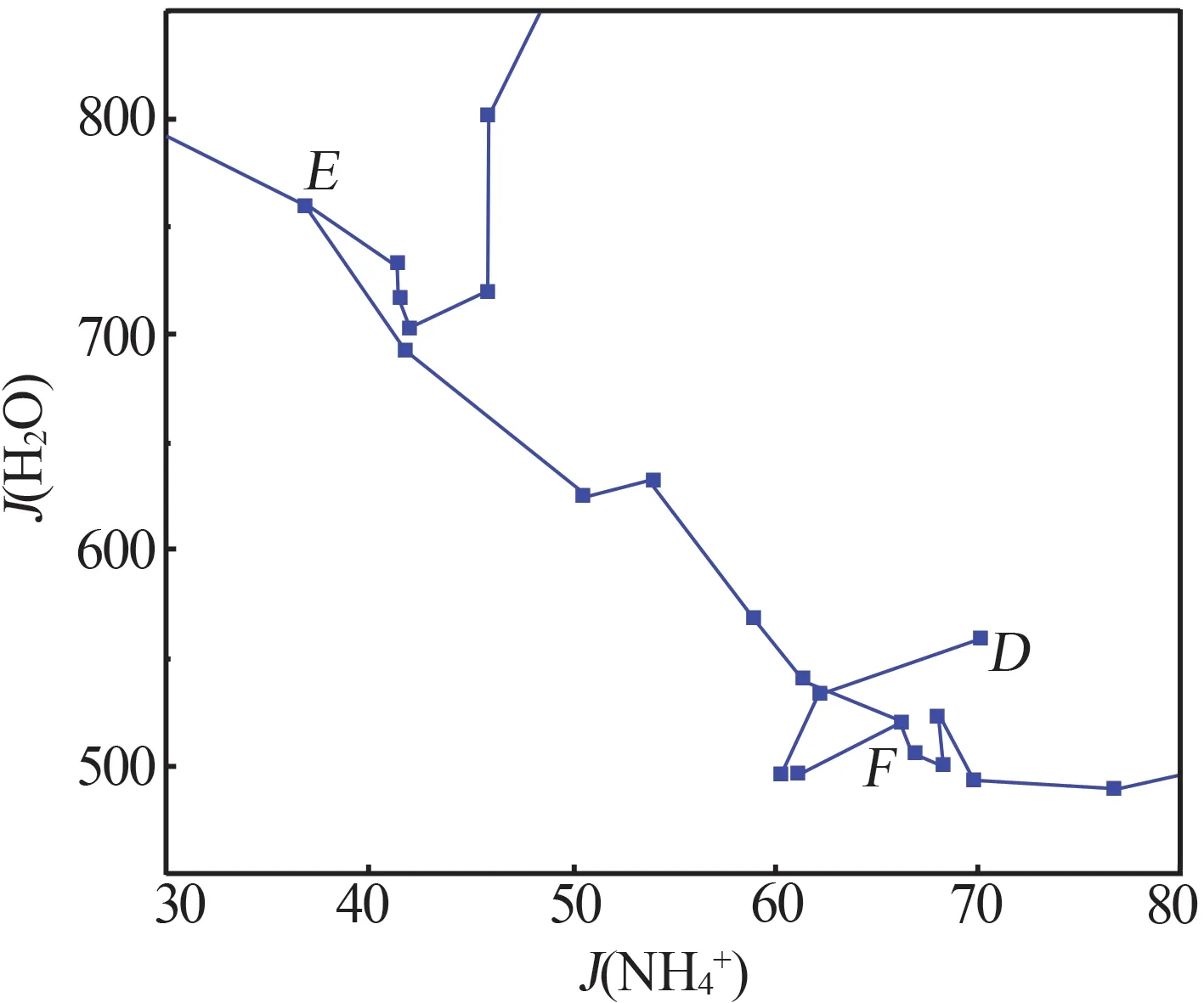
图7 313.15 K时K+,NH4+//Cl-,H2PO4--H2O四元体系水图局部放大图Fig.7 Partial enlarged water diagram of reciprocal quaternary system of K+,NH4+//Cl-,H2PO4--H2O at 313.15 K
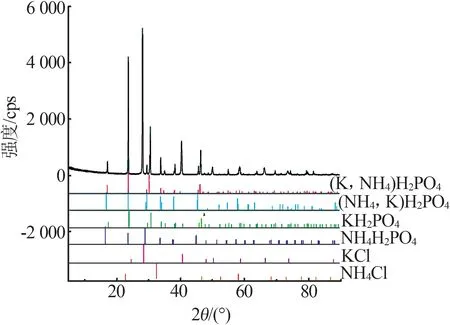
图8 表2中5号样品(共饱和点E)实验平衡固相X射线衍射图Fig.8 Experimental equilibrium solid-state X-ray diffraction pattern of sample 5(co-saturation point E)in table 2
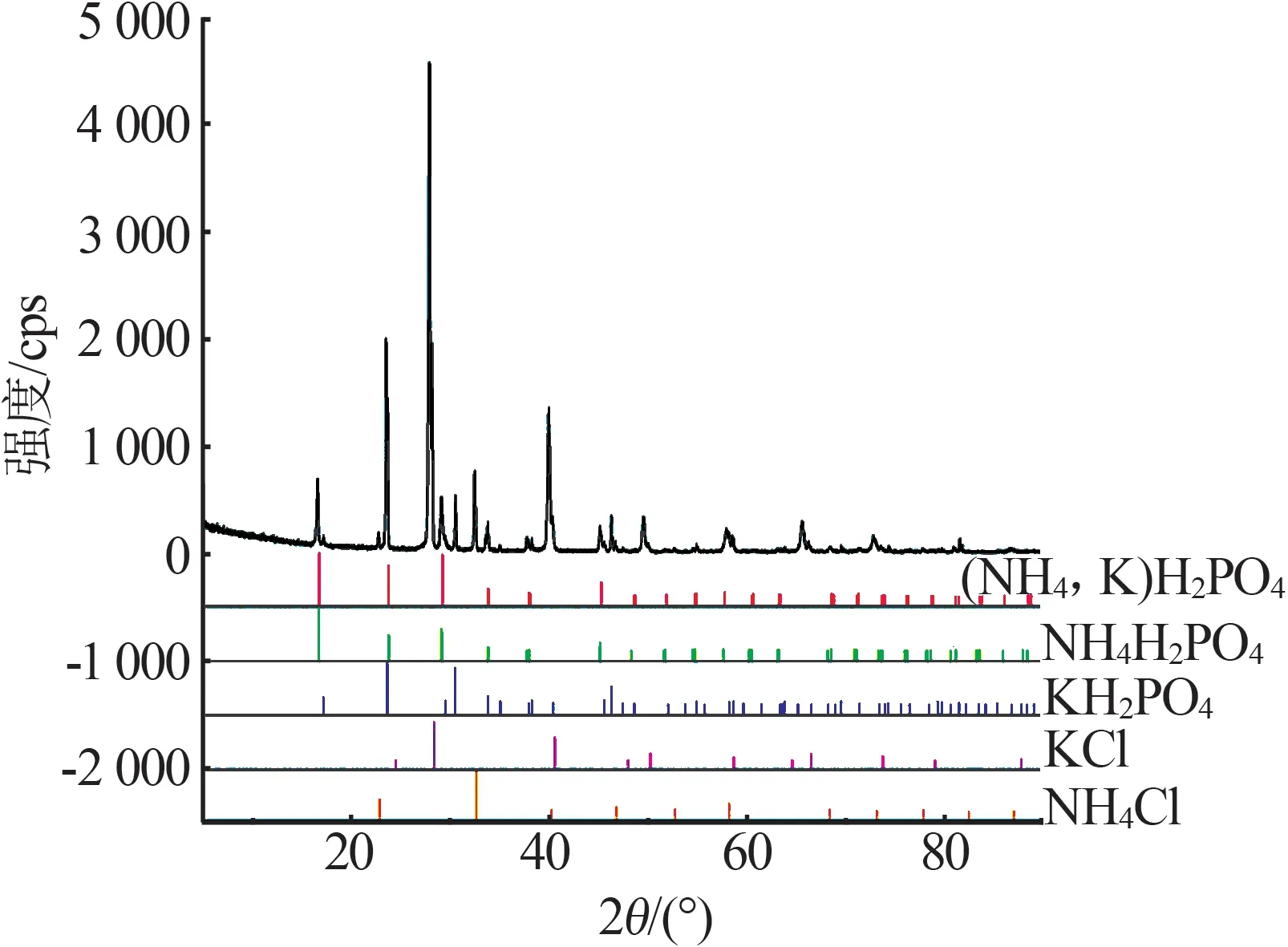
图9 表2中11号样品(共饱和点F)实验平衡固相X射线衍射图Fig.9 Experimental equilibrium solid-state X-ray diffraction pattern of sample 11(co-saturation point F)in table 2
由表2 知,该交互四元体系K+,NH4+//Cl-,H2PO4--H2O的共饱和点E的液相组成为:w(H2PO4-)=6.01%,w(Cl-)=14.52%,w(NH4+)=3.13%,w(K+)=11.63%;F点的液相组成为:w(H2PO4-)=6.99%,w(Cl-)=19.34%,w(NH4+)=7.38%,w(K+)=8.15%。
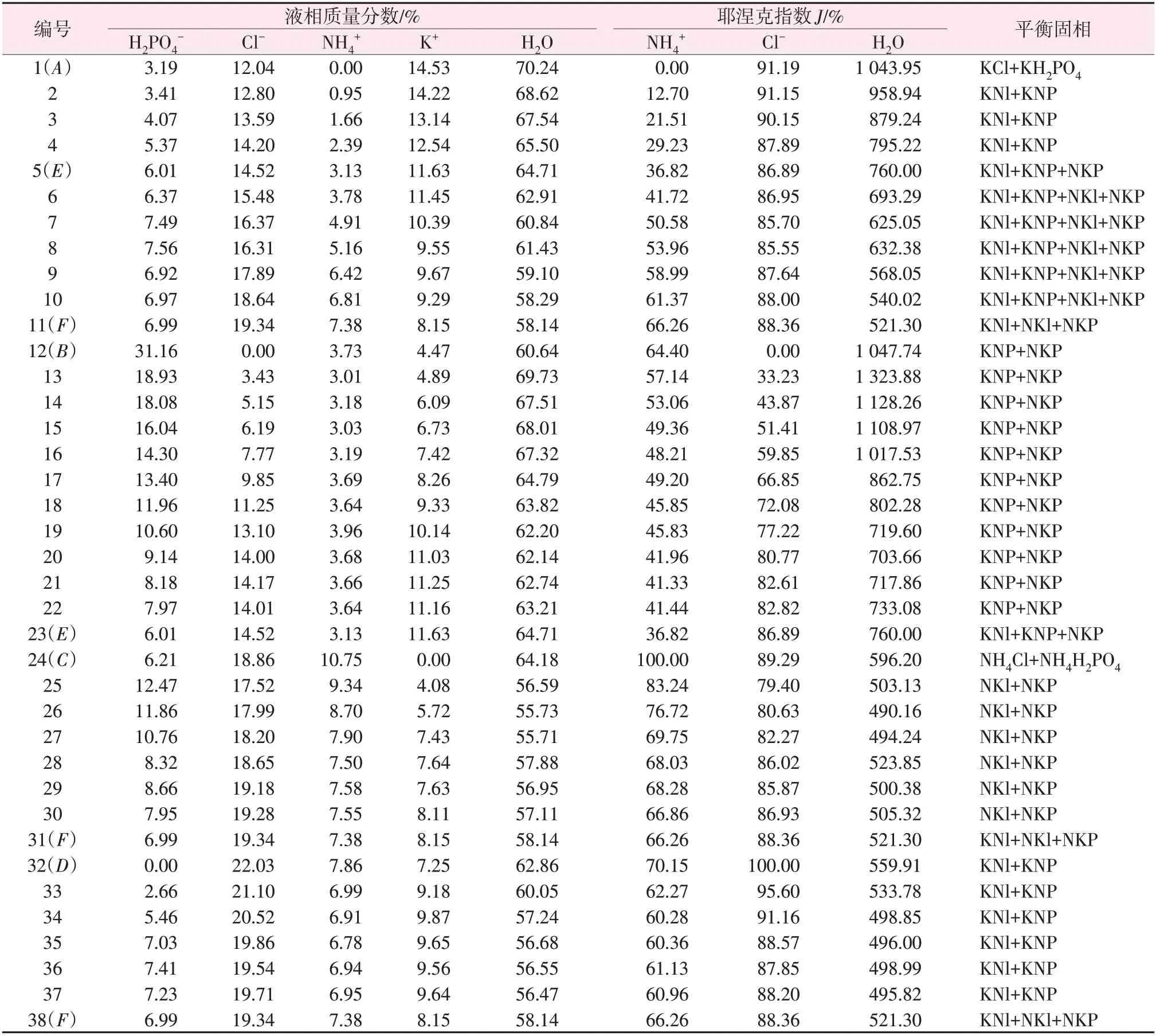
表2 交互四元体系K+,NH4+//Cl-,H2PO4--H2O 313.15 K时溶解度数据Table 2 Solubility data of the reciprocal quaternary system of K+,NH4+//Cl-,H2PO4--H2O at 313.15 K
由表2 数据绘制的等温溶解相图如图5 所示,该交互四元体系的相图上4 个顶点分别对应纯KH2PO4、纯NH4H2PO4、纯KCl 和纯NH4Cl,相图上的4 个边界点分别为A、B、C、D,对应4 个三元体系的共饱和点。313.15 K 下该交互四元体系NH4+,K+//Cl-,H2PO4--H2O 的等温溶解平衡相图包括两个共饱和点(E、F),4 个相区,5 条单变量曲线。其中,5条单变量曲线分别为A-E、B-E、C-F、D-F和E-F曲线,曲线A-E是KCl 和KH2PO4的共饱和溶解度曲线;曲线D-F是NH4Cl 与KCl 的共饱和溶解度曲线;曲线C-F是NH4H2PO4和NH4Cl 的共饱和溶解度曲线;曲线B-E是KH2PO4和NH4H2PO4的共饱和溶解度曲线;曲线E-F是KH2PO4和NH4Cl的共饱和溶解度曲线。
由相图(图5)可知,共饱和点E的平衡固相对应的相区分别为Ⅰ、Ⅱ及Ⅳ,共饱和点F的平衡固相对应的相区分别为Ⅱ、Ⅲ及Ⅳ,因此取共饱和点E、F的平衡固相做了XRD 鉴定,鉴定谱图如图8 和图9 所示。将共饱和点E、F的XRD 谱图与4 个三元子体系的XRD谱图进行比较。在共饱和点E、F时,XRD 谱图(图8~9)中出现了KCl、NH4Cl、KH2PO4、NH4H2PO4、(K,NH4)H2PO4以及(NH4,K)H2PO4标准卡 片,是 因 为 三 元 子 体 系KCl-KH2PO4-H2O[11]、NH4Cl-NH4H2PO4-H2O[12]是个简单体系,没有复盐和固溶体形成,因此实验中会存在单物质的KCl、NH4Cl、KH2PO4、NH4H2PO4,而三元子体系KH2PO4-NH4H2PO4-H2O[13]、KCl-NH4Cl-H2O 是部分互溶体系,KH2PO4与NH4H2PO4、KCl 与NH4Cl 会形成固溶体,其中KCl 与NH4Cl 形成的固溶体与子体系KCl-NH4Cl-H2O 中共饱和点(D)检测的XRD 谱图基本一致,只是呈现出了出峰角度的偏移。将相图(图5)与283.15 K[14]和298.15 K[15]下的相图进行对比,其变化规律基本一致。因此,可以确定相图的4 个相区,Ⅰ为以KH2PO4为主的(K,NH4)H2PO4固溶体的结晶区,Ⅱ为以NH4H2PO4为主的(NH4,K)H2PO4固溶体的结晶区,Ⅲ为以NH4Cl 为主的(NH4,K)Cl 固溶体的结晶区,Ⅳ为以KCl 为主的(K,NH4)Cl固溶体的结晶区。
由图6 与图7 可知,A-E和E-F曲线的水含量随着NH4+含量的增加而减小,而B-E、C-F、D-F曲线的水含量随着NH4+含量增加而整体增加。因此,NH4+的含量对水含量的影响较大。
3 结论
三元体系KCl-NH4Cl-H2O 在313.15 K 下是一个部分互溶体系,有少量的NH4Cl 溶解到KCl 中形成了以KCl 为主的固溶体,少量的KCl 溶解到NH4Cl 中形成了以NH4Cl 为主的固溶体,相图有两条单变量曲线、5 个结晶区;该体系有一个共结晶点D,其 组 成 为:w(KCl)=13.85%,w(NH4Cl)=23.30%,w(H2O)=62.85%。
交互四元体系K+,NH4+//Cl-,H2PO4--H2O 中形成了两种固溶体(KCl、NH4Cl 形成的固溶体与KH2PO4、NH4H2PO4形成的固溶体),该四元体系的相图包括2 个共饱和点、5 条单变量曲线及4 个结晶区。该体系中NH4+的含量对水含量的影响较大。
