长鞘+Navien导管介入术与短鞘+导引导管治疗颅内动脉瘤的效果比较*
2022-10-12李洛赖丹
李洛 赖丹
颅内动脉瘤是指颅内动脉血管壁受外力或自发导致的异常膨隆状凸起,其发病于各个年龄段[1]。颅内动脉瘤常发病隐匿,有着较高的致死率及致残率[2]。颅内动脉瘤年化发病率高达4%~7%,其患病率仅次于脑梗死和脑出血,位列脑血管疾病的第三位[3]。近年来随着我国经济水平快速发展,工作与生活压力增大,颅内动脉瘤发病率逐年上升[4]。颅内动脉瘤严重危害人类健康,破裂可引起颅内蛛网膜下腔出血,导致昏迷,严重的出血累及脑干,引起患者植物生存状态甚至死亡[5]。既往治疗颅内动脉瘤的手段主要是行开颅夹闭术,但疗效并不理想,其存在创面大、并发症多、术中破裂出血等不足[6]。长鞘导管有较强的支撑力和兼容性,近年来越来越多地被用于颅内动脉瘤的治疗,但由于部分患者动脉走行弯曲,导管难以进入,可能会导致血管夹层[7]。新型Navien 导管顺应性强,兼容性好,能够安全通过动脉异常弯曲,但其支撑性和可操作性仍存在一定不足,长鞘+Navien 导管相结合可弥补短板,在介入术中能够有效治疗颅内动脉血管瘤[8]。本研究比较长鞘+Navien 导管介入术与短鞘+导引导管在颅内动脉瘤中的临床疗效,为颅内动脉瘤介入治疗提供依据,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析2017 年1 月-2020 年12 月萍乡市人民医院神经外科接收的80 例颅内动脉瘤患者的临床资料。纳入标准:(1)术前均经DSA 诊断为颅内动脉瘤;(2)均接受血管栓塞治疗;(3)临床资料完整。排除标准:(1)伴严重心、肝、肾脏器病变;(2)术前Hunt-Hess 分级为Ⅴ级[9];(3)中途失访。按照治疗方式将患者分为对照组和观察组,各40 例。本研究已获本院伦理委员会的批准。
1.2 方法
1.2.1 对照组 术前均完成血常规、肝肾功能、心电图及DSA 造影检查,术前口服氯吡格雷[生产厂家:赛诺菲(杭州)制药有限公司,批准文号:国药准字H20056410,规格:75 mg/ 片]75 mg/d 联合阿司匹林(生产厂家:大同市利群药业有限责任公司,批准文号:国药准字H14022744,规格:50 mg/片)100 mg/d,连续3 d。全身麻醉下,经改良Selding 技术常规于右股动脉穿刺,留置6F 股动脉短鞘,滴注肝素钠注射液(生产厂家:成都市海通药业有限公司,批准文号:国药准字H51021209,规格:2 mL∶1.25 万单位)50 U/kg 处理,在导管使用前采用0.9%生理盐水溶液浸泡,后采用泥鳅导丝(0.035 英寸)携导引导管通过主动脉弓抵达预定位置,术前评估为困难的Ⅲ型主动脉弓则采用SIMON 导管,通过更换导管及导丝的方案将导管尽可能置入颈内动脉,指引导管放置在尽可能高的位置,完成置入后在导引导管内经微导管直接栓塞或支架辅助栓塞,栓塞完毕后立即造影,观察动脉瘤栓塞效果。
1.2.2 观察组 术前辅助检查及药物服用、术中麻醉方式、穿刺入路与对照组一致,完成6F 动脉长鞘置入后,长鞘接高压滴注肝素钠50 U/kg,完成肝素化处理,每间隔1 h 追加1.0×105U 肝素,术前采用0.9%生理盐水冲洗Navien 导管(美国美敦力公司生产,进口注册号20143776248),于体外将125 cm 的5F 多功能导管与Navien 导管相套构成同轴系统,6F 长鞘管、造影导管及Navien 导管均连接液体滴注,在5F 多功能导管的辅助下,Navien导管导入长鞘管,并在导丝的引导下,同轴系统同步推进,并在微导管或支架导管的辅助下,让长鞘管在颈内动脉尽可能获取高的位置,后将Navien 导管留置在目标血管位置;置入过程中若为主动脉弓Ⅱ型或Ⅲ型,则采用交换导丝技术推进,并尽可能将导丝超选至颈外动脉,预防导丝对血管的损伤及可能带来的导丝推进中导致颈内动脉斑块脱落。Navien 导管抵达目标位置后,行直接栓塞或支架辅助栓塞,栓塞完毕后,即刻造影,观察栓塞效果。
1.2.3 术后处理 所有患者术后补液均维持正常血容量,若存在破裂出血的患者给予抗血管痉挛治疗;术中采用支架辅助栓塞者继续维持术前氯吡格雷75 mg/d+阿司匹林100 mg/d,连服6 周。术后6~12 个月行DSA 复查与临床随访。
1.3 观察指标及判定标准(1)比较两组手术时间及住院时间。(2)比较两组并发症发生情况,包含术中血管痉挛、术中动脉瘤破裂、术后缺血性并发症、术后出血性并发症。(3)比较两组术后动脉瘤的完全栓塞率(动脉瘤完全不显影)、残余率(瘤体内有造影剂显影)及复发率(栓塞动脉瘤处新增造影剂滞留情况,向外膨出时,表明动脉瘤复发)。(4)比较两组术前和术后3、6 个月的神经功能缺损评分。采用美国国立卫生研究院脑卒中量表(national institute of health stroke scale,NIHSS)评估意识水平、凝视、视野、面瘫、上肢运动、下肢运动、共济失调、感觉、语言、构音障碍、忽视症,得分范围为0~42 分。NIHSS 得分越高,说明神经功能缺损情况越严重[10]。
1.4 统计学处理 采用IMB SPSS 22.0 进行数据整理和统计学分析,计量资料采用()表示,采用t检验;多次测量的计量资料采用重复测量方差分析,两两比较采用LSD 法;计数资料采用率(%)进行表示,若理论频数(T)≥5,采用χ2检验;1≤T<5,采用校正χ2检验;若T<1,采用Fisher 精确概率法,以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组一般资料比较 对照组男23 例,女17 例;年龄54~73 岁,平均(64.20±6.19)岁;体重指数(body mass index,BMI)19.20~25.89 kg/m2,平均(22.41±2.18)kg/m2;基础疾病:高血压19 例,糖尿病12 例,高血脂14 例;动脉瘤部位:前循环32 例,后循环8 例;术前Hunt-Hess 分级:Ⅰ级8 例,Ⅱ级14 例,Ⅲ级13 例,Ⅳ级5 例;英国国家早期预警 评 分(national early warning score,NEWS)评 分2~8 分,平均(4.20±1.35)分。观察组男28 例,女12 例;年龄53~75 岁,平均(64.92±6.60)岁,BMI 18.95~25.35 kg/m2,平 均(22.18±2.30)kg/m2;基础疾病:高血压17 例,糖尿病13 例,高血脂10 例;动脉瘤部位:前循环30 例,后循环10 例;术前Hunt-Hess 分级:Ⅰ级7 例,Ⅱ级15 例,Ⅲ级11 例,Ⅳ级7 例;NEWS 评 分1~8 分,平 均(4.09±1.30)分。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组手术时间与住院时间比较 观察组手术时间及住院时间均短于对照组,差异均有统计学意义(P<0.05),见表1。
表1 两组患者手术时间与住院时间比较()
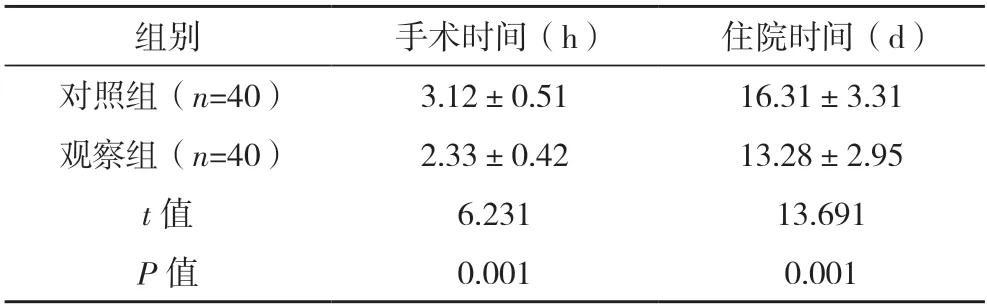
表1 两组患者手术时间与住院时间比较()
2.3 两组并发症发生情况比较 两组术中血管痉挛、术中动脉瘤破裂、术后缺血性并发症、术后出血性并发症发生率比较,差异均无统计学意义(P>0.05),见表2。
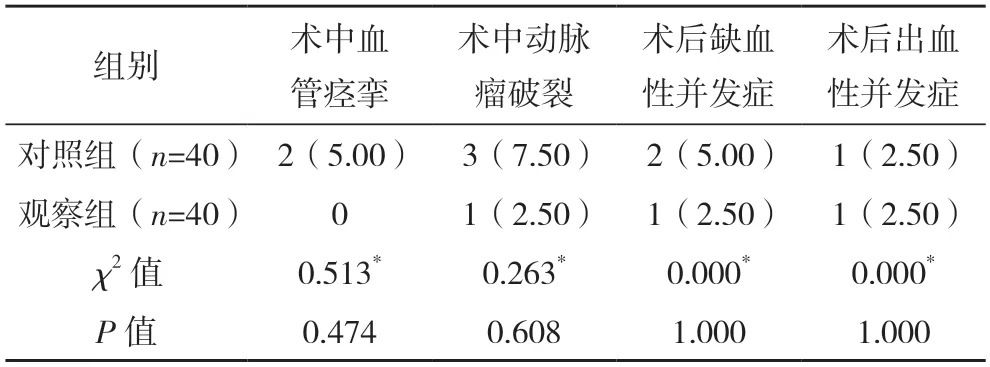
表2 两组并发症发生情况比较[例(%)]
2.4 两组术后动脉瘤完全栓塞率、残余率及复发率比较 两组动脉瘤完全栓塞率、动脉瘤残留率及动脉瘤复发率比较,差异均无统计学意义(P>0.05),见表3。
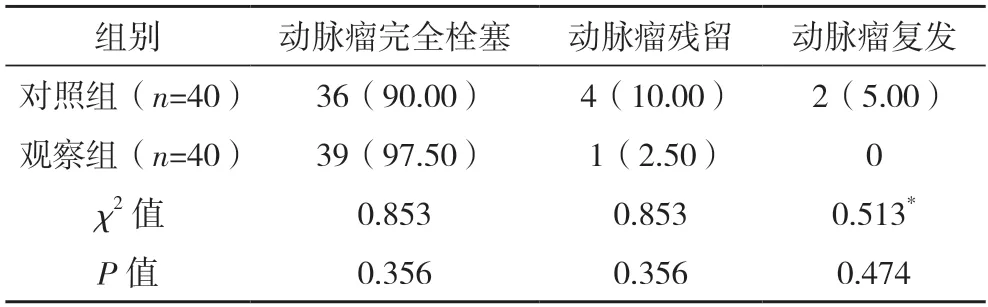
表3 两组术后动脉瘤完全栓塞率、残余率及复发率比较[例(%)]
2.5 两组NIHSS 评分比较 术后3、6 个月,两组NIHSS 评分均低于术前,差异均有统计学意义(P<0.05)。术前,两组NIHSS 评分比较,差异无统计学意义(P>0.05);术后3、6 个月,观察组NIHSS 评分均低于对照组,差异均有统计学意义(P<0.05)。见表4。
表4 两组NIHSS评分比较[分,()]
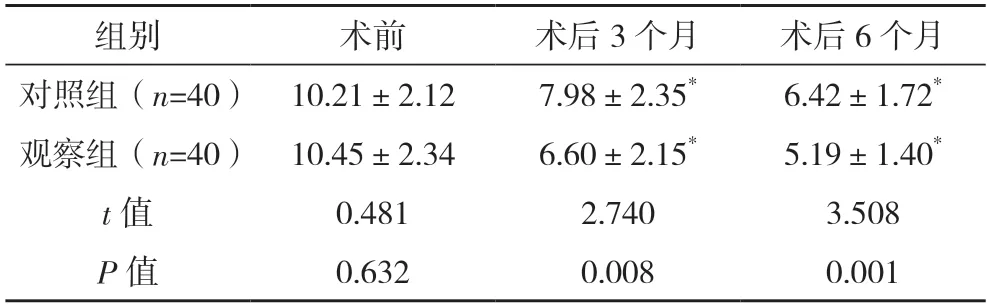
表4 两组NIHSS评分比较[分,()]
*与术前比较,P<0.01。
3 讨论
颅内动脉瘤作为严重的神经外科疾病,其发病隐匿,有着较高的致死率及致残率。对于颅内动脉瘤患者的治疗已由开颅夹闭术转变为介入栓塞。长鞘导管近年来越来越多地被用于颅内动脉瘤栓塞治疗,但由于部分患者动脉走行弯曲,导管难以进入。新型Navien 导管首先具有良好的跟踪性与顺应性,可安全抵达颅内血管;其次术中对颅内动脉瘤实施夹闭时可提供稳定的操作平台;再次Navien 导管管腔较大,可兼容多导管操作,有空间实施造影,利于观察术中颅内动脉瘤栓塞效果[11-12]。Navien 导管近年来已被广泛用于颅内血管的治疗,有报道显示,利用Navien 导管释放血流导向装置治疗前循环动脉瘤,导管顺利抵达颈内动脉、大脑中动脉,未出现导管相关并发症[13]。魏凡策等[14]采用5F 或6F Navien 导管实施血管内治疗68 例患者,Navien导管顺利抵达颈内动脉岩骨水平段45 例,颈内动脉海绵窦段2 例,椎动脉V2 段13 例,V3 段7 例,V4 段1 例,术中均无出血及缺血性并发症。吴德刚等[15]报道了新型Navien 导管应用于15 例颈内动脉严重迂曲的患者血管内治疗,将5F 或6F 导管与长鞘造影导管形成同轴系统,经股动脉导管鞘置于髂动脉内,利用造影导管超选进入需要治疗的血管,Navien 导管均通过严重迂曲血管抵达目标位置,成功完成了颅内动脉瘤栓塞治疗,并经3~6 个月的DSA 随访后,未见动脉瘤复发、支架狭窄及移位、再出血及脑缺血等并发症。由此可见,新型Navien导管在颅内动脉瘤介入治疗总体上是安全、可行、有效的。
本研究显示,观察组手术时间及住院时间均短于对照组,差异均有统计学意义(P<0.05)。说明长鞘+Navien 导管介入术与鞘管+导引导管颅内动脉介入栓塞术比较,可显著缩短手术时间与住院时间。原因主要与Navien 导管柔软的材质,可更好地通过血管迂曲段,减少操作时间有关;同时待导管跨过弯曲血管后,血管与导管间形成相互作用力,在血管弯曲段获得支撑效应,以顺利完成介入栓塞术。颅内血管栓塞治疗术中并发症有血管痉挛、动脉瘤破裂、术后出血性或缺血性并发症,血管痉挛多出现在严重迂曲的血管患者,与指引导管或泥鳅导丝通行过程中对血管的刺激有关[16];动脉瘤破裂多与外部压力作用下突然产生强大的压力有关,引起动脉瘤压力性破裂[17];出血性并发症与血管损伤有关,缺血性并发症与血管阻塞或斑块脱落、移位有关。本研究发现两组术中血管痉挛、术中动脉瘤破裂、术后缺血性并发症、术后出血性并发症发生率比较,差异均无统计学意义(P>0.05)。说明长鞘+Navien 导管并不增加介入术并发症发生率。Navien导管及作为内导管的造影管在抵达预定位置后,十分方便术中置入内导管,且内导管增强了Navien 导管的支撑力,有助于导引导管通过斑块与血管间隙,进而减少斑块脱落风险;且较大的内径可兼容多种操作,实现弹簧圈栓塞治疗,甚至利用支撑导管置入支架辅助完成弹簧圈治疗,正是由于Navien 极大地提升了其在迂曲导管中的通过率及可控的血管刺激因素,拓展了其在颅内病变的应用范围[18],从而提升了栓塞成功率,并改善了栓塞介入治疗的条件,实现彻底栓塞。本研究未发现两组在动脉完全栓塞率、动脉瘤残留率及动脉瘤复发率的差异,考虑原因主要与研究样本数量及动脉瘤位置有关。
颅内动脉瘤大多为先天畸形与后天病理因素所引起的血管壁局限性膨出,颅内动脉瘤具有病情隐匿、高危及致残率与致死率高的特点。报道显示颅内动脉瘤术后多伴不同程度的肢体功能残疾,谢兰军等[19]报道了20 例颅内动脉瘤经介入栓塞术治疗后的Rankin 评分为2.7 分,肢体功能残障程度介于轻度与中度之间。Mahaney 等[20]报道了颅内动脉瘤患者存在明显的神经功能缺损,经显微手术夹闭或介入栓塞治疗,有效减轻了神经功能缺损程度。本研究显示,术后3、6 个月,两组NIHSS 评分均低于术前,差异均有统计学意义(P<0.05)。术后3、6 个月,观察组NIHSS 评分均低于对照组,差异均有统计学意义(P<0.05)。提示,长鞘+Navien 导管可更好地降低神经功能缺损程度。原因主要为:长鞘+Navien 导管栓塞更为彻底,颅内刺激更轻微,血管刺激或斑块脱落风险更低,术后NIHSS 评分改善更为明显。
综上所述,长鞘+Navien 导管介入术与鞘管+导引导管颅内动脉介入栓塞术比较,可缩短手术时间及住院时间,减轻术后神经功能缺损程度评分,值得在临床推广。
