颈动脉重度狭窄合并冠状动脉多支病变分期治疗后院内并发症分析
2022-10-03范承哲张楠梁林许保磊
范承哲 张楠 梁林 许保磊
颈动脉狭窄合并冠心病(左主干及冠状动脉三支或二支病变)在临床中相对常见,颈动脉狭窄的最佳治疗方法目前仍有争议。20世纪90年代早期进行的随机临床试验如北美症状性颈动脉内膜切除试验(North American Symptomatic Carotid Endarterectomy Trial,NASCET)、欧洲颈动脉手术试验(European Carotid Surgery Trial,ECST)、退伍军人事务部合作研究(Veterans Affairs Cooperative Study,VACS)等结果表明,症状性和无症状性颈动脉狭窄患者,颈动脉内膜切除术(carotid endarterectomy,CEA)治疗效果(主要终点事件包括随访过程中的卒中事件、围手术期卒中事件和死亡)优于药物治疗[总体风险降低53% (95%CI:22%~72%)][1-4]。近年来,在部分高龄、具有高风险解剖特征(如既往颈部手术、对侧颈动脉闭塞、喉返神经麻痹等)或其他合并症(如严重心肺疾病、凝血功能异常等)而被认为不适于行CEA的患者中,颈动脉支架置入术(carotid artery stenting,CAS)作为替代CEA的一种微创血管内治疗方法被引入。重度冠心病患者,在接受冠状动脉旁路移植术(coronary artery bypass grafting,CABG)后发生缺血性卒中风险为6%~14%[5]。有研究报道,在冠状动脉病变患者中,尤其是多支病变患者,是否合并颈动脉狭窄对其危险分层尤为重要,合并颈动脉狭窄是发生心脑血管主要不良事件的独立危险因素[6]。严重的颈内动脉疾病(颈内动脉重度狭窄、闭塞等),尤其是近期出现症状的患者,是CABG术后发生卒中的重要危险因素 (OR=4.3, 95%CI:3.2~5.7)[7]。因此,有研究建议,在CABG前(分期)或同时(联合)进行CEA,以防止CABG术后死亡或降低卒中风险[8]。但是,采用上述两种方法的研究不良事件发生率(10%~12%)仍然很高[9]。CEA通常采用全身麻醉方式,且是有创手术,术后恢复较慢;而 CAS可采用局部麻醉方式,支架置入过程中可以实时监测患者的神经功能状态,术后恢复快。鉴于CABG术后卒中不良事件的高风险性,CAS被用来作为传统CEA的微创替代方法[10]。然而,对伴有颈动脉狭窄拟行CABG患者治疗策略仍有争议。尚无指南明确推荐如何处理重度冠心病合并重度颈动脉狭窄病例。部分研究者建议,当冠心病的病情和冠状动脉病变的解剖结构符合CABG指征,同时颈动脉狭窄有CAS和(或)CEA指征,一般情况下优先选择分期或同期CAS+CABG或CEA+CABG[11]。国内目前尚缺乏对冠心病合并颈动脉狭窄的治疗策略的相关研究。
因此,本研究拟回顾性分析首都医科大学附属北京安贞医院近15年以来,颈动脉重度狭窄合并冠状动脉多支病变患者分期行CAS+CABG治疗术后院内并发症发生情况,为冠心病合并颈动脉狭窄治疗策略提供参考。国内近几年虽有同期手术的个案报道[12],但首都医科大学附属北京安贞医院同期行CAS+CABG治疗例数较少,同期或分期行CEA+CABG治疗术后并发症情况国内外研究报道较多,因此,在本文中均不做分析。
1 对象与方法
1.1 对象
回顾性连续纳入2006年4月至2020年12月首都医科大学附属北京安贞医院共30例于6个月内分期完成CAS和非体外循环CABG治疗的颈动脉重度狭窄合并冠状动脉多支病变患者,其中男27例,女3例;年龄54~76岁,平均(64±5)岁;高血压病25例(83.3%),糖尿病13例(43.3%);20例(66.7%)患者至少有1次脑梗死病史,具有轻型卒中病史1例,蛛网膜下腔出血1例;单侧颈动脉狭窄27例,双侧颈动脉狭窄3例,单侧颈动脉闭塞8例,椎动脉狭窄7例;二支冠状动脉病变11例,三支冠状动脉病变19例;所有患者CAS和CABG间隔时间为11~166 d,中位数时间为50 d。
纳入标准:患者均患有冠状动脉三支或二支病变或重度左主干狭窄(狭窄率>50%)且不适合经皮治疗,以及重度颈动脉狭窄;6个月内分期完成CAS和非体外循环CABG治疗。
排除标准:需要紧急行颈动脉或冠状动脉治疗、严重心力衰竭、左心室射血分数≤20%或纽约心脏协会(New York Heart Association,NYHA)心功能分级Ⅳ级、瓣膜病需要手术和术前心房颤动;对阿司匹林或氯吡格雷不耐受;在发病前6周内发生过缺血性卒中,存在腔内血栓、无法使用导管技术的血管疾病;颅内大动脉瘤和主动脉弓解剖不适合经皮介入治疗。
1.2 资料收集及评估标准
收集所有患者的一般资料包括性别、年龄、病史以及临床资料如症状、体征、影像学检查、治疗方式、随访情况等。根据NASCET标准评估颈动脉狭窄程度[13],重度颈动脉狭窄的定义包括有症状患者的颈总动脉或颈内动脉狭窄率>70%,无症状患者颈总动脉或颈内动脉狭窄率>80%。通过颈动脉多普勒超声筛选,并通过术中血管造影确认。高血压病:未使用降压药物的情况下,非同日3次测量诊室血压,收缩压≥140 mmHg和(或)舒张压≥90 mmHg;患者既往有高血压病史,目前正在使用降压药物,血压虽低于140/90 mmHg,仍应诊断为高血压病[14]。糖尿病:空腹血糖≥7.0 mmol/L,葡萄糖负荷后2 h血糖≥11.1 mmol/L[15]。陈旧性心肌梗死:(1)出现病理性Q波(伴或不伴症状);(2)影像学证据显示局部存活心肌丢失(变薄、无收缩),缺乏非缺血性原因;(3)病理发现已经愈合或正在愈合的心肌梗死。满足以上任何一项标准均可诊断为陈旧性心肌梗死[16]。短暂性脑缺血发作:由局灶性脑、脊髓或视网膜缺血引起的短暂性神经功能障碍发作,无急性梗死[17]。轻型卒中:美国国立卫生研究院卒中量表(NIHSS)评分≤3分[18]。缺血性卒中指因脑部血液循环障碍,缺血、缺氧所致的局限性脑组织缺血性坏死或软化[19]。
1.3 CAS及CABG术前检查
所有患者术前行冠状动脉、颈动脉和脑血管筛查。筛查包括冠状动脉CT血管成像(CTA)、颈动脉超声和脑血管MR血管成像(MRA)等。影像由神经血管放射科医师进行评估。必要时进行冠状动脉造影或双侧颈总动脉、颈内动脉和双侧椎动脉DSA检查。冠状动脉造影检查包括主动脉弓造影2次, 第1次显示主动脉弓、弓上动脉血管开口及其近端,第2次显示颅内毛细血管期影像,评估颅内灌注情况。
1.4 CAS治疗
1.4.1手术前准备:术前7 d常规口服阿司匹林100 mg(1次/d)+氯吡格雷75 mg(1次/d),或阿司匹林100 mg(1次/d)+替格瑞洛60 mg(2次/d)。术前6 h禁食 。
1.4.2支架置入:在1%利多卡因穿刺部位局部麻醉下,采用改良Seldinger技术行经股动脉穿刺,放置8 F股动脉鞘,沿股动脉鞘管注入1 ml对比剂观察患者有无不适。如患者无不适,在全身肝素化[术前静脉滴注肝素钠 50 U/kg,术中连续泵入应用0.9%氯化钠注射液稀释的肝素钠(2.5 U/ml)维持活化凝血活酶时间150~250 s]下,行病变侧造影明确狭窄部位。然后沿交换导丝,将导引导管送入颈总动脉,在远端保护装置保护下,行支架[Wallstent自膨式支架(Boston Scientific,美国)]释放。
1.4.3术后处理:CAS术后即刻造影显示残余狭窄率<30%[20],NIHSS评分0分,结束手术;术后送入监护病房监护至少24 h,24 h后经颅多普勒超声监测颅内有无血流异常,颈动脉超声复查支架置入处血管通畅情况和支架形态。CAS术后继续服用抗血小板聚集药物(氯吡格雷或替格瑞洛联合阿司匹林),术后3个月后停用氯吡格雷或替格瑞洛,继续服用阿司匹林。
1.5 非体外循环CABG手术
患者CAS术后如发生院内并发症,则术后6个月内对患者并发症恢复情况进行评估,如患者改良Rankin量表(mRS)评分<3分,则完成非体外循环CABG。CABG术前7 d停用氯吡格雷或替格瑞洛,保留阿司匹林,停用期间加用低分子肝素钠0.6 ml皮下注射,1次/12 h。手术过程:全身麻醉后正中开胸,游离左乳内动脉,同时取大隐静脉备用。静脉予以肝素1 mg/kg,全程监测活化凝血活酶时间,维持活化凝血活酶时间>300 s。切开心包并悬吊,使用心脏稳定器充分显露靶血管,并使手术野无血。首先行左乳内动脉—前降支端-侧吻合,其余靶血管使用大隐静脉吻合,近端吻合口使用主动脉侧壁钳钳夹升主动脉,远端吻合口在2个或2个以上时采用序贯吻合方式。吻合完毕后以鱼精蛋白∶肝素1∶1 中和,严密止血后,逐层关闭手术切口,留置心包、纵隔引流管。有严重左主干狭窄的患者采用预定的主动脉内球囊反搏,以达到血流动力学稳定。术后通过桥血管流量仪测量桥血管流量良好,关胸结束手术;术后24 h行心电图、超声心动图检查和监测心肌酶、肌钙蛋白水平变化。
CABG术后第2天即恢复双抗药物,停用低分子肝素钠,直至CAS术后满3个月后改成阿司匹林单抗治疗。
1.6 研究终点
主要终点是CABG术后院内短暂性脑缺血发作、卒中、心肌梗死或死亡的发生率,次要终点是CAS术后院内短暂性脑缺血发作、卒中、心肌梗死或死亡的发生率。
CAS及CABG术后14 d时均进行电话随访,无影像随访。采用mRS评分评估术后随访时患者预后,mRS评分0~2分为预后良好,3分以上为不良,其中6分为死亡[21]。
1.7 统计学分析

2 结果
CAS术后住院期间发生并发症4例(13.3%),其中短暂性脑缺血发作3例(10.0%),脑梗死1例(3.3%)。见表1。非体外循环CABG术后3例(10.0%)发生院内并发症,其中1例(3.3%)腔隙性脑梗死,2例(6.7%)脑梗死。见表2。所有患者中无心肌梗死及手术或住院死亡病例。
典型病例男,66岁,因“活动后胸闷气短6个月”于2019年7月4日就诊于首都医科大学附属北京安贞医院心外科。患者既往高血压病、糖尿病、高脂血症及陈旧性腔隙性脑梗死,有吸烟史。入院后冠状动脉造影提示冠状动脉三支病变,颈部动脉超声提示右侧颈内动脉起始部重度狭窄,狭窄率为80%,遂转神经介入科先行CAS,术中造影提示右侧颈内动脉起始部(C1段)重度狭窄(图1a),行CAS术后造影提示狭窄解除(图1b),手术顺利,患者安返病房。术后24 h患者出现左侧肢体无力,左侧上下肢肌力Ⅳ级,NIHSS评分3分,头部MR扩散加权成像序列可见右侧半球散在点状高信号,提示新发梗死病灶(图1c),诊断脑梗死,予以抗血小板聚集、降脂及改善循环药物治疗,患者1周后症状改善,NIHSS评分0分,遂出院。CAS术后2周电话随访,mRS评分0分,CAS术后6周于我院顺利完成CABG术,术后无并发症,术后2周电话随访,患者无胸闷气短等不适。
3 讨论
既往研究结果表明,CABG术后卒中发生率为1%~5%[22]。CABG术后卒中的危险因素包括高龄、卒中史、心脏手术史、术前和术后心房颤动、左心室功能下降、颈动脉狭窄和外周血管疾病[23]。CABG术后卒中发病机制可能与动脉粥样硬化及大脑低灌注有关[24]。大多数与CABG相关的卒中发生在围手术期[25-26]。降低CABG术后卒中的策略之一是减少主动脉操作,最好的方法是“主动脉无接触策略”,如非体外循环CABG[27]。既往研究表明,与体外循环 CABG相比,非体外循环CABG具有良好的卒中预后(OR=0.70,95%CI:0.57~0.86)[27]。然而,后续的随机对照试验显示了非体外循环CABG与体外循环CABG相似的卒中发生率和病死率[卒中发生率:2.2%(26/1 187)比2.7%(32/1 207),OR=0.83,95%CI:0.50~1.38,P=0.47;病死率2.6%(31/1 187)比 2.8%(34/1 207),OR=0.92, 95%CI:0.57~1.51,P=0.75][28]。Kowalewski等[29]进一步证明了非体外循环CABG较体外循环 CABG术后卒中风险显著降低(OR=0.72,95%CI:0.56~0.92;P=0.009),卒中事件发生率非体外循环CABG组为1.34%(106/7 925), 体外循环CABG组为2.00%(158/7 904)。截至目前,非体外循环CABG仍然是一种有效的选择,适用于因主动脉操作或心肺分流术手术而导致神经并发症风险特别高的患者。
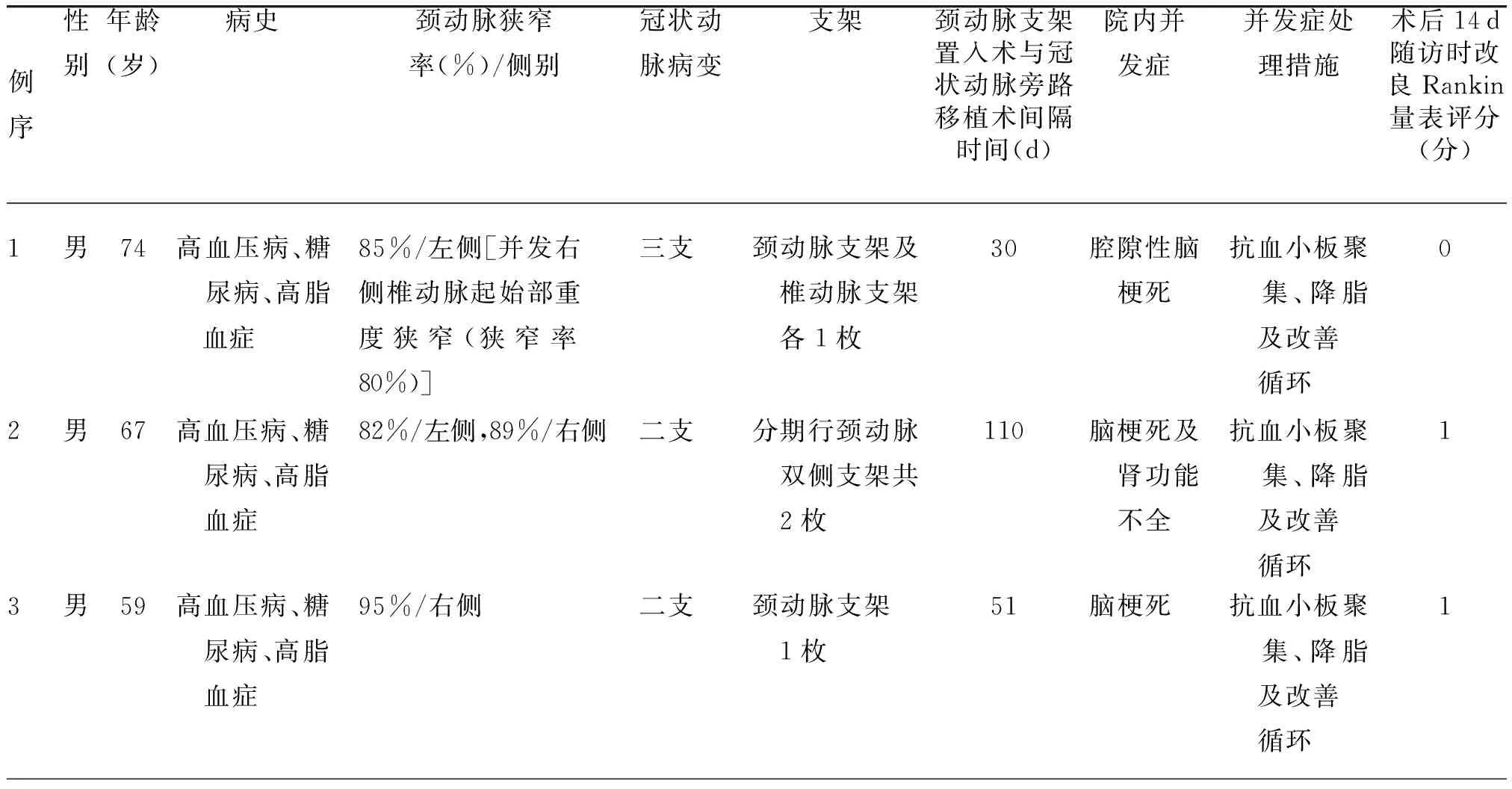
表2 3例冠状动脉旁路移植术后住院期间发生并发症的颈动脉重度狭窄合并冠状动脉多支病变患者的临床资料

颈动脉疾病经常与冠心病并存,对无症状或症状性颈动脉狭窄合并冠心病患者,颈动脉血运重建目前仍有很多争议。美国心脏病学会基金会/美国心脏协会指南(2011年)建议[30]:患者既往有短暂性脑缺血发作或卒中史和50%~99%颈动脉狭窄(Ⅱa类,证据水平:C),考虑颈动脉血运重建术联合CABG是合理的;患者既往无短暂性脑缺血发作或卒中病史,但存在双侧重度颈动脉狭窄(狭窄率为70%~99%)或单侧重度颈动脉狭窄伴对侧闭塞,可以考虑颈动脉血运重建(Ⅱb类,证据水平:C)。然而2017年的一项随机对照研究未能证明同步CEA和CABG较单独CABG更能获益[31-32]。因此本研究重点回顾分析了首都医科大学附属北京安贞医院就诊的颈动脉重度狭窄合并冠状动脉多支病变患者,分期行CAS和非体外循环CABG术后并发症发生情况。

对包括760例患者(356例来自单中心机构)在内的11项研究进行的荟萃分析结果显示,以无症状的颈动脉狭窄为主(占87%)的分期CAS+CABG(包括体外循环和非体外循环)治疗后30 d手术并发症为9.4%(61/649,包括死亡、卒中和心肌梗死)。该荟萃分析中CAS与CABG间隔范围为2~70 d。该研究表明,分期CAS+CABG可以作为CEA+CABG的替代策略[36]。CAS的创伤性小,患者恢复快,同时导致神经并发症的可能性更小[37]。此外,其对血流动力学的损害小于CEA[38]。事实上,本研究中,尽管CAS术后有短暂性脑缺血发作3例,脑梗死1例,但并未出现严重脑血管并发症和死亡事件 。Van der Heyden等[39]报道CAS手术成功率为98%(55/57),死亡、卒中和心肌梗死的合并发生率为12.3%(7/57)。本研究中CAS术后无患者发生心肌梗死和死亡,卒中发生率为13.3%,和国外报道相近;非体外循环CABG术后无患者发生心肌梗死和死亡,脑梗死发生率为6.7%,腔隙性脑梗死发生率为3.3%,总的并发症发生率为10.0%,与荟萃分析结果[36]基本一致。国内Yang等[40]报道中国医学科学院阜外医院39例分期行CAS+ CABG(非体外循环)患者30 d内卒中、心肌梗死或死亡的合并发生率为5.1%(2/39),略好于本中心研究结果;但该研究纳入患者既往脑梗死的比例[31%(12/39)]明显低于本研究中入组患者既往脑梗死患者比例[66.7%(20/30)]。
本研究中,分期行CAS和非体外循环 CABG院内并发症发生情况与国内外报道基本一致。但本研究尚存在几点不足之处:首先本研究是一项单中心、回顾性非随机研究,因此,可能存在选择偏差;此外,研究纳入患者的数量相对较少,未进行远期随访,患者基线资料仍需进一步完善等。
本研究结果表明,分期行CAS和非体外循环 CABG组成的两阶段手术是安全的,但仍然需要进一步多中心随机对照试验进行更深入的研究,提供可靠的数据,为颈动脉狭窄合并冠状动脉多支病变患者治疗提供更优的策略。
