罗沙司他治疗尿毒症合并慢性心力衰竭患者贫血1例并文献回顾*
2022-09-28林少勤雷天香张秋林
林少勤,雷天香,张秋林
(广东省第二中医院(广东省中医药工程技术研究院),广东广州 510095)
终末期肾病(end-stage renal disease, ESRD)患者常合并心血管疾病。据报道,约40%的血液透析患者诊断心力衰竭[1]。贫血是尿毒症合并心力衰竭患者常见的并发症,临床有效管理贫血对改善患者生活质量及预后具有重要意义。尽管30多年来重组人促红细胞生成素(recombinant human erythropoietin, rHuEPO)已被广泛应用于临床,然而,肾性贫血的达标率仍然不尽人意。对于尿毒症合并心力衰竭的患者,由于贫血的发生机制涉及多方面,传统的rHuEPO 治疗并不能完全满足临床需求,甚至出现EPO 抵抗。因此,临床医师迫切需要探索新的治疗策略以改善患者的贫血。罗沙司他作为一种里程碑式的新药用于治疗肾性贫血,临床研究已证实了其安全性及有效性。现报道1 例罗沙司他治疗尿毒症合并心力衰竭患者的贫血有效性及作一文献回顾。
1 病例资料
患者男性,63 岁,因“发现血肌酐升高4 年余,气促1 周”于2020 年8 月28 日入院。患者2016-02-02因双下肢浮肿至中山大学附属第一医院门诊就诊,查尿常规示:尿蛋白3+,血生化示:Scr 121μmol/L,建议患者行肾穿刺活检,患者未重视,拒绝肾活检,后双下肢浮肿未见缓解,遂于2016-02-14 前往该院住院治疗,期间复查Scr 131μmol/L,肾小球滤过率51.82ml/min,血清白蛋白22g/L,予治疗后症状减轻出院。2019-04-30 患者突发高热,自测体温38.9℃,自行服用小柴胡颗粒、大量饮用辣椒水发汗,并自行停用其他药物,1周后体温可逐渐下降,但出现纳差、乏力症状,遂于2019-05-16 前往中山大学附属第一医院门诊就诊,复查Scr 727μmol/L,血红蛋白(Hb)79g/L,患者未重视,拒绝住院治疗。后双下肢浮肿反复加重,多次于我院住院治疗。2019-11-26患者行左上肢自体动静脉内瘘成形术。2019-12-08 患者再次因双下肢浮肿住院,复查Scr 1033.4μmol/L,BUN 39.08mmol/L,于2019-12-17 开始行规律血液净化治疗(血液透析3 次/周,血液透析滤过1 次/半月,干体重设定63kg),并规律皮下注射EPO 10000IU/周纠正贫血,定期每月复查Hb 波动100~110g/L。病程中患者更改透析通路为自体动静脉内瘘。2020-06-24 患者复查Hb 81g/L,予以口服补铁治疗(琥珀酸亚铁片0.1 克,每日2 次)。2020 年7 月28 日患者因“气促1周”住院,入院后急查血常规示Hb 78g/L,予抗心衰治疗基础上,EPO 剂量调整为14000IU/周,分2 次皮下注射,并继续口服琥珀酸亚铁片0.1 克,每日2 次。2020 年8 月28 日患者再次因“气促并咳嗽咳痰”入院,诊断:急性心力衰竭、肺炎,予积极抗心衰、抗感染、加强超滤脱水等综合治疗,入院当日查Hb 67g/L,予加大EPO剂量至16000IU/周,分两次皮下注射;完善贫血原因筛查,查大便常规、小便常规、Coombs试验、呕吐物隐血试验、抗核抗体谱等均无特殊异常;网织红细胞计数7.13×109/L,超敏C 反应蛋白12.4mg/L,降钙素原0.068ng/mL,BNP>5000pg/mL,叶酸3.2ng/L,维生素B12>2000pmol/L,血清铁蛋白138.35ng/mL,转铁蛋白饱和度23%,甲状旁腺激素124pg/mL,KT/V 1.48。建议患者完善骨髓穿刺及EPO 抗体检测,患者拒绝。住院期间出现左上肢动静脉内瘘闭塞失功,行溶栓治疗后内瘘再通。9 月4日、9 月5 日患者分别复查Hb 均为65g/L。患者并无存在活动性出血、失血、溶血等情况,但Hb自2020年6月以来进行性下降,期间虽调整了EPO剂量及给予口服补铁治疗,但Hb 未见回升,考虑到患者可能存在促红素抵抗,因此我们尝试换用了新的纠正肾性贫血药物——罗沙司他。根据患者体重及药品说明书的推荐剂量,我们处方的起始剂量为100mg口服,每周3 次,2020 年9 月9 日起始。2020 年9 月14 日复查Hb 70g/L,9 月22 日复查Hb 79g/L,患者病情好转后出院。出院后患者继续规律血液净化治疗,罗沙司他维持100mg(口服,3 次/周),琥珀酸亚铁片0.1g(口服,2 次/日)。2020 年10 月28 日复查Hb 上升至94g/L。随着时间变化,患者Hb 变化情况及药物使用情况见图1、表1。
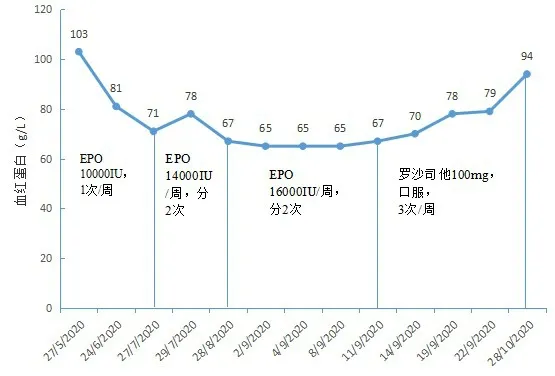
图1 患者血红蛋白变化趋势及药物使用情况
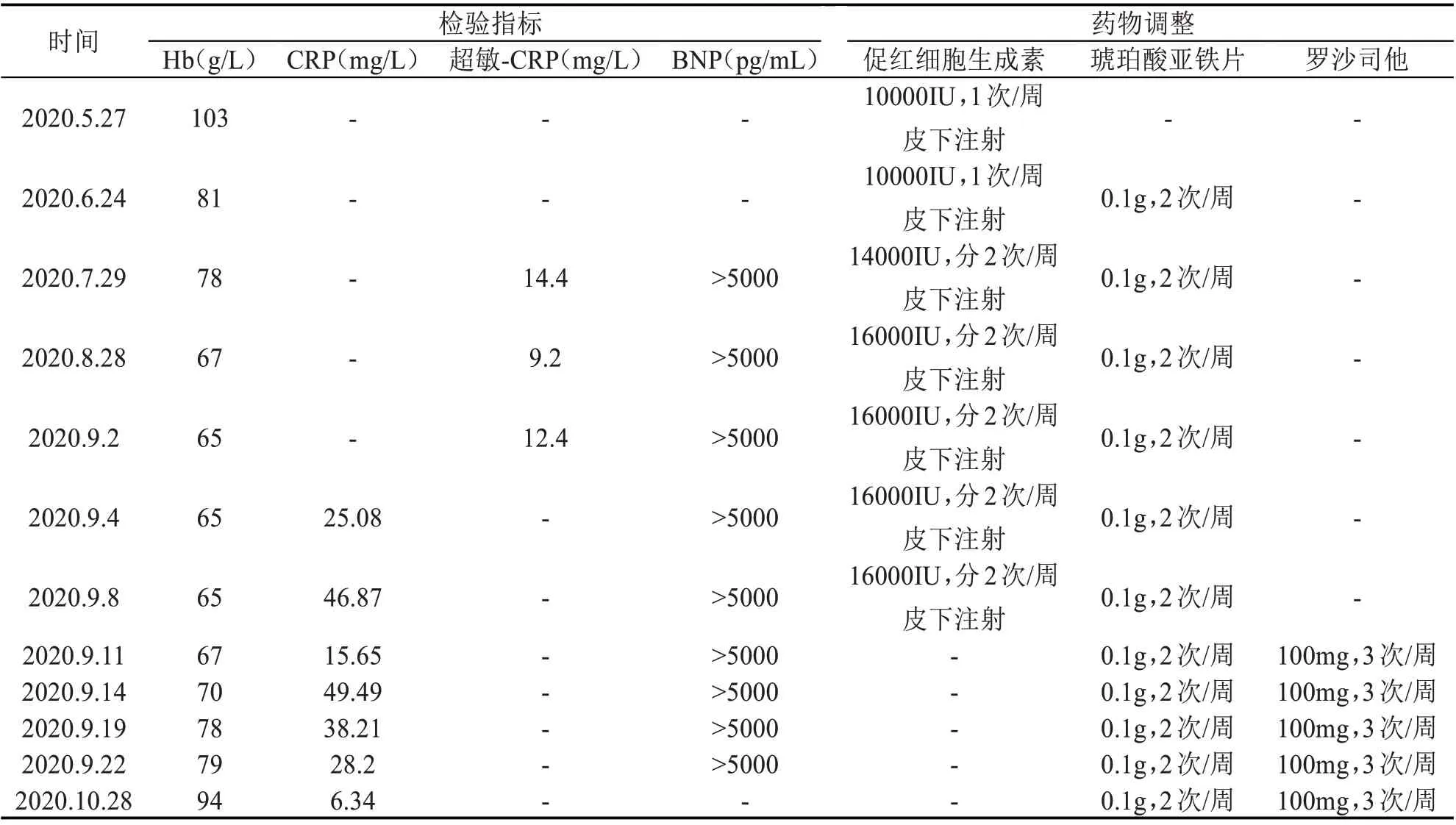
表1 患者Hb、CRP、超敏-CRP、BNP变化及药物调整
2 讨论
贫血是慢性肾脏病(chronic kidney disease,CKD)患者最常见的并发症之一,其患病率和严重程度随着CKD病程进展而逐渐升高[2]。尽管红细胞生成刺激剂(erythropoiesis-stimulating agents,ESAs)是目前公认的治疗肾性贫血的有效手段,其对合并心力衰竭的患者贫血的治疗有效性和安全性仍有争议。早前的随机双盲临床研究[3]显示,ESAs 治疗并不能改善心力衰竭合并轻-中度贫血患者的死亡率和住院率,然而却增加血栓栓塞事件的发生风险。在有效性方面,由于透析患者合并心力衰竭的贫血并不单纯与肾性贫血的发病机理一致,其潜在的炎症状态是导致促红素低反应性(erythropoietin hyporesponsiveness)的重要原因。
根据《肾性贫血诊断与治疗中国专家共识(2018修订版)》标准[4],ESAs低反应性定义为:按照患者体重计算的适量ESAs治疗1个月后,Hb水平与基线值相比无增加,将患者归类为初始ESAs 治疗反应低下。稳定剂量的ESAs 治疗后,为维持Hb 稳定需要两次增加ESAs 剂量且增加的剂量超过稳定剂量50%,则归类为获得性ESAs 反应性低下。在本例维持性血液透析患者中,自2020年6月开始,患者出现血红蛋白进行性下降,贫血加重;虽予积极调整促红素剂量,由每周10000U 加量到每周16000U,贫血未见改善。因此,该患者属于促红素反应低下。引起ESAS 低反应性的原因有多方面,包括铁缺乏、炎症状态、甲状旁腺功能亢进、营养不良、透析不充分等[4]。从该患者住院检查结果看,基本可以排除出血、溶血、矿物质和骨代谢异常等常见因素。虽然患者拒绝行骨髓穿刺,但从外周血网织红细胞计数及随后使用罗沙司他治疗后Hb可逐步回升,提示可以排除骨髓造血功能异常。进一步追溯患者病历资料,笔者发现自2020 年7 月患者多次查C-反应蛋白(C-reactive protein, CRP)或超敏CRP 均有升高;且患者存在慢性心力衰竭,2020 年7 月-2020 年9 月期间多次查BNP>5000pg/ml,虽经加强超滤脱水及宣教后,患者仍不能控制液体摄入量,反复双下肢浮肿,透析间期体重增加超过5%。这些信息提示我们慢性心力衰竭、炎症状态与患者贫血可能存在一定的联系。
炎症是心衰过程的重要组成部分,TNF-α、IL-6以及其他促炎细胞因子在心衰时升高,并且与Hb水平呈负相关[5]。炎症也普遍发生于CKD患者。据文献报道[6],透析患者炎症发生率达50%。CRP 是临床常用的炎症标志物,据统计,大约25%的CKD 患者存在CRP 水平升高[7]。炎症抑制CKD 合并心衰患者促红素活性是多因素的,一方面炎症影响患者EPO的产生,另一方面炎症导致EPO抵抗,其具体的病理生理机制阐释如下。
促红素生成减少是CKD 患者贫血共同的病理特征。研究也发现,心衰患者合并贫血时,其内源性EPO 的生成低于预期,血清EPO 的水平与贫血的程度不成比例[8]。目前对炎症影响促红素生成减少的分子机制尚未阐释清楚。有研究报道,促炎细胞因子IL-1β、TNF-α 通过活化GATA-2和NF-κB 通路,进而抑制EPO基因的表达[9]。
炎症也会导致促红素的反应性下降。Allen等[10]的体外实验显示:用尿毒症伴有炎症的病人自体血清孵育培养的骨髓细胞,对红系的抑制要强于无炎症的对照组,这一效应可在加入抗TNF-α 和(或)抗IFN-γ的中和抗体后被逆转。一方面,炎症状态下的免疫介质可能破坏EPO介导的下游信号传导通路(如JAK-STAT 通路),削弱EPO 受体敏感性[11]。另一方面,炎症引起铁调素水平升高,其机制可能依赖于IL6-铁调素轴的介导[12]。铁调素通过降解铁转运相关蛋白,限制十二指肠铁的吸收及巨噬细胞铁的释放,进而降低铁利用率[13-15]。而血清铁水平与Scribble 蛋白介导的细胞表面EPO 受体数量密切相关。缺铁条件下,转铁蛋白受体2(transferrin receptor 2,TfR2)与Scribble 形成的复合物很快被分解代谢,阻断了Scribble 介导的EPO 受体向红系祖细胞表面的运载,因而导致EPO 反应性下降[16]。此外,EPO/EPO受体信号活性的降低会损害erythroferrone的分泌,后者通常抑制铁调素的表达,增加铁的吸收和动员[17,18]。因此,EPO/EPO 受体反应下降会加剧铁的缺乏,而缺铁又导致EPO 受体数量的减少,对EPO反应降低,如此形成恶性循环。
基于担忧EPO在改善透析合并心衰患者的贫血有效性、及进一步增加ESA 剂量可能带来的安全性问题,我们对本例患者尝试改用了新的纠正肾性贫血药物——罗沙司他。罗沙司他是一种低氧诱导因子脯氨酰羟化酶抑制剂,其作用机制是使低氧诱导因子降解减少,进而提高体内低氧诱导因子水平。低氧诱导因子生理作用不仅使EPO 表达增加,也能使EPO 受体以及促进铁吸收和循环的蛋白表达增加[19]。
罗沙司他在中国进行的三期临床试验已证实了其在改善透析人群肾性贫血的疗效及安全性[20]。亚组分析的结果表明,无论患者的基础CRP水平如何,罗沙司他均能相似地提高Hb水平,并且这种疗效不依赖于剂量的增加。相比之下,接受EPO 治疗的患者,其贫血的改善效果与基础CRP 水平呈负相关。再者,对于基础CRP升高的亚组分析,应用罗沙司他治疗组比EPO 组能更大程度提高患者Hb 水平。这种独立于CRP 水平的治疗效应,表明罗沙司他有可能克服普遍存在于CKD 患者的炎症状态对红细胞生成的影响。
研究推测,罗沙司他可能对炎症状态下铁调素的升高有负性抑制作用[20]。Robert Provenzano 等的研究[21]显示,尽管患者血清铁蛋白水平升高,EPO组的转铁蛋白饱和度、血清铁水平相较于罗沙司他组有更明显的下降,提示后者铁的利用率更高。动物实验也表明,罗沙司他明显降低模型大鼠铁调素水平,并且增加与肠道铁吸收有关的基因表达,包括二价金属转运体-1和十二指肠细胞色素B[22]。
心血管事件是CKD 患者常见的并发症,也是引起CKD 患者死亡的主要病因[23,24]。在本案例中,患者Hb 的明显下降与心衰的发生在时间上存在明显的同步性。同时,我们也观察到,自Hb 开始明显下降后,患者的CRP 或超敏CRP 均有不同程度的升高。尽管我们先后两次增加患者ESA 处方用量,但贫血并未得到改善,提示炎症可能影响EPO 的反应性;反而,在随访过程中患者出现动静脉内瘘闭塞失功。因此,我们给患者更换了治疗方案,选择用罗沙司他纠正贫血。在按照推荐剂量并持续使用罗沙司他2 周后,患者的Hb 逐渐回升;并且在罗沙司他治疗过程中,即便患者并发肺部感染,后者并不影响罗沙司他疗效。笔者承认,在整个治疗过程中,我们忽略了静脉铁剂的使用,原因是考虑感染状态下,静脉铁剂的使用可能会增加氧化应激或产生更多氧自由基[25];然而,这也从侧面验证了罗沙司他能改善炎症状态下铁的利用率、克服炎症对红细胞生成的影响。有意思的是,笔者发现即使是患者贫血得到改善后,其BNP 仍持续超过5000pg/mL,考虑与患者依从性较差,不能控制水液摄入量有关,另一方面也提示我们罗沙司他纠正贫血的疗效可能不依赖于患者心功能状态。今后,我们仍需开展大样本的研究,以总结更多数据,进一步证实罗沙司他在尿毒症合并心力衰竭患者贫血的疗效及安全性;同时,我们也将进一步外推探讨罗沙司他对改善炎症状态下的肾性贫血疗效。
