双极电化学清除钛合金表面铁污染
2022-09-27李游游赵晓燕曹铁山赵杰孟宪明余伟程从前
李游游,赵晓燕,曹铁山,赵杰,孟宪明,余伟,程从前
双极电化学清除钛合金表面铁污染
李游游1,赵晓燕1,曹铁山1,赵杰1,孟宪明2,余伟1,程从前1
(1.大连理工大学,辽宁 大连 116085;2.中汽研汽车工程研究院有限公司,天津 300300)
针对耐蚀合金表面洁整化制造中,清洗介质和零件形状对清除表面异质铁污染的重要影响,提出了一种采用双极电化学清除铁污染的方法。采用COMSOL软件建立双极电化学模型,仿真计算了不同驱动电位和样品位置对表面电位分布及清除速率的影响,对喷丸强化后的钛合金表面进行铁污染清除试验,利用邻菲罗啉显色检验和电化学阻抗验证铁清除效果,分析典型参数对铁污染清除效果的影响。仿真模拟中电解池内的电压呈对称分布,样品表面电位为0 V;样品位于电解池中近正极1/4处时,其清除速率较中间位置时低;随驱动电压增加,有效清除长度减小,清除速率下降;显色检测显示钛合金原始试样表面的铁污染程度不均匀,红色色度值最高为15.5,清洗后合金表面从红色变为无色,阻抗谱图显示合金表面的耐蚀性增加。试验与仿真模拟结果吻合良好,双极电化学可用于钛合金表面铁污染的清除,为钛合金表面高清洁度制造提供了一种新思路。
钛合金;铁污染;双极电化学;显色检测
钛合金作为航空、核电和海洋工程等领域关键零部件用材,其耐蚀性不仅与合金成分组织有关,还与零部件加工制造过程的表面清洁度密切相关[1-3]。例如钛合金表面喷丸强化过程中,铸钢丸在高速击打钛合金表面时可能会残留弹丸碎粒造成铁污染,并且在腐蚀介质中铁污染会加速氢到钛合金内部的扩散,造成氢脆,降低钛合金的使用寿命[4]。目前表面清除铁污染的方法有化学酸洗法、机械法、电化学抛光法。其中化学酸洗法是用如氢氟酸、硝酸、氨基磺酸和柠檬酸等试剂与铁污染物反应,达到清洗效果,其具有成本低的优点,但存在环境污染问题[5-7];喷砂、二次喷丸等机械清除法是利用喷料或喷丸高速击打在钛合金零件的表面,去除零件表层的污染物层。二次喷丸是在一次喷丸的基础上选用强度较小的弹丸流高速撞击合金表面,用于改善一次喷丸造成的弹丸残留,降低表面粗糙度,提高合金表面完整性。机械清除法对于平整的零件的清除效果明显,但是对于一些复杂几何结构件清洁存在不足[8-9]。电化学抛光法是基于阳极溶解的过程从金属或合金表面清除污染的方式,速率较快,清除效果明显,但是阴阳极间的距离以及适合的辅助电极是影响电抛光的重要因素,因此在抛光复杂、精细的零件时会出现过度腐蚀现象,并且其对辅助电极的材料和设计要求苛刻[10-11]。因此,发展绿色便捷的表面铁污染清除方法,成为钛合金零部件高清洁度制造的重要环节。
双极电化学是利用两侧驱动电极产生的电场,使电解质中样品表面不接触就发生极化,进而发生氧化还原反应[12-13],具有设备简单、操作方便、成本低廉的优点,在传感和筛选[14-17]、电沉积[18-19]、腐蚀电化学检测[20-23]等领域受到研究者关注。Dorota等[24]采用硫酸蒸汽作为双极电化学反应的离子介质,施加驱动电压诱导商用锅炉钢发生露点腐蚀,利用双极电化学的电位梯度变化观察不同电位下钢材的腐蚀程度,对钢材进行筛选。结果显示,相较于碳钢和铁素体钢,不锈钢(AISI 347/AISI310)表现出良好的抗露点腐蚀性能。Zhou等[25]利用双极电化学的电位梯度,克服了使用动电位极化测试时扫描速率和曝光时间对测定不同外加电位下黄铜脱锌的影响,得出影响脱锌反应的参数仅仅是样品表面的局部作用电势,且在较低的外加电位下,生成氧化锌腐蚀产物,铜溶解后沉积在黄铜表层,当在较高的外加电位下时锌优先溶解,黄铜表面的腐蚀产物为氧化亚铜。Nashmil等[26]研究发现极化电位差与两侧驱动电压的大小和样品在电场中的位置有关。然而,双极电化学在清洗方面的研究应用鲜有报道。
本文提出采用双极电化学方法清除钛合金表面的铁污染,采用Comsol软件中电化学工程模块来仿真分析钛合金在不同驱动电位和放置位置下的电位变化,结合显色检测和电化学测试,对喷丸强化后的钛合金片进行典型工艺参数下的清洗验证。
1 试验
试验采用铸钢喷丸强化的6 mm钛合金圆片,化学成分(质量分数)为:Ti 6.01%,Al 4.00%,V 0.17%,Fe 0.12%,O 0.03%,C 0.01%,N 0.001%。圆片用酒精清洗吹干并用硅橡胶密封非测试面。采用10 cm×15 cm的铂片作为双极电化学电解池两端的驱动电极,电源为直流电源,清除液为3 mol/L硫酸钠和0.2 mol/L磷酸二氢钠的混合溶液。
采用COMSOL模拟软件构建20 cm×10 cm的二维电解池模型,其中清洗样品尺寸为6 cm×0.2 cm。研究不同驱动电压(2、6、10、30、60 V)以及样品位置对双极电化学电解池中电位分布的影响,取距离样品下表面3 mm处清除液中的电位数据拟合电位分布曲线。
将平均尺寸80 μm的铁粉压在测试面模拟残留的喷丸颗粒制造铁污染[27],采用2 V的驱动电压进行双极电化学清除试验。清洗后运用邻菲罗啉试剂检验铁污染前后的效果,在酸性测试溶液环境中,合金表面的铁污染会与测试液发生显色反应并生成络合物,反应为3phen+Fe2+→[Fe(phen)3]2+(红色络合物)[28-31]。将测试纸浸渍邻菲罗啉显色试剂并贴于样品表而进行显色反应,3 min后对测试纸进行拍照,之后用MATLAB提取图像色素点,通过红色像素的色度来评价测试面铁污染的清除情况。
在室温下,采用CS350型电化学工作站,首先测量铁污染在清除液中的极化曲线,清除液为3 mol/L硫酸钠和0.2 mol/L磷酸二氢钠的混合溶液。采用标准三电极体系,参比电极为Ag/AgCl电极,辅助电极为铂电极,扫描速率为0.5 mV/s,扫描范围为‒1.5~3 V(相对于Ag/AgCl电极),工作面积为0.39 cm2。其次对铁污染清除前和清除后的样品测试面进行动电位极化扫描和阻抗–频率扫描,分析清洗前后样品在一般环境下的耐腐蚀性,电解液为3.5%NaCl,扫描速率为0.5 mV/s,扫描范围为‒0.5~1.5 V(相对于Ag/AgCl电极),工作面积为1.8 cm2。在电化学测试之前,工作电极均在溶液中稳定一段时间,直至获得稳定的开路电位。试验中的所有电极电位都经过校正后换算成标准氢电极(SHE):
she=ag/agcl+0.197‒0.001 1×(‒25) (1)
式中:Ag/AgCl是用氯化银/氯化银参比电极测得的电位;SHE是在试验温度下对应的标准氢电极电位。此外,本研究中Ag/AgCl和SHE的单位为V。
2 结果与讨论
2.1 样品位置和驱动电压对电位分布的影响
图1为施加10 V驱动电压时样品在不同位置下电解池内模拟电位分布云图以及距离样品下表面3 mm处清除液的电位数据。在图1a和图1b中,颜色变化表明电解池中等电位值的变化,可见电位从正极+5 V至负极‒5 V递减,样品表面的电位为0 V[32]。当样品位于近电解池的正极一端时,电位随着样品位置的变化发生波动,右侧颜色范围整体左移,电位为0值的颜色范围向左侧拓展;其中白色实线表示电解池中的电流密度矢量,可以看出样品周围电流密度发生变化,在两端的电流密度较大。图1c中数值曲线表明,当样品位于中间时,电解池中的电位值呈对称分布;将样品放在靠近某一驱动电极端时,电解池中的电位值较小。
图2为不同驱动电压下电解池中的电位数据。如图2a所示,可以看出不同驱动电压下电解池中的电位分布规律大致相同,从左至右电位递减,样品处电位在0值附近。将图2a中样品位置处(红框)放大得到图2b,可以看出电解池两端驱动电压越大,清除液中的电位越大。
2.2 铁污染在清除液中的电化学腐蚀特性和清除速率
图3为纯铁在清除液中的极化曲线。可以看出,铁在清除液中的自腐蚀电位为‒0.39 V,随着电位的升高,电流密度增加,铁在清除液中发生阳极溶解过程,即:Fe‒2e+→Fe2+。当外加电位高于0.65 V时,电流密度突然减小,不随电压的变化而变化,表示待测面处于钝化状态,存在一层稳定的钝化膜[33-35],发生2Fe+3H2O→Fe2O3+6H++6e‒,此时的维钝电流密度为0.000 805 25 A/cm2,处于钝态的金属仍有一定的反应能力,即钝化膜的溶解和修复(再钝化)处于动态平衡[36]。当电压超过1.68 V时,待测表面从钝态变成活性溶解,电流随着电压的升高迅速增大,处于过钝化区。
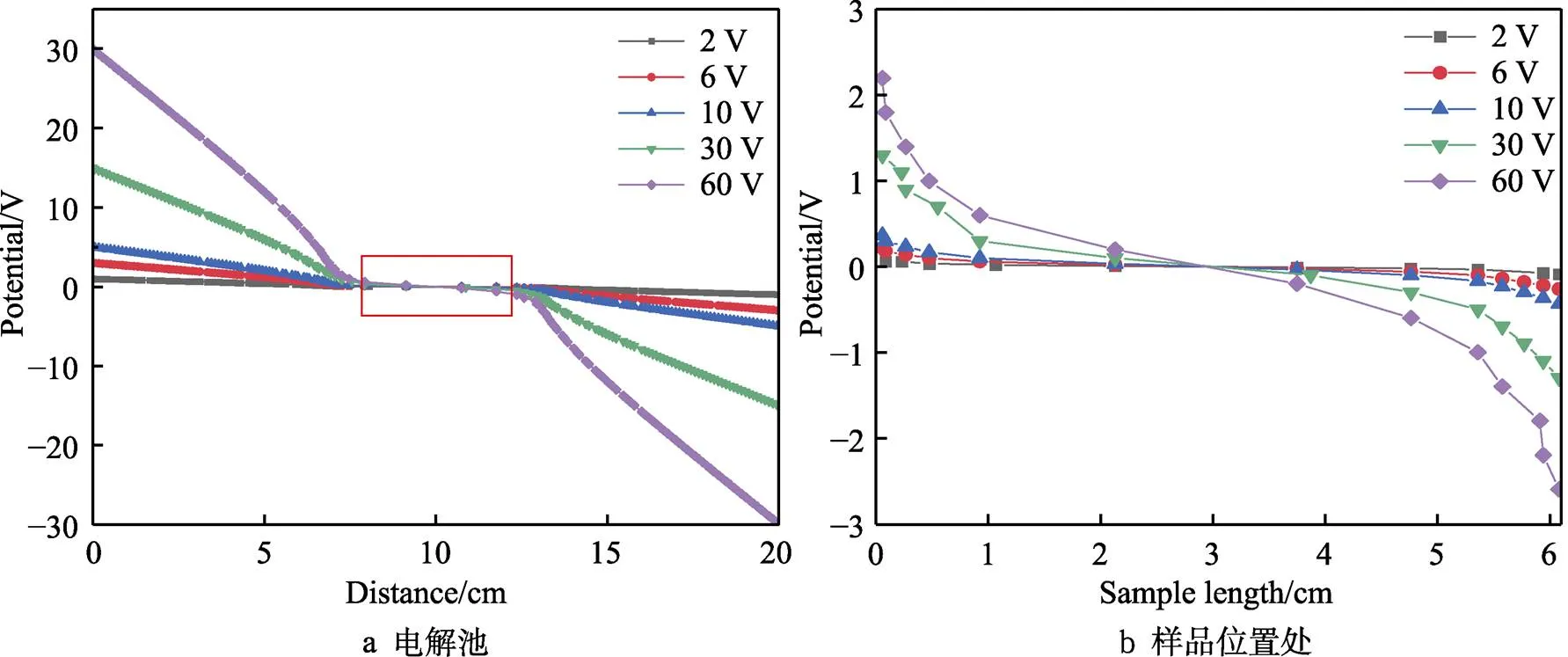
图2 不同驱动电压下电解池中的电位数据
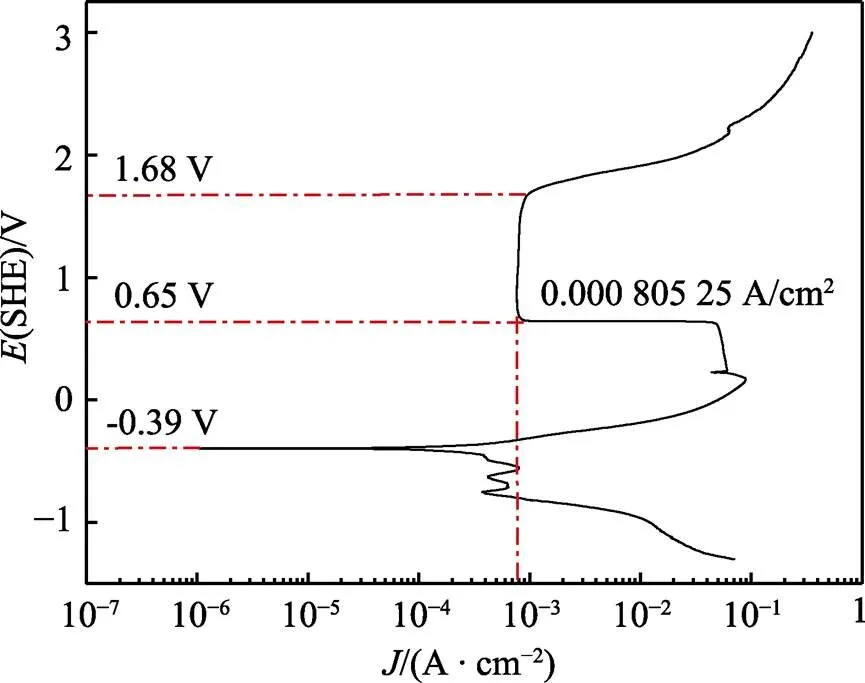
图3 纯铁在3 mol/L硫酸钠和0.2 mol/L磷酸二氢钠混合溶液中的极化曲线
样品表面近驱动电极正极的一侧在电场作用下,作为双极电极的阴极发生反应,相应的近驱动电极负极的一侧作为阳极发生反应,将样品表面的电位(0 V)与清除液间的电位差近似为极化电位,根据图3的极化曲线,获得该电位所对应的电流密度,采用深度指标表征铁污染的清除速率,公式为:
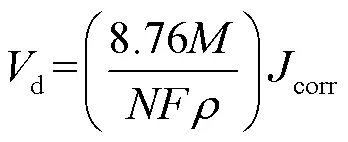
式中:corr为腐蚀电流密度;为金属密度;为得失电子数;为26.8 A·h/mol;为相对原子质量。
图4为不同位置下样品表面与清除液间的电位差(极化电位)分布和铁污染在清除液中的清除速率。从图4a可以看出,当样品位于电解池中间时,表面处于阳极溶解区,而位于近正极1/4处的样品表面,其左侧约0.7 cm的长度处于阴极极化区,并且极化电位较低。从图4b中可以看出,清除速率沿着长度方向变化,位于中间位置处的样品右侧表面因处于活化–钝化过渡区,清除速率下降。
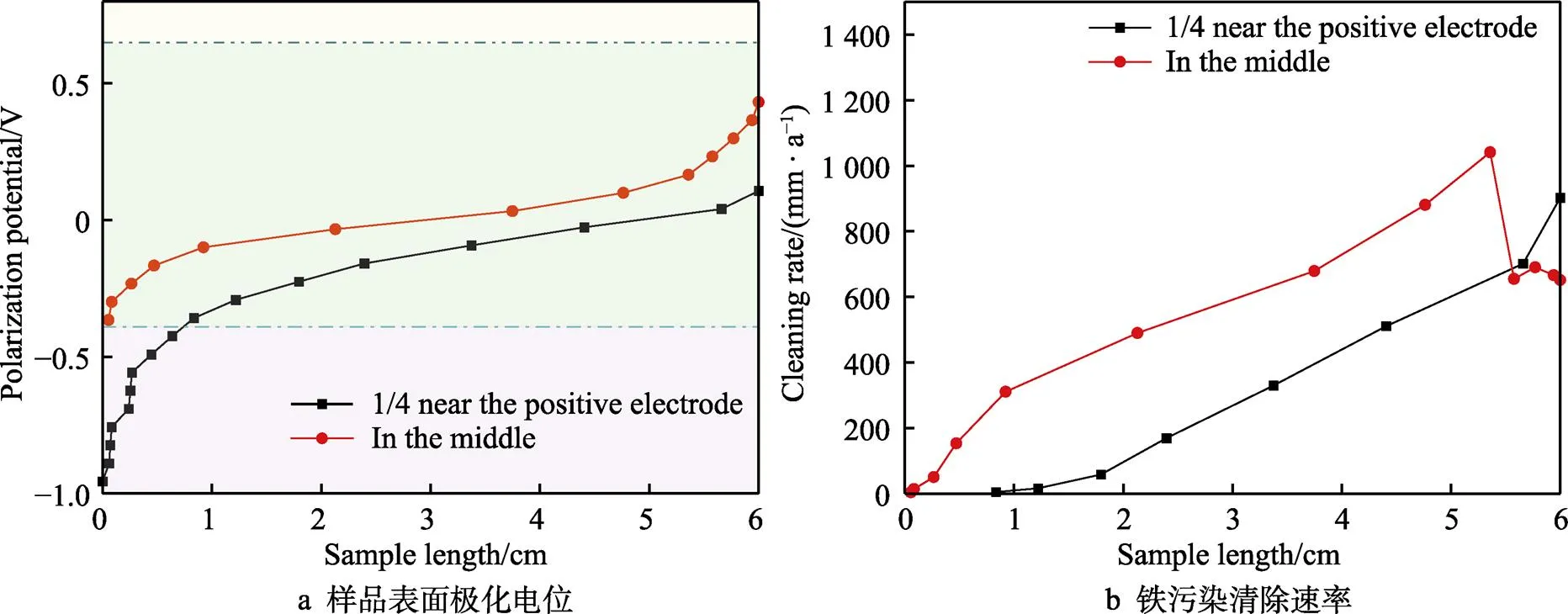
图4 不同位置下样品表面的极化电位分布与清除速率
图5为不同驱动电压下样品表面的极化电位分布和铁污染在清除液中的清除速率。从图5a中可以看出,当驱动电压为2、6、10 V时,整个样品表面处于可清除区;当驱动电压增加至30 V时,样品左侧表面处于阴极极化区,铁污染无法清除,右侧处于钝化区;当驱动电压为60 V时,试样右侧约0.5 cm处发生过钝化。从图5b中可以看出,从样品表面左侧至右侧,清除速率呈上升趋势;随着驱动电压的增加,样品左侧清除速率减小,右侧清除速率没有明显趋势。
假设电解池中样品是钛合金材料,且表面存在一层100 μm厚的铁污染,利用不同条件下清除铁污染的平均速率,得到了铁污染的清除时间(见表1)。

图5 不同驱动电压下样品表面的极化电位分布与清除速率
表1 铁污染的清除时间
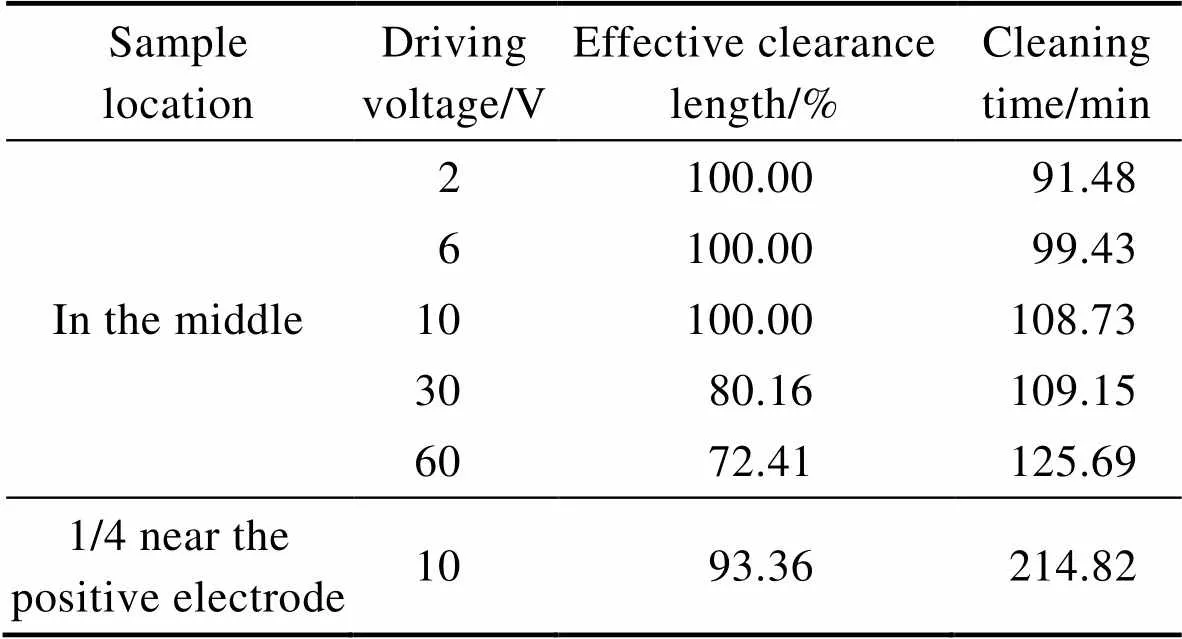
Tab.1 The cleaning time of iron contamination
从表1中可以看出,相同驱动电压下,与中间位置的样品相比,近正极1/4处样品表面铁污染的清除时间较长,清除长度较小。随着驱动电压的增加,有效清除长度减小,清除时间增加。驱动电压为2 V时,清除时间最短,为91.48 min。
2.3 铁污染清除试验结果
将钛合金放入电解池中,驱动电压选择2 V,根据图5数据可知,在此驱动电压下样品整个表面处于阳极极化区。图6为钛合金样品铁污染清除前和清除15 min后的显色三维图,可以看出原始钛合金表面右上方存在明显红色点状显色,色度值最高位为15.50,存在不同程度的铁污染。清除15 min后表面红色色度值在5.9以下,原始表面红色显色处的铁污染已被完全清除。

图6 钛合金表面铁污染清除前后显色三维图
removal: a) original sample; b) cleaning sample
图7为清除前后钛合金的极化曲线和阻抗谱,可以看出铁污染清除前样品表面不平整,极化曲线波动明显,清除后钛合金的极化曲线较为平滑,清洗后阳极极化区左移,整体电流减小,自腐蚀电位增加,自腐蚀电流密度下降,抗腐蚀性能提高。当电压超过1.15 V时,腐蚀电流突然增加,可能是因为当驱动电压为2 V时,样品右侧面部分位置处于活化–钝化过渡区,生成了部分铁氧化物,这些铁氧化物发生了溶解。阻抗图中可以看到在低、中、高频率区域表现出明显的电容特性,即为图上不完整的一段电容弧,表明铁清除后体系的腐蚀过程是由样品表面与电解液之间界面发生的电荷转移所主导。电容弧的半径反映了电荷转移电阻的大小[37]。铁清除后的电容弧半径大于清除前,表明铁清除后的电荷转移电阻更大。
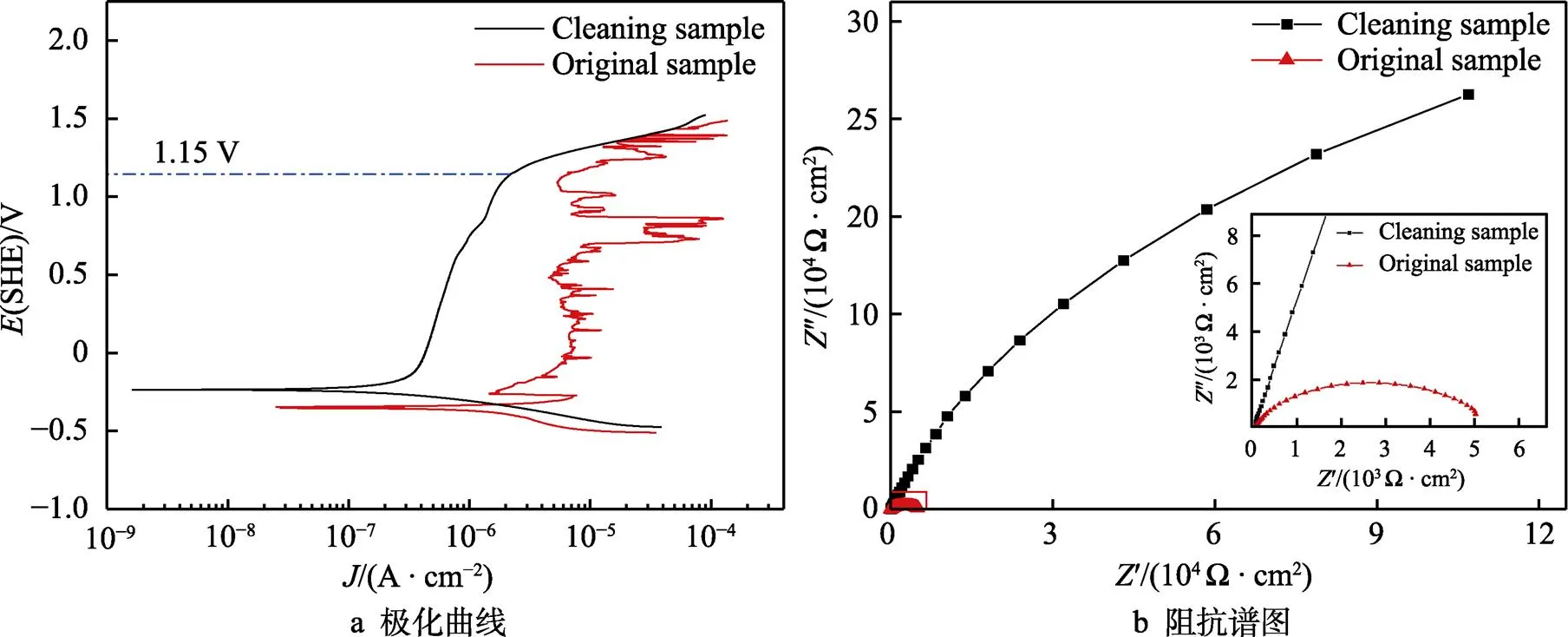
图7铁污染清除前后的电化学数据
3 讨论
电化学抛光又称阳极抛光或电解抛光,是一种基于阳极溶解过程从金属或合金中去除材料的抛光过程。在电解质溶液中工作电极与电源正极相连作为阳极,辅助电极与电源负极相连作为阴极,通电时,基于电解过程,凹凸不平的工作电极表面形成电阻率较大的高黏度氧化物薄膜,突出的部分由于氧化物膜较薄,电阻小,因此被选择性溶解,如表面的铁污染,从而达到抛光和提高表面完整性的目的。但在电化学抛光中,辅助电极与工作电极的面积比和两者间的距离是影响电化学抛光中电流密度以及电位分布的重要因素[38]。因此对于复杂几何零件,在电化学抛光过程中,难以达到工作电极的每个表面与辅助电极距离相等的条件,有些表面存在过度腐蚀的现象,所以为了清除特定地方的污染物,往往需要定制特定的辅助电极,这样的电极不仅结构复杂,价格昂贵,而且适用性不强。然而相对于其他清除方法,电化学抛光具有较快的清除速率、较高的表面完整性等优点,因此为解决辅助电极对电化学抛光的限制,研究了采用双极电化学的方法来进行铁污染清除。
在双极电化学装置中,样品与电源无接触,施加驱动电压后,电解池中形成一定强度的电场,样品两端及其部分表面附近的电解液中会同时发生氧化还原反应,其极性取决于驱动电极。当达到电平衡时,位于电解池中的导体样品作为一个等势体[32],其电势为0 V(见图1)。王蕾等[39]阐述了双极电化学体系的电压分布规律,若样品为一个均匀导体,则样品上的极化电位和样品两端的极化电位差公式为:
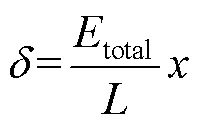
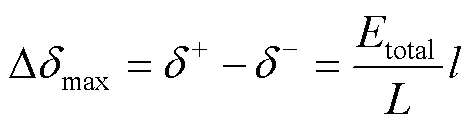
式中:total为驱动电压;为驱动电极的距离;为样品在电解池中的位置;Δmax为样品两端的最大极化电位差;为极化电位;为样品的长度。可以知道,对于同一个双极电化学体系,样品两端的极化电位差与驱动电压有关,随着驱动电压的增加,极化电位差增大,有利于样品两端发生氧化还原反应。从热力学角度看,样品两端发生反应的法拉第要求是样品沿长度的电压降要大于其两端氧化还原反应的电位差[40]。且驱动电极之间的距离不变时,样品上的极化电位沿其长度方向变化,Dorri及其团队[18]就利用这一性质在样品电极表面沉积了梯度分布的纳米铜。当样品在中间时,样品表面与溶液之间的极化电位是对称的,即样品氧化还原反应在样品表面对称分布[41-43]。将样品放在靠近某一驱动电极时,极化电位减小,可清除长度减小,对照图4b可以看出,位于阳极极化区的样品上铁污染的清除速率下降,因此改变样品的放置位置对只想要样品上部分面积发生单一的某一氧化或者还原反应有较大帮助。
本次试验则是利用铁污染与和钛合金在盐溶液中腐蚀电位的差异,以及双极电化学的电位梯度分布,省略了电抛光处理中设计特殊电极的步骤,使得表面铁污染在阳极极化区发生氧化反应,精准清除铁污染,不会存在过腐蚀的现象,但是选用合适的清除液成分以及驱动电压是十分重要的。显色结果验证了双极电化学清除铁污染的可行性,同时发现模拟计算的铁清除速率与试验得到的速率存在差异,分析发现是因为理论模拟中钛合金表面均匀覆盖一层铁污染,而试验中喷丸强化后残留的铁污染是局部分散的(见图6),因此试验时合金表面的铁污染清除速率较快。
4 结论
1)通过模拟和试验表明,双极电化学方法可以用来清除在铁阳极溶解电位范围内发生表面钝化的合金表面的铁污染。模拟计算中,样品与其表面电解液的电位差随着驱动电压的增加而增大,且样品的位置越靠近驱动电极,样品近驱动电极一侧的电位差越小,所对应的氧化还原区域也越小。
2)当样品位于中间位置时,与位于近正极1/4处相比,清除铁污染的速率快,清除长度长;随着驱动电压的增加,可清除区域减小,清除速率下降。
3)在试验中,经过双极电化学试验后的样品表面铁污染被清除,其极化曲线和阻抗谱显示清除后表面耐蚀性增强。
[1] ESKIN G I, SINYAVSKII V S, USOVA V V. Regularities of the Intensifying Effect of Ultrasonic Treatment on Titanium Alloy Pickling[J].Protection of Metals, 2003, 39(6): 551-559.
[2] ZABLER S. Interstitial Oxygen Diffusion Hardening—A Practical Route for the Surface Protection of Titanium[J]. Materials Characterization, 2011, 62(12): 1205-1213.
[3] 王利华, 王力强, 罗长鹏, 等. 激光清洗钛合金表面氧化皮对基体性能的影响[J]. 热加工工艺, 2021, 8(5): 15-21.
WANG Li-hua, WANG Li-qiang, LUO Chang-peng, et al. Effect of Laser Cleaning Titanium Alloy Surface Scale on Matrix Properties[J]. Hot Working Technology, 2021, 8(5): 15-21.
[4] 余存烨. “铁”对钛制化工设备使用影响的讨论[J]. 腐蚀与防护, 2005, 26(9): 407-410.
YU Cun-ye. Effects of "Iron" on the Service of Chemical Equipment Made of Titanium[J]. Corrosion & Protection, 2005, 26(9): 407-410.
[5] 金欢, 李璇, 潘柳, 等. 高温合金零件喷丸后表面铁污染物的去除剂及去除方法: CN105862043A[P]. 2016-08-17.
JIN Huan, LI Xuan, PAN Liu, et al. Remover for Removing Iron Contaminants on Surface of High Temperature Alloy Part after Shot Blasting and Removal Method: CN105862043A[P]. 2016-08-17.
[6] 臧殿荣. 氨基磺酸在不锈钢凝汽器管线清洗中的应用[J]. 清洗世界, 2012, 28(12): 4-8.
ZANG Dian-rong. Amino Acid in a Stainless Steel Condenser Tube Cleaning[J]. Cleaning World, 2012, 28(12): 4-8.
[7] 裴蓓, 易光硕. PTA装置钛材换热器的清洗研究[J]. 聚酯工业, 2016, 29(5): 30-32.
PEI Bei, YI Guang-shuo. Research on the Cleaning of Titanium Heat Exchanger in PTA Plant[J]. Polyester Industry, 2016, 29(5): 30-32.
[8] 徐鲲濠, 汤先辉, 史奎, 等. 一种钛合金叶片及其加工方法: CN107866743A[P]. 2018-04-03.
CAO Ye, ZHANG Yong-zhong, LIU Yan-tao, et al. Double-Alloy Whole Blade Disc and Preparation Method Thereof: CN107866743A[P]. 2018-04-03.
[9] 何嘉禧, 汪舟, 甘进, 等. 二次喷丸42CrMo钢表面完整性的数值模拟研究[J]. 表面技术, 2020, 49(6): 216-223.
HE Jia-xi, WANG Zhou, GAN Jin, et al. Numerical Simulation on Surface Integrity of 42CrMo Steel after Dual Shot Peening[J]. Surface Technology, 2020, 49(6): 216-223.
[10] 王百宁. 钛设备铁污染的危害与防护措施[J]. 钛工业进展, 2004, 21(3): 32-34.
WANG Bai-ning. The Harm and Preventive Measures of Titanium Equipment Stained by Iron[J]. Titanium Industry Progress, 2004, 21(3): 32-34.
[11] HAN Wei, FANG Feng-zhou. Fundamental Aspects and Recent Developments in Electropolishing[J]. International Journal of Machine Tools and Manufacture, 2019, 139: 1-23.
[12] FOSDICK S E, KNUST K N, SCIDA K, et al. Bipolar Electrochemistry[J]. Angewandte Chemie, 2013, 52(40): 10438-10456.
[13] LOGET G, ZIGAH D, BOUFFIER L, et al. Bipolar Electrochemistry: From Materials Science to Motion and beyond[J]. Accounts of Chemical Research, 2013, 46(11): 2513-2523.
[14] SHAYAN M, KIANI A. Digital Versatile Disc Bipolar Electrode: A Fast and Low-Cost Approach for Visual Sensing of Analytes and Electrocatalysts Screening[J]. Analytica Chimica Acta, 2015, 888: 52-58.
[15] CHANG B Y, CROOKS J A, CHOW K F, et al. Design and Operation of Microelectrochemical Gates and Integrated Circuits[J]. Journal of the American Chemical Society, 2010, 132(43): 15404-15409.
[16] 付银鹏, 王红旺, 王靖宵, 等. 双极电化学法制备有机电化学晶体管阵列[J]. 半导体技术, 2020, 45(7): 524-529.
FU Yin-peng, WANG Hong-wang, WANG Jing-xiao, et al. Preparation of Organic Electrochemical Transistor Arrays by Bipolar Electrochemistry Method[J]. Semiconductor Technology, 2020, 45(7): 524-529.
[17] LIN Xiao-mei, ZHENG Li-yan, GAO Gong-min, et al. Electrochemiluminescence Imaging-Based High- Through Put Screening Platform for Electrocatalysts Used in Fuel Cells[J]. Analytical Chemistry, 2012, 84(18): 7700-7707.
[18] DORRI N, SHAHBAZI P, KIANI A. Self-Movement of Water Droplet at the Gradient Nanostructure of Cu Fabricated Using Bipolar Electrochemistry[J]. Langmuir: the ACS Journal of Surfaces and Colloids, 2014, 30(5): 1376-1382.
[19] 许飞. 双极电化学法电沉积镍铜二组分金属的研究[D]. 合肥: 合肥工业大学, 2018: 17-29.
XU Fei. Study of Electrodeposition of Nickel and Copper Two Component Metals by Bipolar Electrochemistry[D]. Hefei: Hefei University of Technology, 2018: 17-29.
[20] MUNKTELL S, TYDÉN M, HÖGSTRÖM J, et al. Bipolar Electrochemistry for High-Throughput Corrosion Screening[J]. Electrochemistry Communications, 2013, 34: 274-277.
[21] MUNKTELL S, NYHOLM L, BJÖREFORS F. Towards High Throughput Corrosion Screening Using Arrays of Bipolar Electrodes[J]. Journal of Electroanalytical Chemistry, 2015, 747: 77-82.
[22] Nadine p, Vincent v. Local Electrochemical Measurements in Bipolar Experiments for Corrosion Studies[J]. Chem Electro Chem, 2016, 3(3): 415-421.
[23] ZHOU Yi-qi, ENGELBERG D L. Fast Testing of Ambient Temperature Pitting Corrosion in Type 2205 Duplex Stainless Steel by Bipolar Electrochemistry Experiments[J]. Electrochemistry Communications, 2020, 117: 106779.
[24] BANKIEWICZ D, VAINIO E, YRJAS P, et al. Application of Bipolar Electrochemistry to Accelerate Dew Point Corrosion for Screening of Steel Materials for Power Boilers[J]. Fuel, 2020, 265: 116886.
[25] ZHOU Yi-qi, MAHMOOD S, ENGELBERG D L. Brass Dezincification with a Bipolar Electrochemistry Technique[J]. Surfaces and Interfaces, 2021, 22: 100865.
[26] KARIMIAN N, HASHEMI P, AFKHAMI A, et al. The Principles of Bipolar Electrochemistry and Its Electroanalysis Applications[J]. Current Opinion in Electrochemistry, 2019, 17: 30-37.
[27] Cheng d, Cao r, Song s, et al. Use of Colour Change Indicators to Quantify Iron Contamination on Stainless Steel[J]. Corrosion Engineering, Science and Technology, 2015, 50(5): 346-354.
[28] 程从前, 曹铁山, 宋冠宇, 等. 一种显色表征不锈钢钝化膜质量的新方法[J]. 原子能科学技术, 2013, 47(10): 1872-1877.
CHENG Cong-qian, CAO Tie-shan, SONG Guan-yu, et al. A New Method of Chromaticity Inspection for Evaluating Quality of Passive Film on Stainless Steel[J]. Atomic Energy Science and Technology, 2013, 47(10): 1872-1877.
[29] CHENG Cong qian, ZHAO Jie, CAO Tie shan, et al. Facile Chromaticity Approach for the Inspection of Passive Films on Austenitic Stainless Steel[J]. Corrosion Science, 2013, 70: 235-242.
[30] 杨树凯, 程从前, 侯艳, 等. 核电站不锈钢表面钝化膜的显色检测应用及质检策略[J]. 材料保护, 2016, 49(12): 91-94, 8.
YANG Shu-kai, CHENG Cong-qian, HOU Yan, et al. Color-Change Inspection Application and Quality Control Strategy for Surface Passivation on Stainless Steel Equipment in Nuclear Power Plant[J]. Materials Protection, 2016, 49(12): 91-94, 8.
[31] 杨树凯, 程从前, 赵杰. 不锈钢钝化膜显色检测评估及其在核电不锈钢阀门的应用[J]. 全面腐蚀控制, 2016, 30(1): 28-32.
YANG Shu-kai, CHENG Cong-qian, ZHAO Jie. The Evaluation of Color-Change Detection on Stainless Steel Passive Film and the Application of the Stainless Steel Valve in Nuclear Power Plant[J]. Total Corrosion Control, 2016, 30(1): 28-32.
[32] QI Zhen-lian, YOU Shi-jie, REN Nan-qi. Wireless Electrocoagulation in Water Treatment Based on Bipolar Electrochemistry[J]. Electrochimica Acta, 2017, 229: 96-101.
[33] MACDONALD D D. The Point Defect Model for the Passive State[J]. Journal of the Electrochemical Society, 1992, 139(12): 3434.
[34] MACDONALD D D, URQUIDI‐MACDONALD M. Theory of Steady-State Passive Films[J]. Journal of the Electrochemical Society, 1990, 137(8): 2395- 2402.
[35] 杜艳芳. 碳钢在碳酸铵溶液中的腐蚀研究试验改进[J]. 大学化学, 2019, 34(6): 33-37.
DU Yan-fang. Improvement in the Experiment of Corrosion of Carbon Steel in Ammonium Carbonate Solution[J]. University Chemistry, 2019, 34(6): 33- 37.
[36] 周天宇, 于宇新, 赵博, 等. 20#碳钢在HCO3‒和Cl‒混合溶液中的点蚀行为研究[J]. 安全、健康和环境, 2020, 20(11): 30-34.
ZHOU Tian-yu, YU Yu-xin, ZHAO Bo, et al. Study on the Pitting Corrosion of 20# Steel in HCO3-and Cl–Mixed Solution[J]. Safety Health & Environment, 2020, 20(11): 30-34.
[37] 孙沛, 古一, 李雅琪, 等. 钛及钛合金多弧离子镀Ta-10W涂层的腐蚀性能[J]. 粉末冶金材料科学与工程, 2019(5): 413-421.
SUN Pei, GU Yi, LI Ya-qi, et al. Corrosion Performance of Ta-10W Coating on Titanium and Its Alloy by Multi-Arc Ion Plating[J]. Materials Science and Engineering of Powder Metallurgy, 2019(5): 413-421.
[38] 姚燕生, 周瑞根, 张成林, 等. 增材制造复杂金属构件表面抛光技术[J]. 航空学报, 2022, 43(4): 244-256.
YAO Yan-sheng, ZHOU Rui-gen, ZHANG Cheng- lin, et al. Surface Polishing Technology for Additive Manufacturing of Complex Metal Components[J]. Acta Aeronautica et Astronautica Sinica, 2022, 43(4): 244-256.
[39] 王蕾, 温利权, 刘红云. 双极性电化学的概述及研究进展[J]. 化学教育, 2017, 38(4): 1-6.
WANG Lei, WEN Li-quan, LIU Hong-yun. Summary and Research Progress of Bipolar Electrochemistry[J]. Chinese Journal of Chemical Education, 2017, 38(4): 1-6.
[40] KARIMIAN N, HASHEMI P, AFKHAMI A, et al. The Principles of Bipolar Electrochemistry and Its Electroanalysis Applications[J]. Current Opinion in Electrochemistry, 2019, 17: 30-37.
[41] KOIZUMI Y, SHIDA N, OHIRA M, et al. Electropolymerization on Wireless Electrodes towards Conducting Polymer Microfibre Networks[J]. Nature Communications, 2016, 7: 10404.
[42] KUMSAPAYA C, LIMTRAKUL J, KUHN A, et al. Bipolar Electrografting on the Inner Wall of Carbon Nanotubes[J]. Chemelectrochem, 2016, 3(3): 410-414.
[43] RAMASWAMY R, SHANNON C. Screening the Optical Properties of Ag-Au Alloy Gradients Formed by Bipolar Electrodeposition Using Surface Enhanced Raman Spectroscopy[J]. Langmuir: the ACS Journal of Surfaces and Colloids, 2011, 27(3): 878-881.
Dipolar Electrochemical Removal of Iron Contamination on Titanium Alloy Surface
1,1,1,2,1,1
(1. Dalian University of Technology, Liaoning Dalian 116085, China; 2. China Automotive Technology and Research Center Co., Ltd., Tianjin 300300, China)
Aiming at the important influence of cleaning medium and part shape on the removal of surface heterogeneous iron contamination in the clean and tidy manufacturing of corrosion-resistant alloy surfaces, a method for removing iron contamination by bipolar electrochemistry was proposed. Firstly, the electrochemical module in COMSOL software was used to establish the bipolar electrochemical model. The size of the electrolytic cell was 20 cm×10 cm, the size of the cleaning sample was 6 cm×0.2 cm, and the cleaning solution was the mixed solution of 3 mol/L Na2SO4and 0.2 mol/L NaH2PO4. The potential distribution of electrolytic cell under different driving voltages (2 V, 6 V, 10 V, 30 V, 60 V) was calculated. The potential distribution changes in the cell were calculated when the sample was located in the middle of the cell and near the positive 1/4 when the driving voltage was 10 V. The potential data fitted with the potential distribution curve in the clearance solution 3 mm away from the lower surface of the sample. Secondly, a standard three-electrode system was used to measure the polarization curve of pure iron in the scavenging solution, in which a reference electrode was Ag/AgCl electrode and an auxiliary electrode was platinum electrode. The corrosion depth index was used to characterize the removal rate of iron pollution, and the removal rate curves under different parameters were drawn. Finally, iron pollution removal test was carried out on the surface of titanium alloy after shot peening. A 10 cm×15 cm platinum plate was used as the driving electrode, and the dc power supply was used. The removal effect was tested by the phenanthroline color reaction. In addition, the dynamic potential polarization scan and impedance-frequency scan were performed on the sample test surface before and after cleaning. This is used to analyze the corrosion resistance of the samples in general conditions before and after cleaning. The electrolyte was 3.5% NaCl, the scanning rate was 0.5 mV/s, and the scanning range was from ‒0.5 V to 1.5 V (relative to Ag/AgCl electrode). The results show that the voltage in the electrolytic cell is symmetrically distributed in the simulation, and the surface potential of the sample is 0 V. The removal rate of the sample in the middle of the electrolytic cell is higher than that near the positive electrode 1/4. With the increase of driving voltage, the effective removal length decreases, and the removal rate increases when the driving voltage exceeds 10 V. The color test shows that the iron contamination on the surface of the original titanium alloy sample is uneven, and the highest red chromaticity value was 15.5. After cleaning, the alloy surface changes from red to colorless, and the impedance spectroscopy shows that the corrosion resistance of the alloy surface increased. The experimental results are in good agreement with the simulation results. The bipolar electrochemistry can be used to remove the iron contamination on the surface of titanium alloy, which provides a new idea for high cleanliness manufacturing of titanium alloy surface.
titanium alloy; ironpollution; bipolar electrochemistry; color detection
2021-08-19;
2021-11-17
LI You-you (1996-), Female, Postgraduate, Research focus: metal corrosion and protection, simulation.
TG174
A
1001-3660(2022)09-0226-08
10.16490/j.cnki.issn.1001-3660.2022.09.000
2021–08–19;
2021–11–17
李游游(1996—),女,硕士研究生,主要研究方向为金属腐蚀与防护、仿真模拟。
程从前(1982—),男,博士,副教授,主要研究方向为不锈钢表面钝化及完整性评价、车身轻量化材料腐蚀与可靠性等。
CHENG Cong-qian (1982-), Male, Doctor, Associate professor, Research focus: stainless steel surface passivation and integrity evaluation, lightweight material corrosion and reliability of car body, etc.
李游游, 赵晓燕, 曹铁山, 等. 双极电化学清除钛合金表面铁污染[J]. 表面技术, 2022, 51(9): 226-233.
LI You-you, ZHAO Xiao-yan, CAO Tie-shan, et al. Dipolar Electrochemical Removal of Iron Contamination on Titanium Alloy Surface[J]. Surface Technology, 2022, 51(9): 226-233.
责任编辑:万长清
