细胞外组蛋白在放射性肺损伤中的诊断作用及机制
2022-09-26刘立杰白立立张小陆霍新龙于晓麟贾洪菊华海侠
刘立杰,银 英,白立立,张小陆,霍新龙,于晓麟,顾 涛,贾洪菊,张 双,华海侠
(秦皇岛市第一医院,河北 秦皇岛066000)
放射治疗是肺癌患者的主要治疗手段之一,可以提高肿瘤的局部控制率。但由于肺是射线敏感器官,其组织细胞容易受到辐射的损坏[1]从而可以引发放射性肺损伤(RILI)。RILI的发病机制可能与炎症反应、肺泡及内皮细胞损伤等有关[2]。在体外研究中,细胞外组蛋白可损伤内皮细胞[3]、刺激细胞因子的释放[4],并可以诱导嗜中性粒细胞细胞外诱捕网的形成和髓过氧化物酶的释放。因此,推测细胞外组蛋白可能作为促炎介质在RILI的发生发展中占据重要地位。本研究拟通过收集接受胸部放疗的肺癌患者并利用细胞实验,测定细胞外组蛋白及相关炎症因子以分析其动态变化规律。
1 资料与方法
1.1 临床资料
选取2018年1月-2020年12月在本院首次诊断并进行放射治疗的75例Ⅰ-ⅢB期肺癌患者进行分析。男性41例,女性34例,年龄45-72岁,中位年龄58岁。按组织病理类型分类:49例NSCLC,26例SCLC。按患者临床TNM分期分类:19例Ⅰ-Ⅱ期,22例ⅢA期,34例ⅢB期。入组患者中36例进行同步或序贯化疗。本研究获医学伦理委员会批准。
纳入标准:(1)经病理证实临床分期为Ⅰ-Ⅲ期的原发性肺癌患者。(2)此前未接受过胸部手术、放疗或化学药物治疗。(3)预计生存时间>6个月。(4)卡氏功能状态(KPS)评分≥70分。
排除标准:(1)放疗未完成或者放疗中未按照规定安排(5F/W)进行治疗的患者。(2)随访时间未满6个月或者死亡者。(3)KPS评分<70分。
1.2 放射治疗
所有入组患者放疗前已完成病史采集和体格检查,行血常规、肝肾功能等检验已确定无放疗禁忌。将患者经CT模拟定位后的图像传输至瓦里安治疗系统,医师在CT定位图像上使用肺窗及纵隔窗逐层勾画靶区,放疗方式采用调强放射治疗,放疗剂量54Gy-66Gy,中位剂量60Gy。处方剂量2Gy/次,1次/日,5次/周。
1.3 方法
于放疗前1天、放疗后第1天,第1、3、5周时抽取患者空腹外周静脉全血3-5 ml,4℃静止低温冷藏于EDTA 抗凝管中。样本处理:标本采集1 h内,3 000 r/min离心10 min。后将上清液提取至Eppendorf管内,-80℃冰箱保存。
采用ELISA方法测定血清细胞外组蛋白水平,采用化学比色法检测血清髓过氧化物酶(MPO)活性,采用ELISA方法测定血清LDH含量,采用Luminex方法测定血清中多项细胞因子。细胞外组蛋白ELISA测定试剂盒及MPO、LDH试剂盒购自德国Roche公司;Luminex检测系列细胞因子试剂盒购自美国Affymetrix eBioscience。具体操作步骤严格按照试剂盒说明书进行。
1.4 体外实验
常规培养人肺上皮细胞系(BEAS-2B)和人单核细胞系(U937),待细胞生长至80%-90%融合度之后,将RILI组患者放疗后1周血清按50%的比例添加,温育培养24小时后取细胞上清液检测LDH和炎症因子。同时,一组细胞给予特异性抗组蛋白H4抗体(20 μg/ml)进行干预。
1.5 RILI评价标准
按照美国放射治疗肿瘤协作组(RTOG)分级标准[5]进行分级评价,根据临床症状、胸部X线片、胸部CT和肺功能丧失进行评分,分成0-Ⅴ级。评分包括三个主观量表和两个客观量表。主观评分包括咳嗽、呼吸困难和胸痛。客观量表包括胸部X线片和胸部CT以及肺功能测试。Ⅰ级及以上即定义为RILI。
1.6 随访及统计学分析
采用SPSS21.0软件对数据进行分析。计量资料正态分布以均数±标准差表示,两组资料比较采用两组独立样本t检验,非正态分布采用中位数及四分位数表示,应用秩和检验分析。P<0.05为差异有统计学意义。
2 结果
2.1 RILI发生率情况
75例肺癌患者中,发生RILI 17例,发生率为22.67%。17例RILI患者的发生时间为放射治疗后1-6个月,中位时间为3.5个月。
2.2 肺癌患者放疗后细胞外组蛋白水平的动态变化
与非RILI组相比,RILI组患者各时间点血清细胞外组蛋白水平(μg/ml) 总体差异有统计学意义(P<0.05),随时间变化,细胞外组蛋白水平逐渐升高,1w达高峰(52.34±1.03) μg/ml,3w、5w保持高水平。见图1。
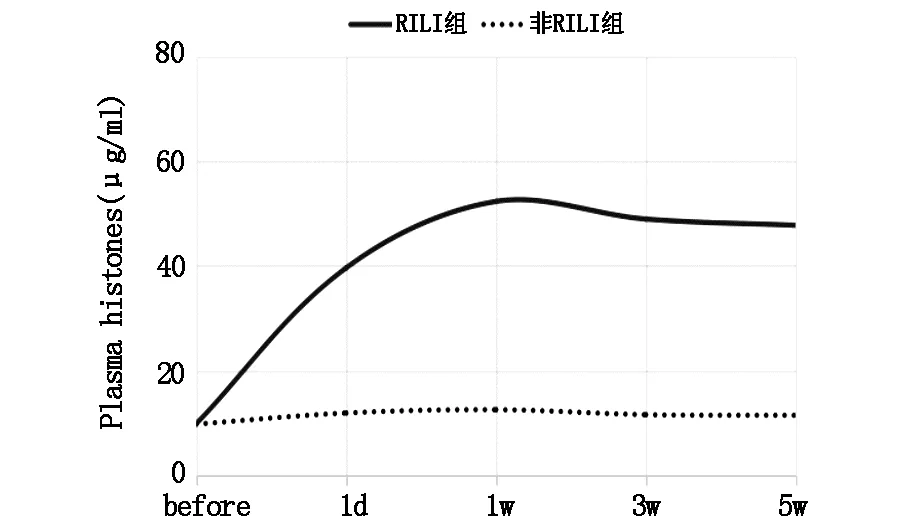
图1 RILI组、非RILI组不同时间血清细胞外组蛋白水平变化
2.3 肺癌患者放疗后LDH、MPO水平的动态变化
与非RILI组相比,RILI组患者各时间点LDH活性(U/L)总体差异有统计学意义(P<0.05),随时间变化,LDH活性在放疗后1 d即开始升高(178.75±1.07)U/L,1w、3w、5w继续保持在高水平。见图2。
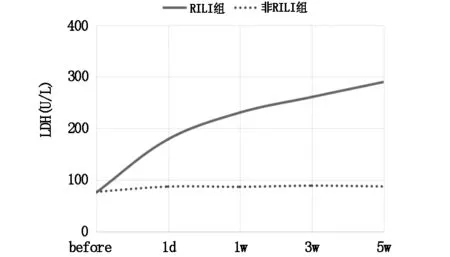
图2 RILI组、非RILI组不同时间LDH活性变化规律
与非RILI组相比,RILI组患者各时间点 MPO活性(U/L)总体差异有统计学意义(P<0.05),随时间变化,MPO活性逐渐升高,3w达高峰(50.24±0.35)U/L,5w仍持续较高水平(图3)。
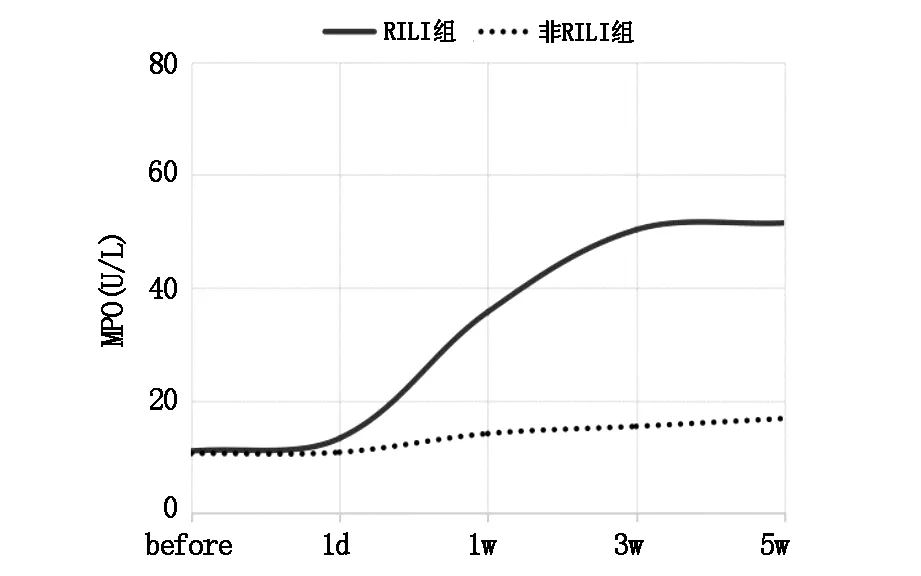
图3 RILI组、非RILI组不同时间MPO活性变化规律
2.4 肺癌患者放疗后细胞因子水平的动态变化
与非RILI组相比,RILI组患者6种细胞因子(IL-1、IL-6、IL-10、IL-18、MCP-1和TNF-α)水平(pg/ml)均升高,并且在1-5w达高峰,差异均有统计学意义(P<0.05),见图4。
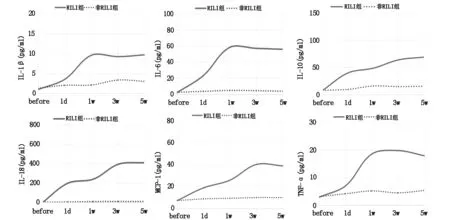
图4 RILI组、非RILI组不同时间6种细胞因子水平变化
2.5 细胞外组蛋白介导炎性损伤的细胞实验
将放疗前患者血清作为对照组,放疗组LDH活性(U/L)明显升高(238.03±1.02)U/L;与放疗组相比,抗体干预组LDH活性则明显降低(136.73±1.17)U/L,但仍高于对照组,差异均有统计学意义(P<0.05),见图5。
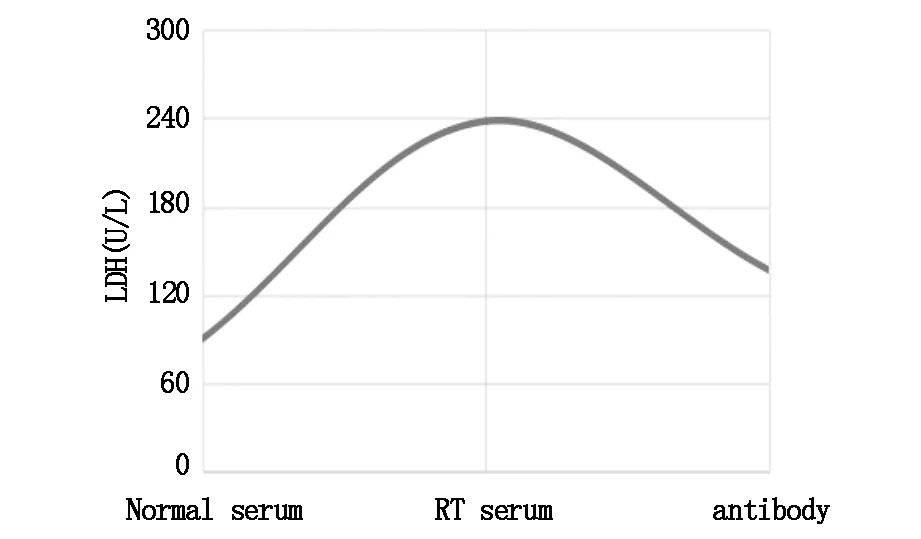
图5 特异性抗组蛋白中和抗体拮抗放疗后患者血清对人肺上皮细胞的损伤效应
与对照组相比,放疗组6种细胞因子(IL-1、IL-6、IL-10、IL-18、MCP-1和TNF-α)水平(pg/ml)显著升高;与放疗组相比,抗体干预组细胞因子水平则显著降低,但仍高于对照组,差异均有统计学意义(P<0.05),见图6。
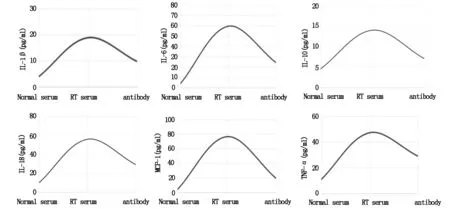
图6 特异性组蛋白中和抗体拮抗放疗后患者血清对人U937细胞的细胞因子生成影响
3 讨论
RILI是肺癌患者放射治疗中常见的剂量限制性并发症,早期主要表现为放射性肺炎,晚期则表现为不可逆肺纤维化[6]。尽管近年来放疗技术在不断进步,但RILI在肺癌放疗患者中的发病率仍高达5%-25%,兼其防治措施有限,已经成为了放射剂量区域、肿瘤控制率等的限制性因素,是影响患者治疗效果及预后的重要因素,严重时会导致患者死亡[7-9]。在RILI复杂多样的发病机制中,炎症占有重要地位。射线可通过细胞凋亡、坏死等引起细胞死亡,导致炎症细胞浸润[10],从而激活细胞外损伤相关分子模式(DAMP)分子的释放。DAMP分子在体内积聚并活化天然免疫细胞,引发不同的模式识别受体,如Toll样受体和炎症因子,继而导致炎症[11]。经射线照射后受损的上皮细胞和其他炎性细胞产生多种细胞因子和趋化因子[12],这些因子在受辐射的肺组织中放大炎症反应并触发成纤维细胞活化与增殖,从而导致胶原沉积及慢性纤维化[13-14]。
组蛋白是高度保守的核内碱性阳离子蛋白,在细胞核内含量丰富且恒定,主要包括5种类型:H1、H2A、H2B、H3、H4[15]。组蛋白在染色质重塑和基因转录中发挥关键作用[16]。研究发现,应激状态时,免疫细胞表面和细胞质内可以检测到组蛋白,其以一种细胞外诱捕网(NETs)的方式从活化的免疫细胞中释放,该网是由中性粒细胞染色体成分和其他的抗菌蛋白所构成的纤维,发挥到捕获与降解入侵微生物的作用[17]。但是,逐渐增多的中性粒细胞胞外诱捕网可以形成一种免疫细胞死亡的方式,该独特的方式被称为“NETosis”[18]。另外,细胞凋亡或坏死时染色质降解,核内组蛋白也可以被释放至细胞外成为细胞外组蛋白[19],通常和吞噬作用受损有关[20]。研究表明,细胞外组蛋白直接具有细胞毒性[21]或作为DAMP分子通过刺激免疫细胞(如中性粒细胞、单核/巨噬细胞和树突细胞等),进而激活下游信号通路产生多种细胞因子,触发全身炎症反应[3,22]。因此,本研究旨在探讨细胞外组蛋白与放疗相关炎症反应的相关性。
在本研究中,观察到放疗后患者血清细胞外组蛋白水平明显增加,同时出现免疫细胞活化和炎症反应,炎性细胞因子及MPO水平升高均提示了放疗后肺癌患者细胞外组蛋白与免疫细胞活化及大多数炎性细胞因子之间存在的明确的相关性。这与之前公布的数据一致[23]。此外,通过研究进一步阐述细胞外组蛋白的病理作用,结果提示放疗后患者血清能直接诱导肺上皮细胞损伤和促进U937细胞释放细胞因子,导致细胞外组蛋白相关炎性细胞因子显著增加;而特异性抗组蛋白H4抗体则可以明显抑制这一损伤效应,从而证实了细胞外组蛋白与放疗相关的全身性炎症之间的因果关系。基于研究观察,可以得出RILI的可能发病机制:放疗导致大量细胞死亡和免疫细胞活化,从而释放细胞外组蛋白,进而促进相关炎症细胞因子的释放,介导炎性损伤。近年来,以细胞外组蛋白为靶点的保护措施亦是研究热点。大量研究发现,特异性抗组蛋白H3、H4抗体[4,24],组蛋白阻断剂如活化蛋白C[25]及肝素[26]可以有效拮抗细胞外组蛋白的毒性作用。可见,若能将细胞外组蛋白阻断,中和或降解其细胞毒性作用,将有望从更深层面控制炎症的发生发展,为临床探索开辟一个新的方向。
总之,本研究结果揭示了细胞外组蛋白与全身性炎症之间的关系。细胞外组蛋白可以作为反映放疗相关系统性炎症的生物标志物。
