自制覆膜支架成功救治冠状动脉左主干破裂1例
2022-09-23王婷婷张东伟
程 锦,赵 勇,段 赟,王婷婷,张东伟
(空军军医大学第二附属医院心血管内科,西安 710000;*通讯作者,E-mail:zhdw0000@126.com)
随着冠状动脉介入手术的发展,复杂经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)手术比例逐年增加,伴随产生的是冠状动脉破裂发生率的比例增加[1,2]。处理冠状动脉破裂常用的方法包括:球囊膨胀、血管栓塞、覆膜支架植入、冠状动脉旁路移植术等,在急性冠状动脉破裂时尤其是血流动力学不稳定甚至需要心包穿刺时,置入覆膜支架成为能够挽救病人生命的重要措施[3,4]。并且越来越多临床试验数据表明,覆膜支架在降低住院死亡率和30 d内临床死亡率方面显示出良好的临床结果[5]。然而大多数中心没有商品化的覆膜支架,而各导管室的药物涂层支架及透明敷料膜很容易获得,而且使用药物涂层支架制作覆膜支架使得覆膜支架的数量和尺寸都更加灵活和更易获得。并且自制覆膜支架与商品化的覆膜支架在短期内不良心血管事件(major adverse cardiovascular events,MACE)事件发生率以及长期死亡率上也具有相似性。因此,在发生急性冠状动脉破裂时,自制覆膜支架成为紧急状态下挽救病人生命的重要措施[6]。本文报道1例由非顺应性球囊扩张压力过大导致的左冠状动脉主干破裂,病人瞬间发生心包压塞,我中心导管室无商品化的覆膜支架,因此术者在心包穿刺抽吸的同时自制覆膜支架置入破裂部位,3 h后破裂部位再次发生渗漏,再次置入第2枚自制覆膜支架后病人经历了Ⅲ度房室传导阻滞及急性心衰后顺利出院。本病例总结了自制覆膜支架的制作和置入经验,并在一定程度说明自制覆膜支架在危及生命的冠状动脉破裂穿孔中应用的可行性。
1 病例报告
1.1 病例资料
患者,男性,69岁。患者2月前(2020年7月25日)因“间断胸痛、气短1月”行冠状动脉造影术。造影结果显示:右冠状动脉(right coronary artery,RCA)闭塞,左冠状动脉主干(left main coronary artery,LM)到前降支(left anterior descending branch,LAD)严重狭窄伴重度钙化。Syntax评分>33,建议行冠状动脉旁路移植术,患者拒绝并要求行PCI术,遂于此次入院前1月(2020年8月26日)开通右冠CTO病变并植入药物支架4枚。术后仍间断有心绞痛发作,此次为处理LAD-LM病变再次入院。患者无冠心病危险因素。发病以来,食纳、夜休可,大小便正常。既往体质一般,否认特殊疾病及用药史,家族中无此类患者。入院时体格检查:体温36.3 ℃,脉搏82次/min,呼吸17次/min,血压110/90 mmHg,身高175 cm,体质量65 kg,BMI 21.2 kg/m2。神志清、精神可,发育正常,营养中等。心肺腹查体未见明显异常。双下肢轻度凹陷性水肿。
1.2 治疗过程
术前给予普通肝素3 000 U,30 min后再按总量100 U/kg给予普通肝素3 500 U,凝血酶原活性(ACT)>250 s。
术中使用6F EBU 3.5指引导管LAD通过Runthrough导丝(泰尔茂,日本)1根;由于LAD全程重度钙化,近段局部严重狭窄(见图1A),2.0/20 mm顺应球囊(波士顿科学,美国)3.0/15 mm非顺应性球囊多次扩张均不能良好扩张LAD局限性钙化结节(见图1B);给予LAD旋磨(波士顿科学,美国)后造影,3.0/15 mm非顺应性球囊(波士顿科学,美国)可均匀扩张(见图1C),预处理LAD近段至LM开口,LAD近段置入3.0/29 mm药物支架Promus PREMIERTM(波士顿科学,美国),LCX开口拘禁2.0/20 mm顺应球囊(波士顿科学,美国)后于LAD-LM开口植入3.5/29 mm Promus PREMIERTM(波士顿科学,美国)药物支架后支架膨胀良好。3.0/15 mm(美敦力,美国)、3.5/12 mm(美敦力,美国)非顺应球囊依次扩张支架后造影显示左主干支架膨胀不均匀(见图2A),4.0/9 mm(美敦力,美国)非顺应性球囊22 atm后扩张左主干支架后造影即出现造影剂外渗,根据Ellis分型[7]属Ellis Ⅲ型(见图2B),病人立即出现意识丧失,血压、心率明显下降,在破裂部位迅速扩张原4.0/9 mm(美敦力,美国)球囊18 atm封堵破口,每5 min放松30 s,封堵期间可见短阵室速发生;同时心包穿刺、抽出200 ml不凝血后病人意识恢复,血压100/60 mmHg,心率119次/min。留置心包引流管,可持续引流出不凝血。期间可见心电监护ST段抬高;封堵30 min后造影仍可见大量造影剂外渗(见图2C),故决定置入覆膜支架。因我中心无商品化覆膜支架,利用3M膜(施乐辉,英国)自制4.0/18 mm覆膜支架(波士顿科学,美国)12 atm覆盖LAD至LM中段封堵破口,但造影仍有明显造影剂渗漏,4.0/12 mm(美敦力,美国)非顺应球囊压力20 atm扩张支架后造影显示封堵良好,无造影剂渗漏(见图2D)。球囊封堵及支架植入中多次发生室速、室颤。观察半小时,未再引流出不凝血,在抗心律失常药物及升压药物持续静滴下血压、心率平稳,留置心包引流管返回重症监护室病房。由于患者置入支架数量多,且为自制覆膜支架,术后持续口服阿司匹林肠溶片、替格瑞洛片,静滴盐酸替罗非班抗血小板治疗。
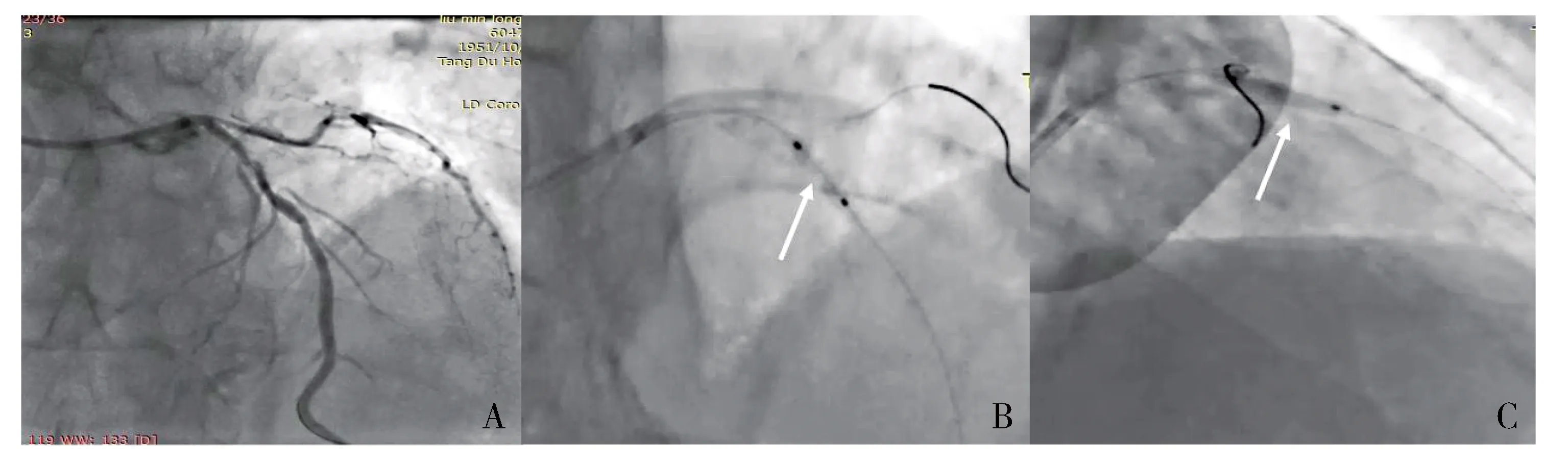
A.术前左冠头位造影显示LAD近段重度狭窄、迂曲、钙化;B.旋磨前顺应球囊膨胀不均(箭头所指);C.旋磨后预扩张球囊膨胀不均处消失(箭头所指)图1 LAD造影及旋磨前后狭窄程度对比
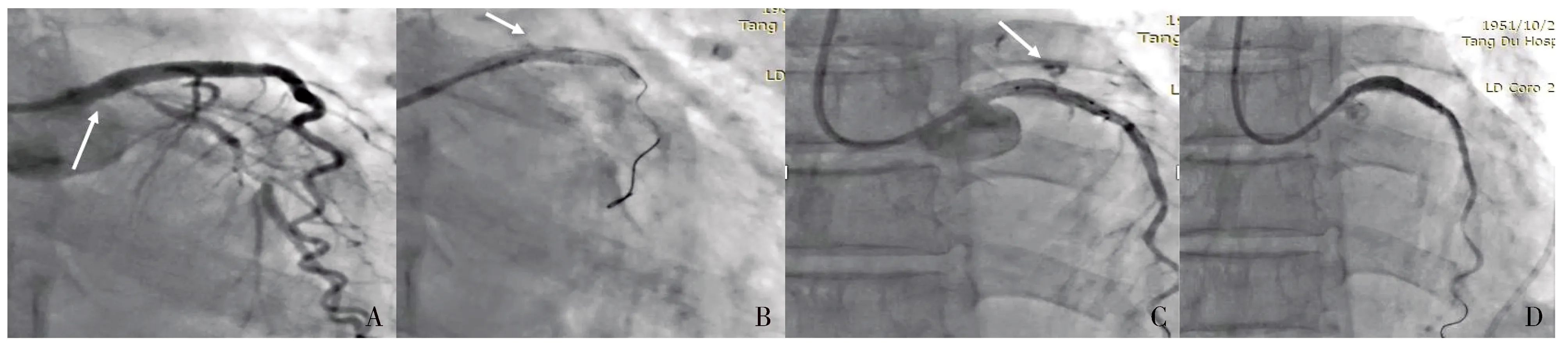
A.LM支架膨胀不全处(箭头所指);B.LM破裂(箭头所指);C.球囊封堵30 min后仍有大量造影剂外渗(箭头所指);D.第1个自制覆膜支架后图2 后扩张LM支架导致冠脉张破裂
术后3 h患者突发意识丧失,血压降至80/40 mmHg,窦性心律,心率126次/min,立即回抽心包引流管,可抽出大量不凝血,抽出200 ml后患者意识恢复;考虑冠状动脉破裂部位再次出现渗漏导致心包填塞,立即准备再次急诊造影,在转运至手术室途中及术中持续心包抽吸-回输(将心包回抽的血液通过股静脉的深静脉置管回输入体内)前给予4 600 U(70 U/kg)肝素,EBU3.5指引导管急诊造影,可见原覆膜支架覆盖处再次出现大量造影剂外渗(见图3A),立即用4.0/8 mm(波士顿科学,美国)非顺应性球囊12 atm封堵破裂处,再次同时制作4.0/29 mm覆膜支架(波士顿科学,美国)再次原支架部位覆盖破口(见图3B),12 atm释放,4.0/9 mm非顺应球囊18 atm后扩张,支架释放后发生多次室速,意识丧失,电除颤后恢复窦性心率,同时静滴盐酸胺碘酮;观察30 min无明显病情变化,返回CCU。此次心包填塞共回抽-输注自体血液约2 500 ml。术后心包积液引流袋仍能以100 ml/h速度引流出不凝血,3 h后引流量明显减少,第2天引流袋再无液体引出(共引流出不凝血约400 ml),心脏超声显示无心包积液,观察24 h心脏超声显示无心包积液后拔除心包引流管。
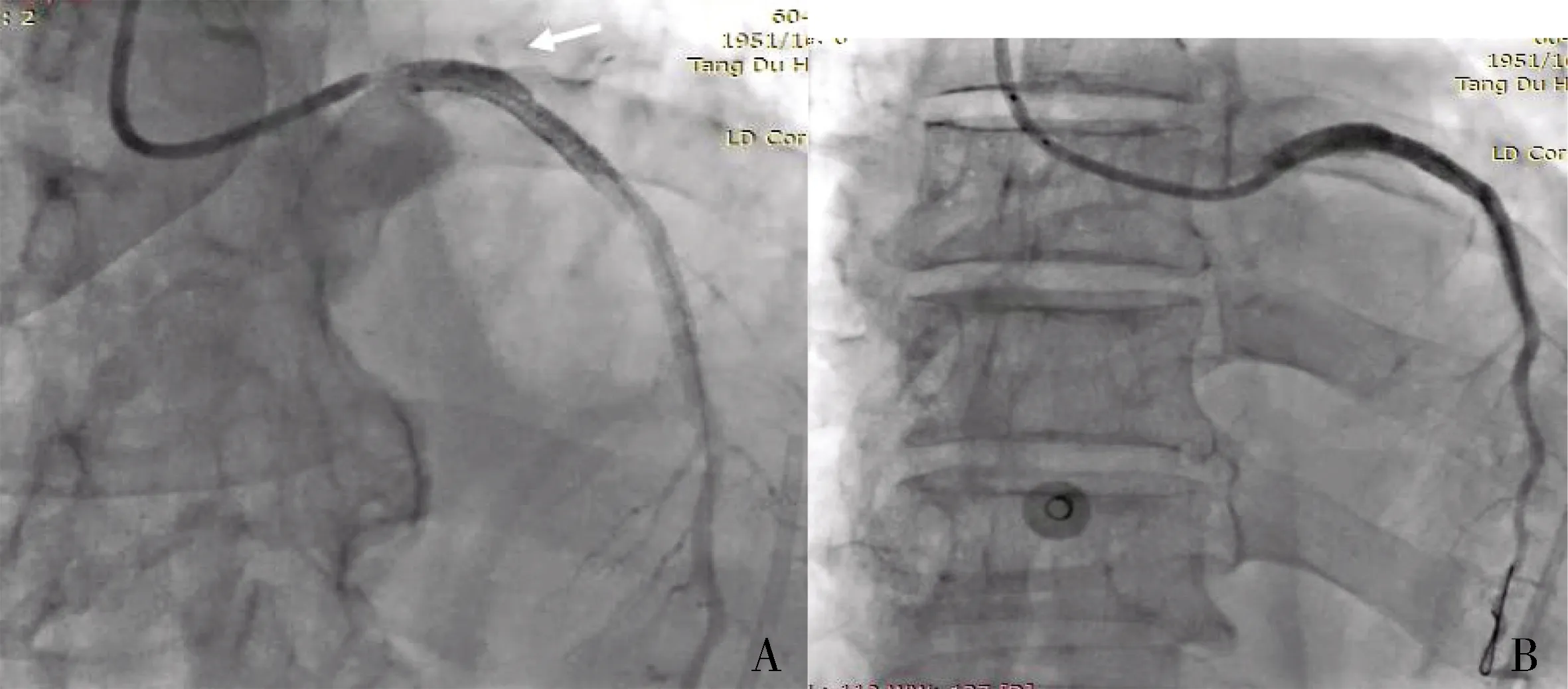
A.二次破裂(箭头处可见造影剂外渗) B.第2个覆膜支架后图3 原覆膜支架封堵处再次出现渗漏
3 d后患者再次突发意识丧失,心电监护显示Ⅲ度房室传导阻滞,急诊置入临时起搏器,同时复查左冠脉造影(见图4),造影显示支架贴壁良好,冠脉血运通畅。5 h后患者诉极度气短,血气提示pH 7.40,PO240 mmHg,PCO232 mmHg,端坐呼吸,咳粉红色泡沫痰,听诊双肺布满湿啰音,超声提示双侧大量胸腔积液,给予胸腔积液穿刺引流、无创呼吸机辅助呼吸、扩张血管、利尿后症状缓解。Ⅲ度房室传导阻滞于3 d后自行恢复。
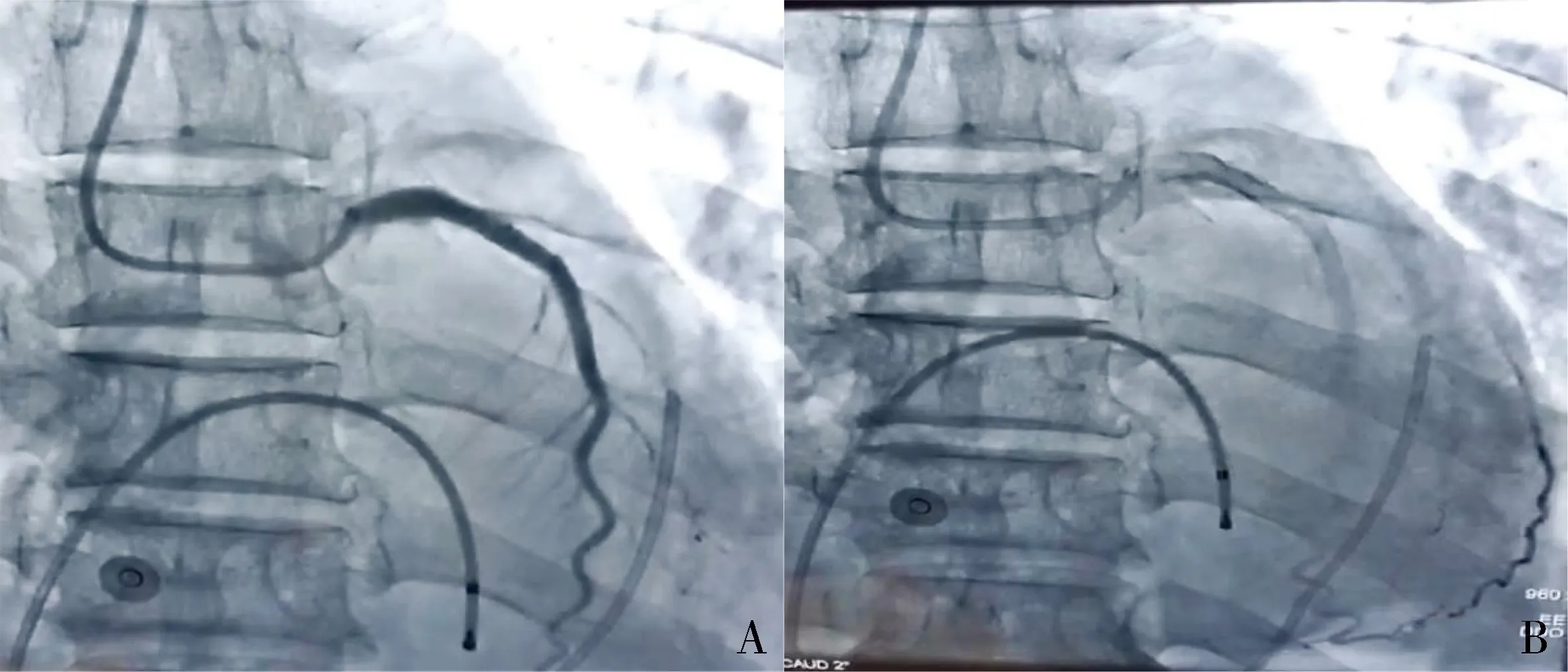
A.支架内血流通畅,未见异常;B.发生Ⅲ度房室传导阻滞时造影显示逆冲血管图4 Ⅲ度房室传导阻滞后造影
病人于覆膜支架置入1周后出院。术后1个月、3个月、半年、1年及1年6个月的随访中诉活动后稍有气短,余无明显不适。
2 讨论
冠状动脉破裂所造成的心包填塞和死亡的比例最主要取决于冠状动脉破裂的类型。ELLIS Ⅲ型发生心包填塞和死亡率分别为21.2%和46.1%[8]。避免冠脉穿孔,主要在预防。在手术前全面评估病变情况,做好各种预案。对于本病例,手术开始就判定为重度钙化伴狭窄的复杂病变,从最开始的器械选择、预处理策略选择到支架置入及后扩张都要有影像学的评估,避免引起冠状动脉破裂的高危操作。本病例中术者由于术前未用血管内超声(intravenous ultrasound,IVUS)评估病变情况,导致非顺应性球囊扩张支架压力过大引起左冠状动脉主干穿孔破裂。在穿孔后术者反应迅速、立即封堵破口,倘若此时及时应用IVUS评估血管和支架情况,就会避免后面的悲剧再次发生。
当然,一旦发生冠脉穿孔破裂,最重要的是早期识别,之后根据穿孔的不同情况采取不同的处理策略,一般可选的策略包括:观察,不作处理、心包穿刺、中和肝素、球囊封堵、穿孔血管栓塞、覆膜支架置入、外科手术等。本例患者为右冠闭塞血管开通术后,左冠状动脉主干在植入支架后发生Ellis Ⅲ型穿孔,且穿孔部位紧邻回旋支,为冠状动脉穿孔中最为严重的类型,死亡率极高。冠脉穿孔后立即心包压塞,术者迅速心包穿刺抽吸置管、球囊封堵破口、自制和置入覆膜支架,在球囊贴壁封堵左主干而导致左冠状动脉缺血而覆膜支架置入后导致回旋支永久性闭塞,因此在球囊封堵过程中和覆膜支架置入后多次发生室速和室颤。
第一次覆膜支架后很快再次发生心包填塞,主要考虑与自制覆膜支架表面的3M膜挛缩引起支架挛缩引起。一方面说明自制覆膜支架的释放压力不能按照原本支架释放的压力,同时在制作覆膜支架时对膜的厚度有一定要求,既要能封堵破口又要不影响支架膨胀,一般建议3M膜包裹支架不超过2层[6]。术后发生Ⅲ度房室传导阻滞的可能原因是覆膜支架导致了间隔支血管的闭塞,使传导系统缺血引起Ⅲ度房室传导阻滞,后来由于侧支循环的逐渐建立,传导阻滞最终消失。
一项关于PTFE膜的商品化覆膜支架的随访显示12个月内支架内血栓的发生率为3%~16%[9];一项关于关于PK Papyrus覆膜支架的注册研究表明,住院期间及12个月随访覆膜支架术后支架内血栓形成为5%及10%[10],6个月支架内再狭窄发生率达31.6%[11]。本病例由于左主干部位植入覆膜支架,且数量较多,术后的关注点主要放在了预防支架内血栓形成,我们给予了阿司匹林肠溶片100 mg(qd)和硫酸氢氯吡格雷75 mg(qd)作为抗血小板的方案。心包引流管保持通畅,需每2 h肝素盐水冲管1次,防止血栓堵塞引流管同时根据血常规、生命体征及回抽情况判断有无再次出血;患者3支血管病变,既往右冠闭塞病变,此次冠脉穿孔导致回旋支闭塞会对病人的心功能产生较大影响,应在术后密切关注症状体征和相关指标,预防急性心衰的发生。此病人在术后1月、3月、半年、1年及1年6个月的随访中除活动后偶有不适外未再次入院。
因此,在PCI手术中,发生重要部位主支血管急性穿孔破裂并伴有血流动力学不稳定而又无可用的商品化覆膜支架时,自制覆膜支架由于制作材料易获得、制作过程快、尺寸和大小、数量灵活等特点能快速封堵破口,为进一步治疗争取时间。
