原发性闭角型青光眼合并白内障患者术后发生干眼症的影响因素研究
2022-09-15龚茫来
龚茫来
通辽市科尔沁区第一人民医院眼科,内蒙古通辽 028000
随着年龄增加,眼部疾病发生率越来越高,如原发性闭角型青光眼(primary angle closure glaucoma,PACG)、白内障等,两种疾病可同时存在,相互影响,随着白内障患者病情加重,膨胀晶状体不断增厚,引起瞳孔阻滞,使得PACG进展[1-2]。临床治疗PACG联合白内障以手术为主,可重新开放前房角,降低眼压,从而改善患者视力,有利于提高生活质量[3]。但随着白内障手术的广泛应用发现,术后患者易发生干眼症,主要表现为眼干、眼部不适等,影响术后恢复[4-5]。因此,深入分析PACG联合白内障患者术后发生干眼症的危险因素,并针对高危因素制订预防方案,对减少术后干眼症发生有重要意义。本研究回顾性分析2019年6月—2021年6月通辽市科尔沁区第一人民医院收治的168例PACG合并白内障患者的临床资料,以探讨术后发生干眼症的影响因素。现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析本院收治的168例PACG合并白内障患者的临床资料,其中男93例,女75例;年龄45~78岁,平均(65.76±3.85)岁;体质量42~85 kg,平均(68.34±2.91)kg;139例单眼发病,29例双眼发病。本研究经本院医学伦理委员会批准,患者自愿签署知情同意书。
1.2 纳入与排除标准
纳入标准:①满足手术指征者;②手术前无干眼症者;③患者意识清楚,能够配合相关检查;④临床资料均完整,未见丢失者。
排除标准:①合并自身免疫性疾病者;②伴有其他眼部疾病者;③合并恶性肿瘤者;④存有认知障碍或精神疾病,难以配合进行资料收集者。
1.3 方法
所有入选者均进行相同的手术方案,由同一手术组完成手术,术中所用设备、器械、药物均一致,术后予以抗感染治疗。术后3个月对患者进行复查及评估,包括问卷调查及眼部检查,判断患者有无干眼症。眼部检查:患者均进行视力检查、裂隙灯检查、泪液分泌试验等。另外,对患者进行干眼症问卷调查,主动询问患者有无眼睛干涩、视疲劳、异物感、眼痒、视物模糊等主观感觉。临床干眼症诊断符合《干眼临床诊疗专家共识(2013)》[6]相关内容:①患者自觉存在视物模糊、眼睛干燥、眼睛异物等主观症状(必备);②泪膜不稳定(必备);③泪液分泌减少(加强诊断);④眼表面损害(加强诊断);⑤泪液乳铁蛋白减少或渗透压增加(加强诊断)。
1.4 观察指标
根据患者术后是否发生干眼症分为发生组与未发生组,统计两组临床资料,包括性别、年龄、切口长度、术前合并糖尿病、术前合并高血压、手术入路方式、术中麻醉方式、术中超声能量释放总和、术眼术中在显微镜下暴露时间,分析PACG联合白内障患者术后发生干眼症的危险因素。
1.5 统计方法
采用SPSS 22.0统计学软件分析数据,符合正态分布的计量资料以(±s)表示,组间差异比较以t检验,计数资料以频数及百分比表示,组间差异比较以χ2检验;多因素使用Logistic回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 168例PACG联合白内障患者术后干眼症检出情况
168例PACG联合白内障患者术后共有40例发生干眼症,发生率为23.81%(40/168)。
2.2 PACG联合白内障患者术后发生干眼症的单因素分析
两组切口长度≥2 mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min的患者占比比较,差异有统计学意义(P<0.05);两组性别、年龄、术前合并高血压、手术入路方式、术中麻醉方式比较,差异无统计学意义(P>0.05)。见表1。

表1 PACG联合白内障患者术后发生干眼症的单因素分析
2.3 PACG联合白内障患者术后发生干眼症的多因素分析
多因素Logistic回归分析显示:切口长度≥2 mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min是PACG联合白内障患者术后发生干眼症的独立危险因素(OR>1,P<0.05)。见表2。
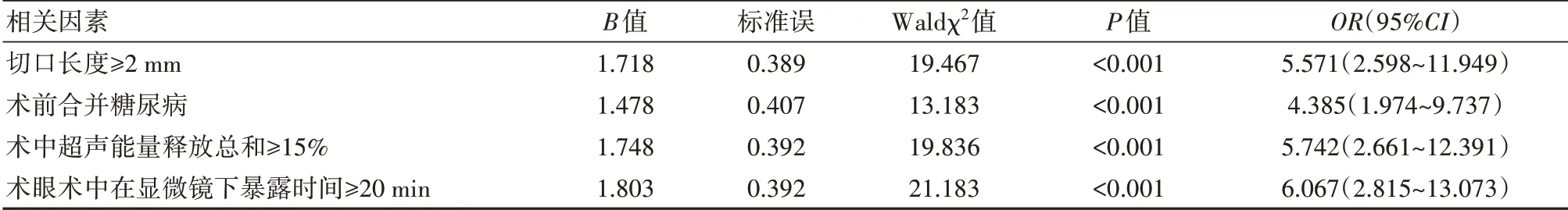
表2 PACG联合白内障患者术后发生干眼症的多因素分析
3 讨论
PACG联合白内障在临床中较为常见,高发于中老年人群,发病后对视力造成的损害较为严重,影响患者日常生活及健康,降低生活质量[7]。临床治疗PACG联合白内障以手术效果最佳,随着眼科技术不断发展,手术方法越来越多,治疗PACG联合白内障效果确切,已获得多方认可,但术后并发症问题日益严峻[8-9]。干眼症为PACG联合白内障患者术后常见的并发症之一,发病机制较为复杂,诱发因素繁多,与泪腺、角膜、睑板腺、结膜等相关,其中任一结构或功能异常均可导致干眼症发生,影响手术效果[10-11]。
干眼症为常见的眼表疾病,常引起结膜杯状细胞丢失,诱发视物模糊、眼干、眼痒等不适症状,甚至会造成角膜上皮细胞凋亡,影响患者视力[12]。PACG联合白内障手术治疗后需要较长时间才可恢复至术前状态,受多方面因素影响,患者极易发生干眼症,全面分析术后发生干眼症的危险因素,提前制订预防措施,对降低干眼症发生风险有重要意义[13-14]。本研究结果显示,168例PACG联合白内障患者术后共有40例发生干眼症,发生率为23.81%(40/168);发生组切口长度≥2 mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min占比高于未发生组(P<0.05);多因素Logistic回归分析显示:切口长度≥2 mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min是PACG联合白内障患者术后发生干眼症的独立危险因素(OR=5.571、4.385、5.742、6.067,P<0.05),表明PACG合并白内障患者术后干眼症发生率较高,且与切口长度≥2mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min相关。陈岚等[15]研究显示,术后3个月,98例患者中术后发生干眼症46例,Logistic回归显示,高血脂、糖尿病、睑脂粘度、睑板腺功能及结膜松弛是术后干眼症发生的危险因素(OR=5.625、3.636、2.620、1.841、3.061,P<0.05),与本研究结果具有相似性。究其原因:①手术切口越大,则术中造成的创伤越大,会影响泪膜稳定性,且术后恢复较慢,会增加术后干眼症的发生风险[16]。②糖尿病会影响患者睑板腺功能,随着血糖水平不断升高,睑板腺分泌功能受到明显影响,导致干眼症发生风险较高[17]。③临床多通过超声手术治疗,利用超声探头高频震动产生能量震碎晶状体,便于吸出,当超声能量释放过多时会损伤角膜内皮,造成内膜剥离及稳定性降低,增加干眼症发生概率。④手术过程中需使用开睑器持续暴露角膜,术眼长时间暴露会导致角膜干燥,临床为缓解此情况,多对角膜进行冲水,会不同程度地损伤角膜上皮,术后角膜修复较慢,导致干眼症发生率较高[18]。
综上所述,PACG合并白内障患者术后干眼症发生率较高,切口长度≥2 mm、术前合并糖尿病、术中超声能量释放总和≥15%、术眼术中在显微镜下暴露时间≥20 min是其独立危险因素,临床应针对高危因素制订预防措施,以降低干眼症发生风险,改善患者预后。
