苯炔与β-二酮硫醚参与的氧杂-[2,3]-σ重排反应研究
2022-08-31闫乐玉徐小波王梦滢曹中艳
闫乐玉, 徐小波, 王梦滢, 曹中艳
(1.黄淮学院 化学与制药工程学院, 河南 驻马店463000;2.河南大学 化学化工学院, 河南 开封475004)
重排反应是有机合成化学中的基本反应之一,其最显著特征是高效的化学键迁移或碳骨架结构的重组,并且通过重排反应可以快速构建复杂多样的新化合物骨架[1-5]。在众多重排反应类型中,硫叶立德由于其高度的稳定性和发生重排反应的多样性而受到广泛关注,硫叶立德参与的重排反应可用于合成各种复杂且具有重要生物活性的含硫分子[6-8]。据文献报道,目前硫叶立德重排反应研究较多的主要有过渡金属催化和苯炔诱发两大类型。前者代表性反应是Doyle-Krimse重排反应[9-13],但该反应不仅需要昂贵的金属参与,而且还需要特殊的重氮化物作为反应底物,因此极大地限制了其应用范围。另一种代表性的硫叶立德重排反应是苯炔参与的Stevens类型重排[14-15],该类型重排应用成熟的Kobayashi试剂即2-(三甲基硅)苯基三氟甲烷磺酸盐作为苯炔前体,可以在非常温和的条件下原位生成苯炔并引发反应[16-17]。
在有机合成化学中,苯炔作为一种高反应活性的缺电子中间体,常被用于新反应的开发以及复杂分子的合成[18-19]。2017年,Xu等[20]首先报道了苯炔与苄基取代硫醚发生[1,2]-Stevens重排反应生成多取代的β-酮硫醚化合物的研究工作,该工作中还探索了苯炔与烯丙基取代硫醚发生[2,3]-Stevens类型的重排反应。同年,Biju和Tan课题组分别独立拓展了苯炔与烯丙基取代硫醚的[2,3]-Stevens重排反应研究[21-22]。基于前期工作基础,继续探索用β-二酮硫醚替代苄基硫醚与苯炔的反应研究。实验结果表明,β-二酮硫醚与苯炔并没有如预期发生[1,2]-Stevens类型的重排反应得到多取代β-酮硫醚化合物,而是经过一种新的氧杂-[2,3]-σ重排反应过程,最终生成高度官能团化的烯醇硫醚产物(图1)。值得注意的是,该重排反应涉及并不常见的羰基极性反转过程[23]。首先,原位生成的苯炔与β-二酮硫醚反应得到硫叶立德中间体,随后该中间体通过分子内电子转移完成氧杂-[2,3]-σ重排反应过程。

图1 苯炔参与的Stevens重排反应和氧杂-[2,3]-σ重排反应
1 实验部分
1.1 仪器与试剂
核磁共振谱用Varian Unit INOVA-400/54型,以TMS为内标,常见氘代试剂是CDCl3,核磁谱图中单位为ppm,1H NMR化学位移(δ)以TMS(0 ppm)或CHCl3(7.26 ppm)为基准,13C NMR化学位移(δ)以CHCl3(77.0 ppm)为基准;高分辨质谱用Bruker Daltonics APEX II47e FT-ICR型质谱仪测定。
所用溶剂和药品除特别说明均为分析纯或化学纯;溶剂在使用前均经过重新蒸馏;无水溶剂均按标准方法或文献方法进行处理。柱层析硅胶(200~300目)和薄层层析硅胶(GF254)为青岛海洋化工厂和烟台化工厂产品;如未特别说明,均采用石油醚(60~90 ℃)/乙酸乙酯(v/v)作为淋洗剂;显色剂用碘或磷钼酸的乙醇溶液(5%);所有萃取溶剂未经说明均为乙酸乙酯或乙醚。
1.2 化合物的合成
1.1.1β-二酮硫醚原料的合成[24-25]
在氮气保护下,将β-溴代酮原料(5.0 mmol, 1.0 equiv)和硫醇(6.0 mmol, 1.2 equiv)溶于30 mL 四氢呋喃溶液中,常温下加入三乙胺(10.0 mmol, 2.0 equiv)反应3小时。TLC检测原料反应完全后用100 mL 乙酸乙酯萃取反应,依次用水(2 × 20 mL)和饱和食盐水(20 mL)洗,无水硫酸钠干燥,减压浓缩后快速硅胶柱层析纯化产物。
1.1.2 烯醇硫醚产物的合成[20-22]
在氮气保护下,将β-二酮硫醚原料(0.5 mmol, 1.0 equiv)、KF(58.0 mg, 1.0 mmol, 2.0 equiv)和18-冠-6(18-crown-6)(132.0 mg, 0.5 mmol, 1.0 equiv)溶于5.0 mL 无水四氢呋喃溶液中,常温下加入2-(三甲基硅)苯基三氟甲烷磺酸盐(0.6 mmol, 1.2 equiv),然后在65 ℃ 下反应4 h。反应完成后减压浓缩并快速硅胶柱层析纯化,得到多取代烯醇硫醚产物。
2 结果与讨论
2.1 最优条件筛选
为筛选最佳的苯炔参与的氧杂-[2,3]-σ重排反应条件,选取β-二酮硫醚1a和Kobayashi苯炔前体2a作为模板反应底物。首先,将0.5 mmol的1a与0.6 mmol(1.2当量)的2a溶于乙腈溶剂,室温条件下加入1.0 mmol(2.0当量)CsF反应4 h,该反应条件结束后得到目标重排产物,收率为48%。以此为基础,在保持模板反应底物不变的情况下,通过逐一改变试剂当量、温度、溶剂、氟源以及添加剂等反应变量,进行反应条件优化(表1)。实验结果显示,温度升高到65 ℃ 时,不仅收率提高,并且反应时间也缩短到2 h。四氢呋喃作溶剂的反应效果优于乙腈,同时,筛选CsF(氟化铯)、TBAT(四正丁基铵二氟代三苯基硅酸盐)、TBAF(四丁基氟化铵)和KF(氟化钾)四种氟源后发现KF收率最佳,并且18-冠-6的加入有助于提高重排反应收率。综合以上实验结果得出,0.5 mmol的β-二酮硫醚1a与1.2当量的2a溶于2 mL四氢呋喃,加入2.5当量的KF和1.2当量的18-冠-6,并在65 ℃下反应2 h(entry 8)是氧杂-[2,3]-σ重排的最优反应条件。

表1 反应条件的优化
2.2 底物拓展
筛选到最佳反应条件后,接下来继续探索β-二酮硫醚与苯炔发生氧杂-[2,3]-σ重排反应的底物适应范围(图2)。发现,苯基取代的β-二酮硫醚换成具有吸电子效应的溴苯取代后收率仍然不变,芳基取代的β-二酮硫醚换成烷基取代如甲基和叔丁基效果仍然非常好,只是有一定位阻效应的叔丁基取代的β-二酮硫醚时收率有所降低。当给电子效应强的双甲氧基取代的苯炔参与反应时仍然以88%的高收率得到目标产物。最后,用对称的β-二酮硫醚换成非对称的苯甲酰基和甲酯取代的β-二酮硫醚,同样以高达90%的收率得到目标产物。
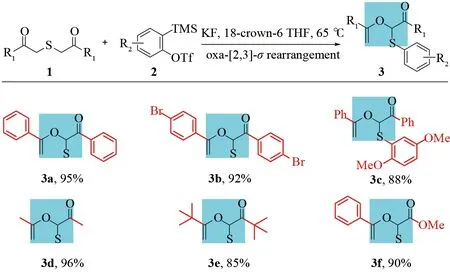
图2 反应底物拓展
值得注意的是,当双酯羰基取代的β-二酮硫醚作为原料时的反应结果与上述情况不一致(图3)。例如用双甲酯取代的β-二酮硫醚与苯炔作用时,反应并没有如预期得到重排产物,而是只检测到简单的硫醚产物苯基硫代乙酸甲酯3g,这可能是重排产物3h不稳定发生了分解。
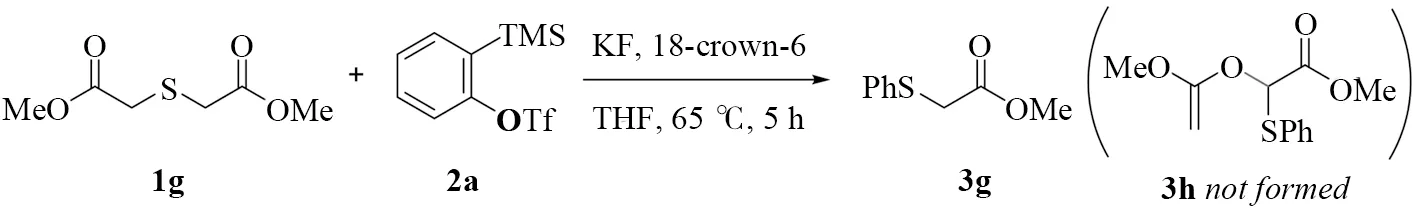
图3 硫代二乙酸二甲酯与苯炔的反应
2.3 应用研究
为进一步研究新方法的应用范围,在参考文献基础上[26-27],将重排产物烯醇硫醚3d与TMSOTf作用,反应经分子内环化过程后得到2,3,5-三取代呋喃衍生物4(图4),收率为52%。该类三取代呋喃衍生物可继续官能团化得到更多具有生理活性的药物分子。

图4 2,3,5-三取代呋喃衍生物的合成
1-Phenyl-2-(phenylthio)-2-((1-phenylvinyl)oxy)ethan-1-one(3a):1H NMR(400 MHz, CDCl3)δ8.08(d,J= 7.5 Hz, 2H), 7.68~7.56(m, 3H), 7.51~7.44(m, 4H), 7.39~7.20(m, 6H), 6.41(s, 1H), 4.88(d,J= 3.6 Hz, 1H), 4.35(d,J= 3.6 Hz, 1H);13C NMR(100 MHz, CDCl3)δ190.2, 157.9, 135.3, 134.0, 133.9, 133.7, 131.2, 129.1, 129.1, 128.9, 128.9, 128.6, 128.2, 125.6, 87.2, 85.3;HRMS(ESI)m/z:[M+Na]+Calcd for C22H18NaO2S 369.092 0; Found 369.091 6。
1-(4-Bromophenyl)-2-((1-(4-bromophenyl)vinyl)oxy)-2-(phenylthio)ethan-1-one(3b):1H NMR(400 MHz, CDCl3)δ7.95~7.87(m, 2H), 7.65~7.58(m, 2H), 7.52~7.44(m, 4H), 7.40(t,J= 11.5 Hz, 2H), 7.30(td,J= 14.9, 7.2 Hz, 3H), 6.32(s, 1H), 4.88(d,J= 3.7 Hz, 1H), 4.35(d,J= 3.7 Hz, 1H);13C NMR(100 MHz, CDCl3)δ189.1, 156.8, 134.1, 134.0, 132.6, 132.0, 131.4, 130.5, 130.5, 129.2, 129.2, 129.1, 127.2, 123.1, 87.7, 85.2;HRMS(ESI)m/z:[M+Na]+Calcd for C22H1679Br2NaO2S 524.913 0; Found 524.912 8。
2-((2,5-Dimethoxyphenyl)thio)-1-phenyl-2-((1-phenylvinyl)oxy)ethan-1-one(3c):1H NMR(400 MHz, CDCl3)δ8.10(d,J= 8.0 Hz, 2H), 7.70~7.64(m, 2H), 7.60(t,J= 7.4 Hz, 1H), 7.48(t,J= 7.7 Hz, 2H), 7.36~7.31(m, 3H), 6.62(d,J= 1.2 Hz, 2H), 6.43(s, 1H), 6.40(s, 1H), 4.89(d,J= 3.6 Hz, 1H), 4.34(d,J= 3.6 Hz, 1H), 3.67(s, 6H);13C NMR(100 MHz, CDCl3)δ190.3, 160.7, 157.9, 135.2, 133.9, 133.7, 133.2, 129.1, 128.9, 128.6, 128.2, 125.6, 110.8, 101.8, 87.2, 85.7, 55.3;HRMS(ESI)m/z:[M+Na]+Calcd for C24H22Br2NaO4S 429.113 1; Found 429.113 0。
1-(Phenylthio)-1-(prop-1-en-2-yloxy)propan-2-one(3d):1H NMR(400 MHz, CDCl3)δ7.52~7.31(m, 5H), 5.78(s, 1H), 4.11(d,J= 3.2 Hz, 1H), 3.72(d,J= 3.2 Hz, 1H), 2.23(s, 3H), 2.02(s, 3H);13C NMR(100 MHz, CDCl3)δ201.2, 158.5, 132.3, 131.4, 127.8, 127.6, 88.3, 82.5, 26.6, 23.5;HRMS(ESI)m/z:[M+Na]+Calcd for C12H14NaO2S 245.060 7; Found 245.060 8。
1-((3,3-Dimethylbut-1-en-2-yl)oxy)-3,3-dimethyl-1-(phenylthio)butan-2-one(3e):1H NMR(400 MHz, CDCl3)δ7.47(dd,J= 6.4, 2.9 Hz, 2H), 7.29(dd,J= 9.6, 6.2 Hz, 3H), 5.80(s, 1H), 4.12(d,J= 3.3 Hz, 1H), 3.75(d,J= 3.3 Hz, 1H), 1.27(s, 9H), 1.12(s, 9H);13C NMR(100 MHz, CDCl3)δ 204.9, 168.8, 133.5, 131.8, 128.8, 128.4, 83.1, 81.5, 43.1, 36.0, 28.3, 27.3;HRMS(ESI)m/z:[M+Na]+Calcd for C18H26NaO2S 329.154 6; Found 329.154 6。
Methyl2-(phenylthio)-2-((1-phenylvinyl)oxy)acetate(3f):1H NMR(400 MHz, CDCl3)δ7.72~7.65(m, 2H), 7.64~7.59(m, 2H), 7.48~7.35(m, 6H), 5.85(s, 1H), 4.98(d,J= 3.8 Hz, 1H), 4.41(d,J= 3.8 Hz, 1H), 3.75(s, 3H);13C NMR(100 MHz, CDCl3)δ167.5, 158.1, 135.5, 134.8, 130.8, 129.4, 129.3, 129.2, 128.5, 126.2, 87.5, 81.6, 53.1;HRMS(ESI)m/z:[M+Na]+Calcd for C17H16NaO3S 323.071 2; Found 323.071 7。
Methyl2-(phenylthio)acetate(3g):1H NMR(400 MHz, CDCl3)δ7.45~7.39(m, 2H), 7.35~7.21(m, 3H), 3.73(s, 3H), 3.68(s, 2H);13C NMR(100 MHz, CDCl3)δ 170.4, 135.2, 130.3, 129.4, 127.3, 52.8, 36.7。
3,5-Dimethyl-2-(phenylthio)furan(4):1H NMR(400 MHz, CDCl3)δ7.47~7.28(m, 5H), 5.85(s, 1H), 2.34(s, 3H), 2.12(s, 3H);MS(ESI)m/z:[M+H]+Calcd for C12H13OS 205.1; Found 205.2。
3 结论
成功利用苯炔与β-二酮硫醚反应合成高度官能团化的烯醇类产物,探索了该反应的底物适用范围。在反应机理的探索中,还发现反应过程涉及不寻常的羰基极性反转并进一步发生氧杂-[2,3]-σ重排。此外,研究中进一步拓展了该反应产物在合成多取代呋喃衍生物方面的应用价值。
