柱前衍生-SPE-GC/MS法测定水中痕量溴代苯酚
2022-08-31葛嘉雨梁海燕刘冬李春灵张丰泉赵茜
葛嘉雨梁海燕刘冬李春灵张丰泉赵茜
(新乡医学院 公共卫生学院,河南 新乡 453003)


在研究水中有机污染检测方法中,固相萃取(solid phase extraction,SPE)具有操作简单、效率高、安全性高、成本低以及适于大体积水样前处理等优点[10];气相色谱-质谱仪(gas chromatography-mass spectrometer,GC/MS)既可以利用气相色谱强大的分离能力,又具有质谱在鉴定未知物方面较高的灵敏度,能够较好地解决水环境介质复杂的问题,也非常适于BPs这类热稳定性好、易挥发物质的定性与定量分析[11].此外,对于BPs的自身特性问题,衍生化反应[12]可以有效地改善BPs极性,进而优化其色谱和质谱响应,提高其分离度和检测方法的灵敏度.因此,拟采用乙酸酐为衍生化试剂,将酰基基团引入BPs分子中,衍生后的BPs经SPE富集纯化,以GC/MS为检测仪器的分析方法,通过加标回收实验评价分析方法,并以市政供水为测试水样验证方法的实用性,建立水相中BPs柱前衍生-SPE-GC/MS检测方法,为今后其分析方法的优化提供参考,并为研究环境、生命、地球、材料等科学领域BPs的控制、削减以及潜在生态风险等问题提供基础.
1 材料与方法
1.1 仪器和试剂
Agilent7890A-5975C 气相色谱质谱联用仪(配备HP-5MS毛细管柱,30 m×0.25 mm×0.25μm)和Agilent7890A 气相色谱仪配备电子捕获检测器(ECD)和30 m×0.32 mm×0.25μm HP-5毛细管柱;Supelco 12位固相萃取装置;C18固相萃取小柱(6 m L,500 mg);PEP固相萃取小柱(3 m L,60 mg);HLB固相萃取小柱(3 m L,60 mg).5种BPs标准品:2-溴酚(2-BP)、2,4-二溴酚(2,4-DBP)、2,6-二溴酚(2,6-DBP)、3,5-二溴酚(3,5-DBP)、2,4,6-三溴酚(2,4,6-TBP)均购于北京百灵威科技有限公司;碳酸钾(0.1 mol/L)、无水硫酸钠和乙酸酐为分析纯试剂(天津市大茂化学试剂厂);甲醇、正己烷均为色谱纯试剂(美国J.T.Baker公司);高纯水(18.2~18.3 MΩ·cm,上海和泰仪器有限公司).
1.2 实验内容
1.2.1 BPs的衍生化反应
向5种BPs标准品中依次加入碳酸钾、乙酸酐,振摇5 min使其充分混匀进行衍生化反应.以2-BP为例,衍生化反应式如下所示:

衍生化反应完成后,进行固相萃取,收集萃取液并洗至中性,经无水硫酸钠脱水后上机待测.通过对目标物峰形、峰面积等色谱信号和行为的考察,进行BPs衍生化反应条件的优化.
1.2.2 固相萃取[13]
固相萃取前安装固相萃取装置和抽真空装置,SPE小柱采用甲醇和超纯水各5 m L依次活化(每次加液需停留5 min),打开真空泵使液体流出.在柱内液面与填料液面稍平时,将100 m L 衍生后水样以5 m L/min的速度通过小柱,富集完成后抽真空20 min去除小柱残余水分,在柱头加入2 m L正己烷并保留2 min,洗脱、收集后进行仪器检测.结合目标物的总离子流图、回收率等检测结果,对该操作步骤进行优化.
1.3 仪器条件
1.3.1 GC/MS参数[14]
色谱条件:进样口250℃;高纯氦气为载气,流速1.50 m L/min;柱温箱起始温度40℃(保持1 min),以15℃/min升至225℃,再以40℃/min升至280℃(保持5 min);不分流进样模式,进样量1.0μL.质谱条件:离子源温度230℃,四级杆温度150℃,接口温度280℃,溶剂延迟5 min;全扫描模式扫描m/z=40~400;选择离子扫描模式(SIM)下不同BPs的检测离子如表1所示.

表1 BPs及其衍生产物的GC/MS检测参数Tab.1 Scan parameters of BPs and BPs derivatives monitored by GC/MS
1.3.2 GC参数
进样口温度250℃;检测器温度280℃;载气为氮气(流速1 m L/min);不分流进样模式,进样量1.0μL;升温程序:起始温度40℃(保持1 min),以15℃/min升至230℃,再以40℃/min升至280℃(保持5 min).
1.4 BP衍生产物工作曲线的绘制
称取5种BPs标准品适量,用正己烷配制质量浓度分别为2、4、6、8、10μg/m L的混合标样,进行衍生化反应后绘制工作曲线。
1.5 质量控制
分别取8份100.0 m L水样,加入BPs标准品,其中4份样品质量浓度为4μg/m L,另4份为6μg/m L,经1.2步骤处理后,进行GC/MS分析.
2 结果与讨论
2.1 检测仪器的选择
沸点较低、热稳定性较好的有机物适于采用GC、GC/MS 作为检测仪器,因此分别采用2 种仪器对10μg/m L BPs标准品进行检测,得到气相色谱图和总离子流图(图1).通过比较这2种仪器检测后的谱图、峰型等色谱行为,可以看出:相比于总离子流图的检测结果(图1b),气相色谱图中2,4-DBP、2,6-DBP和2,4,6-TBP拖尾较严重,同时2-BP和3,5-DBP响应值偏低(图1a).因此,为了便于定量,选择GC/MS作为水样中BPs的检测仪器.

图1 5种BPs的气相色谱和总离子流图Fig.1 Gas chromatogram and total ion flow diagram of five BPs
2.2 衍生化实验条件的优化
由于BPs分子结构中含有酚羟基,使其具有较高的亲水性和极性,在GC/MS检测时会影响自身的色谱信号和行为,如出现峰形不对称、拖尾等现象,进而影响检测结果.化学衍生化技术[12]可以通过衍生化试剂的引入,调整待测物的极性和提供特征离子,从而改善色谱响应和质谱信号强度.目前,乙酸酐是酚类常用衍生试剂之一,相比于其他衍生化试剂(如丹酰氯[15]、五氟苄基溴[16]等),具有操作简单、成本低和毒性小等优点.但过量的乙酸酐会刺激人体眼睛和上呼吸道,并且腐蚀损伤仪器.因此需考察衍生前后、乙酸酐用量等实验条件,使BPs具有好的衍生化效率和色谱响应,便于更好的定性和定量.
2.2.1 衍生前后色谱行为比较
取2份含BPs标准品的高纯水样,其中1份加入乙酸酐进行衍生化反应,之后2份样品均采用SPE 和GC/MS检测,结果显示:未衍生的BPs拖尾明显(图2a),而衍生后的5种BPs衍生产物(2-BP′,2,6-DBP′,2,4-DBP′,3,5-DBP′,2,4,6-TBP′)峰型对称且不拖尾(图2b), 表明采用乙酸酐衍生可以改善BPs色谱峰峰形、拖尾等问题,有利于其定性和定量分析.

图2 衍生前后5种BPs的总离子流对比Fig.2 Total ion chromatograms of five BPs standards:without and with derivatization
2.2.2 乙酸酐的用量
乙酸酐作为衍生化试剂,其用量的变化不仅会影响衍生化效率、自身的酸性、腐蚀性以及黏度等性质还可能会影响操作人员和仪器,因而需对其用量进行探讨.实验结果如表2所示:随乙酸酐用量增加,BPs衍生产物峰面积增加,当其用量增至1.0 m L后,5种BPs衍生产物峰面积趋于稳定.基于衍生化效率和避免乙酸酐残留较多时对人员和仪器的影响,确定乙酸酐用量为1.0 m L.

表2 乙酸酐用量对BPs(4μg/m L)衍生产物峰面积的影响Tab.2 Effect of acetic anhydride on peak area of BPs(4μg/mL)derivatization products
2.3 SPE实验条件的优化
在水相中痕量有机物的多种富集方法中,相比于液液萃取法,SPE 法具有简单快速、时间短、重复性好和成本低[10,17]等优点,且能够处理较大采样体积的水样,适于BPs这类痕量有机污染物的准确定量.因此,选用SPE法对BPs衍生产物进行富集,并对其萃取实验条件进行优化,包括SPE小柱和洗脱时间等.
2.3.1 SPE小柱的选择
通过文献查阅,选用C18、HLB和PEP 3种SPE小柱对5种BPs衍生产物进行富集(图3):HLB柱的萃取效率更高且较稳定,这一结果与Chi等[18]的研究结果一致, 这可能是因为HLB吸附剂为亲脂性二乙烯苯和亲水性N-乙烯基吡咯烷酮[19],适用于酸性、中性和碱性化合物吸附,因而用于BPs衍生产物的富集具有较高且稳定的回收率.
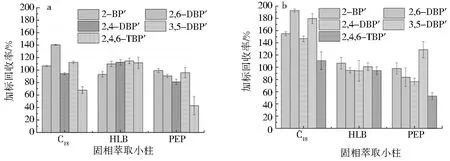
图3 C18、HLB和PEP固相萃取小柱对BPs衍生产物回收率影响Fig.3 Effects of C18,HLB and PEP SPE cartridges on recovery rates of BPs derivatives
2.3.2 洗脱剂保留时间
固相萃取法中,洗脱剂常需在SPE小柱上停留一段时间,以便目标物得到较好的回收率.图4显示:当正己烷在SPE小柱上的停留时间为2 min时,目标物的回收率较高且稳定.在BPs质量浓度为4μg/m L和6μg/m L时,加标回收率分别为72.5%~112.5%和71.8%~104.0%.这可能是因为目标物本身具有一定的挥发性,同时正己烷也较易挥发,故停留时间长,可能对目标物加标回收率的影响更为明显.因此,洗脱剂停留时间定为2 min较为合适.
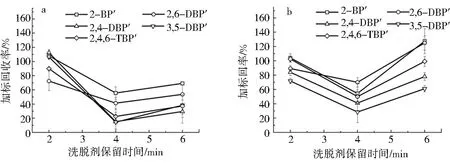
图4 BPs衍生产物回收率随正己烷在HLB柱上停留时间的变化曲线Fig.4 Variation curve of the BPs derivatives recovery rate vs retention time of hexane(HLB)
2.4方法性能指标
BPs标准品溶液中加入1.0 m L乙酸酐和1.0 m L碳酸钾溶液进行衍生化反应,之后加入100.0 m L水样混匀,经活化后的HLB小柱富集,抽真空20 min,采用正己烷(保留2 min)洗脱后,收集、浓缩,经GC/MS检测.
定量检出限定义为噪声信号的10倍所对应的被测物质质量浓度值,定性检出限为噪声信号的3倍所对应的被测物质质量浓度值.结果显示:5种BPs衍生产物的定量检出限为1.7~27.4 ng/m L,定性检出限为0.8~17.7 ng/m L(表3).使用质量浓度为2~10μg/m L的5种BPs标准溶液进行衍生化反应,绘制工作曲线(图5),其线性相关系数为0.999 0~0.999 5,具有良好的线性关系,表明目标化合物质量浓度在2~10μg/m L内可以满足定量要求.

图5 5种BPs衍生产物的工作曲线Fig.5 Working curves of five BPs derivatives

表3 5种BPs衍生产物的检出限Tab.3 Detection limits of five BPs derivatives
2.5 实际水样中BPs的加标回收率
为了评价本方法的实用性和重复性,采用市政供水和高纯水为水样,在已经确定好的前处理方法和仪器条件下,进行BPs的加标回收实验(表4),2种质量浓度条件下,5种BPs经过已建立的分析方法衍生后其空白加标回收率为93.2%~114.5%,市政供水水样的加标回收率为68.3%~110.1%(仅2,4,6-TBP较低,为68.3%~73.0%),相对标准偏差均小于20%,显示出良好回收率和重复性.

表4 市政供水水样中5种BPs衍生产物的加标回收率Tab.4 Recoveries of five BPs derivatives in municipal water
目前,有关BPs的测定方法多用于研究土壤或生物等样品,如李利荣等[20]针对土壤介质,利用超声提取目标物,净化、浓缩后,经GC/MS测定后,2,4,6-TBP平均加标回收率为57.9%;徐英江等[21]采用凝胶渗透色谱净化-乙酸酐衍生-气相色谱质谱法测定水产品中的BPs,其加标回收率为70.2%~102%.虽然介质不同,但BPs作为亲脂性较高的有机物来说,其在土壤或生物等介质中的含量远高于水相中,目标物被检出的概率相对较大.实际水样中对溴酚经表面活性剂辅助-凝固-漂浮分散液液微萃取,采用高效液相色谱仪检测,其加标回收率为96.6%~105%[22],与本方法的加标回收率近似,但此方法成本相对较高.因此,与以上已报道的分析方法相比,所建立的水中BPs测定方法的各项方法性能指标还是具有一定的优势,适于环境水样中BPs的测定.
3 结论
针对水相中的溴酚类物质含量少、毒性大,且尚未有标准检测方法等问题,本实验建立了以柱前衍生-SPE为前处理方法,GC/MS为检测仪器的水相中痕量BPs的测定方法,探讨了影响衍生化反应和SPE 的因素,确定了较为合适的实验条件.所建立的以乙酸酐为衍生化试剂,HLB 小柱萃取,GC/MS检测的分析方法中,5种BPs标准品的定性检出限为0.8~17.7 ng/m L,空白加标回收率为93.2%~114.5%,市政供水的加标回收率为68.3%~110.1%(仅2,4,6-TBP较低),相对标准偏差均小于20%.表明该方法的灵敏度、回收率和重复性均较好,且对实际水样也具有良好的适用性,能够为今后BPs分析方法的优化、检测和监测、削减和控制以及潜在生态风险研究提供参考和基础.
