复发缓解型多发性硬化患者特立氟胺治疗的有效性及安全性
2022-08-26王健丞石紫燕陈虹西周红雨
王健丞 石紫燕 陈虹西 周红雨
多发性硬化(multiple sclerosis,MS)是一种可严重致残的中枢神经系统脱髓鞘性疾病,病变主要累及脑白质,临床表现多种多样,具有空间多发及时间多发的特点[1]。疾病修饰治疗(disease-modifying therapy,DMT)可降低MS患者的复发率及残疾进展,因而被国内外MS治疗指南推荐用于治疗MS患者[2]。特立氟胺作为中国批准上市的疾病修饰治疗的药物之一,在前期针对MS患者的TOWER[3]、TEMSO[4]等三期临床试验中显示,与安慰剂比较,特立氟胺可明显降低MS患者的年复发率,并有较好的安全性。在一项丹麦的真实世界研究中发现,MS患者由其他疾病修饰治疗转换为特立氟胺治疗后,其转换前后年复发率未见明显改变,而使用特立氟胺的患者约80%无残疾程度的进展[5]。由于该药在中国上市时间较晚,目前尚无中国复发缓解型MS(relapsing-remitting multiple sclerosis,RRMS)患者使用特立氟胺的有效性及安全性的研究报道。基于此,本研究对真实世界中RRMS使用特立氟胺的有效性及安全性进行评估。
1 对象和方法
1.1 研究对象本研究为单中心、开放性、前瞻性研究。收集2016年6月至2020年7月在四川大学华西医院多发性硬化中心使用特立氟胺的RRMS患者。所有数据资料来源于作者医院的中枢神经系统脱髓鞘疾病患者数据库和登记系统。纳入标准:(1)符合2017年McDonald诊断标准[6],明确诊断为RRMS;(2)每日口服特立氟胺治疗且连续超过6个月;(3)来自四川省的汉族人群;(4)基线安全性指标(血常规、肝功能和肾功能)检测结果正常者。排除标准:(1)合并其他免疫系统疾病;(2)依从性差,间断或不规律服药;(3)用药时间小于6个月;(4)合并精神疾病或不能配合随访;(5)基线资料或随访资料不完全。
该研究获得了四川大学华西医院伦理委员会的批准[2018(28)],所有纳入的患者均签署了知情同意书。
1.2 方法
1.2.1治疗方案:口服特立氟胺14 mg/d治疗。之后每个月监测基线安全性指标(血常规、肝功能和肾功能)1次,连续3个月无明显异常可每3个月监测1次。治疗期间出现复发的患者,予以甲泼尼龙1000 mg/d冲击治疗,连续5 d,冲击治疗过程中不停服特立氟胺。所有入组患者最小用药时间为6个月,用药截止时间为患者停止用药时间或本研究观察截止时间(2020年7月31日)。
1.2.2临床信息评估:每半年进行1次面对面随访,记录用药6个月以上患者的人口统计学信息、首发时间和症状及入组前药物治疗情况〔包括免疫抑制剂或其他DMT治疗使用情况;入组后复发时间;用药前后年复发率(annualized relapse rate,ARR),用药起始及末次随访的扩展残疾量表评分(expanded disability status scale,EDSS),以及用药相关不良反应记录〕。此外,采用多发性硬化行走功能量表(MSWS-12)和25英尺行走时间(T25FW)评估患者行走功能,由经过培训的神经科医生进行相关资料登记和量表评估;记录由干扰素β-1b转换为特立氟胺前后患者年复发率的情况,并进行亚组分析。
1.2.3结局指标:(1)主要结局指标:治疗期间无复发率、治疗前后年复发率改变。(2)次要结局指标:用药前后EDSS评分及行走功能比较、残疾进展情况、不良反应以及中断治疗情况。
复发定义:运动、感觉及自主神经障碍持续加重超过24 h,并且MRI明确有导致相关症状的病灶[1-2]。
残疾进展定义:随访时EDSS评分增加≥1.5分(基线EDSS为0分),或≥1分(基线EDSS评分<5.5分),或≥0.5分(基线EDSS评分≥5.5分)[3]。
1.3 统计学处理所有数据经统计软件IBM SPSS 23.0处理。计量资料以中位数(范围)表示。计数资料采用例数及百分比(%)表示。用药前后ARR、EDSS评分、MSWS-12评分、T25FW均使用Wilcoxon符号秩检验进行比较,率的比较使用Fisher检验进行比较。均采用双侧检验,以P<0.05认为差异具有统计学意义。
2 结果
2.1 入组患者基本资料本中心使用口服特立氟胺的RRMS患者共90例,排除用药6个月内中断治疗8例、治疗时间未满6个月12例、基线资料不全8例以及失访2例,最终共纳入60例患者,其中男16例(26.67%)、女44例(73.33%),年龄中位数(范围)31.5(16.0~58.0)岁,首次发病年龄25.5(14~58)岁,病程3.58(0~24.25)年,连续使用特立氟胺时间13(6~56)个月。末次发作至入组时间6(1~108)个月;入组前1年内发作1(0~3)次,2年内发作1(0~5)次;入组前EDSS评分2.0(0~6.0)分;入组前2年内DMT治疗情况:使用β干扰素15例(25.00%),富马酸二甲酯(BG12)1例(1.67%)。
2.2 特立氟胺治疗疗效分析
2.2.1复发情况:未出现复发47例(78.33%)。13例(21.67%)复发,复发时间中位数(范围)为5(2~20)个月,其中7例复发1次,5例复发2次,1例复发3次。用药后年复发率较用药前显著降低(P<0.001;表1)。
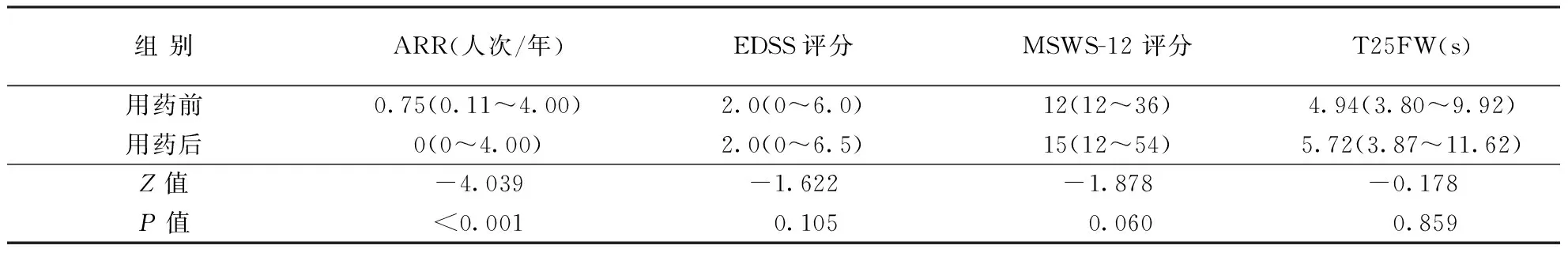
表1 使用特立氟胺前后RRMS患者有效性评估〔n=60,中位数(范围)〕
2.2.2用药前后EDSS评分及行走功能比较:用药后EDSS评分中位数(范围)较用药前差异无统计学意义(P=0.105)。60例患者中,用药后20例患者EDSS评分增加,其中18例EDSS评分增加≥1分。 患者用药后MSWS-12评分、T25FW较用药前升高,但差异无统计学意义(均P>0.05)。具体见表1。
2.2.3初始DMT治疗为重组人干扰素β-1b患者转换为特立氟胺治疗前后疗效比较:60例患者中15例初始DMT用药为重组人干扰素β-1b,转换为特立氟胺前后无复发率、ARR、EDSS评分、MSWS-12评分以及T25FW均差异无统计学意义(P>0.05;表2)。
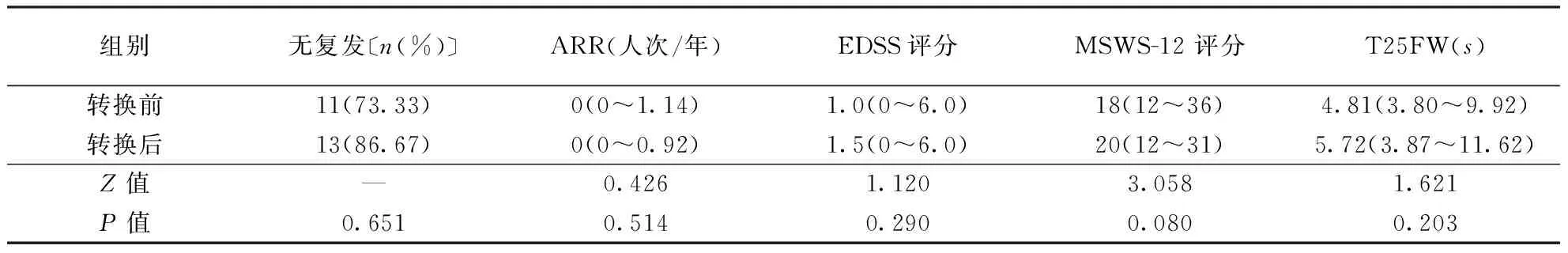
表2 初始行重组人干扰素β-1b治疗的RRMS患者转换为特立氟胺治疗前后疗效比较〔n=15,中位数(范围)〕
2.3 不良反应60例患者中21例报告27次不良反应,其中脱发17例(28.3%;患者报告持续脱发数月后症状即自行停止,具体时间不详),白细胞减少4例(6.7%),唇炎、用药初期一过性皮疹(持续2~3 d自行消失)各2例(3.3%),肝酶异常及月经紊乱各1例(1.7%)。随访过程中无严重不良反应事件出现。
2.4 治疗中断情况共16例患者特立氟胺治疗中断,停药时间中位数(范围)为11.5(6.0~31.0)个月。其中因反复复发/病情进展而换药10例(62.5%),无法忍受副作用1例(6.3%),经济原因4例(25.0%),备孕1例(6.3%)。
3 讨论
本次研究观察并探讨了60例RRMS患者使用特立氟胺的短期有效性及安全性。使用特立氟胺6个月以上的患者中无复发率为78.33%,年复发率显著下降,同TOWER、TEMSO等研究结果相似[3-4],提示特立氟胺能有效减少RRMS患者复发。本组患者用药至少6个月后TF25W、EDSS评分较用药前未见明显差异,但三分之一患者EDSS评分较用药前增加。而此前TOWER研究中显示被判定为残疾进展的患者比例为13%[3],在TEMSO研究中患者的残疾评分相对稳定,本组患者该指标高于上述两个研究,后续仍需更大样本、更长观察时间以及多中心的研究中进一步明确。
本组中部分患者初始治疗为重组人干扰素β-1b,之后转换为特立氟胺治疗。转换治疗前后的ARR、EDSS评分均无显著差异,提示特立氟胺和重组人干扰素β-1b针对复发型MS患者延缓残疾进展及减少复发方面的疗效相当,均能有效减少ARR[7]。
本组患者中观察到出现脱发(28.3%)、白细胞减少(6.7%)、唇炎(3.3%)、一过性皮疹(3.3%)、肝酶异常(1.7%)、月经紊乱(1.7%)等不良反应,以脱发最为突出,其比例高于国外MS相关研究报道[4,8],其可能与研究的人种差异有关,仍需进一步扩大样本量以明确;但患者报告脱发持续数月后症状即自行停止,与之前Miller等[9]的研究结果相似。相比于TEMSO[4]及近期意大利的一项多中心研究[7],本组患者中白细胞减少及肝酶异常患者比例相对偏低,且无肿瘤等事件,同时亦未见严重不良反应病例,提示目前口服特立氟胺有相对较好的安全性。
本研究仍存在一定缺陷:使用特立氟胺治疗的中位观察时间为13个月,时间较短,样本量较小,且为单中心观察研究,后续还需更大样本、更长观察时间的多中心研究来进行评价。另外,本研究仅使用年ARR、EDSS评分、TF25W和MSWS-12来评估患者的复发和残疾进展情况,后续研究可加入影像学指标、患者病灶数量评估以及脑容积变化指标,更精确评估患者用药后的复发和病情进展情况。
综上,本研究中在13个月的中位观察时间内,特立氟胺治疗能有效减少RRMS患者复发,观察时间内残疾保持稳定,安全性较好,未出现严重不良反应。
