巢湖蓝藻与干麦草混合厌氧发酵产沼气研究
2022-08-16汪平生
王 磊,洪 磊,汪平生,许 可,杨 彪
(1.合肥学院 生物食品与环境学院,合肥 230601;2.合肥环境工程研究院,合肥 230601;3.安徽省环境污染防治与生态修复协同创新中心,合肥 230601)
多年来,巢湖水体逐渐呈现富营养化形态,巢湖蓝藻暴发频繁,引起社会各界的广泛重视[1-3]。2020年打捞藻浆近110万t,有研究指出可以基于巢湖蓝藻,来提取天然色素、生理活性物质、胞外多糖,还能够将巢湖蓝藻生产单细胞蛋白等,这些目前处于初步研究阶段[4-8]。巢湖蓝藻中有机物含量丰富,通过厌氧发酵实现其资源化是一种有效的手段。李慧等[9]在27 ℃平均温度发酵条件下,对巢湖蓝藻进行50 d发酵后,TS产气潜力达到368.53 mL/g,甲烷均含量达到64.65%。张东彦等[10]研究发现在20.5 ℃发酵条件下新鲜蓝藻TS产沼潜力可达487.5 mL/g,甲烷含量达到64.95%。农作物秸秆通常含有较高的碳氮比,是调节蓝藻厌氧发酵碳氮比的优良选择,其中干麦草的碳氮比高达93,根据安徽省统计年鉴数据,2020年合肥市干麦草产量达61.7万t,且巢湖蓝藻和干麦草混合厌氧发酵,尚未见文献报道。鉴于此,本文将巢湖蓝藻和干麦草作为实验底料展开实验研究,为巢湖蓝藻和农作物秸秆的资源化利用提供新的路径。
1 材料与方法
1.1 材料
新鲜蓝藻取自巢湖藻水分离站(未加絮凝药剂);干麦草取自安徽阜阳市郊,秸秆碱洗后烘干粉碎过1 mm筛,实验接种物为颗粒污泥,取自蚌埠市某柠檬酸厂IC反应器。主要指标见表1。
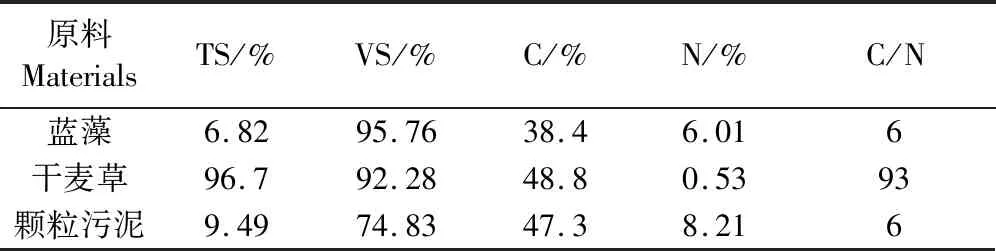
表1 原料主要组分Table 1 Main components of the materials
1.2 实验装置及运行
实验装置由发酵瓶、集气瓶和集水瓶等3个部分组成,由硅胶软管按图1进行连接并检验气密性。实验以1.0 L发酵瓶作为反应器,控制反应物料干物质重量为50 g,巢湖蓝藻、干麦草、颗粒污泥按表2配比分别投加至4组实验装置中,1~4号实验装置中反应物料干麦草∶蓝藻∶颗粒污泥的干物质重量比分别为9∶0∶1、0∶9∶1、2∶7∶1、2∶7(超声40 min)∶1,然后加纯水并搅拌至800 mL,初始pH调至7.0±0.5,充氮气排出发酵瓶中空气后迅速封盖,将反应器置于(35±1)℃的恒定水浴箱中,实验周期为30 d。每24 h手动摇动发酵瓶一次,持续时间30 s,每日记录产气量。
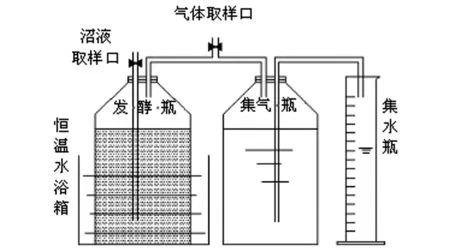
图1 发酵实验装置图Figure 1 Schematic diagram anaerobic fermentation system

表2 实验原料初始特征Table 2 Initial characterization of materials in anaerobic digestion equipment
1.3 方法
干麦草的碱洗:将干麦草浸泡在装有6%的NaOH溶液的烧杯中,再将烧杯放置于85 ℃的恒温水浴锅中3 h,然后将碱洗后的干麦草反复冲洗至pH 7.0,再放入105 ℃的烘箱中,烘干过1 mm筛备用。pH值测定采用pHS-3C型pH测定仪;总固体(TS)采用105 ℃烘干恒重法测定[11];挥发性固体(VS)采用600 ℃烘干恒重法测定[11];COD测定采用重铬酸钾法(GB 11914—1989)[12];NH3-N测定采用纳氏试剂分光光度法(HJ535—2009)[12];甲烷含量测定:气相色谱仪(FUJI GC9790),色谱柱为不锈钢填充柱(1 m*6 mm,I.D.),填料为5A分子筛,柱温85 e,汽化温度100 e,检测器温度100 e,载气为氮气,进样量100 μL。载气为氩气,进样量100 μL。碳氮元素采用元素分析仪(Euro EA3000)测定。
2 结果与分析
2.1 混合厌氧发酵过程中累积产气量
经过30 d的厌氧发酵,反应物料累积产气量如图2所示。4号实验装置的累积产气量和单位挥发性固体产气量最高,分别为15 807 mL、333.78 mL,1、2号实验装置累积产气量和单位挥发性固体产气量均较差。3、4号实验装置累积产气量远高于1、2号实验装置,表明干麦草与蓝藻混合发酵产气显著优于纯干麦草或纯蓝藻单一物料发酵。由表1可知,1号、2号实验装置物料碳氮比分别为93和6,3号、4号实验装置物料碳氮比均为20,表明适宜的碳氮比是厌氧发酵顺利进行的关键指标。发酵体系的碳氮比过高,容易产生酸积累,影响产甲烷菌的生长;碳氮比过低,产生氨积累也会对产甲烷菌产生抑制作用[13-15]。产甲烷细菌是一种专性严格厌氧菌,对酸碱度变化非常敏感,最适pH值范围为6.8~7.2,如果pH值低于6.5,或高于8.2的环境中,产甲烷菌群会受到严重抑制[16]。秦凯等[17]研究碳氮比对水稻秸秆厌氧发酵产甲烷和秸秆降解作用,研究发现碳氮比在20~25效果最好。如图2所示,4号实验装置累积产气量优于3号实验装置,可能是蓝藻超声预处理过程中受超声空化作用影响,使得蓝藻细胞壁破裂,胞内物质溶出,加快了蓝藻的水解酸化时间,提高了发酵的累计产气量[18]。
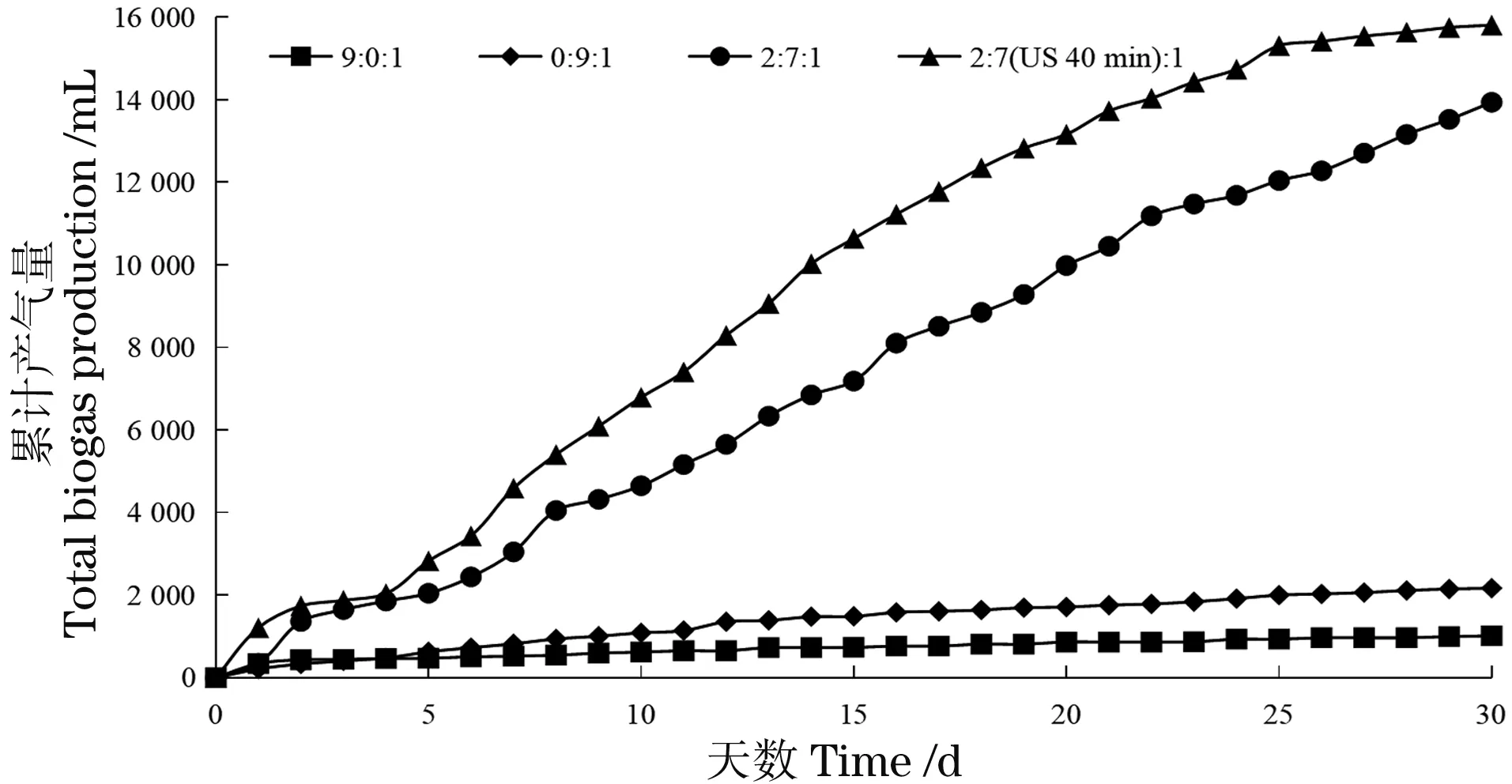
图2 混合厌氧发酵过程中累积产气量Figure 2 Total biogas production during mixed anaerobic fermentation process

表3 反应结束时产气量Table 3 Biogas production at the end of reaction
从图3单日产气量变化看,1号实验装置日产气量很少且极不稳定,多次出现不产气的情况,其产气高峰出现在第1和2天,峰值分别为341和93 mL;2号实验装置日产气量略好于1号实验装置,12~30 d的日产气量普遍优于0~11 d,产气高峰出现在第1和12天,峰值分别为210和214 mL;3、4号实验装置日产气量显著优于1、2号实验装置,3号实验装置产气高峰出现在第2、8和16 天,峰值分别为1 011、1 003和920 mL;4号实验装置产气高峰出现在第1、7和14天,峰值分别为1 207、1 154和962 mL。4号实验装置产气高峰较3号实验装置出现略有提前且产气峰值略高,其原因可能是4号实验装置中的蓝藻物料进行了超声预处理,水解酸化速度快于3号实验装置,4号实验装置优先进入产甲烷阶段且产甲烷菌群所需原料充足。
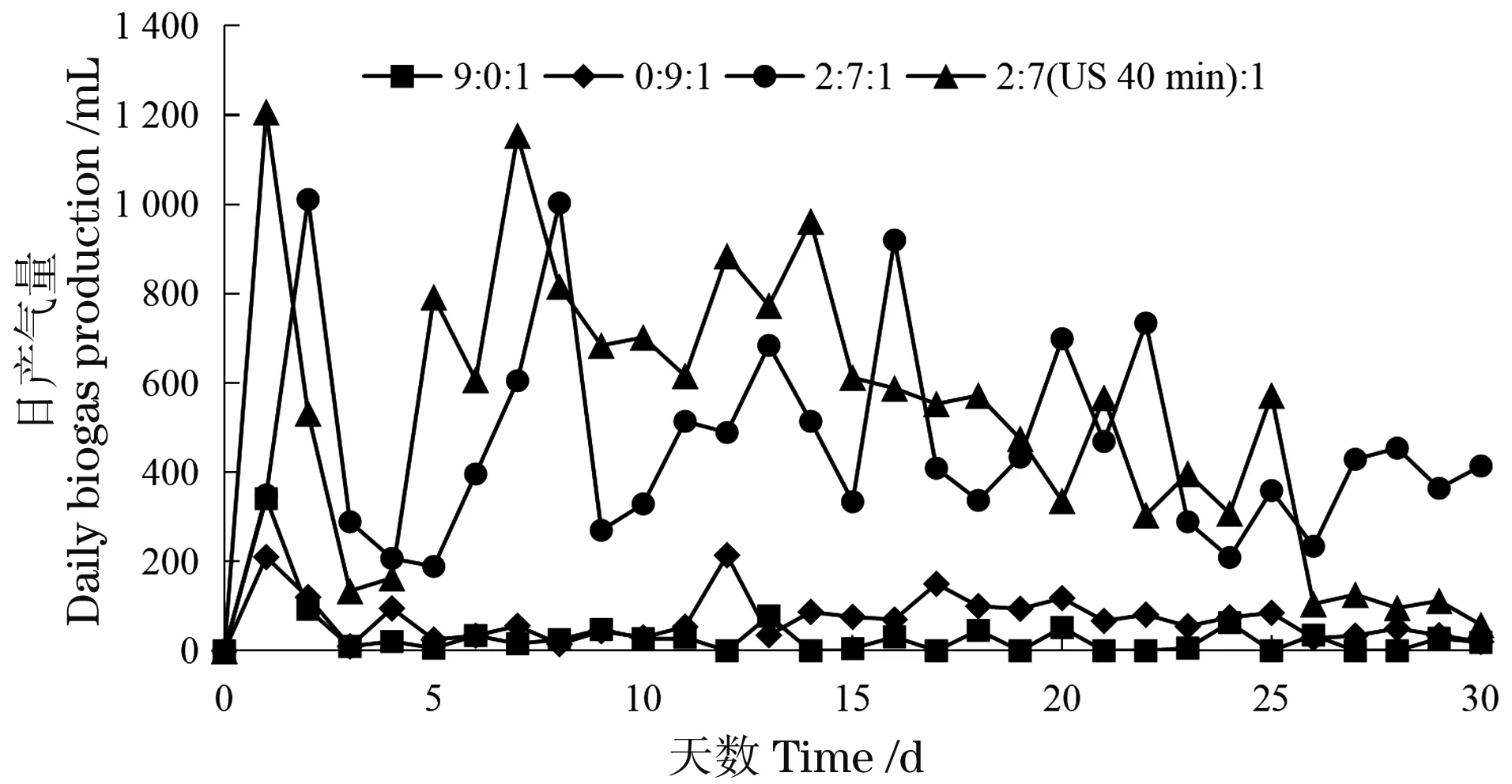
图3 混合厌氧发酵过程中单日产气量Figure 3 Daily biogas production during mixed anaerobic fermentation process
1号和2号实验装置产气高峰均出现在第1天,其原因可能是发酵液本底可溶性有机物发酵产生了H2和CO2等气体,随着发酵物料水解酸化的进行,由于1号碳氮比过高,2号实验装置碳氮比过低,对产甲烷菌的生长均产生较强的抑制作用,使得1号和2号实验装置后续呈现出间歇性产气,且产气量较少。
2.2 混合厌氧发酵过程中发酵液pH值
混合厌氧发酵过程中发酵液pH值变化见图4。如图4所示,1~4号实验装置发酵液pH值整体上均呈现出先降后升的趋势,其原因为发酵初期物料处于水解酸化阶段,物料中的多糖、纤维素、木质素、蛋白质等复杂物质被产酸菌降解为小分子有机酸和CO2,使发酵液pH值不断下降,发酵中后期物料处于产甲烷阶段,此阶段产甲烷菌以发酵初期的有机酸为原料,产生甲烷,又使发酵液的pH值上升[19]。1号实验装置0~6 d pH值持续下降,在第6天达到最低值5.67,6~30 d pH值波动性回升,但pH值始终小于7,其原因与发酵液碳氮比过高,酸化作用大于氨化作用,发酵液中原有的NH3+H+=NH4+平衡被打破[20-21];2~4号实验装置发酵液pH值经历发酵初期下降后,又缓慢回升至7以上,发酵液呈现出弱碱性。
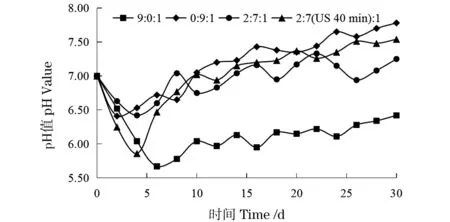
图4 混合厌氧发酵过程中发酵液pH值Figure 4 pH value of fermentation fluid during mixed anaerobic fermentation process
2.3 混合厌氧发酵产气中甲烷含量
如图5所示,6~30 d,1~4号实验装置甲烷产量随发酵天数的增加整体上呈不断上升趋势,甲烷含量最大值分别为44%、55%、54%和57%,2~4号实验装置的甲烷含量普遍高于1号实验装置,其原因主要是1号实验装置发酵液酸化所致。4号实验装置的甲烷含量普遍高于其他组,这主要与其发酵物料水解酸化较为彻底,为产甲烷阶段提供了良好的反应底物。2号实验装置反应物料主要是蓝藻,蓝藻主要成分为多糖和蛋白质,较容易进入产甲烷阶段。
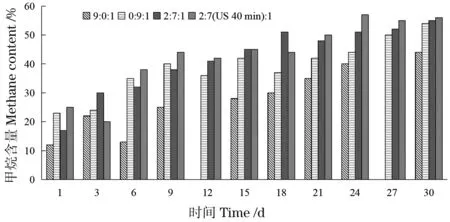
图5 混合厌氧发酵过程中甲烷含量Figure 5 Methane content during mixed anaerobic fermentation process
2.4 混合厌氧发酵过程中发酵液COD和NH3-N变化
由图6可以看出,3号实验装置发酵液COD曲线在第5和15天均呈现出一定程度的增加,发酵液COD最大值为30 565 mg/L,出现在第5天,实验结束时,发酵液COD值为8 875 mg/L。厌氧发酵过程中,发酵液COD的变化在一定程度上可以表征发酵物料的水解过程[22],发酵液COD值第5天达到峰值,主要是由于实验初期发酵物料中大分子有机物被水解成溶解态,从而增加发酵液COD值[23]。
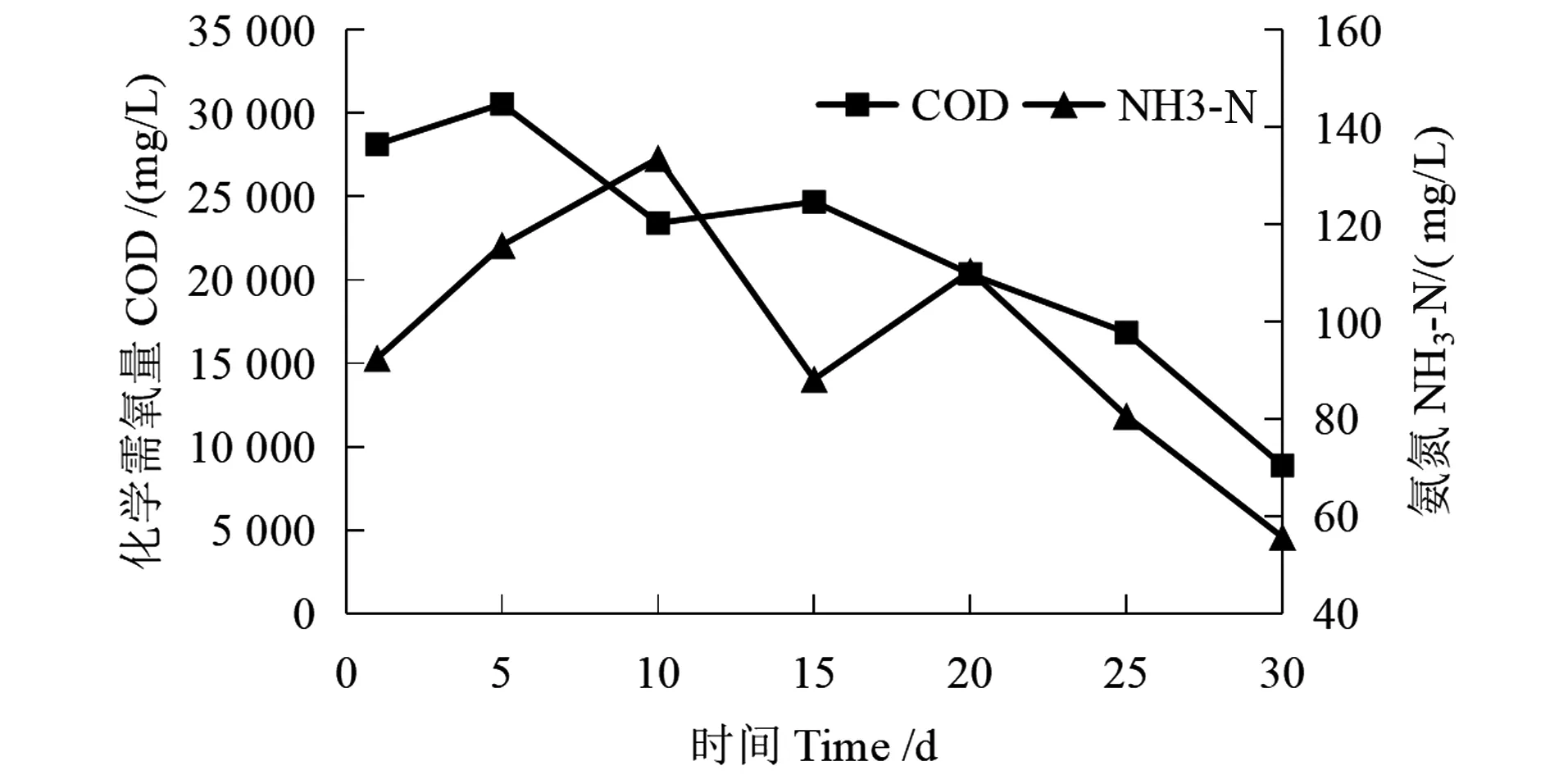
图6 3号实验装置发酵液COD和NH3-N变化Figure 6 Variation of COD and NH3-N of fermentation fluid for No.3 experimental device
由图7可以看出,4号实验装置发酵液COD最大值出现在第1天,为31 812 mg/L,而后一直呈下降趋势,实验结束时,发酵液COD值为7 847 mg/L。3号实验装置NH3-N曲线呈现出较大波动,0~10 d,NH3-N呈现先降后升的趋势,最大值137.2 mg/L,出现在第10天,而后逐渐降低,实验结束时,发酵液NH3-N浓度为55.7 mg/L;4号实验装置NH3-N浓度最大值为184.2 mg/L,出现在第0天,而后呈现出下降趋势,实验结束时,NH3-N浓度值为45.4 mg/L。
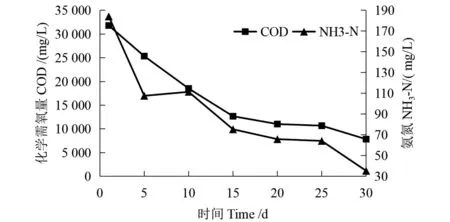
图7 4号实验装置发酵液COD和NH3-N变化Figure 7 Variation of COD and NH3-N of fermentation fluid in No.4 experimental device
3 讨论
3.1 各指标之间的相关性
利用SPSS软件对数据进行分析。3号实验装置的产气量与发酵液COD表现出显著正相关(r=0.916**,** 为在0.01水平上显著相关),产气量的变化可以通过发酵液COD来进行表征;4号实验装置的发酵液COD和NH3-N呈现出显著正相关(r=0.969**,** 为在0.01水平上显著相关)。王震宇等[24]研究蓝藻厌氧发酵过程中产气量与化学需氧量(COD)有显著差异,且产气量与挥发性脂肪酸(VFA)含量呈显著正相关。3号实验装置研究结果与上述研究结果一致,而4号实验装置差异较大,其原因可能是蓝藻超声预处理加快蓝藻胞内物质溶出,使得蛋白质较早进入水解和氨化,其相关性尚需进一步研究。
3.2 发酵液COD变化特征
3号和4号实验装置发酵液COD呈现出不同的变化曲线,发酵液COD值与发酵物料的水解速率和产气量相关[25],水解过程会促使发酵液COD值升高,发酵液COD消减量又贡献给了产气量。后期需增加VFA含量测定以及发酵液COD检测频次,进一步探索其关联性。
3.3 实验产气、产甲烷特征
1号和2号实验装置产气量较少,主要原因是两组物料碳氮比过高(1号实验装置)和过低(2号实验装置)。碳氮比过高,发酵液酸化阶段产生大量有机酸,使发酵液pH值大幅下降,容易导致产甲烷菌酸中毒;碳氮比过低,会促进氨化微生物生长,产生氨积累,又致使产甲烷菌氨中毒。3号和4号实验装置反应物采用干麦草/蓝藻颗粒污泥混合物料,碳氮比为20,产气量显著高于1号和2号实验装置,但甲烷浓度普遍不高且不稳定,后期将对接种微生物进行驯化并对其投加量进行研究。
