曲妥珠单抗联合长春瑞滨治疗晚期乳腺癌患者的临床疗效及对生存情况的影响
2022-08-10韩艳艳是蔷杨姗姗
韩艳艳,是蔷,杨姗姗
焦作煤业(集团)有限责任公司中央医院内科,河南 焦作 454000
乳腺癌是多发于女性的恶性肿瘤之一,其在女性中的发病率仅次于宫颈癌,发病原因可能与遗传因素、饮食不调或性激素刺激有关[1]。晚期乳腺癌恶性程度较高,发病后患者会出现乳头回缩、乳腺皮肤呈“酒窝”状或腋窝淋巴结肿大等,相较于早期病变,其临床症状更具有典型性[2]。目前,已有大量研究证实曲妥珠单抗与化疗联合治疗晚期乳腺癌可取得良好的效果,但在化疗方案的选择上争议较大。曲妥珠单抗联合吉西他滨或长春瑞滨是临床常用于晚期乳腺癌的治疗方案,但哪种方案更好,仍缺乏定论[3-4]。本研究分析曲妥珠单抗联合长春瑞滨治疗晚期乳腺癌的临床疗效及对生存情况的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年1月至2018年12月焦作煤业(集团)有限责任公司中央医院收治的晚期乳腺癌患者。纳入标准:①符合《中国抗癌协会乳腺癌诊治指南与规范(2015版)》[5]中乳腺癌的诊断标准;②经临床及病理检查确诊为乳腺癌;③乳房皮肤出现橘皮样改变;④临床资料完整;⑤临床分期为Ⅳ期。排除标准:①对曲妥珠单抗过敏;②存在化疗禁忌证;③合并其他器官感染或肿瘤;④合并认知功能障碍导致无法完全配合治疗。依据纳入和排除标准,本研究共纳入118例患者。根据治疗方法的不同将患者分为对照组和观察组,每组59例,对照组患者接受曲妥珠单抗联合吉西他滨治疗,观察组患者接受曲妥珠单抗联合长春瑞滨治疗。两组患者的年龄、病程、肿瘤类型、临床分期及淋巴结转移情况比较,差异均无统计学意义(P>0.05)(表1),具有可比性。本研究经医院伦理委员会审批通过,所有患者均知情同意并签署知情同意书。

表1 两组患者的临床特征
1.2 治疗方法
对照组患者接受曲妥珠单抗联合吉西他滨治疗。第1、8、15天静脉滴注吉西他滨1000 mg/m2,然后静脉滴注曲妥珠单抗,初次滴注剂量为4 mg/kg,之后调整为2 mg/kg,每周1次。
观察组患者接受曲妥珠单抗联合长春瑞滨治疗。第1、8天静脉滴注酒石酸长春瑞滨25 mg/m2,第1天联合静脉滴注曲妥珠单抗8 mg/kg,从第2天开始将曲妥珠单抗调整为6 mg/kg。
3周为1个疗程,两组患者均持续治疗4个疗程。
1.3 观察指标及评价标准
①采用实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)[6]评价两组患者的临床疗效,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)及疾病进展(progressive disease,PD)。疾病控制率=(CR+PR+SD)例数/总例数×100%。②分别于治疗前后采集两组患者的空腹静脉血3 ml,采用化学发光法检测癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原 125(carbohydrate antigen 125,CA125)、糖类抗原15-3(carbohydrate antigen 15-3,CA15-3)水平,试剂盒均购自珠海华澳生物科技有限公司,仪器选择贝克曼库尔特AU480全自动生化分析仪。③记录两组患者的不良反应发生情况,包括水肿、皮肤红疹和骨髓抑制。④所有患者均随访3年,记录两组患者的生存情况,主要包括无进展生存期(progression-free survival,PFS)和总生存期(overall survival,OS)。
1.4 统计学方法
采用SPSS 22.0软件对数据进行统计分析,符合正态分布的计量资料以均数±标准差(±s)表示,组间比较采用t检验;计数资料以例数和率(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效的比较
观察组患者的疾病控制率为94.92%(56/59),高于对照组患者的81.36%(48/59),差异有统计学意义(χ2=5.187,P=0.023)。(表2)

表2 两组患者的临床疗效[n(%)]*
2.2 肿瘤标志物水平的比较
治疗前,两组患者的CEA、CA125、CA15-3水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者的CEA、CA125、CA15-3水平均低于本组治疗前,且观察组患者的CEA、CA125、CA15-3水平均低于对照组,差异均有统计学意义(P<0.05)。(表3)
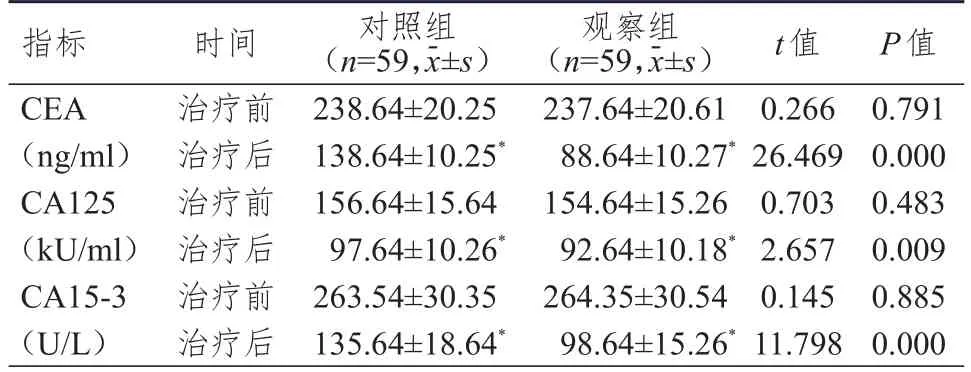
表3 治疗前后两组患者肿瘤标志物水平的比较
2.3 不良反应发生情况的比较
观察组患者的不良反应总发生率为8.47%(5/59),低于对照组患者的22.03%(13/59),差异有统计学意义(χ2=4.196,P=0.040)。(表4)
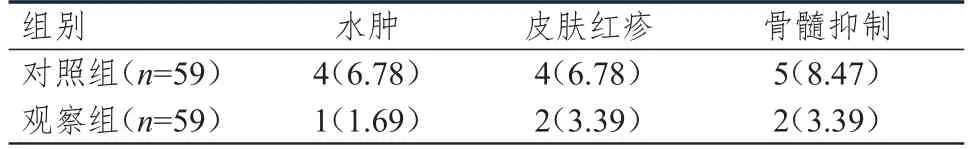
表4 两组患者的不良反应发生情况[n(%)]
2.4 生存情况的比较
观察组患者的中位PFS为19.58个月,长于对照组患者的15.30个月,差异有统计学意义(χ2=6.870,P<0.05);观察组患者的中位OS为32.60个月,长于对照组患者的26.80个月,差异有统计学意义(χ2=7.850,P<0.05)。
3 讨论
乳腺癌具有较高的病死率,尤其是晚期乳腺癌,近几年乳腺癌的发病率在中国呈持续上升趋势,对中国女性的身心健康造成严重威胁[7]。由于晚期乳腺癌患者多数存在脑转移、骨转移或肝脏转移等内脏远处转移情况,失去了手术指征,无法对其开展保乳手术或肿瘤根治术,因此化疗逐渐成为晚期乳腺癌的首选治疗方案之一[8]。曲妥珠单抗联合化疗是目前临床常用于治疗晚期乳腺癌的方法之一,其治疗效果较为显著,但在化疗方案的选择上仍存在一定争议,既往临床主要采用曲妥珠单抗与吉西他滨联合治疗,但该疗法不良反应较大,长期治疗易引起大量不良反应,不利于患者预后[9-10]。
曲妥珠单抗是临床常用于治疗乳腺癌的药物,对人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)具有靶向作用,因此在治疗前需要对晚期乳腺癌患者的HER2水平进行检测,若HER2水平升高,即可使用该药物治疗[11]。曲妥珠单抗进入人体后能够与HER2特异性结合,从而调控细胞的信号传递,促使HER2蛋白降解,同时通过抗体依赖性细胞的作用聚集免疫杀伤细胞,并对肿瘤细胞进行攻击,达到抑制肿瘤细胞生长的目的,其治疗效果较为显著[12-13]。长春瑞滨进入人体后可通过与微管蛋白相结合的方式抑制肿瘤细胞的有丝分裂,进而抑制肿瘤细胞生长。采用长春瑞滨与曲妥珠单抗联合治疗,可发挥协同作用,有助于进一步提高晚期乳腺癌对化疗药物的敏感性,进而发挥强效抗肿瘤作用,对控制病情进展具有重大意义[14-15]。本研究结果显示,观察组患者的疾病控制率高于对照组,治疗后观察组患者的CEA、CA125、CA15-3水平均低于对照组,差异均有统计学意义(P<0.05)。说明曲妥珠单抗联合长春瑞滨治疗晚期乳腺癌患者可有效抑制肿瘤细胞生长,在一定程度上提高临床治疗效果。曲妥珠单抗作为晚期乳腺癌的靶向治疗药物,进入人体后能够抑制肿瘤细胞生长及肿瘤新生血管生成。长春瑞滨相较于吉西他滨而言,其作用靶点不同,该药物对HER2的抑制作用更为显著,可有效阻断细胞生长因子信号转导,避免乳腺癌细胞快速增长,有助于延长患者的生存期。研究表明,曲妥珠单抗与长春瑞滨联合治疗乳腺癌有助于控制疾病转移和复发,在延长患者生存期方面具有重要意义[16-17]。本研究结果显示,观察组患者的中位PFS、OS均长于对照组(P<0.05)。提示曲妥珠单抗联合长春瑞滨治疗晚期乳腺癌可延长患者的生存时间。曲妥珠单抗在晚期乳腺癌的治疗中具有高度特异性,可在减小对周围正常组织损伤的前提下发挥强效抗肿瘤作用,且安全性较高,治疗后不会引起较多不良反应[18-19]。长春瑞滨的心脏毒性较低,与曲妥珠单抗联合应用不会增加不良反应,有助于进一步提高治疗的安全性,避免治疗后引发大量不良反应[20-21]。本研究结果显示,观察组患者不良反应总发生率低于对照组(P<0.05)。本研究发现,观察组仍有5例患者出现不良反应,针对出现不良反应的患者,临床还需根据其不良反应对症下药,并明确引发不良反应的原因,以便下次治疗时提前做好预防方案。例如,针对出现水肿的患者,可在水肿部位进行热敷、冷敷或按摩,并为其做好饮食护理,同时可以在下次治疗前给予患者甘露醇或速尿等脱水药物;针对出现皮肤红疹的患者,首先需考虑引发红疹的原因,若患者为药物过敏性红疹,需及时找出导致患者过敏的药物,并立即停用,同时给予患者相应的抗过敏药物,若患者为免疫力低下而引发红疹,可通过针对性的措施增强其机体免疫力;针对出现骨髓抑制的患者,需给予适量的升血药物,并做好皮肤、发热、饮食护理等,同时将其隔离。
综上所述,曲妥珠单抗联合长春瑞滨治疗晚期乳腺癌具有较好的临床疗效,安全性较高,而且能够在一定程度上延长患者的生存期。
