UPLC法同时测定风热感冒颗粒中13种成分
2022-07-22李婷婷黄晓婧孔卫东
李婷婷,王 淼,王 欣,黄晓婧,孔卫东,曾 桢,刘 莉*
(1.成都市药品检验研究院,国家药品监督管理局中药材质量监测评价重点实验室,四川 成都 610045;2.成都市农业质量监测中心,四川 成都 610041)
风热感冒颗粒由板蓝根、连翘、薄荷、荆芥穗、桑叶、芦根、牛蒡子、菊花、苦杏仁、桑枝、六神曲11味药材制成,具有清温解毒、宜肺利咽之功效,常用于治疗风热感冒、鼻塞、头痛、咳嗽、多痰等症[1],该制剂现行质量标准主要是《卫生部药品标准》中药成方制剂第一册,但仅有性状、制剂通则检查项,无含量测定项。现有文献[2-5]也主要集中于牛蒡子苷、连翘苷、苦杏仁苷、绿原酸等成分的含量测定,不能从整体上控制风热感冒颗粒内在质量。
现代药理研究表明,(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸A、异绿原酸B、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元为风热感冒颗粒活性成分[6-14]。因此,本实验参考文献[15-18],将建立UPLC法同时测定风热感冒颗粒中上述13种成分的含量,以期更全面、科学、快速地控制该制剂质量。
1 材料
1.1 仪器 Waters Acquity H Class超高效液相色谱仪(美国沃特世科技公司);XPE26(0.001 mg)、ME204E电子天平(0.1 mg)(瑞士梅特勒-托利多公司);SK250H超声仪(上海科导超声仪器有限公司)。
1.2 试剂与药物 (R,S)-告依春(批号111753-201706,纯度100.0%)、绿原酸(批号110753-201817,纯度96.8%)、苦杏仁苷(批号110820-201808,纯度88.2%)、连翘酯苷A(批号111810-201707,纯度97.2%)、连翘苷(批号110821-201816,纯度95.1%)、牛蒡苷(批号110819-201812,纯度95.0%)对照品均由中国食品药品检定研究院提供;新绿原酸(批号19042305,纯度≥98%)对照品由成都普菲德生物技术有限公司提供;隐绿原酸(批号MUST-20042403,纯度99.07%)、连翘酯苷I(批号MUST-20041612,纯度98.26%)、异绿原酸B(批号MUST-20031602,纯度99.05%)、异绿原酸C(批号MUST-20031603,纯度99.84%)、牛蒡苷元(批号MUST-19060509,纯度99.62%)对照品均由成都曼斯特生物科技有限公司提供;异绿原酸A(批号ST03860120,纯度≥98.0%)对照品由上海诗丹德标准技术服务有限公司提供。风热感冒颗粒共12批(A企业,批号S1;B企业,批号S2、S3;C企业,批号S4、S5;D企业,批号S6;E企业,批号S7;F企业,批号S8;G企业,批号S9;H企业,批号S10、S11;I企业,批号S12)。甲醇、乙腈、磷酸为色谱纯;其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件 Waters Acquity UPLC Hss T3色谱柱(150 mm×2.1 mm,1.8 μm);流动相乙腈(A)-0.01%磷酸(B),梯度洗脱(0~5 min,5%A;5~10 min,5%~11%A;10~11 min,11%~12.5%A;11~20 min,12.5%~19%A;20~30 min,19%~28%A;30~35 min,28%~31%A;35~40 min,31%~40%A;40~45 min,40%A);体积流量0.5 mL/min;柱温30 ℃;检测波长0~4 min 240 nm,4~9.2 min 327 nm,9.2~11.5 min 207 nm,11.5~26 min 327 nm,26~45 min 227 nm。
2.2 溶液制备
2.2.1 对照品溶液 精密称取各对照品适量,甲醇溶解,摇匀,滤过,即得[各成分质量浓度分别为(R,S)-告依春541.00 μg/mL、新绿原酸502.94 μg/mL、绿原酸630.17 μg/mL、苦杏仁苷452.02 μg/mL、隐绿原酸571.34 μg/mL、连翘酯苷I 548.68 μg/mL、连翘酯苷A 719.09 μg/mL、异绿原酸B 520.61 μg/mL、异绿原酸A 618.38 μg/mL、异绿原酸C 504.79 μg/mL、连翘苷505.84 μg/mL、牛蒡苷1 040.44 μg/mL、牛蒡苷元626.51 μg/mL]。
2.2.2 供试品溶液 精密称取本品5.0 g,置于锥形瓶中,精密加入25 mL甲醇,称定质量,超声提取30 min,放冷,甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.3 阴性样品溶液 按处方比例,制备缺板蓝根、菊花、苦杏仁、连翘、牛蒡子、桑叶、桑枝的阴性样品,按“2.2.2”项下方法制备,即得。
2.3 系统适应性考察 精密吸取对照品、供试品、阴性样品溶液适量,在“2.1”项色谱条件下各进样1 μL 测定,结果见图1。由此可知,各成分色谱峰峰形良好,阴性无干扰。
2.4 方法学考察
2.4.1 线性关系考察 精密量取对照品溶液适量,甲醇稀释成系列质量浓度,在“2.1”项色谱条件下进样测定。以对照品质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,结果见表1,可知各成分在各自范围内线性关系良好。
2.4.2 精密度试验 精密吸取同一份对照品溶液,在“2.1”项色谱条件下进样测定6次,测得(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸B、异绿原酸A、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元峰面积RSD分别为1.38%、1.42%、1.41%、1.31%、1.37%、1.47%、1.47%、1.29%、1.48%、1.48%、1.40%、1.41%、1.47%,表明仪器精密度良好。

1.(R,S)-告依春 2.新绿原酸 3.绿原酸 4.苦杏仁苷 5.隐绿原酸 6.连翘酯苷I 7.连翘酯苷A 8.异绿原酸B 9.异绿原酸A 10.异绿原酸C 11.连翘苷 12.牛蒡苷 13.牛蒡苷元1.(R,S)-epigoitrin 2.neochlorogenic acid 3.chlorogenic acid 4.amygdalin 5.cryptochlorogenic acid 6.forsythoside I 7.forsythoside A 8.isochlorogenic acid A 9.isochlorogenic acid B 10.isochlorogenic acid C 11.forsythin 12.arctiin 13.arctigen图1 各成分UPLC色谱图Fig.1 UPLC chromatograms of various constituents
2.4.3 稳定性试验 精密吸取同一份供试品溶液,于0、4、8、12、16、24 h在“2.1”项色谱条件下进样测定,测得(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸B、异绿原酸A、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元峰面积RSD分别为2.58%、2.19%、2.18%、2.08%、1.31%、1.38%、1.95%、1.76%、1.69%、1.86%、2.02%、2.25%、2.42%,表明溶液在24 h内稳定性良好。
2.4.4 重复性试验 取同一批样品,按“2.3”项下方法平行制备6份供试品溶液,在“2.1”项色谱条件下进样测定,测得(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸B、异绿原酸A、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元含量RSD分别为2.05%、1.62%、2.28%、2.72%、1.85%、2.75%、1.10%、1.98%、1.84%、1.79%、1.51%、1.85%、1.72%,表明该方法重复性良好。
2.4.5 加样回收率试验 精密称取各成分含量已知的本品(批号20190101)粉末约2.5 g,共9份,每3份为1组,分别按50%、100%、150%水平精密加入对照品溶液适量,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样测定,计算回收率。结果,(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸B、异绿原酸A、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元平均加样回收率分别为96.14%、99.11%、99.46%,103.52%、99.87%、100.73%、100.33%、97.65%、97.89%、98.69%、95.42%、101.19%、100.25%,RSD分别为2.29%、1.41%、2.89%、2.33%、1.50%、2.25%、1.59%、1.98%、2.05%、2.01%、2.89%、2.39%、2.75%。
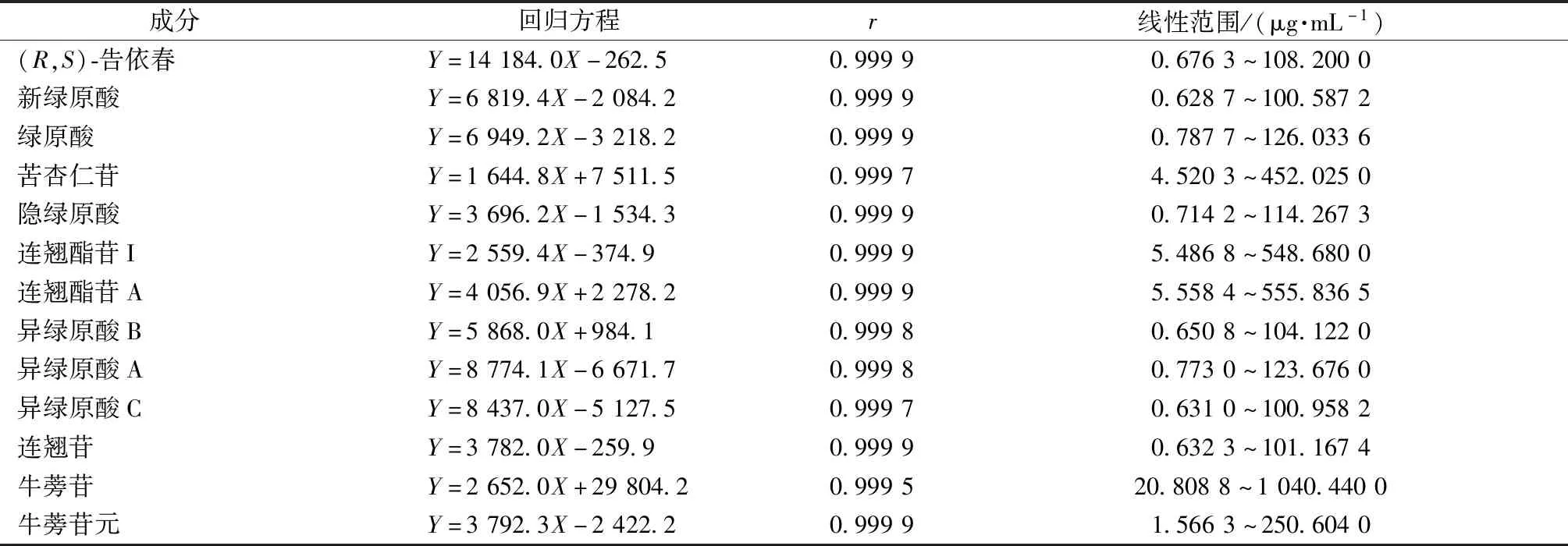
表1 各成分线性关系Tab.1 Linear relationships of various constituents
2.5 样品含量测定 取12批样品,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样测定,计算含量(其中样品S10、S11中牛蒡苷含量超出标准曲线范围,故再分别精密量取1 mL至10 mL量瓶中,甲醇稀释至刻度,重新进行计算),结果见表2。
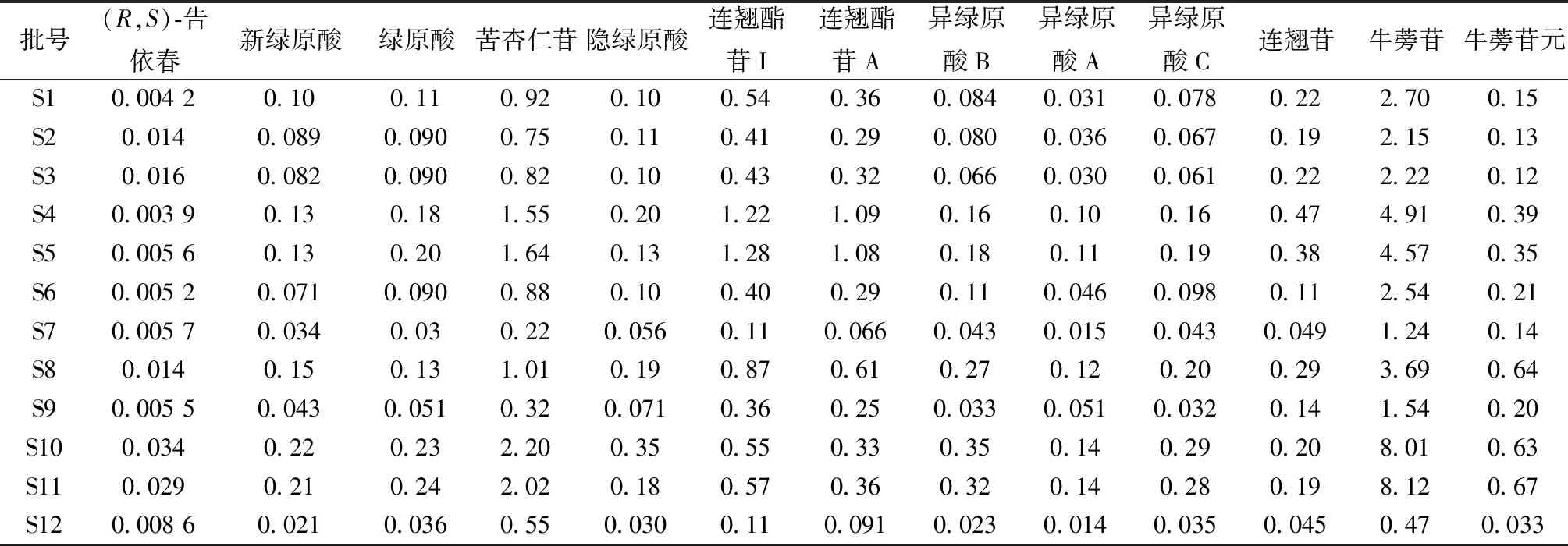
表2 各成分含量测定结果(mg/g,n=3)Tab.2 Results of content determination of various constituents (mg/g,n=3)
3 讨论
3.1 提取方法筛选 本实验考察了不同提取方式(回流、超声)、提取溶剂、提取溶剂体积、提取时间对各成分提取率的影响,最终确定为25 mL甲醇超声提取30 min。
3.2 流动相系统筛选 由于风热感冒颗粒药味较多,各成分化学性质相差较大,故采用梯度洗脱。再考察了乙腈-磷酸、甲醇-磷酸流动相(磷酸体积分数为0.01%、0.02%、0.03%),发现乙腈-0.01%磷酸洗脱时各成分色谱峰峰形对称,分离较好。
3.3 检测波长筛选 由于各成分紫外光谱差异较大,不能在同一波长下测定,为了兼顾其最大吸收波长,提高灵敏度,减少干扰,选择240、327、207、227 nm波长切换模式。
3.4 含量分析 表2显示,不同批次风热感冒颗粒中各成分含量存在较大差异,以(R,S)-告依春、连翘酯苷A、牛蒡苷更明显,可能与原药材产地、采收季节、企业生产工艺等因素有关。
4 结论
本实验建立UPLC法同时测定风热感冒颗粒中(R,S)-告依春、新绿原酸、绿原酸、苦杏仁苷、隐绿原酸、连翘酯苷I、连翘酯苷A、异绿原酸B、异绿原酸A、异绿原酸C、连翘苷、牛蒡苷、牛蒡苷元的含量,该方法简便、快速、准确,可为更全面科学地评价和控制该制剂质量提供依据。
