贵金属Pd-X(X=Ag, Ni, Sn)体系的相图热力学研究
2022-07-18廖林刘树红杜勇
廖林,刘树红,杜勇
贵金属Pd-X(X=Ag, Ni, Sn)体系的相图热力学研究
廖林,刘树红,杜勇
(中南大学 粉末冶金国家重点实验室,长沙 410083)
对贵金属Pd-X(X=Ag, Ni, Sn)体系的相图热力学文献数据进行严格评估的基础上,采用替代溶液模型描述该3个二元系中液相和FCC_A1相的吉布斯自由能,分别采用亚点阵模型(Pd,Sn)1Sn2、(Pd)0.25(Pd,Sn)0.75和(Pd)0.2(Pd,Sn)0.8描述PdSn2、PdSn3和PdSn4相,通过CALPHAD(calculation of phasediagram)方法获得描述贵金属Pd-X (X=Ag, Ni, Sn)体系的热力学参数。相较于文献报道,本研究得到的热力学参数能更合理地描述Pd-X (X=Ag, Ni, Sn)体系的实验相图数据和热力学数据,尤其在Pd-Ag相图、Pd-Ag体系和Pd-Ni体系FCC_A1的混合焓及Pd-Sn相图富Sn端零变量反应的描述方面。计算结果与实验数据的比较表明本工作获得的热力学参数的准确性。
Pd-X (X=Ag, Ni, Sn);CALPHAD;相图;热力学性质
近年来,基于健康安全和环境保护的考虑,传统锡铅焊料正逐渐被新型无铅焊料替代。Ag-Sn焊料被认为是替代锡铅焊料最有前途的材料体系之一[1−2]。然而,由于Ag-Sn焊料与铜基板发生界面反应产生金属间化合物,严重影响微电子封装中焊点的可靠性[2−4]。因此,通常在Ag-Sn焊料与基体之间设计Ni/Pd涂层作为扩散阻挡层,用来限制金属间化合物层的生 长[5−6]。相图热力学信息对于焊料和中间涂层材料的成分设计,以及涂层跟焊料和基体之间的界面反应机理研究至关重要。经过多年的探索与改进,CALPHAD (calculation of phase diagram)方法已在材料研发过程中发挥重要作用[7−8]。因此,为了实现Ag-Sn焊料的高效研究和开发,Ag-Ni-Pd-Sn体系准确的相图热力学描述是必要基础。目前已有对Pd-Ag、Pd-Ni和Pd-Sn体系的热力学描述,但均存在一定的局限性。例如:GHOSH等[9]最早报道了Pd-Ag体系的热力学参数,但基于该参数计算的1 673 K液相混合焓与LUEF等[10]的实验数据偏差较大。最近俄罗斯的CHUDNENKO[11]在研究Ag-Au-Pd体系组元的热力学性质时已重新获得Pd-Ag体系的热力学参数,但基于该参数计算的600 K FCC_A1相的混合焓与早前的实验结果[12]相差较大,并且基于该参数计算的Pd-Ag相图与实验数据也存在较大的误差[13−15]。GHOSH等[9]报道的Pd-Ni体系的热力学参数能够描述大部分Pd-Ni体系的实验数据,但计算的1173 K FCC_A1相的混合焓与BIDWELL等[16]的实验信息偏差较大。CUI等[17]基于2020年以前的研究结果重新优化了Pd-Sn体系,认为Pd5Sn7是稳定相,但与文献[18−19]的实验信息存在出入。此外,CUI等[17]计算的富Sn端零变量反应温度与NYLÉN等[18]采用差示扫描量热法(differential scanning calorimetry, DSC)测得的包晶反应温度相差较大。基于上述研究成果与存在的不足,本文作者在对贵金属Pd-X(X=Ag,Ni,Sn)体系的相图热力学文献数据进行严格评估的基础上,采用替代溶液模型描述3个二元系中液相和FCC_A1相的吉布斯自由能,分别采用亚点阵模型(Pd,Sn)1Sn2、(Pd)0.25(Pd,Sn)0.75和(Pd)0.2(Pd,Sn)0.8描述PdSn2、PdSn3和PdSn4相,通过CALPHAD方法获得描述贵金属Pd-X (X=Ag, Ni, Sn)体系更准确的热力学参数,为四元Ag-Ni-Pd-Sn体系的热力学描述提供准确的边界二元系参数。
1 文献评估
1.1 Pd-Ag体系
Pd-Ag体系具有液相和固相完全混溶的特点。时隔55年,RUER等[13]及SAVITSKIJ等[14]先后采用热分析法(thermal analysis, TA)方法测定了Pd-Ag相图的液相线和固相线。SOPOUŠEK等[15]采用DSC法重新测定了液固相变温度,得到的液相/FCC_A1两相区与RUER[13]和SAVITSKIJ等[14]的实验结果一致。
LUEF等[10]通过传统滴热仪(conventional drop calorimeter, CDC)测得Pd-Ag体系1 673 K的液相混合焓。VATOLIN等[20]采用量热法(calorimetry,CA)测定1 873 K液相中Ag的活度,与SOPOUŠEK等[15]采用克努森容器质谱法(Knudsen cell mass spectrometry, KCMS)测得的结果一致。LAURIE等[21]、RAYCHAUDHURI等[22]以及FENG等[12]采用电动势法(electromotive force, EMF)分别测定了1 000 K、1 100 K以及550、600和650 K时FCC_A1中Ag的活度。此外,FENG等[12]采用EMF测得600 K时FCC_A1的混合焓。LAURIE等[21]的实验结果与RAYCHAUDHURI等[22]以及FENG等[12]的实验结果不一致,本研究主要考虑RAYCHAUDHURI等[22]以及FENG等[12]的实验结果。
1.2 Pd-Ni体系
Pd-Ni体系也具有液相和固相完全混溶的特点,但与Pd-Ag体系不同的是,Pd-Ni二元合金的液相和FCC_A1相具有相同的熔融点。HEINRICH[23]和FRAENKEL等[24]采用TA测定了Pd-Ni体系的液相线和FCC_A1固相线。BIDWELL等[25]通过X射线衍射分析(X-ray diffraction, XRD)测定FCC_A1相的晶格参数,进一步验证了Ni和Pd在FCC_A1相中的完全混溶。FRAENKEL等[24]指出Pd-Ni体系低温时存在混溶间隙,但随后HULTGREN等[26]基于XRD研究结果未发现该现象。GHOSH等[9]研究了FCC_A1合金的居里温度与磁矩的成分依赖性,并基于热力学计算获得FCC_A1相的磁相互作用参数。
VATOLIN等[27]采用TA法测定了1 873 K的液相混合焓。OISHI等[28]采用EMF测定了1 833 K液相中Ni和Pd的活度。BIDWELL等[16]采用EMF法测定1 173 K FCC_A1相的混合焓以及1 073~1 473 K 时FCC_A1中Ni和Pd的活度。
1.3 Pd-Sn体系
很多研究者都对Pd-Sn体系的实验相图进行了研究[18, 21, 29−32]。其中KNIGHT等[29]、SCHUBERT等[30]和SARAH等[32]采用TA、XRD和微观分析(microscopic analysis,MA),LAURIE等[21]采用EMF,ELLNER[31]采用XRD,分别测定了Pd-Sn相图,这些工作获得的富Pd端Pd-Sn相图具有良好的一致性。ROMAKA 等[33]采用差速离心法(differential centrifugation, DC)分离出Pd5Sn7相,但NYLÉN等[18]及后来的JANDL等[19]均未在二元和三元体系相平衡实验中发现该Pd5Sn7相,且截至目前还没有Pd5Sn7相的相平衡及相关热力学信息的报道。因此,本研究暂时未考虑Pd5Sn7相。NYLÉN等[18]、KNIGHT等[29]和 SCHUBERT等[30]分别报道了富Sn端3个包晶反应的温度。其中NYLÉN等[18]的结果基于DSC升温曲线,KNIGHT 等[29]和SCHUBERT等[30]的结果基于TA降温曲线,本研究主要考虑NYLÉN等[18]的实验结果。
SCHALLER等[34]采用EMF法测定了298 K时 FCC_A1相的混合焓。GUADAGNO等[35]采用TA测得273 K时PdSn、PdSn2和PdSn4等3个化合物的形成焓。BRYANT等[36]采用溶解量热法(solution calorimetry,SCA)测定320 K时Pd3Sn、Pd2Sn、Pd3Sn2、PdSn、PdSn2、PdSn3和PdSn4等7个化合物的形成焓。CHROMIK等[37]采用EMF法测定了298 K时PdSn4相的形成焓。CICCIOLI等[38]采用克努森熔池蒸气法(Knudsen effusion cell vapor, KECV)测得298 K Pd7Sn2和Pd0.85Sn0.15的形成焓。AMORE等[39]采用CA法测定了298 K时PdSn2相的形成焓。其中,只有AMORE等[39]测定的PdSn2相形成焓远负于BRYANT等[36]的测定结果,其他的形成焓实验数据基本一致。
基于以上信息,表1列出Pd-Ag、Pd-Ni和Pd-Sn体系的相图热力学实验数据,对Pd-Ag和Pd-Ni体系重新进行热力学优化。由于CUI等[17]对Pd-Sn体系的热力学描述可描述大部分实验数据,本研究仅对该体系中PdSn2、PdSn3和PdSn4相的热力学参数进行修正。

表1 Pd-Ag、Pd-Ni和Pd-Sn体系相图的实验数据和热力学数据总结
a:Indicates whether the data are used or not used in the parameter optimization: +, used; −, not used.
2 热力学模型
2.1 纯组元热力学模型
纯组元的吉布斯自由能G()可表示为:
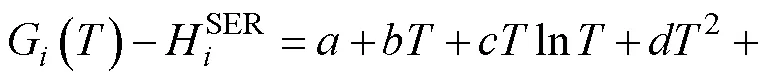
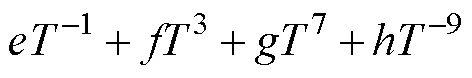
2.2 溶体相热力学模型
在Pd-X(X=Ag, Ni, Sn)体系中,采用置换溶液模型描述液相、面心立方相(FCC_A1)和体心四方相(BCT_A5),其吉布斯自由能可表示为:


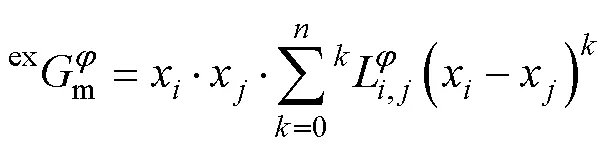

式中:和为待优化的参数。根据文献[9],式(2)中FCC_A1相吉布斯能量的磁性贡献可表示为:



2.3 亚点阵模型
Pd-Sn体系存在多个中间化合物,本工作主要对PdSn2、PdSn3及PdSn4等3个化合物的热力学参数进行修正细化,故主要对这3个化合物的热力学模型进行描述。考虑3个化合物的晶体结构信息和稳定成分范围,分别采用亚点阵模型(Pd,Sn)1(Sn)2、(Pd)0.25(Pd,Sn)0.75和(Pd)0.2(Pd,Sn)0.8来描述PdSn2、PdSn3和PdSn4。以PdSn2相为例,每摩尔PdSn2相的吉布斯自由能可表示为:
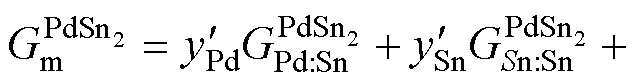

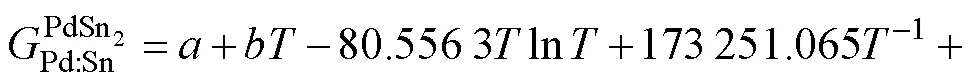
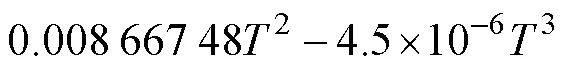
3 热力学优化结果与讨论
基于对相图数据和热力学性质的严格评估,采用Thermo-Calc软件中的PARROT模块[41]对Pd-Ag、Pd-Ni和Pd-Sn体系进行优化,获得各体系的相关热力学参数。
3.1 Pd-Ag体系
对于Pd-Ag体系,首先考虑1 673 K液相混合焓及1 510 K液相中Ag的活度对液相参数进行优化,随后根据液相线和固相线的实验数据进一步调整液相参数,并优化FCC_A1相参数,最后考虑所有可靠的实验数据,同时进行优化,得到一组自洽的描述Pd-Ag体系的热力学参数,如表2所列。
图1所示为利用基于本研究结果获得的热力学参数计算的Pd-Ag体系相图和文献报道的实验数据[13−15]与计算结果[11]。相对于CHUDNENKO[11]的计算结果,本工作获得的热力学参数可更合理地描述Pd-Ag体系实验数据[13−15]。

表2 Pd-Ag体系热力学参数总结

图1 本工作计算的Pd-Ag相图与实验数据[13−15]和CHUDNENKO[11]的计算结果比较
图2(a)和(b)所示为计算的1 673 K液相混合焓和1 510 K液相中Ag的活度,参考态为当前计算温度下的液相Ag和Pd。其中本工作计算的1 673 K液相混合焓最小值出现在(Pd)为35%时,为−5 417 J/mol- atoms,对应的实验结果为(−5 440±180) J/mol-atoms,计算结果在实验结果[10]的误差范围内。
图3(a)和(b)所示为计算的600 K FCC_A1相混合焓以及600 K和1 100 K FCC_A1相中Ag的活度,参考态为计算温度下的FCC_A1结构的Ag和Pd。从图3(a)可知,计算的600 K FCC_A1相混合焓随成分的变化曲线呈现对称性,最小值为−2 358 J/mol-atoms。与CHUDNENKO[11]的计算结果对比,本工作获得的热力学能更合理地描述实验信息。

图2 本工作计算的Ag-Pd液相热力学性质与实验数据[10, 15, 20]和CHUDNENKO[11]计算结果的比较
(a) Enthalpies of mixing at 1 673 K; (b) Activities of Ag at 1 510 K

图3 本工作计算的Ag-Pd体系FCC_A1相热力学性质与实验数据[12, 21−22]和CHUDNENKO[11]计算结果的比较
(a) Enthalpies of mixing at 600 K; (b) Activities of Ag at 600 K and 1 100 K
3.2 Pd-Ni体系
对于Pd-Ni体系,首先利用1 873 K的液相混合焓和1 173 K的FCC_A1相混合焓对液相和FCC_A1相参数进行优化,随后根据液相线和固相线的实验数据进一步调整液相参数和FCC_A1相参数,最后考虑所有可靠的实验数据同时进行优化,得到一组自洽的热力学参数,如表3所列。

表3 Pd-Ni体系热力学参数总结
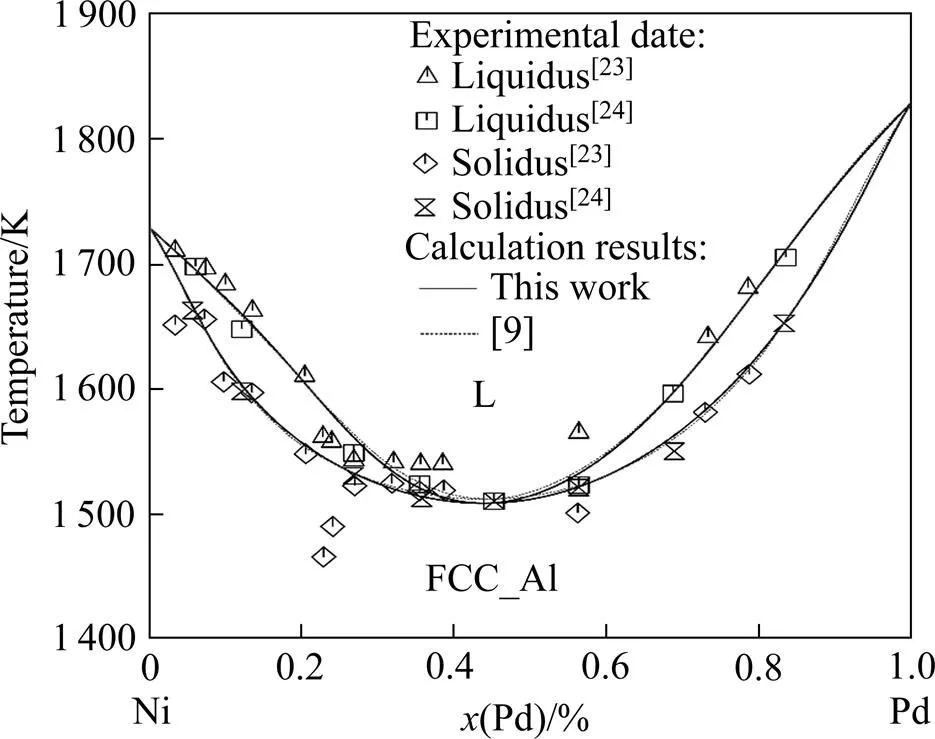
图4 本工作计算的Pd-Ni相图与实验数据[23−24]和GHOSH等[9]的计算结果比较
图4所示为Pd-Ni体系相图,可见本工作的计算结果与GHOSH等[9]的计算结果相差不大,可以合理地描述大部分实验相图信息[23−24]。根据当前计算,L-FCC_A1的一致熔融反应温度为1 508 K,对应合金的Pd摩尔分数为43.8%。图5(a)和(b)分别为计算的 1 873 K液相混合焓和1 833 K液相中Ni与Pd的活度,参考态为计算温度下的液相Ni和Pd。从图5(a)可知,计算的1 873 K液相混合焓为正,最大值为2 320 J/mol-atoms,与文献[27]的实验结果吻合。从图5(b)看出,1 833 K液相中Ni和Pd活度的计算值与文献[28]的实验值具有良好的一致性。
图6(a)和(b)所示为计算的1 173 K FCC_A1相混合焓以及1 173 K FCC_A1相中Ni和Pd的活度,参考态为1 173 K FCC_A1的Ni和Pd。文献[16]的实验数据显示1 173 K下FCC_A1相的混合焓在富Ni端为正数,最大值为639 J/mol-atoms,在富Pd端为负数,最小值为−1 385 J/mol-atoms,本工作的计算结果比GHOSH等[9]的计算结果有较大改进,与实验数据更接近,证明当前的热力学描述的可靠性。
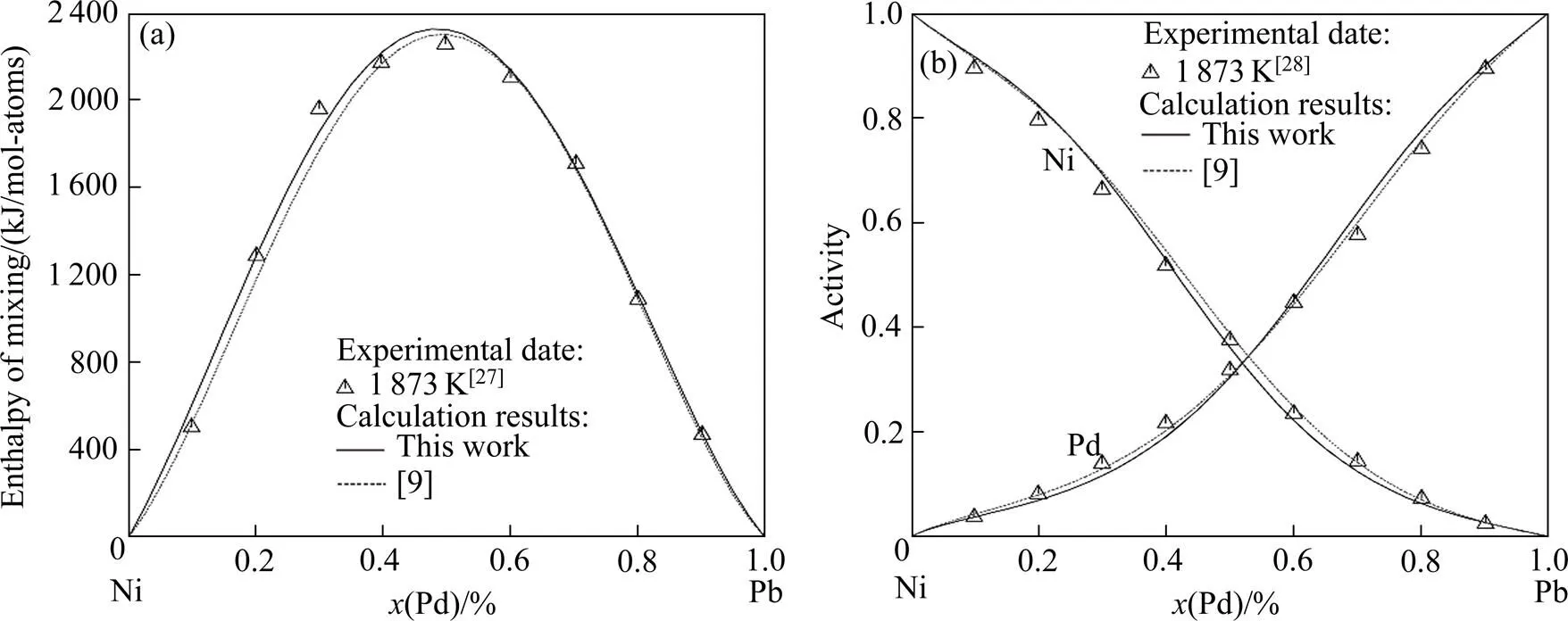
图5 本工作计算Ni-Pd的液相热力学性质与实验数据[27−28]和GHOSH等[9]计算结果的比较
(a) Enthalpies of mixing at 1873 K; (b) Activities of Ni and Pd at 1833 K

图6 本工作计算的FCC_A1相1 173 K热力学性质与实验数据[16]和GHOSH等[9]计算结果的比较
(a) Enthalpies of mixing; (b) Activities of Ni and Pd
3.3 Pd-Sn体系
本工作在CUI等[17]的参数基础上对Pd-Sn体系的3个化合物相PdSn2、PdSn3和PdSn4的热力学描述进行细化和改进,综合考虑298 K下PdSn2、PdSn3和PdSn4相的形成焓和相图信息,获得相关热力学参数,如表4所列。
表5所列为Pd-Sn体系富Sn端零变量反应的计算结果,并与实验数据进行对比。图7所示为计算的Pd-Sn体系相图。如1.3中所述,由于缺乏充分的相平衡和热力学实验数据,本工作暂未考虑Pd5Sn7相。计算出3个包晶反应PdSn+L↔PdSn2,PdSn2+L↔PdSn3,PdSn3+L↔PdSn4的温度分别为890、643和603 K,与NYLÉN等[18]的实验结果一致,高于KNIGHT和RHYS[29]以及SCHUBERT等[30]的实验数据,以及CUI等[17]的计算结果。计算的(Pd)与实验测定值相差不到1.4%。计算的PdSn2、PdSn3和PdSn4相的液相线数据与LAURIE等[21]和文献[34−39]的实验数据吻合。图8所示为Pd-Sn体系298 K形成焓的计算结果,参考态为FCC_A1的Pd和BCT_A5的Sn。从图中可看出本文的计算结果与CUI等[16]的计算结果差异主要表现在富Sn端。由于本工作中未考虑Pd5Sn7相,所以计算的298 K形成焓稍正,能合理描述实验数据[34−39]。

表4 Pd-Sn体系热力学参数总结

表5 实验[18, 29−30]和计算[17]得到的Pd-Sn体系富Sn端零变量反应以及各相的Sn含量
4 结论
1) 严格评估了Pd-Ag、Pd-Ni和Pd-Sn体系的相图数据和热力学性质数据,包括混合焓、活度、中间化合物的生成焓,基于CALPHAD方法对这3个体系进行热力学优化,各自得到一套自洽的热力学参数。

图7 本工作计算的Pd-Sn相图与实验数据[18, 21, 29−32]和CUI等[17]计算结果的比较

图8 本工作计算Pd-Sn化合物在298 K的形成焓与实验数据[34−39]和CUI等[17]的计算结果的比较
2) 相较于文献报道的计算结果,基于本工作获得的热力学参数,计算的Pd-Ag体系相图以及Pd-Ag体系和Pd-Ni体系的FCC_A1相混合焓与实验结果吻合更好,计算的Pd-Sn相图能够更准确合理地描述富Sn端的零变量反应。
[1] LI J F, AGYAKWA P A, JOHNSON C M. Kinetics of Ag3Sn growth in Ag-Sn-Ag system during transient liquid phase soldering process[J]. Acta Materialia, 2010, 58(9): 3429−3443.
[2] 余强, 刘文胜, 马运柱, 等. 等温时效对Cu/Sn-3.5Ag/ Ni(P)UBM互连焊接件界面微观组织及剪切性能的影响[J]. 粉末冶金材料科学与工程, 2017, 22(3): 390−398.
YU Qiang, LIU Wensheng, MA Yunzhu, et al. Effects of isothermal aging on interface microstructure and shear properties of Cu/Sn-3.5Ag/Ni(P) UBM interconnection solder joints[J]. Materials Science and Engineering of Powder Metallurgy, 2017, 22(3): 390−398.
[3] HE H, HUANG S, YE Y, et al. Microstructure and mechanical properties of Cu joints soldered with a Sn-based composite solder, reinforced by metal foam[J]. Journal of Alloys and Compounds, 2020, 845(2): 156240.
[4] 刘文胜, 汤娅, 马运柱, 等. 回流次数对Au80Sn20/Cu焊点显微组织及剪切性能的影响[J]. 粉末冶金材料科学与工程, 2016, 21(2): 303−310.
LIU Wensheng, TANG Ya, MA Yunzhu, et al. Effects of multiple reflows on microstructure and shear properties of Au80Sn20/Cu joint[J]. Materials Science and Engineering of Powder Metallurgy, 2016, 21(2): 303−310.
[5] GHOSH G. Interfacial microstructure and the kinetics of interfacial reaction in diffusion couples between Sn-Pb solder and Cu/Ni/Pd metallization[J]. Acta Materialia, 2000, 48(14): 3719−3738.
[6] ZHAO P, PECHT M G, KANG S, et al. Assessment of Ni/Pd/Au-Pd and Ni/Pd/Au-Ag preplated leadframe packages subject to electrochemical migration and mixed flowing gas tests [J]. IEEE Transactions on Components and Packaging Technologies, 2006, 29(4): 818−826.
[7] DU Y, LIU S H, ZHANG L J, et al. An overview on phase equilibria and thermodynamic modeling in multicomponent Al alloys: focusing on the Al-Cu-Fe-Mg-Mn-Ni-Si-Zn system[J]. Calphad, 2011, 35(3): 427−445.
[8] 刘树红, 金波, 傅太白, 等. 相图热力学数据库及其计算软件: 过去、现在和将来[J]. 中国科学: 化学, 2019, 49(7): 966−977.
LIU Shuhong, JIN Bo, FU Taibai, et al. Thermodynamic databases and software: past, present and future[J]. Science in China Chemistry: Chemistry, 2019, 49(7): 966−977.
[9] GHOSH G, KANTNER C, OLSON G B. Thermodynamic modeling of the Pd-X (X= Ag, Co, Fe, Ni) systems[J]. Journal of Phase Equilibria, 1999, 20(3): 295−308.
[10] LUEF C, PAUL A, FLANDORFER H, et al. Enthalpies of mixing of metallic systems relevant for lead-free soldering: Ag-Pd and Ag-Pd-Sn[J]. Journal of Alloys and Compounds, 2005, 391(1): 67−76.
[11] CHUDNENKO K V. Thermodynamic properties of components in the Ag-Au-Pd system[J]. Russian Journal of Inorganic Chemistry, 2020, 65(1): 94−99.
[12] FENG D, TASKINEN P. Thermodynamic properties of silver- palladium alloys determined by a solid state electrochemical method[J]. Journal of Materials Science, 2014, 49(16): 5790−5798.
[13] RUER R. Über die legierungen des palladiums mit silber[J]. Zeitschriftfur Anorganische Chemie, 1906, 51(1): 315− 319.
[14] SAVITSKIJ E M, PRAVOVEROVN L. Kurnakov phases in the palladium-silver system[J]. Russian Journal of Inorganic Chemistry, 1961, 6(3): 253−254.
[15] SOPOUŠEK J, ZEMANOVÁ A, VŘEŠŤÁL J, et al. Experimental determination of phase equilibria and reassessment of Ag-Pd system[J]. Journal of Alloys and Compounds, 2010, 504(2): 431−434.
[16] BIDWELL L R, SPEISER R. The relative thermodynamic properties of solid nickel-palladium alloys[J]. Acta Metallurgica, 1965, 13(2): 61−70.
[17] CUI S, WANG J, YOU Z, et al. Critical evaluation and thermodynamic modeling of the Pd-Sn system[J]. Intermetallics, 2020, 126(4): 106945.
[18] NYLÉN J, GARCIA F J G, MOSEL B D, et al. Structural relationships, phase stability and bonding of compounds PdSnn(= 2, 3, 4) [J]. Solid State Science, 2004, 6(1): 147−155.
[19] JANDL I, RICHTER K W. The Sn-rich corner of the system Ni-Pd-Sn: a phase diagram study[J]. Journal of Alloys and Compounds, 2017, 697(1): 310−317.
[20] VATOLIN N A, TIMOFEEV A I, DUBININ E L. Vapour pressure of liquid palladium alloys[J]. Russian Journal of Inorganic Chemistry, 1971, 45(8): 1149−1150.
[21] LAURIE G H, PRATT J N. Electronic constitution and partial thermodynamic properties of liquid tin+palladium+silver alloys [J]. Transactions of the Faraday Society, 1964, 60(2): 1391−1401.
[22] RAYCHAUDHURI, KUMAR P. Mass Spectrometric and Galvanic Cell Studies of the Thermodynamic Properties of Solid Silver-palladium Alloys[M]. Evanston, USA: Pro Quest, 1971: 111−185.
[23] HEINRICH F. Metallographische mitteilungen aus dem institut für physikalische chemie der universität göttingen. LXXXVI. Über die legierungen des palladiums mit nickel[J]. Zeitschrift fur Anorganische Chemie, 1913, 83(1): 322−327.
[24] FRAENKEL W, STERN A. Über gold-palladium- nickellegierungen[J]. Zeitschrift fur Anorganische Chemie, 1927, 166(1): 164−165.
[25] BIDWELL L R, SPEISER R. Unit-cell dimensions of Ni-Pd alloys at 25 ℃ and 900 ℃[J]. Acta Crystallographica, 1964, 17(11): 1473−1474.
[26] HULTGREN R, ZAPFFE C A. An X-ray study of the iron-palladium and nickel-palladium systems[J]. Transactions of the American Institute of Mining and Metallurgical Engineers, 1939, 133(2): 58−68.
[27] VATOLIN N A, KOZLOV Y S, PASTUKHOV E A. Structure and physicochemical properties of palladium-nickel and palladium-silicon melts[J]. Russian Metallurgy, 1977, (5): 226− 227.
[28] OISHI T, NISHI S, ONO K. Thermodynamic studies of the liquid Ni-Pd alloys by mass spectrometric and solid state EMF measurements[J]. Transactions of the Japan Institute of Metals, 1986, 27(4): 288−292.
[29] KNIGHT J R, RHYS D W. The systems palladium-indium and palladium-tin[J]. Journal of the Less Common Metals, 1959, 1(4): 292−303.
[30] SCHUBERT K, LUKAS H, MEIßNER H, et al. Zum aufbau der systeme kobalt-gallium, palladium-gallium, palladium-zinn und verwandter legierungen[J]. International Journal of Materials Research, 1959, 50(9): 534−540.
[31] ELLNER M. Zusammenhang zwischen strukturellen und thermo-dynamischen eigenschaftenbei phase nderkupfer-familie in T10-B4-systemen[J]. Journal of the Less Common Metals, 1981, 78(2): 21−32.
[32] SARAH N, ALASAFI K, SCHUBERT K. Kristallstruktur von Pd20Sn13, Pd6AgPb4und Ni13ZnGe8[J]. International Journal of Materials Research, 1981, 72(7): 517−520.
[33] ROMAKA V V, TKACHUK A, ROMAKA V A. Pd5Sn7—a novel binary stannide in Pd-Sn system[J]. Journal of Alloys and Compounds, 2010, 496(1/2): L7−L9.
[34] SCHALLER H J, BRODOWSKY H. Thermodynamic properties of Pd-Sn alloys[J]. Zeitschrift fur Metallkunde, 1978, 69(2): 87−93.
[35] GUADAGNO J R, POOL M J. Liquid palladium-tin alloys [J]. The Journal of Physical Chemistry, 1968, 72(7): 2535−2538.
[36] BRYANT A W, BUGDEN W G, PRATT J N. Calorimetric and galvanic cell studies of the thermodynamic properties of palladium-tin alloys[J]. Acta Metallurgica, 1970, 18(1): 101− 107.
[37] CHROMIK R R, COTTS E J. A Study of the kinetics and energetics of solid state reactions in Pd/Sn diffusion couples[J]. MRS Online Proceedings Library Archive, 1995, 398(2): 233− 239.
[38] CICCIOLI A, BALDUCCI G, GIGLI G, et al. Vaporization behaviour and some thermodynamic properties of the Pd-In, Pd-Pb, Pd-Sn systems[J]. Intermetallics, 2000, 8(3): 195−201.
[39] AMORE S, DELSANTE S, PARODI N, et al. Thermochemistry of Pd-In, Pd-Sn and Pd-Zn alloy systems[J]. Thermochimica Acta, 2009, 481(1/2): 1−6.
[40] DINSDALE A T. SGTE data for pure elements[J]. Calphad, 1991, 15(4): 317−425.
[41] ANDERSSON J O, HELANDER T, HÖGLUND L, et al. Thermo-Calc & DICTRA, computational tools for materials science[J]. Calphad, 2002, 26(2): 273−312.
Thermodynamic investigation on the Pd-X(X=Ag, Ni, Sn) systems of the precious metals
LIAO Lin, LIU Shuhong, DU Yong
(State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China)
Based on the critical re-assessment on the phase diagram and thermodynamic data available in literature of the Pd-X(X=Ag, Ni, Sn) systems, Gibbs energies of the liquid and FCC_A1 phases in three binary systems were described by the substitutional solution model. Three phase, PdSn2, PdSn3and PdSn4,were described by the sublattice model of (Pd,Sn)1Sn2, (Pd)0.25(Pd,Sn)0.75, and (Pd)0.2(Pd,Sn)0.8, respectively. Thermodynamic parameters for the Pd-X(X=Ag, Ni, Sn) systems were then obtained by the CALPHAD (calculation of phase diagram) approach. The presently obtained thermodynamic parameters can describe the measured phase diagram and thermodynamic properties more reasonably comparing with the previous reports, especially in the phase diagram of Pd-Ag system and enthalpies of mixing of FCC_A1 in both Pd-Ag and Pd-Ni systems, as well as the Sn-rich side of the phase diagram of the Pd-Sn system. Comprehensive comparisons between the calculated results and experimental data indicated the accuracy of the presently obtained thermodynamic parameters.
Pd-X (X=Ag, Ni, Sn); CALPHAD; phase diagrams; thermodynamic property
10.19976/j.cnki.43-1448/TF.2022003
TG113.12
A
1673-0224(2022)03-246-11
云南省贵金属基因工程重大科技项目(Grant No.202002AB08001-1)
2022−01−11;
2022−03−12
刘树红,研究员,博士。电话:13017383345;E-mail: shhliu @csu.edu.cn
(编辑 汤金芝)
