液相色谱-电感耦合等离子体质谱联用法测定鱼类干制品中甲基汞含量的测量不确定度评估
2022-07-15杨凯峰韩章华程文东孙武勇
杨凯峰 李 俊 韩章华 程文东 王 锁 孙武勇*
1.河南安必诺检测技术有限公司 河南郑州 450000
2.海南省市场监督管理局食品综合协调与抽检监测处/海南省食品药品检验所五指山分所 海南海口 570100
3.郑州轻工业大学 河南郑州 450000
汞是一种剧毒元素,具有元素汞、无机汞、有机汞多种形态,而有机汞中甲基汞危害最为严重[1]。在日常环境中,通过各种生物或非生物作用,水环境中的无机汞可能转化成甲基汞,并且在受污染的环境中,由于生物富集作用,鱼类体内可能积累大量的甲基汞[2],可以通过食物链等方式传递,从而危害人体健康。因此对水产制品的甲基汞含量检测对保障食品安全就显得尤为重要。
GB 5009.17-2021《食品安全国家标准 食品中总汞及有机汞的测定》[3],首次规定适用范围包括水产动物及其制品甲基汞的测定,并新增LC-ICP-MS法。该法前处理过程简单、干扰小、线性范围广、检出限低,可以很好地对试样中的汞进行形态分析和含量检测[4]。采用该法测定鱼类干制品中的甲基汞含量,并根据JJF1059.1-2012《测量不确定度评定与表示》[5]和CNAS-GL006-2019《化学分析中不确定度的评估指南》[6]提供的方法,通过对测量结果产生影响的主要因素进行分析,评估测量不确定度。
1 材料与方法
1.1 仪器与试剂
实验中所用试剂一般为优级纯(另有说明除外),水为GB/T6682一级水;
标准溶液(甲基汞),盐酸,氨水,甲醇(色谱纯),L-半胱氨酸,乙酸铵(分析纯);
高效液相色谱仪(Ultimate 3000赛默飞)与电感耦合等离子体质谱仪(Icap qc赛默飞)联用;
电子天平(AUX120),电子天平(AUW220D),均为岛津;
高速冷冻离心机(3K15),德国Sigma;
超声波清洗器(SB-25-12DTD),宁波新芝。
1.2 试验方法
根据GB 5009.17—2021《食品安全国家标准 食品中总汞及有机汞的测定》[3]规定的LC-ICP-MS开展实验。
1.2.1 溶液配制
氨水溶液(1+1):将氨水(50mL)加入水(50mL)中混匀。
盐酸溶液(5mol/L):盐酸(208mL)用水稀释至500mL。
L-半胱氨酸溶液(10g/L):将L-半胱氨酸(0.1g)溶于水(10mL)中混匀,现用现配。
甲醇水溶液(1+1):将甲醇(100mL)与水(100mL)混匀。
流动相(3%甲醇+0.04mol/L乙酸铵+1g/L L-半胱氨酸):L-半胱氨酸(0.5g)与乙酸铵(1.6g)溶于水(100mL)中,加甲醇(15mL),然后用水稀释至500mL。过0.45μm有机滤膜,超声脱气30min,现用现配。
1.2.2 样品前处理
购买来自市场售卖的鱼类干制品样品粉碎后,充分搅拌混匀,称取样品0.5g至塑料离心管(15mL)中,加入5mol/L盐酸溶液(10mL)。室温下超声水浴提取60min,期间振摇数次。4℃,8 000r/min离心15min。准确移取上清液(2.0mL)至容量瓶(5mL)中,逐滴加入氨水溶液(1+1),至样液pH值3~7。加入10g/L L-半胱氨酸溶液(0.1mL),用水定容。过0.45μm有机滤膜,待测。空白试验同上。
1.2.3 仪器条件
(1)液相色谱条件。
色谱柱:C18分析柱(150mm×4.6mm,5μm)。
流动相:3%甲醇+0.04mol/L乙酸铵+1g/L L-半胱氨酸。
流速:1.0mL/min。
进样量:50μL。
(2)电感耦合等离子体质谱仪条件。
射频功率:1 500W。
采样深度:8mm。
雾化室温度:2℃。
载气(氩气)流量:0.85L/min。
补偿气(氩气)流量:0.15L/min。
积分时间:0.5s。
检测质荷比(m/z):202。
1.3 测定结果的数学模型
按公式(1)计算试样中甲基汞的含量(以Hg计)。
(1)
式中:
X—试样中甲基汞的含量(以Hg计),mg/kg;
c—经标准曲线得到的测定液中甲基汞的浓度,μg/L;
c0—经标准曲线得到的空白溶液中甲基汞的浓度,μg/L;
v—加入提取试剂的体积,mL;
f—稀释因子,2.5;
m—试样称样量,g;
1 000—换算系数。
2 结果与分析
2.1 引入不确定度的来源
通过研究食品中甲基汞检测的实验过程和评估测量不确定度的方法,分析对测定结果产生影响的原因,以此确定不确定度分量来源。测定结果主要受样品测量重复性、样品的称量过程、样品前处理过程、标准溶液及标准曲线拟合等方面的影响。
2.2 不确定度分量的评估
2.2.1 评估重复测量引入的不确定度urel(rep)
样品中甲基汞的测定结果见表1。
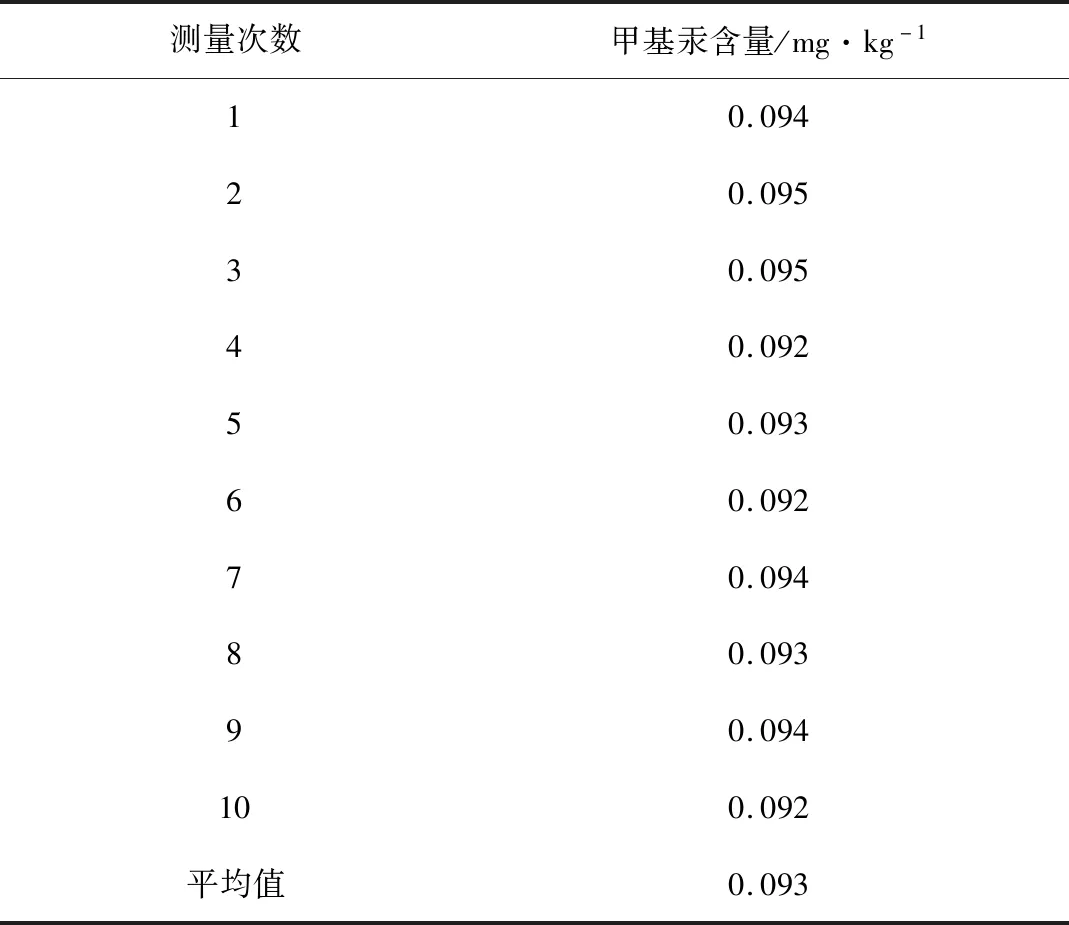
表1 样品中甲基汞的测定结果Table 1 Measurement results of methylmercuryin samples
检测实验室用于食品中甲基汞检测新方法开验的样品之一鱼类干制品经过反复测定,确认含量稳定,称取过程应保持稳定,尽量降低结果偏差。准确称取混匀后鱼类干制品样品10份,分别测定其中的甲基汞含量。
测量重复性以通过贝塞尔公式(2)计算得标准偏差表示:
(2)
其中:
xi—第i次的测量值;
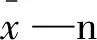
n—独立重复测量次数;
计算样品中,甲基汞重复性实验引入的标准不确定度:
相对标准不确定度:
2.2.2 评估样品称量引入的不确定度urel(m)
样品采购于周口某市场,检测备样保存期满后,实验室新方法开验选用,粉碎充分、均匀,此处不考虑其引入的不确定度。在此过程中对样品称量结果影响较大的是电子天平的使用。通过对使用的万分之一电子天平的校准证书进行查询,结果显示:U=0.0009g,k=2。
根据检测方法操作,称量样品0.500g,引入的标准不确定度如下:
u(m)=U/k=0.00045g
相对标准不确定度:
urel(m)=u(m)/m=0.0009
2.2.3 评估样品前处理过程引入的不确定度urel(v)
样品前处理过程中,因移取提取液及定容等操作需要用到10mL、1mL移液器和5mL容量瓶。
实验温度在(20±5)℃时,ΔT=5℃,此时水的膨胀系数为α=0.00021/℃。
温度引入的标准不确定度计算公式(3):
(3)
移液器(10mL、1mL)和容量瓶(5mL)的使用而引入的不确定度见表2。
合成计算得样品前处理过程中引入的不确定度评定结果:
2.2.4 评估标准溶液引入的不确定度urel(c)
标准溶液的使用要考虑其纯度,储备液的配制过程,中间工作液的配制过程以及标准曲线系列溶液的配制过程等方面的影响,相关不确定度的评估从这几方面入手。
(1)评估标准溶液纯度引入的不确定度urel(c1)。
查询标准溶液(甲基汞)证书((63.5±2.4)μg/g,k=2),折算单体纯品率93%,标准不确定度为:
u(c1)=2.4/2=1.2μg/g。
相对标准不确定度:
urel(c1)=1.2/63.5=0.019
(2)评估储备液配制引入的不确定度urel(c2)。
①评估称量引入的不确定度urel(c2-1)。
通过查询此过程所用的十万分之一电子天平的校准证书可得,校准结果显示:载荷值0.1g时,U=0.00006g,k=2。准确称量标准物质0.0847g,计算得标准不确定度:
u(c2-1)=U/k=0.00003g
相对标准不确定度:
urel(c2-1)=u(c2-1)/m=0.0004
②评估定容引入的不确定度urel(c2-2)。
定容用容量瓶(5mL)。温度引入的标准不确定度计算方法同上。
使用5mL容量瓶引入的不确定度评定结果见表3。

表3 使用5mL容量瓶引入的不确定度评定结果Table 3 Uncertainty Evaluation Results Introduced by Using a 5 mLvolumetric Flask
合成计算得标准溶液储备液配制引入的不确定度评定结果:
(3)评估中间工作液配制引入的不确定度urel(c3)。
该过程引入的不确定度主要受使用移液器(1mL)和容量瓶(10mL)的影响。温度引入的标准不确定度计算方法同上。
使用移液器(1mL)和容量瓶(10mL)引入的不确定度评定结果见表4。

表4 标准溶液中间工作液配制引入的不确定度评定结果Table 4 Evaluation Results of Uncertainty Introduced in the Preparation of Standard Solution Intermediate Working Solution
合成计算得标准溶液中间工作液配制所引入的不确定度评定结果:
(4)评估标准曲线系列溶液配制引入的不确定度urel(c4)。
该过程引入的不确定度主要是需要使用容量瓶(1mL),移液器(1mL,0.2mL)的影响,配制浓度分别为0.5、1、5、10、20、50ng/mL,用0.2mL移液器分别移取0.005、0.01、0.05、0.1、0.2mL,用1mL移液器移取0.5mL。温度引入的标准不确定度计算方法同上。
容量瓶(1mL)共使用6次,引入的不确定度见表5。
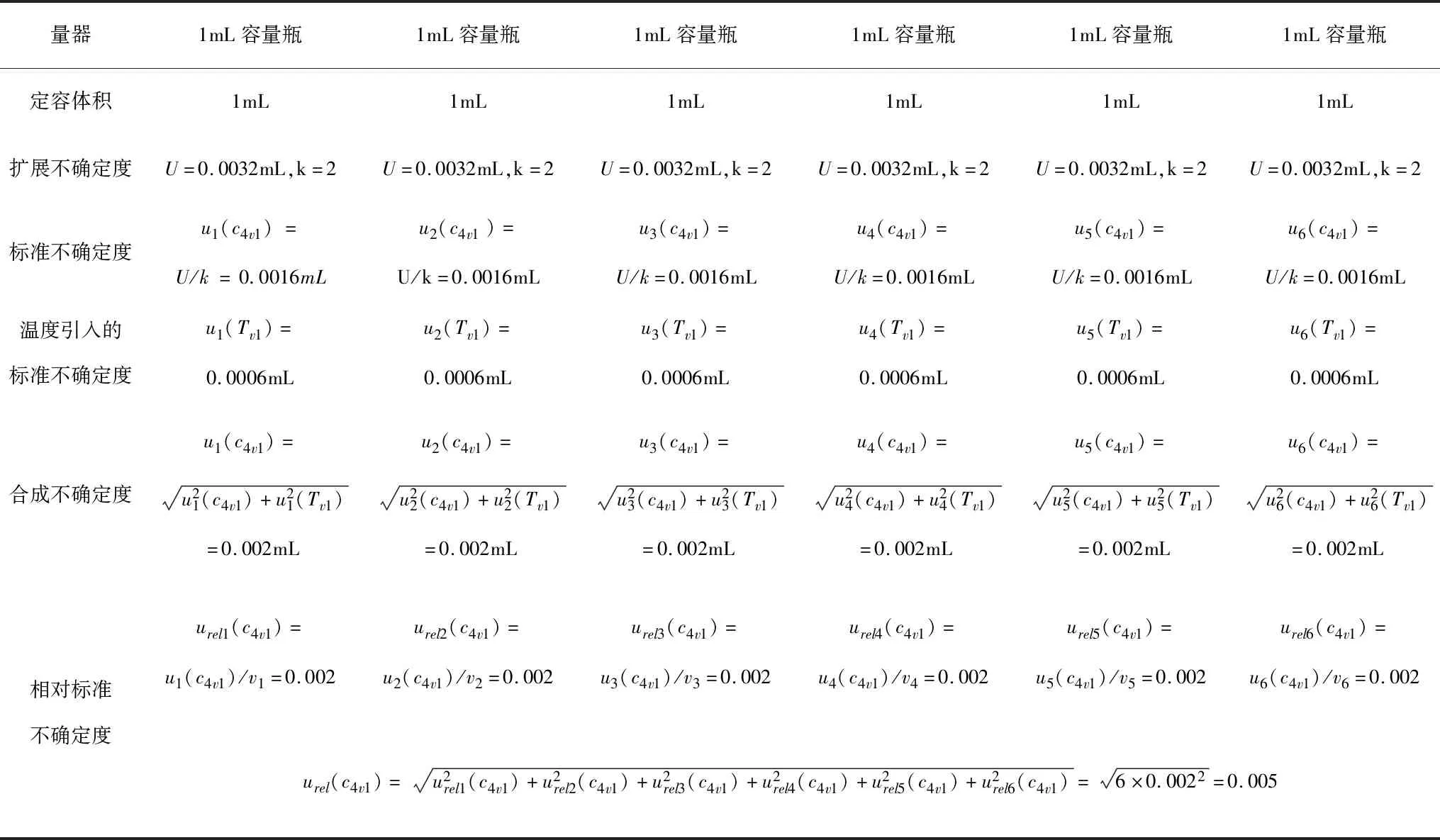
表5 使用1mL容量瓶引入不确定度评定结果Table 5 Using a 1mL volumetric flask to introduce uncertainty evaluation results
0.5、1、5、10、20、50ng/mL系列标准溶液配制引入不确定度评定结果见表6。

表6 标准曲线系列溶液各点引入不确定度评定结果Table 6 Evaluation results of introducing uncertainty at each point of standard curve series solution

续表6
合成计算得标准曲线系列溶液的配制引入不确定度评定结果:
最后合成计算得引入的不确定度评定结果:
urel(c)=
2.2.5 评估标准曲线拟合引入的不确定度urel(q)
根据所得的甲基汞标准曲线Y=aX+b,对各浓度系列标准溶液进行重复测定,标准曲线系列溶液测定结果见表7。
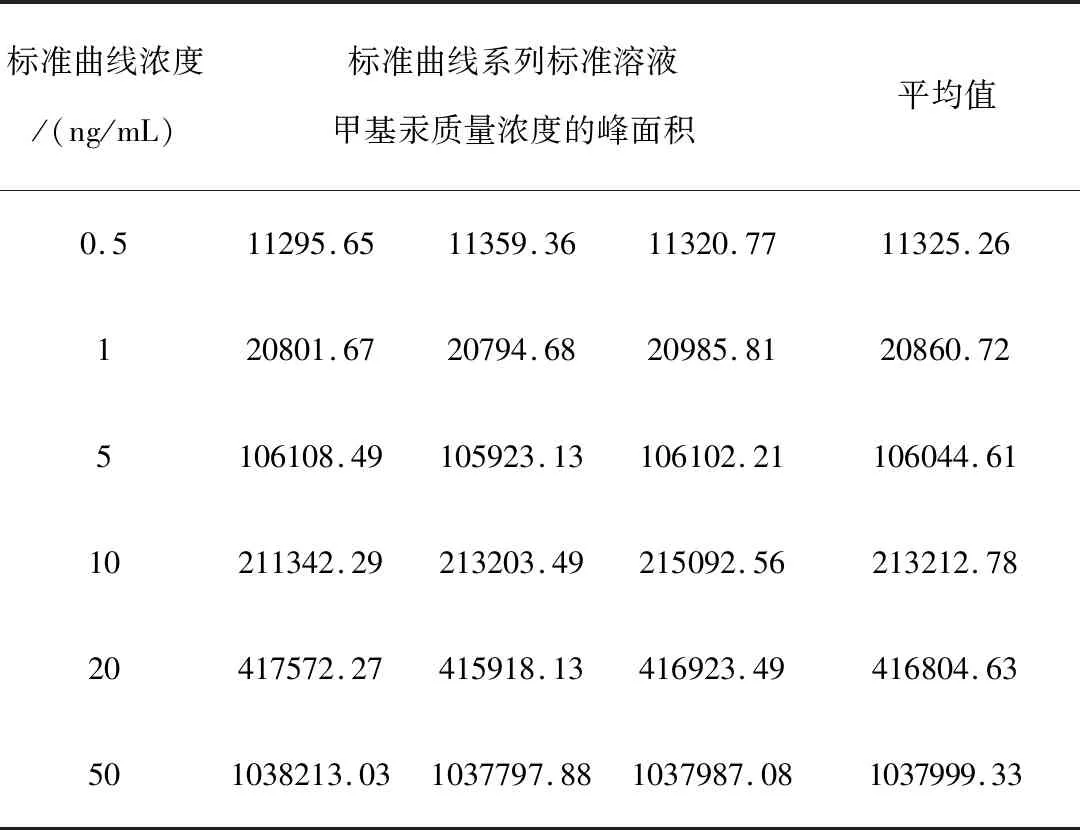
表7 标准曲线系列溶液浓度测定结果Table 7 Standard curve series solution concentration determination result
标准曲线拟合所引入的不确定度可以通过公式(4)和公式(5)进行计算[7]。
标准曲线标准差计算公式为:
(4)
(5)
式中:
Ci—实际绘制拟合直线各点标准溶液浓度,ng/mL;
X—标准曲线系列标准溶液浓度,ng/mL;
S—标准曲线标准偏差;
Ai—标准曲线系列标准溶液质量浓度的峰面积;
a—斜率20 731.0560;
b—截距2 168.4969;
n—校准溶液测试总次数18;
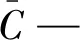
P—样品测试次数10;
C0—样品实测平均浓度。
经计算得出:

C0=1.8700ng/mL
S=2075.7889
标准曲线拟合引入的标准不确定度:
u(q)=0.049ng/mL
标准曲线拟合引入的不确定度评定结果:
2.3 合成标准不确定度
各分量相对标准不确定度评定结果见表8。

表8 各分量相对标准不确定度评定结果Table 8 Evaluation results of relative standard uncertainty of each component
合成相对标准不确定度:
urel(X)=
鱼类干制品中甲基汞含量测定的平均值为0.093mg/kg。
合成标准不确定度:
u(X)=urel(X)×0.093mg/kg=0.007mg/kg
2.4 扩展不确定度及不确定度结果报告
置信区间为95%的情况下,取包含因子k=2,扩展不确定度评定结果为:
U(X)=k×u(X)=0.014mg/kg
鱼类干制品中甲基汞含量结果:
(0.093±0.014)mg/kg,k=2
3 结论
采用GB 5009.17—2021《食品安全国家标准 食品中总汞及有机汞的测定》中第二篇第二法,液相色谱-电感耦合等离子体质谱联用法,测定鱼类干制品中甲基汞含量,并进行测量不确定度评定。从不确定度评定过程来看,考虑到该样品是用于新方法开验样品之一,实验人员严格规范控制实验过程,操作谨慎,同时样品中甲基汞含量较低,测量过程中对结果影响较大的因素主要是标准溶液纯度及配制、曲线拟合,但作为日常检测中测量不确定度主要来源的测量重复性同样重要,日常检测工作的开展要应重点关注这些方面。由此可知实验设备的精度、操作的规范性,对测量不确定度有较大影响,实验过程中注意对各因素进行有效控制可以提高检测准确性。
