内镜下双极电止血导管治疗放射性直肠炎出血的疗效观察
2022-07-13胡柯峰李琪儿朱春霞李桑金燕平叶国良
胡柯峰,李琪儿,朱春霞,李桑,金燕平,叶国良
放射性直肠炎(RP)是指盆腔恶性肿瘤(包括宫颈癌、子宫内膜癌、卵巢癌、前列腺癌或膀胱癌等)患者因接受放射治疗而引起的直肠损伤。尽管放射科学取得了长足的进步,但因上述疾病接受放疗后仍有高达30%的患者遭受RP[1]。临床分为急性放射性直肠炎(ARP)和慢性放射性直肠炎(CRP)[2],CRP 症状迁延,可表现为反复腹痛、腹泻、里急后重,或伴有便血、狭窄、肠瘘等,严重影响患者生活质量。目前,已有包括内科药物、内镜及外科手术等多种方法处理RP。大多数ARP 病例对药物或停止放疗有效,而上述措施及对症支持治疗对于缓解CRP 症状,尤其是直肠出血,效果并不尽如人意。因而内镜治疗已成为处理CRP 伴出血患者的常用方法,目前最常用的内镜治疗方法是氩离子凝固术(APC),临床成功率高,但报道严重并发症发生率为4%[1],包括结肠瘘、穿孔、爆炸或狭窄。也有学者应用热探头、射频消融术等治疗RP 出血,取得一定效果。本文应用内镜下双极电止血导管治疗RP 出血,取得较好效果,现报道如下。
1 资料与方法
1.1 一般资料 收集2018 年1 月至2021 年12 月宁波大学医学院附属医院根据临床表现、肠镜及病理等检查,确诊为RP 出血的患者14 例,排除感染性肠炎、溃疡性直肠炎及直肠肿瘤等患者。其中男2 例,女12 例;年龄47 ~82 岁,平均62.2 岁。原发疾病为膀胱癌1 例,结肠癌1 例,宫颈癌9 例,子宫癌3 例。症状出现时间距放疗为7 ~26 个月,平均12.3 个月。患者均有下消化道出血表现,以反复便血为主,均合并贫血,所有患者内镜治疗前曾有药物治疗史。5例患者内镜治疗前曾接受输血治疗,3例患者结肠镜检查发现存在RP 合并直肠溃疡。所有患者签署知情同意书,本研究通过本院伦理委员会审查。
1.2 方法
1.2.1 术前准备 完善术前检查,如心电图、胸片、血常规、凝血功能、肝肾功能、电解质、血型、输血前检查等;常规肠道准备。器械:PCF-Q260AZI、CF-H290I 电子肠镜(Olympus),CO2送气泵及送水泵(Olympus),200D电外科工作站(ERBE),D-201-13404、D-201-14304 透明帽(Olympus);InjectionGoldProbe双极电止血导管M00560160(Boston Scientific)。
1.2.2 操作方法(1)内镜进镜完成全结肠检查,观察病灶位置、出血情况,是否合并溃疡、瘘、狭窄等,若有活动性出血,先予0.9%氯化钠溶液冲洗、吸引,去除肠腔内积血,暴露病灶;(2)经钳道插入双极电止血导管,直视下将导管前端部的纯金螺旋电极直接接触并紧贴病灶部位,施加一定压力,模式设置:BIPOLAR SOFT(双极柔和电凝),功率设置:15 W,脉冲持续时间1 ~5 s,可重复多次进行;(3)治疗终点:肉眼可见病灶全部消除,出血停止,出现白色凝固物。
1.2.3 术后处理与随访 术后禁食24h,常规补液。观察患者腹痛腹胀、体温、有无消化道出血等情况。术后24 h 开始流质饮食。术后监测大便隐血及血红蛋白水平。术后第1、3、6 及12 个月复查肠镜了解病灶残留及复发情况。若随访过程中再次出现消化道出血及血红蛋白下降,立即复查肠镜并再次内镜下止血治疗。
2 结果
2.1 手术情况 14 例均成功接受内镜下止血术,手术时间8 ~32 min,平均19.3 min。9 例患者仅行1 次内镜下治疗,4 例行2 次内镜下治疗,1 例行4 次内镜下治疗,平均1.5 次。均未出现与内镜治疗相关的并发症。
2.2 随访结果 术后随访3 ~45 个月,平均20.1 个月,所有患者术后出血控制,血红蛋白稳定,复查肠镜提示病灶消退满意。典型病例见图1。
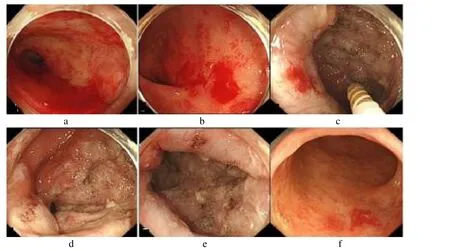
图1 典型病例
3 讨论
RP 是盆腔恶性肿瘤患者接受放射治疗后面临的一大困扰。由于直肠在盆腔中位置相对固定,导致其更易发生放射性损伤。直肠出血可发生于1%~5%的RP 患者[3],是其就诊的首要原因。本文中14 例患者症状出现在放疗后7 ~26 个月,平均12.3 个月,均以反复便血为主诉。根据上述临床表现及盆腔放疗史,临床应怀疑诊断为RP,结肠镜检查可进一步证实。CRP 的内镜下表现有时会干扰术者判断的准确性,因此在诊断时,需要进行详细观察,并排除炎症性肠病、缺血性肠病、感染性肠炎或恶性肿瘤等,尤其当CRP 合并感染性肠炎如艰难梭菌感染时,鉴别诊断困难,导致延误诊断或甚至误诊。由于直肠活检可能引发溃疡、甚至瘘的发生,因此应尽量避免,活检只有在怀疑为恶性肿瘤或有重要治疗价值的情况下才考虑[4]。
由于缺乏对RP 各种治疗方法的综合评价研究,现有的治疗策略大多是从临床试验、病例报告和系统化的经验中提炼出来的[5]。CRP 的治疗措施包括药物、内镜和外科手术。直肠内灌注福尔马林临床报道较多,但其广泛应用的一个主要问题是严重的治疗相关并发症,如直肠肛管狭窄、大便失禁[6]和直肠阴道瘘[7]等,因此需谨慎使用。
目前内镜治疗方法以APC 最为常用。APC 技术成熟,效果满意,临床成功率达87%,但存在4%的严重并发症发生率,包括结肠瘘、穿孔、爆炸或狭窄[1]。与双极电凝相比,前者为非接触性点状热凝固,穿透深度仅2 ~3 mm,而后者与病灶接触面积大、热凝固深度可能达到黏膜下层,可直接凝固2 mm 以下的小血管,因而大大提高工作效率及疗效。也有学者应用热探头和射频消融术等治疗CRP 出血,发现这些方法安全、有效,具有一定前景。荟萃分析显示射频消融术的总体临床成功率高达99%[8],不良反应轻微,其工作特征之一为消融深度统一,约0.5 mm,只涉及到黏膜的表层,与双极电凝相比,穿透深度较浅。但射频消融术价格高昂,需要特殊器械,限制了其应用与推广。
本研究采用的双极电止血导管属于接触性热凝固治疗范畴。与单极装置不同,双极电凝工作时,电流被限制在探头头端电极之间的组织中,不需要返回电极板。探头直径分为7 F 和10 F 两种,本研究所用双极电止血导管直径为7 F,普通内镜的工作钳道即可通过。而探头尺寸、功率、接触压力、持续时间和次数等参数因病变的不同而异[9]。本研究采用的模式设置为BIPOLAR SOFT(双极柔和电凝),功率设置为15 W,脉冲持续时间1 ~5 s。双极电止血导管治疗CRP出血操作简单、安全,疗效确切,本研究中所有患者随访期内未再出血,血红蛋白维持稳定,复查肠镜发现病灶消退满意。笔者操作体会如下:(1)使用方便,患者身上无需贴电极,探头直接通过内镜钳道到达病灶;(2)操作过程中导管前端部的电极直接接触并紧贴病灶部位,需要施加一定压力,以增加接触面积并使电凝作用深度足够,从而提高治疗效果;(3)黏膜面肉眼可见的扩张毛细血管清除后常常会显露出一根稍粗的血管渗血,从组织学上推测,该血管可能为扩张、扭曲的黏膜下层小静脉,对此类血管予双极电止血导管压迫电凝,使病变主干血管热凝固,可提高治疗效果,减少复发;(4)导管前端高密度陶瓷圆柱体可防止组织因电凝形成焦痂而引起粘连,但多次电凝后导管表面会附着坏死组织,影响电凝效果,需及时清除;(5)探头为黄金螺旋电极设计,低温止血,避免灼伤,操作安全,避免消化道穿孔发生。上述体会与我们报道的用于治疗胃窦毛细血管扩张症[10]类似。
本研究对14 例CRP 出血患者实施双极电止血导管止血,均取得满意疗效,展现了双极电止血导管止血的独特优势,具有一定的临床应用前景。尽管如此,仍需要高质量、随机的前瞻性研究来证实其短期和长期的有效性和安全性。
