参白药效部位纳米混悬剂的剂型工艺优化及其升白作用的研究
2022-07-09简凤娇郭敏吴沛杭李孝栋
简凤娇,郭敏,吴沛杭,李孝栋
(福建中医药大学药学院,福建 福州 350122)
据世界卫生组织统计[1],截至2020年底,全球恶性肿瘤发病例已达1 929万,死亡人数高达995万人。在肿瘤化疗过程中,最常见的毒副作用是骨髓抑制,突出表现为白细胞减少症[2-3]。白细胞作为免疫系统的重要组成部分,一旦持续减少,将使机体处于易感染状态,极大降低肿瘤化疗的治疗效果和预后,严重者可引起死亡[4]。临床上,西医主要通过口服或注射升白药物、成分输血以及胚胎干细胞移植等方法治疗白细胞减少症,虽然短期疗效显著,但常常伴有不良反应且治疗费用高[5-6]。中药基于中医辨证论治的理念,已广泛应用于化疗患者,具有多靶点、长效、毒副作用小的优势,如八珍汤、参苓白术散等[7-8]。但中药成分复杂,存在使用周期长、见效慢的缺点,开发以有效部位为原料的中药制剂可提高中药的治疗效果[9]。
参白方出自谭支绍教授主编的《药用寄生》,主要由黄芪、银耳、党参、绞股蓝等组成,用于治疗癌症放化疗后的白细胞减少症[10]。文献[11-14]显示黄芪多糖、银耳多糖、党参多糖以及绞股蓝皂苷对白细胞减少症均具有良好的治疗效果,故以总多糖与总皂苷为参白方的主要有效部位。多糖为大分子物质,难以透过细胞膜的磷脂双分子层;总皂苷以绞股蓝皂苷为主,溶于水后易析出[15-16]。纳米混悬剂具有提高药物溶出度与促进吸收等优点[17-18],多糖具有一定的黏性,能降低药物粒子的沉降速度,减少稳定剂的使用,克服纳米混悬剂物理稳定性差的问题。本文以参白方提取的总多糖与总皂苷混合物为药物原料,采用高压均质技术,开展参白有效部位纳米混悬剂(Shenbai Effective Parts Nanouspension,SBEP-NS)剂型工艺的研究,对优化制得的纳米混悬剂进行表征和升白药效的研究,为参白方纳米新剂型的研发奠定基础。
1 材料
1.1 动物 清洁级小鼠[合格证号:SCXK(闽)2016-0002],体质量(20±2)g,雄性,由福建医科大学实验动物中心提供。小鼠于动物笼中饲养,环境温度为(20±2)℃,湿度为(45%±3%),可自由饮食。
1.2 试药 大豆卵磷脂(上海源叶生物科技有限公司,批号:20211011);十二烷基硫酸钠(西陇化工股份有限公司,批号:1506012);吐温80(国药集团化学试剂有限公司,批号:20171207);泊洛沙姆188(北京凤礼精求商贸有限责任公司,批号:WPCE634B);注射用环磷酰胺(Baxter Oncology GmbH,批号:0E384A);生理盐水(福州海王福药制药有限公司,批号:国药准字H35020289);地榆生白片(成都地奥集团天府药业股份有限公司,批号:国药准字Z20026497);血细胞分析用溶血剂(天津海迈医用科技有限公司,批号:12006132);血细胞分析用稀释液(天津海迈医用科技有限公司,批号:12109021);总多糖粗提物(含量47%)与总皂苷粗提物(含量30%)由本课题组制备。
1.3 仪器 AH-100D高压均质机(加拿大ATS公司);pocH-100iV Diff全自动血液分析仪(日本SYSMEX株式会社);Nicomp 380ZLS激光粒度电位检测仪(美国PSS粒度仪公司);JJ-2组织捣碎匀浆机(常州金坛良友仪器有限公司);H-7650透射电子显微镜(日本Hitachi公司)。
2 方法
2.1 总多糖的提取 称取银耳180 g、黄芪和党参各450 g,浸渍30 min,加入25倍量的清水煎煮3次,每次煎煮4 h,过滤,合并滤液,浓缩至含总生药材1 g·mL-1。浓缩液中加入4倍量的95%乙醇,静置过夜,抽滤,将滤饼干燥后即得总多糖。
2.2 总皂苷的提取 称取绞股蓝675 g,合并“2.1”项下总多糖提取的药渣,加入8倍量80%乙醇浸泡30 min,回流提取2次,每次2 h,过滤,合并两次滤液,浓缩至含总生药材1 g·mL-1。将浓缩液用3倍量水饱和正丁醇溶液萃取3次,合并水饱和正丁醇层,回收正丁醇,干燥即得总皂苷。
2.3 SBEP-NS的制备 称取总多糖和总皂苷粗提物各2.5 g,加入50 mL溶有适量稳定剂的蒸馏水溶液中,组织匀浆机1 000 r·min-1下分散3 min,得粗混悬液;粗混悬液在高压均质压力下,循环均质,得到SBEP-NS。
2.4 单因素试验
2.4.1 稳定剂筛选 固定药物与稳定剂的比例为1∶1,稳定剂分别为大豆卵磷脂、吐温80、十二烷基硫酸钠(SDS)、泊洛沙姆188,按“2.3”项下方法制备粗混悬液。各粗混悬液在800 bar压力下,均质15次,制得纳米混悬剂。测定上述各纳米混悬剂的粒径与PDI,静置后观察其沉降与聚集现象。
2.4.2 稳定剂的用量 使药物与大豆卵磷脂的质量比为2∶1、1∶1、1∶2,按“2.3”项下方法制备粗混悬液,粗混悬液于800 bar压力下,均质循环20次,制得SBEP-NS并测定粒径,考察大豆卵磷脂的用量对SBEP-NS粒径的影响。
2.4.3 均质压力 固定药物与大豆卵磷脂的质量比为1∶1,按“2.3”项下方法制备粗混悬液,粗混悬液分别在200、400、600、800、1 000 bar压力下,均质循环20次,得SBEP-NS并测定粒径。
2.4.4 均质次数 固定药物与大豆卵磷脂的质量比为1∶1,按“2.3”项下方法制备粗混悬液,粗混悬液在800 bar均质压力下,分别均质2、4、6、8、10、12、14、16、18、20次,得SBEP-NS并测定粒径。
2.5 正交试验
2.5.1 正交试验设计 在单因素试验的基础上,以药物与大豆卵磷脂的质量比(A)、均质压力(B)、均质次数(C)为主要影响因素,各因素水平见表1。根据正交试验表,按“2.3”项下方法分别制备SBEP-NS,以粒径(X)和PDI(Y)为评价指标优化SBEP-NS的制备工艺。
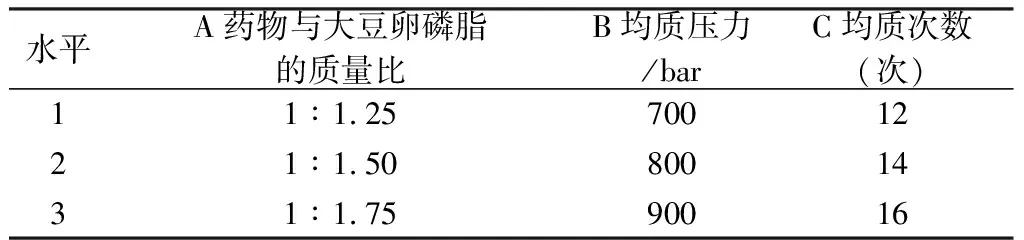
表1 正交因素水平
2.5.2 优化结果的验证 按优选工艺平行制备3批SBEP-NS,并测定其粒径与PDI,验证正交优化结果。
2.6 正交样品的沉降考察与纳米混悬剂的表征
2.6.1 沉降的考察 取正交试验的9批SBEF-NPS,在室温下放置,分别于第1、2、4个月观察各正交样品的沉降状态。
2.6.2 形态观察 取优选工艺制备的SBEP-NS稀释至6.25 mg·mL-1,取20 μL滴至铜网上,晾干,滴加4%磷钨酸溶液染色,静置5 min后用滤纸从铜网边缘吸干多余液体,置于透射电镜下观察形态。
2.6.3 粒径、多分散指数及Zeta电位测定 按优选工艺平行制备3批SBEP-NS,分别取适量稀释4倍后置于粒径分析仪上,分别测定粒径、PDI和Zeta电位。
2.7 升白药效实验
2.7.1 分组造模与给药 健康ICR小鼠60只,随机分为空白组、模型组、地榆升白片0.12 g·kg-1阳性对照组[19]、SBEP-NS 1、2、4 g·kg-1低中高3个剂量组,每组10只。饲养3 d后,除空白组外,其余各组小鼠均腹腔注射环磷酰胺(CTX)80 mg·kg-1,连续3 d,复制化疗所致的白细胞减少模型[20-21]。造模完成后,各药物组灌胃给予相应剂量的药物混悬液,空白及模型组给予等容积的生理盐水,20 mL·kg-1,每天1次,连续15 d。
2.7.2 外周血白细胞(WBC)计数 造模后第7、15天,给药30 min后,分别取各组小鼠眼眶血,全血细胞自动分析仪上检测白细胞数量。
2.7.3 免疫器官指数 造模后第15天,称量小鼠体质量(g),脱颈处死后,取小鼠胸腺与脾脏,称量重量(mg)并计算免疫器官指数(免疫器官指数=免疫器官质量/小鼠体质量)。
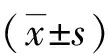
3 结果
3.1 单因素试验结果
3.1.1 稳定剂的筛选 加入等量的稳定剂,在相同的制备条件下,加入大豆卵磷脂制得的SBEP-NS粒径最小且稳定,结果见表2。结果表明,大豆卵磷脂最适合作为稳定剂。

表2 稳定剂的筛选
3.1.2 稳定剂用量的筛选 在同一条件下,由图1可知,随着大豆卵磷脂用量的增加,SBEP-NS粒径逐渐减小,当药物与大豆卵磷脂质量比为1∶2时,粒径最小。
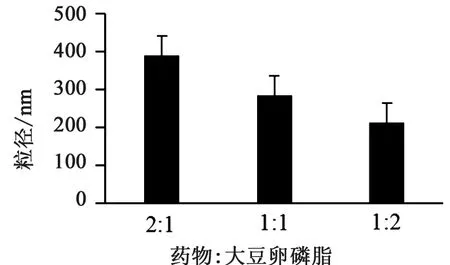
图1 稳定剂比例对粒径的影响
3.1.3 均质压力对粒径的影响 由图2可知,随着压力的增加,粒径逐渐减小,当均质压力为800 bar时,粒径最小。故选择700、800、900 bar作为正交试验因素水平。
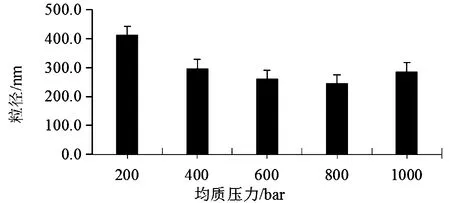
图2 均质压力对粒径的影响
3.1.4 均质次数对粒径的影响 在相同的制备条件下,考察不同均质压力对SBEP-NS粒径的影响,由图3可知,均质14次时,SBEP-NS的粒径最小。
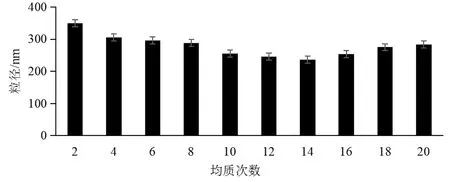
图3 均质次数对粒径的影响
3.2 正交试验与验证 按照正交试验设计进行SBEP-NS的制备工艺优化,由表3~4可知,A因素(药物与大豆卵磷脂的质量比)、B因素(均质压力)、C因素(均质次数)对SBEP-NS的粒径影响由大到小为C>A>B,选取的最佳工艺为A2B2C2,即药物与大豆卵磷脂的质量比为1∶1.50,在800 bar压力下,均质14次。正交优选工艺验证结果见表5,结果表明:优选工艺制得的SBEP-NS粒径小且分布均匀,由此可判断,优选的工艺可行、稳定。
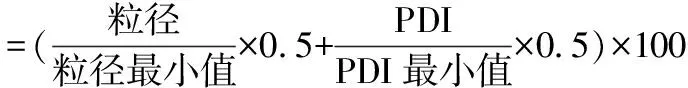
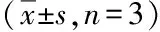
表3 正交试验设计与结果
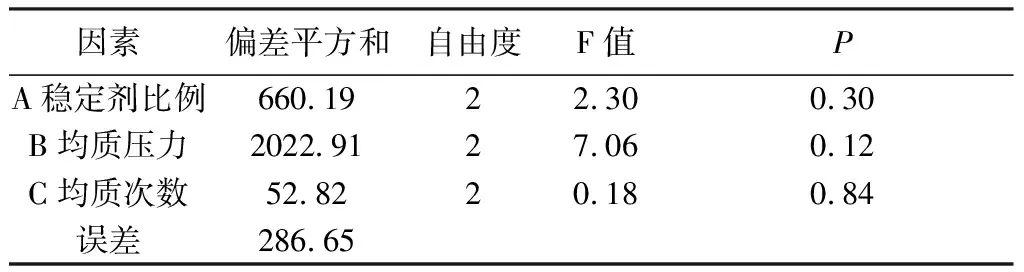
表4 方差分析
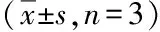
表5 SBEP-NS制备工艺正交验证结果
3.3 正交样品的沉降考察与纳米混悬剂的表征
3.3.1 沉降考察 由图4所示,放置4个月后,第1号至第5号样品出现明显粒子沉降和霉变现象,而第6号至第9号样品仍处于稳定状态,上述最佳工艺制得的样品也位于其间,进一步证明了正交最佳剂型工艺确定的准确性。

图4 正交样品的沉降观察 注:从左往右依次是第1、2、4月
3.3.2 形态观察 由图5可知,SBEP-NS的粒子间无黏连现象,多为球形或类球形囊泡状结构,可能与稳定剂大豆卵磷脂的双亲性结构有关。
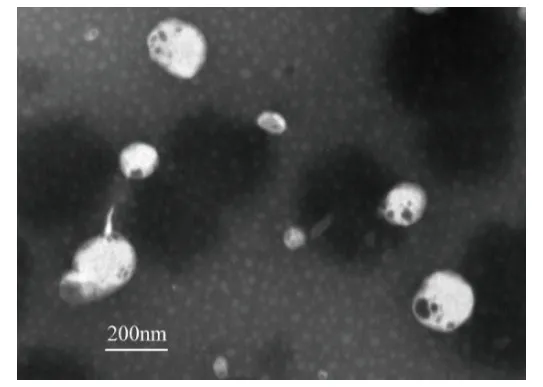
图5 SBEP-NS透射电镜图
3.3.3 粒径、多分散指数及Zeta电位测定 SBEP-NS的平均粒径为(141.4±2.46)nm,PDI为0.025±0.002,Zeta电位为(-31.47±0.26)mV。SBEP-NS粒径较小,分散均匀(见图6)。Zeta电位均小于-30 mV,说明体系处于稳定状态。
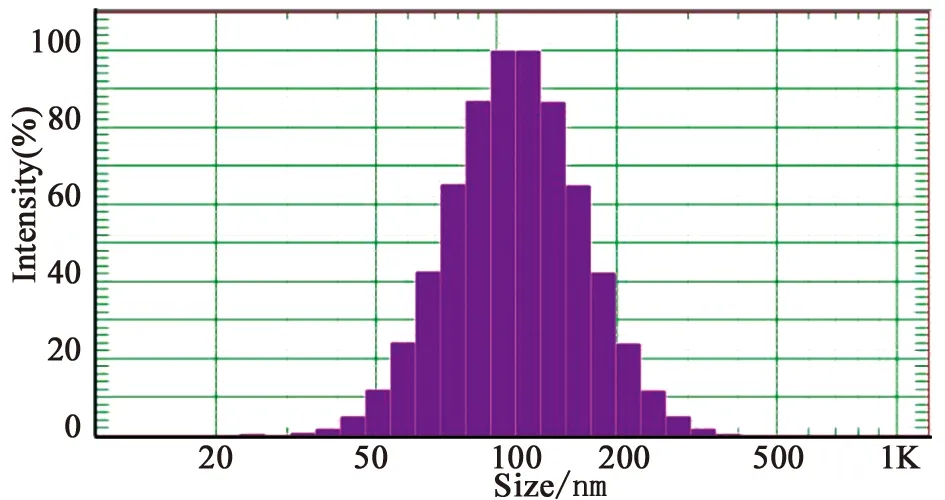
图6 SBEF-NPS的粒径分布图
3.4 升白药效实验 由表6可知,第7天测得的高剂量组白细胞水平显著高于模型组、阳性药组与其他剂量组;第15天时,SBEP-NS各剂量组的白细胞水平高于模型组与阳性药组,具有统计学意义,效果优于地榆升白片。SBEP-NS高剂量组的胸腺指数显著高于模型组与阳性药组;SBEP-NS各剂量的脾脏指数均大于模型组,高剂量组与空白组、阳性药组组间无显著性差异,说明SBEP-NS对环磷酰胺所致的胸腺、脾脏萎缩有良好的恢复作用,效果与地榆升白片相当,结果见图7~8、表6。
图7 小鼠外周血白细胞数
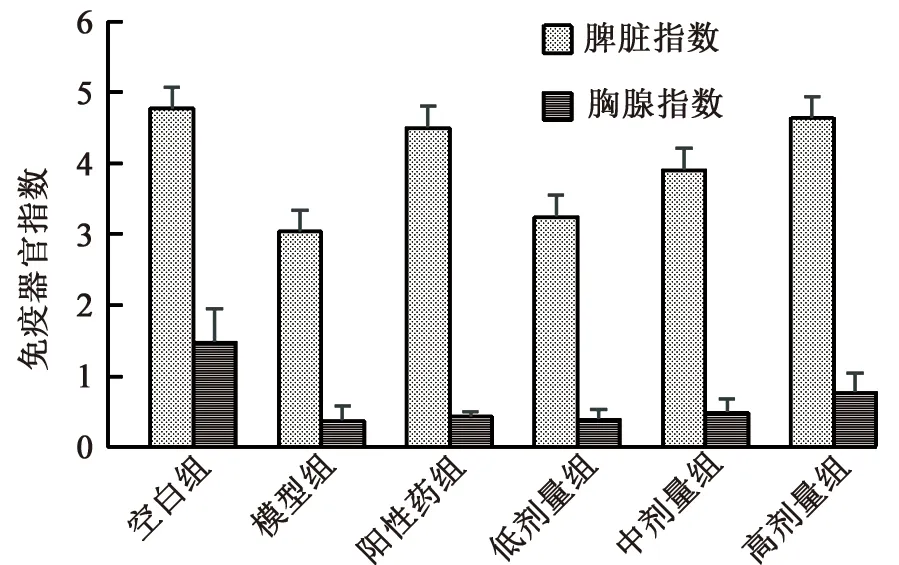
图8 小鼠免疫器官指数
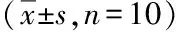
表6 SBEP-NS对小鼠外周血白细胞和免疫器官指数的影响
4 讨论
本实验以参白方中的总多糖和总皂苷为研究对象,由于多糖分子量较大,皂苷的水溶性差,故将其制成纳米混悬剂以提高生物利用度。本实验采用高压均质法制备纳米混悬剂,相较于沉淀法,可以减少有机试剂的使用,提高安全性。前期试验,对泊洛沙姆188、SDS、大豆卵磷脂和吐温80等不同类型的稳定剂进行了考察,综合考虑粒径、PDI与沉降现象等多个指标,最终确定以大豆卵磷脂为稳定剂。大豆卵磷脂通过吸附在药物粒子表面,提供电荷斥力,防止药物粒子的聚集,以维持SBEP-NS的稳定性。通过正交试验结果可知,均质压力对粒径的影响最大,重复验优选工艺,制得的SBEP-NS粒径小于正交试验所得纳米混悬剂的最小粒径,说明优选工艺稳定可行。根据透射电镜图可知,SBEP-NS为囊泡状,可能因为大豆卵磷脂是一种两亲性结构,它可能与皂苷和多糖类成分形成复合物或将其包裹,从而能够帮助提高药物的肠吸收程度和生物利用度。另外,最佳剂型工艺制得的纳米混悬剂处于未发现明显沉降的样品6号至9号之间,说明中药总多糖和绞股蓝总皂苷等有效部位与大豆卵磷脂的混合有助于纳米混悬剂的稳定,加上升白药效的良好结果,证明了参白有效部位纳米混悬剂剂型优化工艺确定的可靠性。至于样品6号至9号显示无霉变的机制,可能与大豆卵磷脂的用量较大以及和有效部位药物形成胶束的充分度有关,具体原因有待进一步的研究。
从药效实验结果发现,环磷酰胺会导致小鼠白细胞水平显著降低,而SBEP-NS对白细胞减少有一定的恢复作用,在给药15 d后,小鼠白细胞水平已经恢复,且超过正常水平,这可能与小鼠出现免疫亢进现象有关[19]。环磷酰胺作为广谱的抗肿瘤药物,不具有特异性,也会杀伤正常细胞,可导致免疫器官的萎缩,故以免疫器官指数作为辅助参考指标。实验结果表明,环磷酰胺对胸腺和脾脏有明显的抑制作用,给药15 d后,小鼠的胸腺指数仍然保持在较低的水平,而脾脏指数已经有大幅度的恢复,这就说明SBEP-NS对胸腺和脾脏抑制有恢复作用,但是在短期内无法解除环磷酰胺对小鼠胸腺的抑制影响。通过比较分析,高剂量组与地榆生白片在升高白细胞的作用上疗效相当,在恢复免疫器官指数作用上,高剂量组优于地榆生白片。综上,通过高压均质法制得的SBEP-NS粒径较小,分布均匀,且能维持稳定,对环磷酰胺所致的白细胞减少症具有良好的恢复作用。
