替格瑞洛中7个异构体的毒理评价及含量测定研究
2022-07-09漆欣筑祝晶何劼毅聂鹏
漆欣筑,祝晶,何劼毅,聂鹏
(贵州省食品药品检验所,贵州 贵阳 550004)
替格瑞洛是一种新型环戊基三唑嘧啶类口服抗血小板药物,可通过激活P2Y12受体,可逆性地阻滞ADP介导的血小板活化和聚集,有效抑制动脉粥样硬化[1-3]。国际多中心PLATO 研究结果显示,替格瑞洛弥补了氯吡格雷抗血小板作用起效慢、个体差异性大等不足[4]。替格瑞洛于2010年12月由阿斯利康公司率先研制而成,2011年获美国食品药品监督管理局(FDA)批准用于急性冠状动脉综合征的治疗[5]。替格瑞洛结构式为(1S,2S,3R,5S)-3-(7-{[(1R,2S) -2-(3,4-二氟苯基)环丙基]氨基}-5-(硫丙基) -3H-(1,2,3)三唑( 4,5-d)嘧啶-3-基) -5-(2-羟基乙氧基)环戊烷-1,2-二醇[6],具有6个不对称手性中心[7],理论上将可能产生64种对映异构体[8],但在实际合成过程中,只存在7种含量相对较大的异构体(见图1)。

图1 替格瑞洛各异构体
目前替格瑞洛已在全球超过85个国家获批上市,于2012年在中国获批上市。截至目前,该药在产厂家共有22家,共计40个批文,国内共有8家生产企业自拟了相关检验标准。由于各企业的合成方法和生产环节不一致,其控制的检验项目和限定参数均存在较大差异,其中仅有两个厂家对异构体的含量进行了控制。我们从临床用药安全的角度出发,认为有必要对该系列异构体的毒性进行全面评价,同时构建7个异构体的统一检验分析方法,并对其进行方法学试验研究;最后,基于我们建立的分析方法,对目前中国市场上在售的8个厂家生产的共计179批次替格瑞洛片的异构体进行含量分析。
1 软件、仪器与试药
1.1 软件版本 ADMET 性质预测软件ADMET PredictorTM(Version 10.0,美国Simulations Plus公司);Gastroplus数据库(Version 9.8.2000)。
1.2 仪器 高效液相色谱仪(型号:e2695,美国Waters公司);XS-205型电子分析天平(瑞士梅特勒公司);超声仪(型号:KQ-500DE,昆山市超声仪器有限公司);纯水机(UPL-I-30EZ,四川优普超纯科技有限公司)。
1.3 试药试剂 乙腈(批号:20025138,美国TEDIA试剂公司);甲醇(批号:21015240,美国TEDIA试剂公司);正己烷(批号:160830,昌泰兴业有限公司);无水乙醇(批号:210302,天津市科密欧化学试剂有限公司);三氟乙酸(批号:20210503,天津市科密欧化学试剂有限公司);替格瑞洛对照品(批号:430050-202101,中国食品药品检定研究院);替格瑞洛7个异构体对照品均来源于Sinco Pharmachem;自制超纯水。
2 方法与结果
2.1 毒理预测结果 从总体情况看,替格瑞洛该系列异构体的毒性预测打分均低于2.0,即毒性较小。但各异构体生不良反应的可能性都较高,应注意控制剂量,最大推荐治疗剂量MaxRTD(针对一般成年人体)需低于3.16 mg·(kg·d)-1。该系列异构体在环境毒性、内分泌毒性、心脏毒性、急性毒性、基因毒性方面均无相关毒性。过敏性预测方面,均无呼吸过敏性。致癌性预测方面(Rat TD50和Mouse TD50),均有产生小鼠致癌性的可能。生殖毒性预测方面(Repro Tox),异构体Y2有产生生殖毒性的可能性。肝脏不良反应预测方面,各杂质均有潜在的肝脏毒性(见表1)。
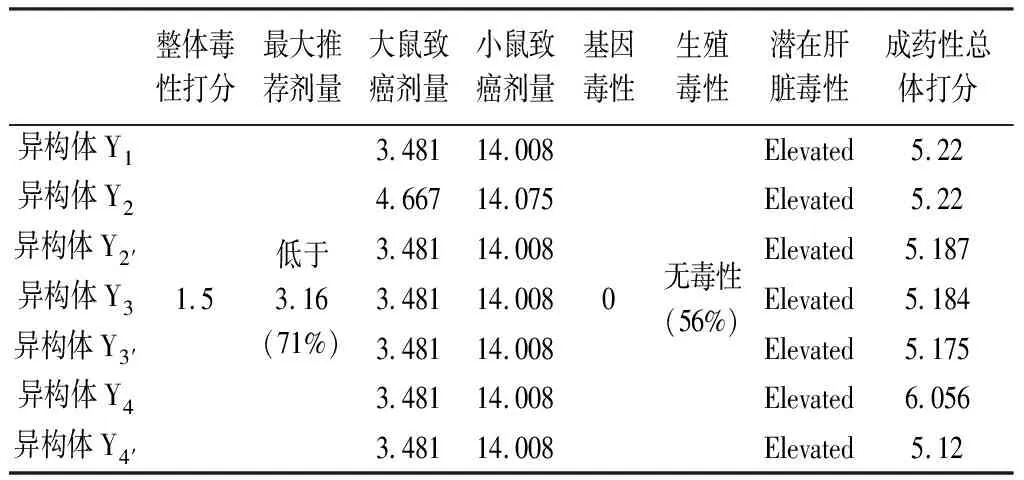
表1 异构体毒理评价预测结果
2.2 常规检验 本次涉及的8个厂家中,只有两个厂家(厂家A与厂家B)的检验标准对制剂中的异构体含量进行了控制。其中厂家A控制了Y1和Y2(限度均为≤0.2%),厂家B控制Y1、Y2和Y2′(限度Y1≤0.2%,Y2+Y2′≤0.2%)。有5个厂家(厂家C、D、E、F、G)的原料药为自己合成,其中两家企业在原料药标准中对异构体的含量进行了控制,各厂家原料药标准中异构体的含量控制具体情况见表2。

表2 各厂家原料药中异构体控制情况
2.3 方法学验证试验 在含量测定的检验项目中,用异构体对照品进行试验,检测异构体是否会在检验条件下,影响替格瑞洛主峰的含量。结果表示在各厂家相应标准的含量测定条件下,异构体Y1、Y2和Y2′和主峰的出峰时间一致,其含量会影响主药的含量控制。异构体Y3、Y3′、Y4、Y4′和主峰可以分开。
2.3.1 色谱条件 仪器及色谱条件:仪器:高效液相色谱仪Waters e2695,色谱柱:Chiralpak AD-H,流动相:正己烷∶无水乙醇∶三氟乙酸(85∶15∶0.2),检测波长:255 nm,柱温:40 ℃,流速:1.0 mol·L-1,进样量:10 μL。
2.3.2 溶液配制 系统适应性溶液的配制:分别取替格瑞洛对照品和7个异构体对照品适量,用无水乙醇溶解并制成每1 mL含各异构体均为10 μg,替格瑞洛为2.0 mg的混合溶液。作为系统适应性溶液。
供试品溶液的配制:取本品细粉适量(约含替格瑞洛50 mg),置100 mL容量瓶中,用无水乙醇溶解并稀释至刻度,摇匀,过滤,取续滤液作为供试品溶液。
对照溶液的配制:取供试品续滤液1 mL至200 mL,用无水乙醇溶解并稀释至刻度,摇匀,即得对照溶液。
2.3.3 专属性试验 系统适应性结果:各成分出峰顺序依次为:Y4、Y3′、Y3、替格瑞洛、Y2′、Y2、Y4′、Y1。各峰之间且与主峰之间分离度符合要求,空白溶剂无干扰(见图2)。
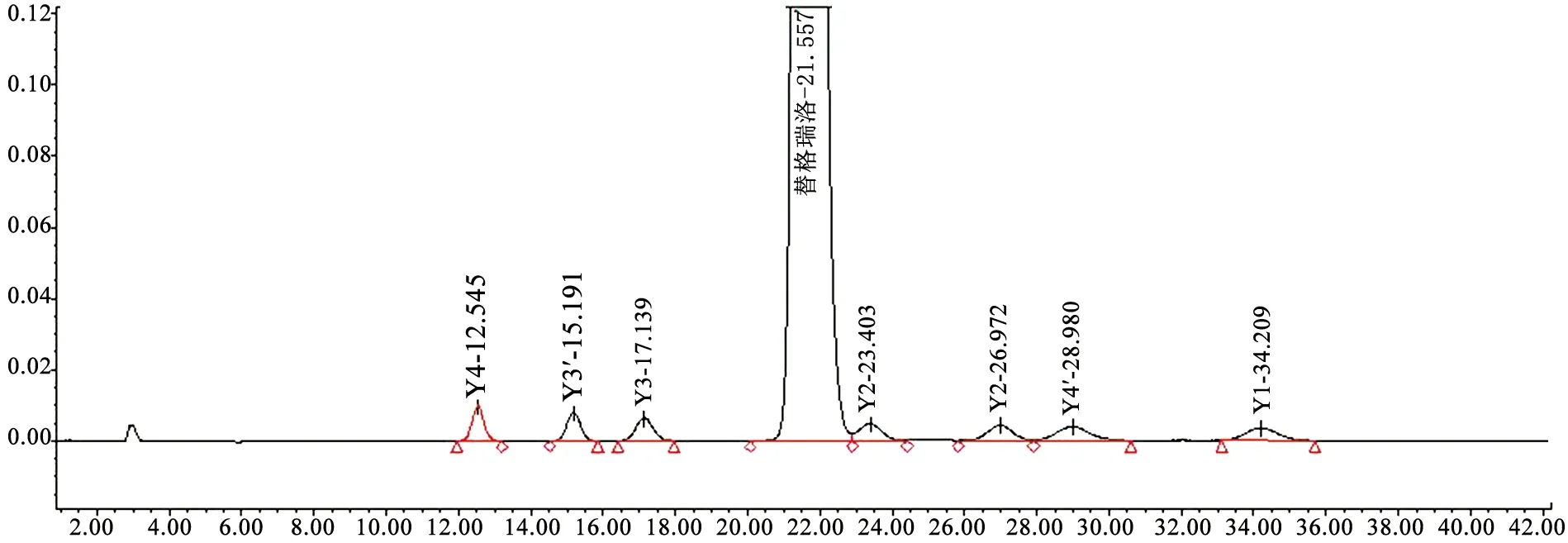
图2 系统适用性图谱
2.3.4 检测限及定量限试验 定量限:各取异构体对照品适量,用无水乙醇溶解并稀释成每1 mL中约含各异构体均为2 μg的溶液,调整进样量,得各异构体的定量限和检出限。此检验方法能满足含量0.001%的异构体检验(见表3)。

表3 各异构体检出限及定量限
2.3.5 异构体含量分析 经本方法检测,8个厂家179批样品中,其中厂家C、D、E、F、G、H的样品中均未检出,厂家A样品中检出Y2,厂家B样品中检出Y1、Y2(见表4)。厂家A与厂家B的3批次样品检验结果与常规检验结果基本一致(见表5~6)。
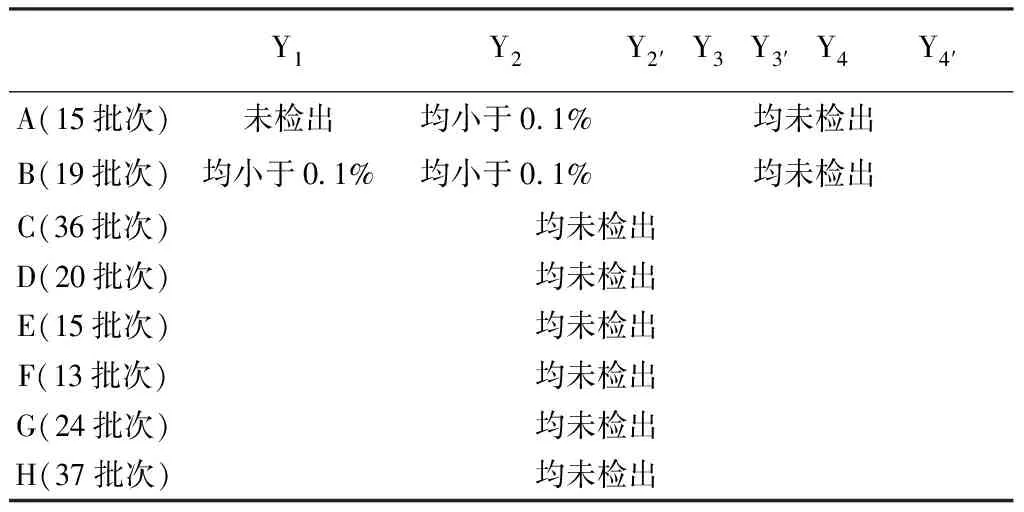
表4 各异构体含量

表5 厂家A 3批次样品中的异构体含量
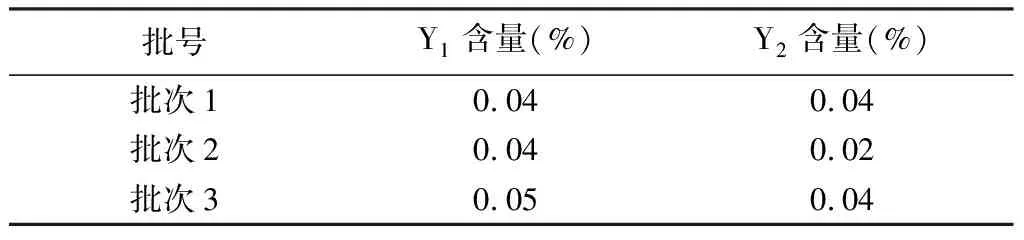
表6 厂家B 3批次样品中的异构体含量
3 讨论
根据ICH M7指导原则的要求,对于药物中杂质的毒理学研究,除采用试验数据外,同时也认可(定量)构效关系[(Q)SAR]评价结果。按照指导原则的要求,对于药物的遗传毒性杂质,我们主要关注其致突变性。ADMET predictor分析结果显示,替格瑞洛的各异构体均存在不良反应的可能性和肝脏毒性,建议各药品生产企业严格控制该药品摄入量。同时,各异构体均存在引起心脏毒性和小鼠致癌的可能性,异构体Y2可能存在生殖毒性。基于ICH M7的要求,我们有必要对该系列异构体进行研究和控制。但ADMET predictor在对药物毒性进行分析时,主要是基于该药物化学结构中是否存在相关的毒性警示结构,因此使用该软件在对同分异构体进行毒性分析时,并不能完全区分异构体间的不同的毒性。因此,建议药品生产企业深入研究该系列异构体的毒理学研究,重点关注相关异构体和不良反应症状之间的关联、动物实验中动物给药量与肿瘤生成的内在联系,论证异构体控制的必要性和相关限度。
通过该高效液相方法,替格瑞洛相关异构体与主峰和其他杂质峰分离度良好,能在同一条件同一系统里区分该7个异构体与主成分,专属性强。该系列异构体的检测限为4~8 ng,定量限为10~16 ng,能有效辨别异构体的种类和分析药品中各异构体的含量。该方法专属性强、操作简单、检验效率高。经本方法检验,企业B检出异构体Y1,企业A、B检出异构体Y2,各异构体的含量低于限度(0.1%),均在可控范围内,其结果为符合规定,其他企业未检出有关异构体。各企业的多批次样品的结果偏差也较小,产品稳定性均较好,检验同一厂家的三批次药品,其Y1、Y2含量的偏差均较小,说明该系列企业的合成路径设置均较为合理,分离纯化方法也较为彻底,能有效地去除原料药中的相关异构体杂质。按此方法检验,可有效地辨别和测定该药品的相关异构体,为高效检验和控制该药品的质量提供了方法借鉴和数据支撑。
