EGCG与β-伴大豆球蛋白/大豆球蛋白相互作用对蛋白质结构的影响
2022-07-07田泽鹏薛丽莹衣艳娇孙书境隋晓楠
黄 国,田泽鹏,薛丽莹,陈 骐,王 迪,衣艳娇,李 萌,孙书境,隋晓楠,*
(1.东北农业大学食品学院,黑龙江 哈尔滨 150030;2.东北农业大学生命科学学院,黑龙江 哈尔滨 150030)
大豆蛋白是我国优质植物蛋白的重要来源,由于其良好的功能特性和丰富的营养品质,被广泛应用于各种食品加工领域中。-伴大豆球蛋白(-conglycinin,7S)和大豆球蛋白(glycinin,11S)是大豆蛋白中的主要储藏蛋白,其含量占大豆蛋白总量的70%。7S蛋白(150~180 kDa)是由3个不同的(67 kDa),’(71 kDa)和(50 kDa)亚基组成的三聚体,这些亚基主要通过疏水相互作用和氢键连接;11S蛋白(约360 kDa)是由两个三聚体堆叠而成的六聚体,每个三聚体包含3个亚基,每个亚基由酸性多肽A(35 kDa)和碱性多肽B(20 kDa)通过二硫键连接。近年来,由于食品级蛋白质对生物活性物质具有潜在的传递和包埋作用,大豆蛋白作为其生物活性物质的载体而备受关注。一方面,大豆蛋白中含有丰富的疏水性/亲水性,带电氨基酸,这使大豆蛋白具有通过静电相互作用、氢键、疏水相互作用等与小分子相互作用的潜力。这些相互作用使多酚等小分子活性物质包埋在大豆蛋白的三维网络中,例如VB、姜黄素、花青素、原花青素等,能够保留其生理活性并将其释放到体内的目标部位。另一方面,与生物活性化合物的络合可以改变大豆蛋白的结构、功能特性和营养价值。例如:大豆分离蛋白(soy protein isolate,SPI)与单宁的相互作用导致SPI发生交联,从而影响了蛋白质的凝胶特性。花青素与SPI的结合诱导了SPI二级、三级结构的变化,进而改善了SPI的稳定性和消化特性。儿茶素可以增强7S蛋白的抗氧化性并促进了7S蛋白消化率的提高。尽管已经有大量的研究关注大豆蛋白与多酚等小分子的相互作用,然而这主要集中于大豆蛋白的混合物,如SPI,或单一的大豆蛋白组分,如7S/11S蛋白。正如前所述,7S和11S蛋白的分子质量和构象差异可能导致大豆蛋白与多酚等小分子的相互作用发生变化。因此,了解不同大豆蛋白组分和多酚等小分子之间的相互作用方式及其结合机理是有必要的。
表没食子儿茶素没食子酸酯((–)-epigallocatechin-3-gallate,EGCG)是绿茶中最主要的儿茶素,约占绿茶中儿茶素的40%。EGCG具有3个芳香环,1个吡喃环和8个酚羟基。与其他多酚相比,芳香环上大量活性酚羟基赋予EGCG优异的理化和功能特性,如抗氧化、抗肿瘤和抗病毒作用等,因此也被广泛用作食品添加剂。另一方面,EGCG分子可以通过酚羟基与环形结构形成氢键和疏水相互作用与蛋白质发生相互作用。当将EGCG添加到大豆蛋白的食品中时,EGCG与大豆蛋白之间的互作可能赋予大豆蛋白更好的功能特性和一些额外的健康益处。You Yaohui等通过荧光光谱法发现SPI和EGCG之间相互作用力主要是依靠疏水相互作用和氢键,并表示EGCG使SPI结构变得松散,SPI的起泡性、乳化性和抗氧化性得到改善。EGCG的加入导致SPI二级结构螺旋与-折叠发生一定的转变,并增强了SPI的热稳定性。此外,EGCG还可以通过疏水相互作用和氢键与大豆蛋白形成不溶性聚集体,提高了大豆蛋白水解液中蛋白质的回收率。尽管EGCG的添加可能会影响大豆蛋白的结构与功能特性,但大多数研究仅限于大豆蛋白混合物或单一的蛋白组分。对于7S蛋白、11S蛋白与EGCG之间的作用机理的差异需要进一步研究。
因此,本实验主要研究中性条件下7S/11S蛋白与EGCG之间的相互作用方式及结合机理,通过紫外-可见光谱及荧光光谱表征大豆蛋白与EGCG结合特性,并分析其相互作用类型与热力学特征;还通过傅里叶变换红外(Fourier transform infrared,FTIR)光谱提供相关蛋白质二级结构变化信息;最后利用分子对接了解7S/11S蛋白与EGCG之间的相互作用的类型和参与相互作用的氨基酸残基。以期在分子水平上提供不同蛋白质组分和多酚的相互作用机制的见解,同时也为大豆蛋白功能性食品的设计和开发提供一定的理论基础。
1 材料与方法
1.1 材料与试剂
大豆(绥农53号) 国家大豆工程技术研究中心;EGCG(纯度≥98.0%) 西安通泽生物科技有限公司;8-苯胺基-1-萘磺酸钠(sodium 8-anilino-1-naphthalenesulfonate,ANS-Na,纯度>97.0%) 东京化成工业株式会社;实验室中所用试剂均为分析纯;所用实验用水均为去离子水。
1.2 仪器与设备
UV-2600紫外-可见分光光度计、RF-6000荧光分光光度计 日本Shimadzu公司;F-7100荧光分光光度计日本Hitachi公司;Nicolet iS50 FTIR光谱仪 美国赛默飞世尔科技(中国)有限公司;FD5-3型冷冻干燥机美国SIM公司;KQ100超声波清洗机 昆山舒美超声仪器有限公司。
1.3 方法
1.3.1 7S/11S蛋白的制备
参考Nagano等的方法并稍作修改。大豆粉碎,过60 目筛,将大豆粉按照料液比1∶3(g/mL)分散于正己烷中,并在室温下搅拌2 h后,富集上清液正己烷进行冷凝回收,重复脱脂5 次。将沉淀物进行干燥,得到的大豆脱脂豆粉。将其按料液比1∶10(g/mL)分散于去离子水中,用2 mol/L NaOH溶液调节pH 7.5,室温搅拌1 h后,在4 ℃、10 000×离心30 min,除去沉淀物,向上清液中加入0.98 g/L干燥的亚硫酸氢钠。用2 mol/L HCl溶液调节pH 6.4后在4 ℃条件下保持过夜,在4 ℃、6 500×离心20 min,得到11S沉淀物。为了制备7S蛋白,在上述步骤得到的上清液加入0.25 mol/L的固体NaCl,并用2 mol/L HCl溶液调节pH 5.0,搅拌1 h。而后在4 ℃、10 000×离心30 min,除去沉淀物。将得到的上清液用相同体积的冰冷水稀释,用2 mol/L HCl溶液调节pH 4.8,室温静置1 h后,在4 ℃、6 500×离心20 min,得到7S沉淀物。
将7S/11S沉淀物进行5 次水洗后,并分散于10 倍的去离子水中重新溶解并调节pH 7.5。分别将悬浮液透析48 h(3 500 Da),每6 h换一次水,而后进行冷冻干燥研磨贮存。经杜马斯法(N×6.25)分析测定,分别得到蛋白质质量分数为(90.30±0.15)%、(96.7±0.10)%的7S/11S蛋白。
1.3.2 7S/11S蛋白-EGCG复合体系的构建
将7S/11S蛋白分散于0.01 mol/L pH 7.0磷酸盐缓冲溶液(phosphate buffered saline,PBS),室温搅拌2 h后,4 ℃冰箱过夜充分水化,最终蛋白母液质量浓度为0.2 mg/mL。将EGCG分散于0.01 mol/L pH 7.0 PBS中,避光室温搅拌2 h后定容,得到64 μmol/L EGCG母液。超声10 min进行脱气处理,4 ℃冰箱备用。将蛋白溶液与EGCG溶液按照不同梯度进行稀释混合至所需浓度,在设置温度下反应2 h后,冰水浴30 min终止反应,以获得大豆蛋白-EGCG复合体系。
1.3.3 紫外-可见光吸收光谱分析
参考刘英杰等的方法并稍作修改。将7S/11S蛋白与EGCG溶液进行混合,最终蛋白质量浓度为0.1 mg/mL,EGCG浓度分别为0、0.5、1、2、4、8、16 μmol/L。在298 K水浴恒温反应2 h,冰水浴30 min后,取出恢复室温后进行紫外-可见光吸收光谱分析。波长范围设置为250~350 nm,速率为中速,狭缝宽为2 nm。其中以未添加EGCG即EGCG浓度为0 μmol/L的蛋白样品为空白对照,下同。
1.3.4 内源性荧光光谱分析
将1.3.3节配制好的7S/11S蛋白与EGCG混合溶液,在298、304、310 K水浴恒温反应2 h,冰水浴30 min后,取出恢复室温后进行内源性荧光光谱测量。使用RF-6000荧光分光光度计测定,激发波长设置为280 nm,发射波长为300~460 nm,激发和发射狭缝宽带均为5 nm,扫描速率为2 000 nm/min。
1.3.5 外源性荧光光谱分析
使用ANS疏水荧光探针法测定蛋白质的表面疏水性。将1.3.3节所配制好的7S/11S蛋白与EGCG混合溶液,在298 K水浴恒温反应2 h,冰水浴30 min后,取出恢复室温后进行外源性荧光光谱测定。将50 μL的8 mmol/L ANS溶液添加到5.0 mL的7S/11S蛋白与EGCG混合溶液中,旋涡振荡30 s,避光反应15 min后测量其荧光强度。使用F-7100荧光分光光度计测定,激发波长设置为390 nm,发射波长为400~600 nm,激发和发射狭缝宽带均为5 nm,扫描速率为1 200 nm/min,电压为500 V。
1.3.6 FTIR光谱分析
将EGCG粉末按EGCG∶大豆蛋白为0∶1、1∶2(/)比例添加至1 g/100 mL的7S/11S蛋白溶液中,避光搅拌2 h,以确保充分反应。将混合物置于透析袋(3 500 Da)中以除去游离的EGCG,并在4 ℃条件下透析48 h。每6 h更换一次去离子水,最后将透析袋中的悬浮液冷冻干燥以获得大豆蛋白-EGCG复合物。将蛋白质样品与KBr粉末以1∶100(/)充分混合研磨后压片,进行FTIR光谱分析。测定波数范围为4 000~500 cm,并以1 cm的分辨率扫描32 次。利用Peak Fit 4.12软件对所获得的扫描图谱中的1 700~1 600 cm酰胺I带进行蛋白质二级结构相对含量分析。
1.3.7 分子对接
使用Pymol 16.0软件对大豆蛋白晶体模型(7S,PDB ID:1UIK;11S,PDB ID:1OD5)进行预处理。而后使用Autodocking Tool 4.12软件对EGCG与预处理的大豆蛋白进行分子对接,获得EGCG与大豆蛋白的结合构象和对接作用最小能量模式图。
1.4 数据统计分析
每组实验平行测定重复3 次,利用SPSS Statistics 23软件对数据进行ANOVA差异显著性分析及相关性分析,<0.05,差异显著。采用Origin 9.1、Peak Fit 4.12等软件进行数据分析、图表制作以及FTIR光谱蛋白吸收峰进行拟合。
2 结果与分析
2.1 EGCG对大豆7S/11S蛋白紫外-可见光吸收光谱的影响
紫外-可见光吸收光谱是研究小分子和蛋白质之间互作的常见方法。在250~350 nm的波长范围内,蛋白质中Trp和Tyr残基的共轭双键在280 nm波长处附近具有吸收峰。蛋白质分子中的氨基酸残基的微环境变化会导致蛋白质的最大吸收波长发生红移或蓝移,从而引起蛋白质构象的改变。如图1所示,随着EGCG添加量增大,7S/11S蛋白吸收谱强度均有增加,这可能是由于EGCG与Trp和Tyr残基之间形成了新的共轭体系,π-π电子对能级跃迁,吸光度增加。同时,7S/11S蛋白的最大吸收值峰位发生了轻微的蓝移,这表明EGCG与大豆蛋白的相互作用改变了Trp和Tyr残基的微环境,蛋白质构象发生改变,这与Wang Chen等的研究结果一致。
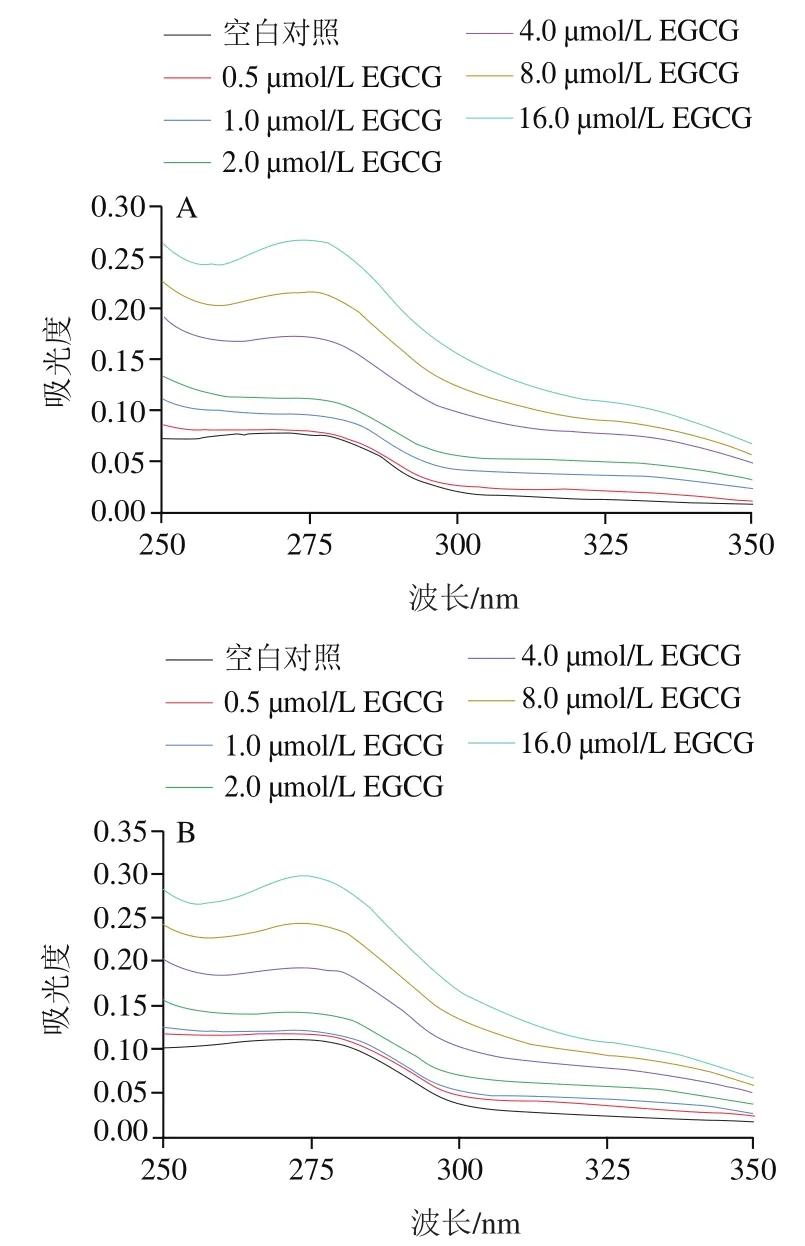
图1 不同EGCG浓度下7S(A)、11S(B)紫外-可见光吸收光谱曲线Fig. 1 UV-Vis absorption spectra of 7S (A) and 11S (B) in the presence of different EGCG concentrations
2.2 内源性荧光光谱分析
2.2.1 EGCG对7S/11S蛋白内源性荧光光谱的影响
荧光光谱法是研究受体与配体相互作用的常见方法,因其方便、快捷、灵敏度高被而广泛使用,从而确定受体与配体分子的结合方式与结合类型。当激发波长为280 nm时,蛋白质的固有荧光主要是来自于Trp与Tyr残基,而Phe残基由于量子产率低而常忽略不计。如图2所示,与7S蛋白相比,11S蛋白显示出更强的荧光强度,这是由于其蛋白含有较高含量的Trp与Tyr,与这与Li Jufang等的报道一致。当添加EGCG时,7S/11S蛋白的荧光强度下降,这表明EGCG对7S/11S蛋白具有猝灭作用,且猝灭效果与EGCG添加量有较强的依赖性。EGCG的添加使得7S/11S蛋白最大荧光峰的波长发生了轻微的红移,这表明EGCG与7S/11S蛋白之间发生了相互作用,蛋白质主肽链变得舒展,埋藏于蛋白质内部中的Trp与Tyr残基暴露至更亲水性的环境。除此之外,当EGCG添加量最大时,EGCG对7S/11S的猝灭效率分别为(58.75±1.34)%、(67.07±2.05)%,这说明EGCG与11S蛋白相互作用更强。

图2 不同EGCG浓度下7S(A)、11S(B)荧光光谱曲线Fig. 2 Fluorescence spectra of 7S (A) and 11S (B) in the presence of different EGCG concentrations
2.2.2 荧光猝灭类型分析
为了解EGCG与7S/11S蛋白之间相互作用的荧光猝灭机理,通过Stern-Volmer方程(1)进行相关猝灭常数的计算。猝灭常数是判定分子之间动态与静态猝灭的关键数据。具体而言,在静态猝灭中,猝灭常数随温度的升高而降低;而对于动态猝灭,其变化趋势与静态猝灭相反。
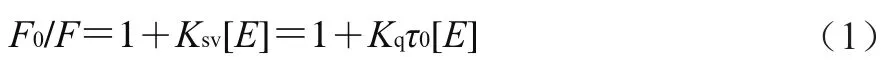
式中:、分别为不添加EGCG与添加EGCG后大豆7S/11S蛋白的荧光强度;[]为EGCG浓度/(mol/L);为动态猝灭常数/(L/mol);为分子猝灭速率常数/(L/(mol·s));为不添加猝灭剂时荧光分子的平均寿命10s。
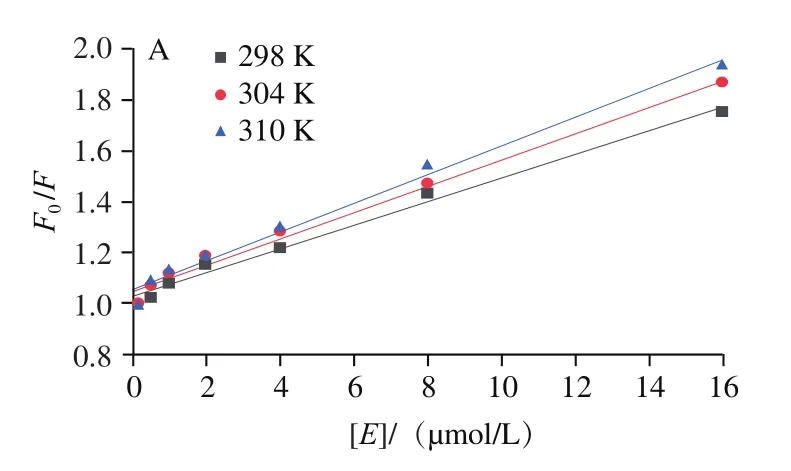
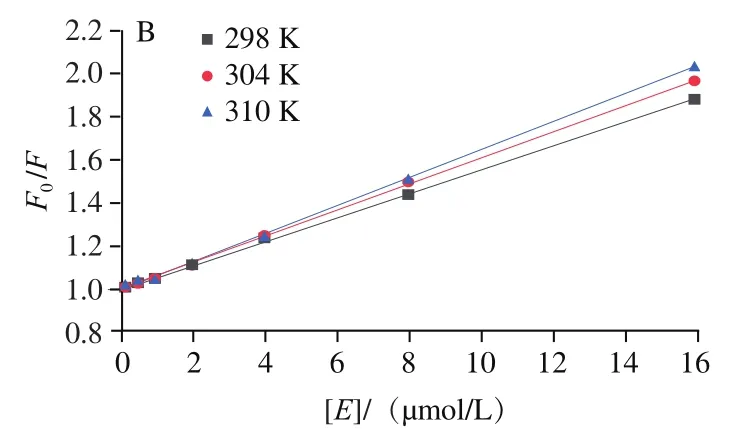
图3 不同温度下7S(A)、11S(B)与EGCG相互作用的Stern-Volmer图Fig. 3 Stern-Volmer curves for the interaction of different temperatures of EGCG with 7S (A) and 11S (B)
如图3和表1所示,7S蛋白和11S蛋白的和值随温度升高而增加。这些结果表明EGCG与大豆蛋白两者之间由于分子间碰撞而引起了动态猝灭。此外,7S/11S蛋白的值远高于最大动态猝灭常数(2.0×10L/(mol•s)),该结果表明以形成基态稳定复合物的静态猝灭方式在大豆蛋白与EGCG结合中起着重要作用。因此,综上表明7S/11S蛋白与EGCG的相互作用方式是动态和静态猝灭同步发生,这与Zhang Jing等研究结论一致。同样,王晨等研究了小麦谷蛋白与矢车菊素-3--葡萄糖苷的相互作用,结果发现矢车菊素-3--葡萄糖苷以动态和静态猝灭相结合的方式使得小麦谷蛋白发生荧光猝灭现象。

表1 不同温度下7S、11S的荧光猝灭常数及线性相关系数Table 1 Stern-Volmer quenching constants (KSV) and molecular quenching constants (Kq) for 7S and 11S at different temperatures
2.2.3 结合常数与结合位点的计算
对于静态猝灭,结合常数和结合位点数可以通过双对数方程(2)进行计算。
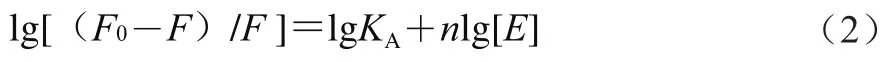
式中:、分别为不添加EGCG与添加EGCG后大豆7S/11S蛋白的荧光强度;[]为EGCG浓度/(mol/L);为结合常数;为结合位点。


图4 不同温度下7S(A)、11S(B)与EGCG相互作用的双对数回归曲线Fig. 4 Double logarithmic regression curves for the interaction of EGCG with 7S (A) and 11S (B) at different temperatures
如图4和表2所示,在相同温度下,7S蛋白的值比11S蛋白低,这表明11S蛋白与EGCG的结合能力更高。7S/11S蛋白的值随着温度的升高而降低,这表明7S/11S蛋白与EGCG的反应是一个放热反应,升高温度不利于大豆蛋白-EGCG复合物稳定性的提高。在298、304 K和310 K温度下,7S/11S蛋白的值近似接近于单个结合位点,表明大豆蛋白和EGCG能够以1∶1的物质的量比形成稳定的静态复合物;此外,观察到7S/11S蛋白的值大小与值趋势一致,进一步说明与7S蛋白相比,11S蛋白与EGCG之间的亲和力更高。

表2 不同温度下7S和11S与EGCG结合的结合位点数、表观结合常数及线性相关系数Table 2 Apparent binding constants, number of binding sites and linear correlation coefficients for the interaction of 7S and 11S with EGCG at different temperatures
2.2.4 热力学参数与相互作用类型判断
大豆蛋白与EGCG之间的相互作用可能涉及不同类型的结合力,这主要是由一种或多种结合力驱动的。为进一步探究大豆蛋白与EGCG相互作用的主要结合力,通过Van’t Hoff方程(3)、(4)计算了包括吉布斯自由能变(∆)、焓变(∆)、熵变(∆)在内的热力学参数。

式中:为实验温度/K;R为气体常数(8.314 J/(mol·K));为对应温度下的结合常数。
如表3所示,所有Δ值均为负值,表明大豆蛋白与EGCG的结合是自发过程。同时,根据Li Yuting等的研究,7S/11S蛋白的∆和∆值均为负值,这表明氢键和范德华力在大豆蛋白与EGCG的结合中起关键作用。刘勤勤等报道了类似发现并指出茶多酚与SPI之间的结合主要依靠范德华力和氢键驱动,在EGCG与米糠蛋白相互作用中也发现了类似的报道。这可能是由于EGCG含有两种活性基团:没食子酰基和酚羟基,且酚羟基数量较多,可以形成大量的氢键与大豆蛋白进行结合。然而,与其他类似的文献报道不同,Zhang Jing等研究了7S/11S蛋白与VB的相互作用,发现疏水作用是主要的结合力;在Ren Cong等的研究中发现,7S/11S蛋白与矢车菊素-3--葡萄糖苷之间的相互作用力主要是静电相互作用。大豆蛋白和EGCG等其他酚类物质的相互作用受其自身的复杂结构和各种因素影响,其他作用力也可能同时参与结合的过程。未来的研究应结合其他技术手段进一步研究大豆蛋白与EGCG之间的相互作用。

表3 不同温度下EGCG与7S、11S结合的相关热力学参数Table 3 Thermodynamic parameters for the interaction of 7S and 11S with EGCG at different temperatures
2.3 外源性荧光光谱分析
在有和无EGCG的情况下,可以通过7S/11S蛋白的ANS结合相对荧光强度表征其表面疏水性。如图5所示,相比于7S蛋白,11S具有较高的表面疏水性,这可能归因于11S蛋白中疏水性和不带电荷的氨基酸含量较高,从而使11S蛋白具有较高的荧光强度。7S/11S蛋白的表面疏水性随着EGCG浓度的增加而逐渐降低。其降低结果可能归因于3个主要原因:首先,当EGCG与7S/11S蛋白的疏水区域结合时,EGCG干扰了ANS疏水性探针与疏水性氨基酸残基结合,使其两者的结合的可能性降低;其次,EGCG具有多个酚羟基,当EGCG与7S/11S蛋白结合时,由EGCG引入的额外羟基会增加7S/11S蛋白的表面亲水性;同时,由于EGCG与7S/11S蛋白的相互作用改变了7S/11S蛋白构象,一些埋藏在蛋白质内部的亲水区域可能会由于蛋白质分子的部分展开而暴露于蛋白质表面,这可能也是7S/11S蛋白与EGCG相互作用后表面疏水性降低的一个原因。相同的结果在Ren Cong等的研究中也有报道:矢车菊素-3--葡萄糖苷与大豆蛋白的相互作用导致蛋白质表面疏水性的下降。此外,11S蛋白的相对荧光强度下降的更加明显,进一步说明11S蛋白与EGCG之间的相互作用更强。
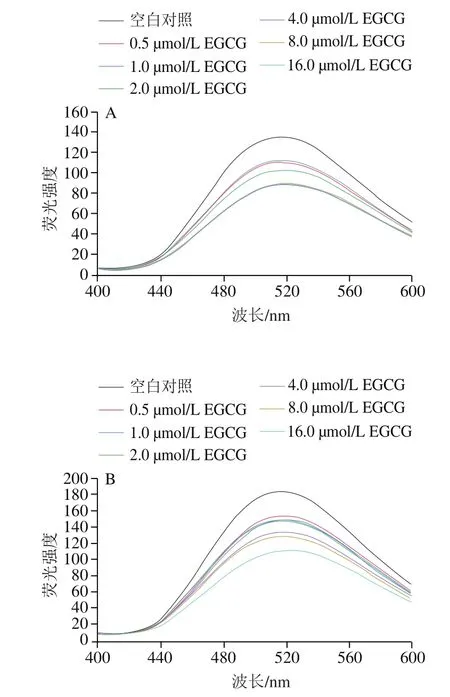
图5 298 K条件下7S(A)、11S(B)与EGCG相互作用的表面疏水性Fig. 5 Effect of interaction with EGCG on surface hydrophobicity of 7S (A) and 11S (B) at 298 K
2.4 EGCG对大豆7S/11S蛋白FTIR光谱的影响

图6 7S和11S及其与EGCG复合物的全局(A)、酰胺I(B)和酰胺II(C)FTIR光谱Fig. 6 Global FTIR spectra (A), amide I spectra (B) and amide II spectra (C) of 7S and 11S and their complexes with EGCG at pH 7.0
应用FTIR光谱法研究大豆蛋白-EGCG复合物,以了解形成复合物的相互作用以及添加EGCG后对大豆蛋白质二级结构的影响。酰胺A带(3 300 cm附近)代表分子间的氢键以及O—H和N—H的拉伸振动,酰胺B带(2 960 cm附近)代表蛋白质的C—H拉伸振动。酰胺I带(1 700~1 600 cm)和酰胺II带(1 540 cm附近)分别是由蛋白质C=O拉伸振动、N—H弯曲和C—N拉伸所导致。如图6所示,EGCG的添加,7S/11S蛋白的酰胺A带、酰胺B带、酰胺I带和酰胺II带位置均发生了偏移,通过改变酰胺I带和酰胺II带的位置,可以推断出大豆蛋白通过C=O、C—N和N—H与EGCG结合;同时,在酰胺A带和酰胺B带位置的变化也证实了EGCG主要与大豆蛋白形成氢键和疏水相互作用。Zhao Qian等研究了胶原蛋白、酪蛋白与没食子酸的相互作用,并指出没食子酸与蛋白质结合并通过氢键和疏水相互作用形成复合物。在茶多酚与豆浆蛋白相互作用中也发现了类似的结论,并表示两者之间的疏水相互作用和氢键能够影响豆浆蛋白的稳定性。
7S/11S蛋白及复合物的蛋白质二级结构定量分析结果如表4所示。-折叠是7S/11S蛋白的主要二级结构,该结果与以往的报道一致。添加EGCG之后,7S蛋白二级结构由-螺旋、-折叠转变为-转角、无规卷曲;这与Sui Xiaonan等的研究结果一致。而11S蛋白二级结构由-折叠、-转角转变为-螺旋、无规卷曲,这与Zhou Siduo等的研究结果一致。无规卷曲是一种无序结构,无序结构的增多表明了蛋白质的解折叠。在大豆蛋白与多酚的相互作用中,相关蛋白质二级结构的变化未得出一致的结论。橙皮苷结合7S蛋白能够诱导-折叠向-转角与-螺旋转变,使得蛋白质结构部分展开呈现较松散的构象状态;在7S/11S蛋白与VB相互作用中,VB促进7S/11S蛋白的-螺旋、-折叠和-转角相对含量的增加,进而增强大豆蛋白质构象的致密性。矢车菊素-3--葡萄糖苷的添加,使得7S/11S蛋白中的-折叠结构向-螺旋、-转角、无规卷曲结构转换,进而降低蛋白质结构的稳定性。这可能是多酚与大豆蛋白质构象、结合量与结合方式的不同导致蛋白质内部氢键重排,对蛋白质氢键和疏水作用有干扰作用,从而导致二级结构发生了不同的变化,在胶原蛋白/酪蛋白-单宁酸、-酪蛋白/-酪蛋白-蓝莓花色苷,乳球蛋白/-酪蛋白-木糖醇等相互作用研究中也观察到了类似的趋势。此外,与未处理的7S/11S蛋白相比,所有添加了EGCG的7S/11S蛋白样品均显示出-折叠相对含量的降低,无规卷曲相对含量的升高。7S蛋白的无规卷曲相对含量比11S蛋白增加更多,7S蛋白的-折叠相对含量比11S蛋白的减少更多。EGCG可能会对7S蛋白二级结构有更大的影响,这可能与蛋白质的固有的构象有关。11S蛋白是一个具有较高聚集度和分子质量的六聚体蛋白;而7S蛋白是一个三聚体,具有较低的聚集度与分子质量,且有较大比例的柔性结构的蛋白。当EGCG作用于7S/11S蛋白时,由于7S蛋白较低的聚集度,可能会更好的作用于7S蛋白,使其无规卷曲相对含量增加更多。这与Wang Yuting等的结果一致,并表示超声处理后的7S/11S蛋白的二级结构相对含量变化有较大的差异,这可能与蛋白质之间构象不同有关。总之,FTIR光谱分析表明,EGCG与7S/11S蛋白结合并通过氢键和疏水相互作用形成复合物,从而导致大豆蛋白质的二级结构改变。此外EGCG会诱导7S/11S蛋白质解折叠,使得-折叠向无规卷曲转变,无规卷曲相对含量的增加可能有利于大豆蛋白质功能性质的改善。

表4 7S和11S及其与EGCG的复合物在pH 7.0条件下的二级结构分析Table 4 Secondary structure analysis of 7S and 11S and their complexes with EGCG at pH 7.0
2.5 大豆7S/11S蛋白-EGCG分子对接分析
分子对接是一种有效的分子互作分析方法,可以提供更多有关EGCG与7S/11S蛋白之间相互作用的信息。如表5所示,Δ为负值,表明EGCG与7S/11S蛋白的反应是自发结合的,并且发现大豆11S蛋白Δ大于7S蛋白Δ,表明EGCG与11S蛋白之间亲和力更高。是Δ的主要结合能来源,这表明包括范德华力、氢键和疏水相互作用在内的多种非共价相互作用力参与了复合物的形成。负值的还表明静电相互作用对大豆蛋白和EGCG之间的结合具有一定的贡献,但不是主要的驱动力,这与热力学参数计算一致。此外,与11S蛋白相比,7S蛋白具有较多的带电氨基酸,带电氨基酸残基电荷密度高,更强。氨基酸分布如图7所示,EGCG位于大豆蛋白的疏水腔,并被一些疏水性和亲水性氨基酸残基包围。在7S蛋白中,共有13个残基参与了对接,其中,EGCG中的羟基与Asn-317、Glu-219、Asn-316、Ala-314、Asp-327和Asn-805残基相互作用形成8个氢键。与7S蛋白类似,11S蛋白中共有10个残基参与了与EGCG的对接,其中Arg-522、Val-523、Asp-531、Glu-533、His-534和Gly-542残基参与形成了6个氢键。在7S/11S蛋白中,EGCG的结合行为发生在蛋白质的疏水口袋,并观察到疏水相互作用、氢键和范德华力的存在,特别是氢键在结合过程中起主要作用,这有助于蛋白质构象的稳定性,从而促进了蛋白质疏水腔内EGCG的空间位置的稳定。这表明在大豆蛋白分子中通过多种形式的作用力为大豆蛋白-多酚复合物提供了必不可少的稳定作用。

表5 EGCG与大豆7S/11S蛋白对接的结果具体能量数值Table 5 Energy values for molecular docking of EGCG with 7S/11S
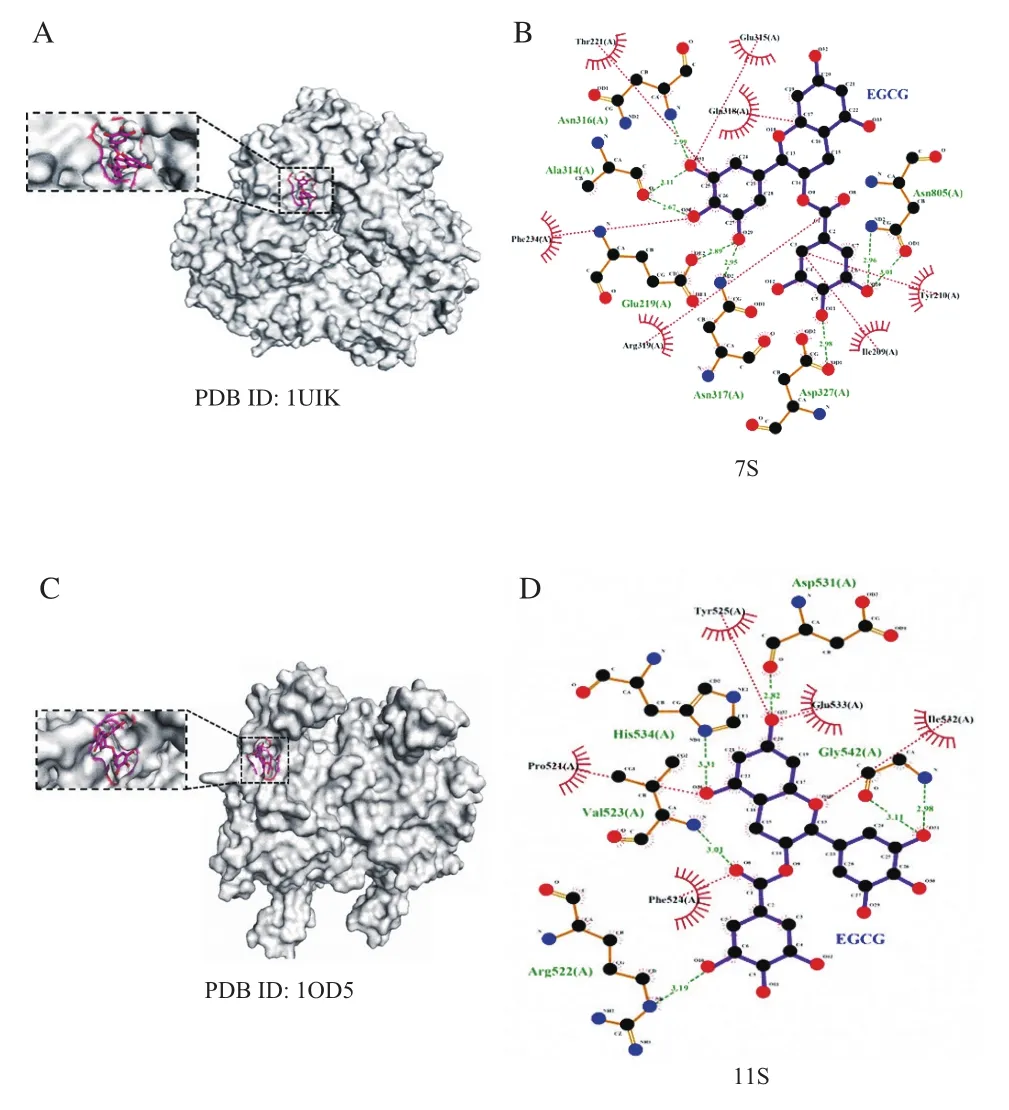
图7 7S(A)、11S(C)与EGCG结合位点及7S氨基酸残基(B)、11S氨基酸残基(D)与EGCG相互作用图Fig. 7 Binding sites between 7S (A)/11S (C) and EGCG, and interaction of amino acid residues in 7S (B)/11S (D) with EGCG
3 结 论
通过荧光光谱、紫外吸收、FTIR光谱和分子对接等分析了EGCG与7S/11S蛋白的相互作用的机理及两者之间相互作用的差异比较。结果显示,在中性条件下,EGCG可与7S/11S蛋白发生动态和静态猝灭,主要通过氢键与范德华力以物质的量比1∶1自发的结合形成复合物,并使得7S/11S蛋白表面疏水性下降;与7S蛋白相比,11S蛋白的猝灭效率、值更高且表面疏水性下降得更为明显,EGCG对11S蛋白具有更高的亲和力;FTIR光谱和分子对接结果表明除氢键,疏水相互作用在EGCG与7S/11S蛋白相互作用中起着重要作用;EGCG的添加能够引起7S/11S蛋白二级结构不同的改变,主要表现为-折叠的减少与无规卷曲的增加,导致大豆蛋白发生解折叠。
