正红菇菇位土壤可培养细菌多样性与网络结构分析
2022-06-23王英浩满家银张桃香练春兰
王英浩,满家银,张桃香 ,练春兰
(1.福建农林大学林学院,福建 福州 350002;2.福建农林大学森林共生生物学国际联合实验室,福建福州 350002;3.东京大学亚洲自然环境科学中心,日本 东京 188-0002)
0 引言
【研究意义】正红菇(Russula griseocarnosa)隶属于担子菌门(Basidiomycota),伞菌纲(Agaricomycetes),红菇目(Russulales),红菇科(Russulaceae),红菇属(RussulaPers.),又名灰肉红菇、大红菌、红锥菌、真红菇,是一种野生的可食用的珍贵外生菌根真菌,一年出菇2 茬,一般发生在每年农历4 月中旬至5 月中旬和农历8 月中旬至9 月中旬,出菇地点相对固定,俗称“菇位”[1]。由于正红菇对其生长环境条件要求极为苛刻,目前尚无法进行人工培育[2]。土壤中的微生物可以调控外生菌根及其子实体的形成[3-6],能促进外生菌根形成的微生物被称为菌根促生菌(Mycorrhization helper bacteria,MHB)[7],这些微生物对菌根的形成具有重要的影响,尤其是在促进菌根真菌菌丝生长和提高菌根侵染率等方面[8-10]。正红菇菌根根际是正红菇菌根形成以及正红菇子实体分化和生长的重要场所。研究正红菇菌根根际土壤细菌多样性对筛选正红菇菌丝体生长和子实体形成分化的菌根促生菌具有重要意义。【前人研究进展】近年来,学者对正红菇的研究主要集中在林分组成和土壤理化性质等对红菇生长的影响等方面[11-13],正红菇菌根根际土壤微生物的研究主要是利用变性梯度凝胶电泳分析[14,15]和通过高通量测序[16]的方法来开展的。有研究表明,通过高通量测序显示出高丰度的细菌与可培养的方法获得的细菌存在显著的差异,并且可培养的方法可以获得一些高通量测序显示的较低丰度的细菌[17]。【本研究切入点】对正红菇菌根根际微生物分离培养是筛选正红菇菌根辅助细菌的关键一步,目前采用分离培养的方法对正红菇菌根根际土壤细菌的研究鲜有报道。【拟解决的关键问题】以正红菇菇位土壤为研究对象,通过纯培养与16S rRNA 基因序列相结合的方法对正红菇菇位土壤内可培养细菌进行分离培养鉴定,分析正红菇菇位细菌群落组成与多样性,及该群落中物种间的网络相互作用,为筛选促进正红菇菌丝体生长和子实体形成分化的菌根促生菌奠定基础。
1 材料与方法
1.1 土壤样品采集
于2020 年9 月在福建省三明市砂蕉村台江国有林场正红菇试验地采集土壤样品,在野外发现正红菇子实体后,采集其子实体并在原位插上标牌以定位,在定位的正红菇位点采集正红菇菇位土壤6 份。先用灭菌的镊子拨开表面的腐殖质,用直径8 mm的打孔器收集正红菇子实体正下方0~5 cm 土壤,每份样品采集5 个样品混合作为一份样品,放进无菌的50 mL 的离心管内,迅速放入保温箱内,低温运回实验室,并储存于4 ℃冰箱中。
1.2 土壤微生物的分离纯化
本试验采用LB 培养基和ISP2培养基进行分离培养[18]。分离培养步骤:称取土壤样品10 g,置于盛有90 mL 无菌水的三角瓶中,200 r·min-1振荡20 min。取土壤悬浮液1 mL 置于9 mL PBS 缓冲液中,逐级稀释至10-6倍,分别取10-3、10-4和10-5含量的土壤悬浮液均匀涂布于LB 培养基和ISP2培养基,每个梯度重复3 次,涂板均匀后将培养平板倒置于37 ℃恒温下培养,期间观察记录可培养细菌的菌落特征并计数,同时从平板上挑取不同培养性状的单菌落,继续在对应平板上划线纯化,直至获得纯培养细菌菌株。用灭菌的牙签轻轻挑取单菌落,接种在装有对应液体培养基的离心管中,置于摇床内30 ℃,200 r·min-1继续培养,最后用30%的甘油将细菌保存于-80 ℃冰箱中。
1.3 可培养微生物的分子鉴定
细菌的DNA 提取采用菌落PCR 的方法。具体方法如下:(1)用经灭菌的牙签挑取纯菌落于PCR 管中,加入20 μL ddH2O,置于PCR 仪中,98 ℃加热10 min。经过离心的上清液即为细菌DNA。(2)将所提取的DNA 进行16S rDNA 的PCR 扩增。PCR 扩增所用引物[19-20]:16S 27F:5′-AGAGTTTGATCCTG GCTCAG-3′和16S 1492R:5′-TACGGYTACCTTGTT ACGACTT-3′。PCR 扩增所用反应体系:DNA 模板1 μL,上下游引物(10 μmol·L-1)各1 μL,PCR Mix 12 μL,用ddH2O 补足至25 μL 反应体系。PCR 反应程序:95 ℃ 3 min;95 ℃ 15 s,55 ℃ 20 s,72 ℃ 1 min,35 个循环;72 ℃ 10 min;保温:4 ℃。将经过琼脂糖凝胶电泳检测在1 500 bp 附近有明显条带的PCR扩增产物送广州擎科生物技术有限公司进行序列测定。
1.4 数据分析
将测序结果与NCBI 网站GenBank 数据库中的序列进行Blast 比对,选取相似度大于97%且相似度最高菌株的16S rRNA 序列,将比对到同一序列的细菌菌株划分到一个操作分类单元(Operational taxonomic units,OTUs)。运用MEGA 5 软件进行系统发育分析,根据序列的同源程度初步确定待鉴定的菌株在分类学上的地位。系统发育树构建方法采用Neighborjoining,自展数(Bootstrap)为1 000,选定2 条Aquifex pyrophilus序列[21]为外群。
根据鉴定结果,计算正红菇菇位土壤微生物的相对分离率[22](指分离到的某种细菌占分离到细菌总株数的百分率,用来衡量某种细菌的优势度)与正红菇菇位土壤细菌群落结构多样性[23]。多样性指数计算公式:

式中,S表示正红菇菇位土壤细菌的种类数,N表示正红菇菇位土壤细菌的总株数,Pi表示某种细菌的相对分离率。
细菌群落间的网络结构可视化与网络的嵌套结构(Nestedness metric based on overlap and decreasing fill,NODF)、物种依赖度(Species strength)、有效合作值(Effective partners)和亲密度(Closeness)等网络结构参数均使用R 语言(4.1.2)的Bipartite包[24]进行分析和计算,并通过与零模型相比较以确定正红菇菇位细菌群落的组装是否为一个随机过程[25]。
2 结果与分析
2.1 正红菇菇位土壤可培养细菌的组成
采用稀释平板分离法,利用LB 和ISP2两种培养基从6 份正红菇菇位土壤样品中一共分离到128 株细菌。对分离到的细菌提取总DNA,使用引物27F 和1492R 进行PCR 扩增后送公司测序,将测序结果在NCBI 网站上进行BLAST 比对,共鉴定到34 个OTUs,隶属于3 门16 属,其具体信息如表1 所示。以34 个OUTs 的16S rRNA 序列及其参考序列构建的系统进化树如图1 所示。正红菇菇位土壤可培养细菌主要分为3 个大类:第一大类为厚壁菌门(Firmicutes),包括芽孢杆菌属(Bacillus)、赖氨酸芽孢杆菌属(Lysinibacillus)、类芽孢杆菌属(Paeinibacillus)等;第二大类为变形菌门(Proteobacteria),包括伯克霍尔德氏菌属(Burkholderia)、副伯克霍尔德氏菌属(Paraburkholderia)、沙雷氏菌属(Serratia)等;第三大类为放线菌门(Actinobacteria),主要是链霉菌属(Streptomyces.)的细菌。
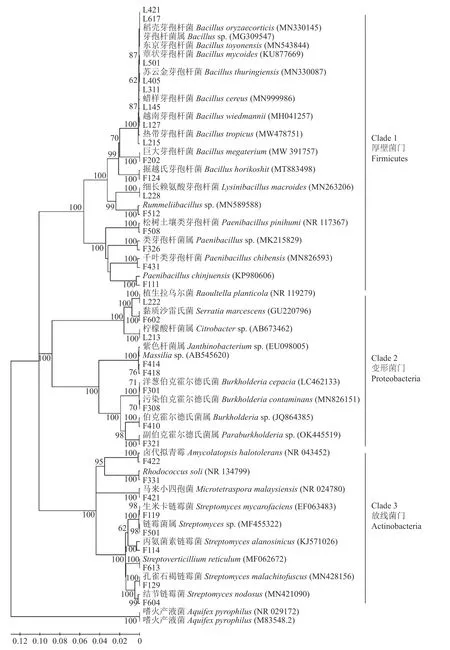
图1 基于正红菇菇位土壤中34 个OUTs 细菌的16S rRNA 序列及其参考序列的系统进化树Fig. 1 Phylogenetic tree based on 16S rRNA sequences of 34 OUTs isolated from rhizosphere soils of R.griseocarnosa and reference

表1 正红菇菇位土壤中分离出的34 个OUTs 细菌的16S rRNA 基因序列比对结果Table 1 16S rRNA gene sequences of 34 OUTs microbes isolated from R.griseocarnosa rhizosphere soil
2.2 正红菇菇位土壤可培养细菌多样性分析
6 个正红菇菇位土壤样品中的可培养细菌丰度组成如图2 所示,样品1~6 中具有的优势类群不同,分别是厚壁菌门的芽孢杆菌属(Bacillus)、放线菌门的链霉菌属(Streptomyces.)和变形菌门的伯克霍尔德氏菌属(Burkholderia)的细菌(样品1);变形菌门的伯克霍尔德氏菌属(Burkholderia)、厚壁菌门的芽孢杆菌属(Bacillus)和放线菌门的链霉菌属(Streptomyces.)(样品2);变形菌门的伯克霍尔德氏菌属(Burkholderia)、厚壁菌门的芽孢杆菌属(Bacillus)和变形菌门的副伯克霍尔德氏菌属(Paraburkholderia)的细菌(样品3);厚壁菌门的芽孢杆菌属(Bacillus)、变形菌门的蓝黑紫色杆菌属(Janthinobacterium)和变形菌门的伯克霍尔德氏菌属(Burkholderia)的细菌(样品4);厚壁菌门的芽孢杆菌属(Bacillus)、变形菌门的伯克霍尔德氏菌属(Burkholderia)和放线菌门的链霉菌属(Streptomyces.)的细菌(样品5);厚壁菌门的芽孢杆菌属(Bacillus)、放线菌门的链霉菌属(Streptomyces.)和变形菌门的伯克霍尔德氏菌属(Burkholderia)的细菌(样品6)。通过对6 份正红菇菇位土壤样品获得的128 株细菌隶属的结果进行分析得知,丰度前3 的属分别是厚壁菌门的芽孢杆菌属(Bacillus)(占53.13%)、变形菌门的伯克霍尔德氏菌属(Burkholderia)(占20.31%)、放线菌门的链霉菌属(Streptomyces.)(占9.38%)。对6 个正红菇菇位土壤可培养细菌多样性结果如表2 所示,各样品的香农指数在2.94~3.72,辛普森指数在0.81~0.91,丰富度指数在3.19~4.41,均匀度指数在1.22~1.38。

表2 6 个正红菇菇位土壤样品可培养细菌多样性指数Table 2 Diversity index of culturable microbes in 6 rhizosphere soil samples from sites of R.griseocarnosa

图2 不同正红菇菇位土壤样品中属水平可培养细菌丰度组成Fig. 2 Abundant culturable microbes at genus level in different rhizosphere soils
2.3 正红菇菇位土壤可培养细菌群落的网络结构分析
正红菇菇位土壤可培养细菌属水平与采样品的网络结构分析结果表明(图3),分离细菌中丰度最大的是芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia),可在所有采样品分离到;部分细菌属仅在特定的采样品中分离到,如柠檬酸杆菌属(Citrobacter)和拉乌尔菌属(Raoultella)仅在样品2 中分离到;红球菌属(Rhodococcus)和副伯克霍尔德氏菌属(Paraburkholderia)仅在样品3 中分离到;拟无枝酸菌属(Amycolatopsis)、蓝黑紫色杆菌属(Janthinobacterium)和小四孢菌(Microtetraspora)属仅在样品4 中分离到;Rummeliibacillus属仅在样品5 中分离到;轮枝链霉菌属(Streptoverticillium)仅在样品6 中分离到。

图3 正红菇菇位土壤可培养细菌(属水平)在不同采样品的分布Fig. 3 Distribution of culturable microbes at genus level in rhizosphere soil sampled at R.griseocarnosa sites
分析正红菇菇位土壤可培养细菌属间的相互作用结果表明(表3),芽孢杆菌属(Bacillus)的物种依赖程度最高为3.10,其次是伯克霍尔德氏菌属(Burkholderia)为1.21;芽孢杆菌属(Bacillus)、伯克霍尔德氏菌属(Burkholderia)、赖氨酸芽孢杆菌属(Lysinibacillus)和类芽孢杆菌属(Paenibacillus)的有效合作值较其他细菌属更高,分别为5.79、4.68、4.00 和4.00;芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)的亲密度较高,为0.08;对网络中各细菌的依赖度、有效合作值和亲密度分析表明,芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)在细菌群落中被其他属的细菌所依赖程度较高,并可能拥有更多的相互作用。与零模型相比,正红菇菇位土壤可培养细菌(属水平)与采样品的网络嵌套性(NODF=44.66)差异不显著(P=0.29),即样品中分离菌株在属水平的分布具有随机嵌套性。
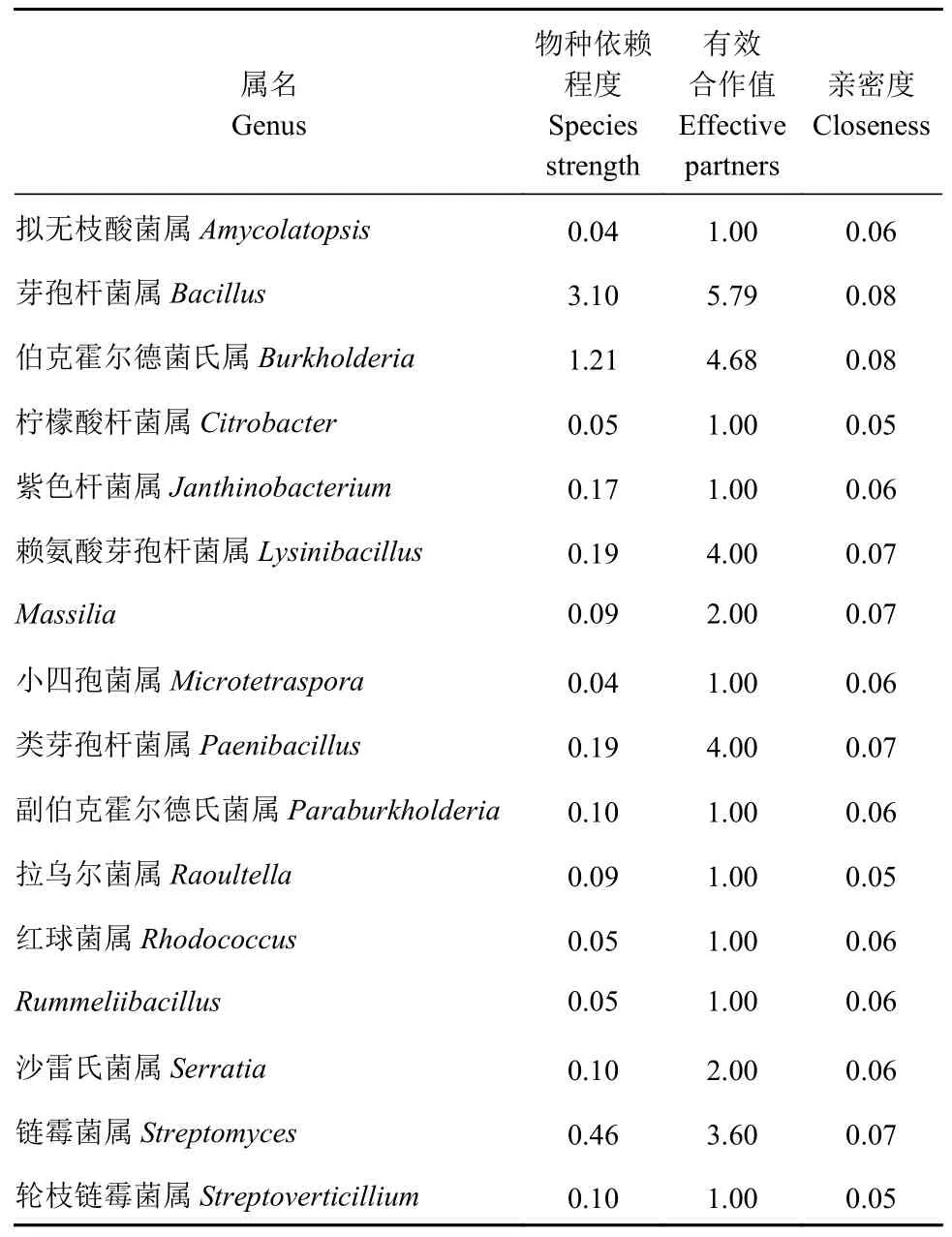
表3 正红菇菇位土壤中可培养细菌属间的网络相互作用Table 3 Network interactions among culturable microbial genera in R.griseocarnosa rhizosphere soil
3 讨论
本研究通过传统分离培养的方法从正红菇菇位土壤中分离到可培养细菌128 株,其分别隶属于3 个门16 个属,可以划分为34 个OTUs。丰度排前三的属中,芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)在6 个样品中均可以分离到,链霉菌属(Streptomyces.)仅可以在样品1、3、5、6 中分离到。近年来,大量研究通过变性梯度凝胶电泳和高通量测序分析了正红菇菌根际微生物多样性。肖冬来等[14]发现正红菇菌根根际土壤细菌主要分为7 个类群:α-变形菌门(Alphaproteobacteria)、β-变形菌门(Betaproteobacteria)、γ-变形菌门(Gammaproteobacteria)、酸杆菌门(Acidobateria)、浮霉菌门(Planctomycetes)、疣微菌门(Verrucomicrobia)及分类地位未知的不可培养细菌;Yu 等[16]利用16S 扩增子测序对正红菇菌根根际细菌进行了研究,结果表明正红菇菌根根际细菌的多样性比对照组更低,伯克霍尔德菌属-副伯克霍尔德菌属(Burkholderia-Paraburkholderia)、分枝杆菌属(Mycobacterium)、堆囊菌属(Sorangium)、酸杆菌属(Acidobacterium)、Roseiarcus属和Singulisphaera属的细菌可能对正红菇的生长具有一定的促进作用。然而以上研究无法获得正红菇菌根根际土壤微生物的纯培养,难以进一步开展土壤微生物与正红菇关系的相关研究。我们通过传统分离培养的方法对正红菇菇位可培养细菌进行了研究,表明其优势菌属是芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)。
菌根对其生长环境中的微生物存在选择和调控的作用,同时环境微生物也影响着菌根的形成和生长以及基因的表达[26-28]。姜华等在6 个松口蘑菌塘土壤中分离到的最多也是芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)的细菌[21];安忠琦等在金钗石斛根际可培养细菌多样性的研究中分离到的最多也是芽孢杆菌属(Bacillus)的细菌[29];而万山平等在攀枝花块菌-华山松菌根根际土壤可培养细菌的多样性研究中分离到的最多是伯克霍尔德氏菌属(Burkholderia)的细菌[30]。同时,本研究从正红菇菇位土壤中也分离到了大量芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)的细菌。有研究表明,从Tuber borchii中分离到的芽孢杆菌属(Bacillus)的细菌可以降解几丁质[31],以此来促进Tuber borchii产生孢子和形成子实体;从Laccaria laccata菌根和根际中分离到的芽孢杆菌可以促进外生菌根真菌菌丝的生长以及外生菌根的形成[32,33];类芽孢杆菌(Paenibacillus)可以利用可溶性代谢物促进松茸生长[34]。盛江梅等[35]分到一株蜡样芽孢杆菌(Bacillus cereus)可以促进美味牛肝菌(Boletus edulis)菌丝体的生长并且促进其与宿主黑松形成菌根从而促进宿主植物生长。然而,芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)的细菌与正红菇菌丝的生长和菌根形成的互作关系及影响机理还未见报道,有待开展进一步的研究。
Rivett 等[36]学者认为,细菌的相对丰度在一定程度上反映了其在群落中的重要程度,相对丰度较高的细菌在群落中的相互作用可能更多。本研究中的芽孢杆菌属(Bacillus)和伯克霍尔德氏菌属(Burkholderia)具有相对较高的丰度同时也具有较高的相互作用,是正红菇菇位土壤中细菌群落的关键类群。但是,Franck 等[17]的研究中通过高通量测序方法显示出具有较高丰度假单胞菌属的细菌种,在其传统分离培养和高通量测序的网络互作分析中都显示出较低的相互关系。因此,判断细菌在群落中的重要程度不仅要看其相对丰度,其在网络互作中的相互关系一样需要受到关注。除此之外,通过高通量测序和传统分离培养2 种方法检测到的细菌在群落组成和相对丰度上存在明显的差异,在正红菇菇位土壤可培养细菌丰度占前5 的细菌属中仅伯克霍尔德氏菌属(Burkholderia)是高通量测序分析结果中相对丰度前8 的主要类群之一,且正红菇菇位土壤可培养细菌丰度最高的芽孢杆菌属(Bacillus)在高通量测序研究中并没有显示出较高的丰度[37]。因此将传统纯培养方法和高通量测序技术相结合才能更好地研究正红菇菌根根际中的细菌多样性。
