脾脏EB病毒阳性的炎性滤泡树突细胞肉瘤伴肝脏转移1例
2022-06-21胡袺袺张雪珂张品南
胡袺袺,张雪珂,张品南
温州市人民医院病理科,浙江温州325000
EB病毒(Epstein-Barrvirus, EBV)阳性的炎性滤泡树突细胞肉瘤(folliculardendriticcellsarcoma, FDCS)是一种很罕见的低度恶性肿瘤,是FDCS的一种少见亚型。大多数病例临床症状和影像学特异性不显著,且病理形态与很多肿瘤难以鉴别,易造成误诊或漏诊。笔者报告1例中年男性患者脾脏EBV阳性的炎性FDCS伴肝脏转移的病例,以提高临床和病理医师对本病的认识。
1 病例资料
患者,男,44岁,2021年7月因“体检发现脾脏和肝脏占位性病变”就诊于温州市人民医院。患者自诉近期体质量减轻,2个月减轻5kg,偶有腹胀,其他无殊。实验室检查:血红蛋白127g/L,白蛋白39.6g/L,超敏C反应蛋白30.2mg/L,肿瘤标志物正常。腹部MR增强检查:脾实质内见一团片状稍低密度影,边界欠清,大小约114mm×105mm(见图1),中心可见坏死;右肝后下段见结节状低密度影,边界清,直径约20mm,影像诊断:脾脏占位,考虑恶性肿瘤伴肝右叶转移可能。在充分术前准备后,行全脾脏及右肝病变区域部分肝组织切除术。
巨检:脾脏切面见一肿物,大小10cm×10cm×8.9cm(见图2),切面灰白灰黄,实性质中,局部偏硬,局部坏死,界清,无包膜;肝组织见一肿块,大小2.3cm×2cm×2cm,灰白灰黄,质实,稍偏硬,界清,无包膜。

图1 脾脏MRI影像
图2 脾脏肿瘤巨检
镜检:脾脏肿物:在大量淋巴细胞、浆细胞背景中,可见散在或密集分布的圆形、卵圆形及梭形细胞,肿瘤细胞呈束状、编织状或席纹状排列(见图3A)。瘤细胞胞界不清,胞质淡染、透明,细胞核圆形、卵圆形,空泡状,染色质细颗粒状,可见单个小核仁,核膜清晰,核异型性不大,核分裂象少见(见图3B)。肝脏肿物:瘤组织与周围正常组织分界较清楚(见图4A),在炎症细胞背景下,肿瘤细胞弥漫分布,细胞圆形、卵圆形或胖梭形,细胞体积大,胞浆丰富,嗜酸性,核浆比增高,核空泡状,易见小核仁,核膜不规则,有时可见双核细胞(见图4B)。
免疫组化:脾脏肿瘤细胞CD21(+)、CD23(+)、CD35(+)、平滑肌肌动蛋白(smoothmuscleactin, SMA)(+/-)、肌动蛋白束蛋白(fascin)(+/-)、D2-40(-)、CD68/KP(-)、间变型淋巴瘤激酶(anaplasticlymphomakinase, ALK)(-)、Ki-67(+,低于10%)。肝脏肿瘤细胞CD23(+)、SMA(+/-)、fascin(+)、CD21(-)、CD35(-)、D2-40(-)、CD68/KP(-)、ALK(-)、Ki-67(+,约20%)。原位杂交显示肝脏和脾脏肿瘤EBV早期RNA(Epstein-BarrvirusearlyRNA, EBER)均(+),见图5。
术后病理诊断:脾脏EBV阳性的炎性FDCS伴肝脏转移。术后随访半年,患者无复发,无转移。
2 讨论
EBV阳性的炎性FDCS是一种生物学行为相对惰性、低度恶性的肿瘤,发病机制尚不清楚。肿瘤主要来源于滤泡树突细胞(folliculardendriticcell, FDC)。FDC是一种免疫辅助T细胞,正常分布于初级和次级淋巴滤泡内,参与免疫应答作用。1996年,SHEK等[1]报道了首例原发性肝脏FDCS,组织学与炎性假瘤(inflammatorypseudotumor, IPT)相似,并与克隆性EBV增殖有关。2001年,CHEUK等[2]发现IPT样FDCS是一种独特的实体肿瘤,并报道了11例发生于腹腔内的病例。这类病例有独特的形态特征,并和EBV感染有关,因肿瘤组织中有较多淋巴细胞与浆细胞的背景,与IPT十分相似,故而称其为IPT样,同时,肿瘤细胞对FDC相关标记抗体呈阳性反应而证实其来源于FDC,故而命名为IPT样FDCS。2019版WHO消化系统肿瘤改名为EBV阳性的炎性FDCS。

图3 脾脏肿瘤镜检

图4 肝脏肿瘤镜检
EBV阳性的炎性FDCS好发于青年至中年人群(患者年龄19~82岁,中位年龄56.5岁),以女性多见,虽然病例的地理分布既包括东方国家也包括西方国家,但更多的报道来自亚洲国家(特别是中国、韩国和日本),提示该肿瘤可能具有种族或地域倾向。本病常累及肝脏或脾脏,少数也可以累及消化道[3]。临床表现无明显特异性,有些患者可能出现发热,体质量减轻,左上腹疼痛与不适。实验室检查可能显示贫血,低蛋白血症,C反应蛋白升高,CA125升高,偶尔会出现外周嗜酸性粒细胞增多。本例患者为中年男性,临床表现及实验室检查结果基本符合。
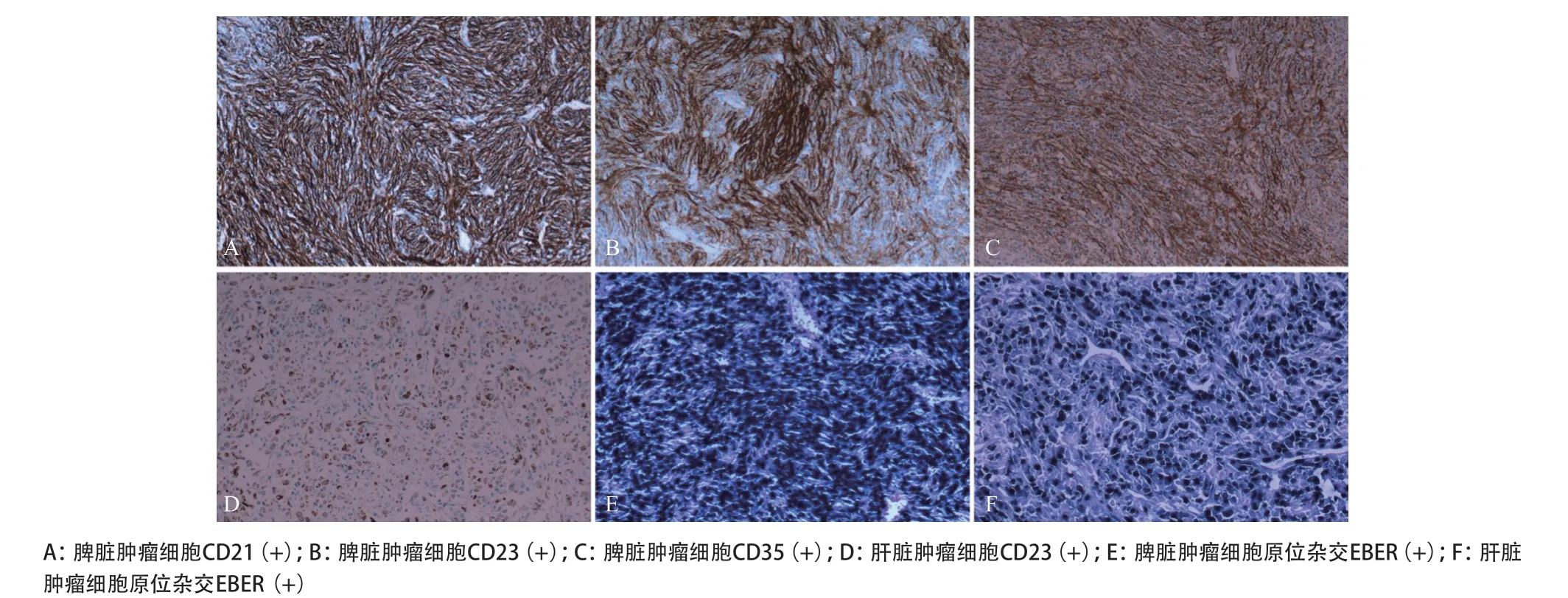
图5 脾脏和肝脏肿瘤细胞免疫组化图片(×200)
EBV阳性的炎性FDCS大体所见多为脾脏或肝脏实质内境界清楚的单发性肿块,直径为3~22cm,切面棕色或灰白色,均质,质硬;镜下特点为大量的淋巴细胞、浆细胞背景中散在或密集分布卵圆形至梭形的肿瘤细胞,肿瘤组织呈束状、编织状或席纹状排列,细胞核为卵圆形,核染色质空泡状,可见小的嗜碱性核仁,没有明显的细胞异型性,核分裂象罕见[4]。本例脾脏肿瘤病理组织形态基本符合,而肝脏肿瘤细胞分布更密集,胞体更大,核浆比增高,易见小核仁,核异型性较明显。脾脏肿瘤和肝脏肿瘤的形态差异,可能与肿瘤原发灶和转移灶生长机制不同有关。
免疫组化显示瘤细胞特异性表达FDC标记,但有研究[5]表明通常会至少丢失一个抗体,所以通常采用一组FDC标记,其中CD21和CD35被广泛用作首选的FDC标记物,其他FDC标记包括CD23、CNA.42、CXCL13、簇连蛋白(clusterin)、fascin、TUBB3、D2-40、g-synuclein。肿瘤细胞灶区表达CD68、SMA、HHF-35 和S-100。肿瘤细胞不表达结蛋白(desmin)、ALK、CD30、上皮膜抗原(epithelialmembraneantigen, EMA)。本例中,脾脏肿瘤细胞表达CD21、CD23、CD35,而在肝脏仅表达CD23和fascin,未表达CD21和CD35。这可能提示转移灶肿瘤细胞比原发灶更易丢失表面抗原。
EBV被认为在炎性FDCS的发生中发挥关键作用[6]。几乎所有炎性FDCS通过原位杂交显示EBER阳性。EBV及FDC标记抗体检测对此瘤的诊断与鉴别诊断具有重要作用。本例中,脾脏和肝脏的肿瘤均显示原位杂交EBER阳性。
鉴别诊断:①经典的FDCS:FDCS肿瘤细胞更密集,间质中淋巴细胞分散;EBV阳性的炎性FDCS肿瘤细胞是散在或局部密集分布,背景中见大量淋巴细胞、浆细胞。原位杂交在区分两者之间很有帮助,前者很少表达,而后者EBER总是阳性。②炎性肌成纤维细胞肿瘤(inflammatorymyofibroblastictumor, IMT):IMT是一种分化性的梭形纤维细胞/肌成纤维细胞组成的肿瘤,间质内常伴有大量的浆细胞和淋巴细胞。组织形态和EBV阳性的炎性FDCS很相似,但IMT好发于儿童和青少年(平均年龄为10岁),极少数病例可发生于40岁以上,多数病例表达ALK、SMA和desmin,不表达FDC标记,EBER阴性。③经典型霍奇金淋巴瘤(classicalHodgkinlymphoma, CHL):CHL是一种淋巴细胞性肿瘤,少数诊断性R-S细胞及其变异型细胞散在分布于炎性背景中。与EBV阳性的炎性FDCS不同,CHL特征性表达CD30和CD15,可加以区分。④淋巴瘤样肉芽肿病(lymphomatoidgranulomatosis, LYG):两者均有EBV阳性、背景中丰富的淋巴细胞,但LYG预后不好,中位生存期不足2年,组织学特征为淋巴细胞性血管炎,免疫组化方面特征性表达CD20、CD79a;而EBV阳性的炎性FDCS不具有这些特点。⑤IPT:IPT是反应性或炎症性瘤样增生性病变,有炎症细胞和增生的梭形细胞构成,是排他性诊断。IPT表达Vim、SMA,不表达ALK和FDC标记。
总之,EBV阳性的炎性FDCS生物学行为相对惰性,肿瘤完整切除后,预后良好,很少复发或转移。本例肿瘤原发于脾脏,手术治疗前即已发生肝脏转移,实属罕见。
