畲药铜丝藤根化学成分的分离鉴定
2022-06-20张晓芹袁宙新倪京丽王娜妮
张晓芹 袁宙新 倪京丽 王娜妮
1.浙江省丽水市中医院药剂科,浙江丽水 323000;2.浙江省中医药研究院,浙江杭州 310007
铜丝藤根,是畲族习用药材,系海金沙科植物海金沙[Lygodium japonicum(Thunb.)Sw.]的干燥根及根茎[1],具有清热解毒、利湿消肿之功效,主治水湿肿满、风湿痹痛[2-3],是畲族民间治疗骨关节炎的常用药物[2-3]。铜丝藤根孢子的乙醇提取物可通过抑制核因子κB通路发挥抗炎作用[4-5],水煎液对痛风性关节炎具有治疗作用[6]。铜丝藤根中已报道化合物主要为黄酮类、甾体类、酚酸类、脂肪酸类及挥发类成分[7-8],但化合物种类仅有20 余种,尚需要进一步探索。
1 仪器与试药
1.1 仪器
高效液相色谱仪(Agilent 1100,美国安捷伦科技有限公司);制备液相色谱仪(ZR,江苏智润科技有限公司);核磁共振波谱仪(AVANCE-Ⅲ,德国Bruker 公司);红外光谱仪(FTIR-650,天津港东科技有限公司)。
1.2 试药
甲醇、乙腈(色谱级和制备级,上海星可高纯试剂有限公司)。铜丝藤根样品采自浙江省丽水市,由浙江省丽水市中医院林娜主任中药师鉴定为海金沙科植物海金沙[Lygodium japonicum(Thunb.)Sw.]的地下根及根茎。
2 方法与结果
2.1 提取分离
10 kg 铜丝藤根药材,80%乙醇回流提取3 次,每次2 h,浸膏依次用石油醚、乙酸乙酯、正丁醇萃取,浓缩,得石油醚部位(51.17 g)、乙酸乙酯部位(237.75 g)、正丁醇部位(199.12 g)。乙酸乙酯部位经硅胶柱色谱Sephadex LH-20 层析,以石油醚-乙酸乙酯梯度洗脱,薄层检测,合并浓缩后得到的Fr.1~11 分别经制备型高效液相色谱、硅胶柱层析等方法纯化得到化合物1~13,见图1。

图1 提取分离流程图
2.2 结构鉴定
化合物1:黄色粉末。红外吸收光谱法(infrared absorption spectrum,IR)(KBr,cm-1):3369、2964、1660、1649、1577、1336、1266、1034、885、727。紫外可见光谱法(ultraviolet-visible spectrometr,UV):204.2、266.7、346.6 nm。氢-1 核磁共振波谱法(1H nuclear magnetic resonance spectroscopy,1H-NMR)(400 MHz,DMSOd6)δ∶7.77(1H,s)、7.30(1H,s)、6.68(1H,s);1.12(6H,d,J=6.8 Hz)、3.10(1H,m)、2.24(3H,s)。核磁共振碳谱(13C Nuclear Magnetic Resonance Spectroscopy,13C-NMR)(100 MHz,DMSO-d6):低场区共有10 个C 信号,含2 个羰基信号185.1 和183.4。高场区有3 个C 信号。与文献[9]比较,确定为6-羟基-2-异丙基-7-甲基-1,4-萘醌。
化合物2:白色粉末。IR(KBr,cm-1):3329、3228、1645、1597、1533、1441、1296、1164、876、812、754、631。UV:205.3(max)、230.1、278.6、311.9 nm。1H-NMR(400 MHz,CD3OD)δ∶7.33(1H,dd,J=7.6,2.0 Hz)、7.32(1H,s)、6.92(1H,d,J=7.6 Hz)、9.71(1H,s)。13C-NMR(100 MHz,CD3OD)显示7 个C 信号,与文献[10]比较,确定为原儿茶醛。
化合物3:无色油状物。1H-NMR(400 MHz,CD3OD)δ∶1.03(3H,s,H-12)、1.06(3H,s,H-11)、1.26(3H,d,J=6.4 Hz,H-10)、1.93(3H,s,H-13)、2.17(1H,d,J=16.8 Hz,H-2b)、2.49(1H,d,J=16.8 Hz,H-2a)、4.33(1H,m,H-9)。13C-NMR(100 MHz,CD3OD)δ∶42.4(s,C-1)、50.7(t,C-2)、201.2(s,C-3)、127.1(d,C-4)、136.9(d,C-7)、130.0(d,C-8)、68.6(d,C-9)、23.5(q,C-10)、23.8(q,C-11)、24.5(q,C-12)、19.6(q,C-13)。与文献[11]比较,确定为吐叶醇。
化合物4:黄色粉末。IR(KBr,cm-1):3464、1619、1601、1445、1281、1189、1155、1111、1012、966、804、565。UV:221.8、249.0、338.2(max)nm。1H-NMR(400 MHz,CD3OD)δ∶2.36(3H,s,4-H)、6.57(1H,d,J=16.0 Hz,1-H)、7.54(1H,d,J=16.0 Hz,2-H)、7.10(1H,d,J=2.0 Hz,2’-H)、6.81(1H,d,J=8.4,2.1 Hz,5’-H)、7.01(1H,dd,J=8.4,2.1 Hz,6’-H)。13C-NMR(100 MHz,CD3OD)δ∶27.0(C-4)、115.3(C-2’)、116.6(C-5’)、123.5(C-2)、124.7(C-6’)、127.8(C-1’)、6.8(C-1)、146.9(C-3’)、150.0(C-4’)、201.5(C-3)。与文献[12]比较,确定为(E)-3,4-二羟基苯亚甲基丙酮。
化合物5:白色粉末。IR(KBr,cm-1):3386、1672、1602、1450、1312、1245、1215、1173、1012、978、831、557、515。UV:204.2、266.7 nm。1H-NMR(400 MHz,CD3OD)δ∶7.46(2H,d,J=8.6 Hz)、6.82(2H,d,J=8.6 Hz)、7.61(1H,d,J=16.0 Hz)、6.30(2H,d,J=16.0 Hz)。13C-NMR(100 MHz,CD3OD)δ∶146.6(C-1)、115.7(C-2)、171.0(C-3)、127.3(C-1’)、116.8(C-2’,6’)、131.1(C-3’,5’)、161.2(C-4’)。与文献[13]比较,确定为对羟基肉桂酸。
化合物6:白色粉末。IR(KBr,cm-1):3367、1684、1589、1381、1302、1248、1207、769、694。UV:212.4、252.5 nm。1H-NMR(400 MHz,CD3OD)δ∶:7.96(1H,d,J=2.0 Hz)、7.81(1H,dd,J=8.4,1.6 Hz)、6.96(1H,d,J=8.4 Hz)。13C-NMR(100 MHz,CD3OD)δ∶1 个羧基C 信号168.8;1 个苯环连氧(羟基)的C 信号158.8;3 个CH,分别为132.9、131.0 和117.1;2 个季碳信号为124.0 和121.7。与文献[14]比较,确定为3-氯-4-羟基-苯甲酸。
化合物7:黄色粉末。IR(KBr,cm-1):3421、1658、1604、1508、1450、1362、1207、1061、1012、970、833。UV:212.4、252.5 nm。1H-NMR(400 MHz,CD3OD)δ∶8.09(2H,d,J=8.8 Hz)、6.91(2H,dd,J=8.8 Hz);6.43(1H,d,J=2.0 Hz)、6.23(1H,d,J=2.0 Hz);5.15(1H,d,J=7.2 Hz)、4.59(1H,brs);1.14(3H,d,J=6.0 Hz)。13CNMR(100 MHz,CD3OD)δ∶179.4(C-4),166.1(C-7),163.0(C-5),161.5(C-4’),159.4(C-2),158.6(C-9),135.5(C-3),132.4(C-2’,6’),122.8(C-1’),116.2(C-3’,5’),105.7(C-10),100.0(C-6),94.9(C-8),glc(C-1~C-6)为104.6、75.8、78.2、72.3、77.2,68.6.rha(C-1~C-6)为102.4、71.5、72.1、73.9、69.7、17.9。与文献[15]比较,确定为山柰酚-3-O-芸香糖苷。
化合物8:白色粉末。IR(KBr,cm-1):3211、1660、1591、1452、1284、1219、1163、839、820、696、602、505。UV:220.6、262.0 nm。1H-NMR(400 MHz,CD3OD):7.79(2H,d,J=8.6 Hz)、6.93(2H,d,J=8.6 Hz)、9.78(1H,s)。13C-NMR(100 MHz,CD3OD)共有5 个C 信号,与文献[16]比较,确定为对羟基苯甲醛。
化合物9:白色粉末。1H-NMR(400 MHz,Pyr-d5)显示三萜皂苷的特征信号。13C-NMR(100 MHz,Pyrd5)显示共有1 组双键C 信号140.7 ppm 和121.7 ppm;1 个糖上端基C 信号102.4 ppm,与78.4、78.3、77.9、75.1、62.4 ppm,共同构成葡萄糖的骨架C 信号。与文献[17]比较,确定为胡萝卜苷。
化合物10:黄色粉末。UV 谱显示:232.4、207.2 nm。1H-NMR(400 MHz,CD3OD)显 示:7.51(2H,d,J=7.2 Hz)、6.83(2H,d,J=7.2 Hz);7.60(1H,d,J=16.0 Hz)、6.63(1H,d,J=16.0 Hz);2.36(3H,s)。13C-NMR(100 MHz,CD3OD)显示有1 个羰基信号201.5 ppm,1 个甲基信号27.1 ppm,苯环季碳信号161.6 ppm,一组对取代苯环的CH 质子信号131.6 ppm 和116.9 ppm。与化合物4 的核磁图谱比较,确定为对羟基亚苄基丙酮。
化合物11:白色粉末。1H-NMR(400 MHz,CD3OD)δ ∶6.81(1H,d,J=7.4 Hz)、7.44(1H,s)、7.43(1H,d,J=7.4 Hz)、3.84(3H,s)。3C-NMR(100 MHz,CD3OD)低场区显示共有7 个C 信号,含有酯羰基C 信号、苯环信号、季碳信号。与文献[18]比较,确定为3,4-二羟基苯甲酸甲酯。
化合物12:白色粉末。IR(KBr,cm-1):3462、3343、1696、1619、1535、1437、1372、1260、1198、1051、1001、768。UV:214.7、272.7 nm。1H-NMR(400 MHz,CD3OD):7.06(2H,s)、3.83(3H,s)。13C-NMR(100 MHz,CD3OD)低场区显示有5 个C 信号,高场区1 个甲氧基C 信号52.3 ppm。确定为没食子酸甲酯。
化合物13:黄色粉末。IR(KBr,cm-1):3284、1667、1608、1550、1454、1412、1350、1251、1147、962、812。UV:219.5、249.0、369.1 nm。1H-NMR(400 MHz,CD3OD)δ∶7.29(1H,d,J=16.0 Hz)和6.58(1H,d,J=16.0 Hz);6.77(1H,d,J=8.0 Hz)、6.94(1H,dd,J=8.0,1.6 Hz)和7.02(1H,d,J=1.6 Hz);5.56(1H,d,J=1.6 Hz)和6.14(1H,d,J=1.6 Hz);3.87(3H,s)。13C-NMR(100 MHz,CD3OD)结合DEPT 显示:该化合物含有14 个C 信号,其中7 个CH(137.0、121.7、116.4、116.3、114.6、101.1、88.3),1 个OCH3(56.6)。与文献[19]比较,确定为4-甲氧基-6-(3’,4’-二羟基苯乙烯基)-2-吡喃。
13 种化合物的化学结构式见图2。
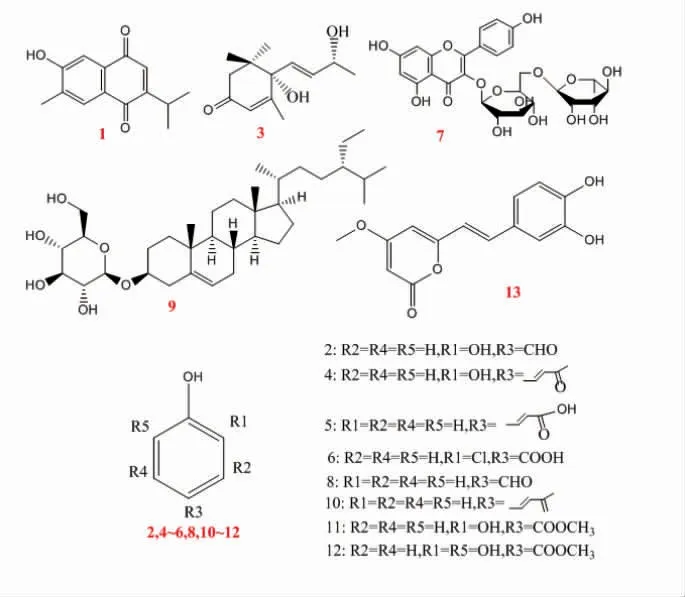
图2 铜丝藤根化学成分图
3 讨论
本研究从铜丝藤根中分离得到13 个化合物,其中酚类9 种、醌类2 种、黄酮类1 种、甾醇类1 种。化合物2~8、10~13 为首次从该植物中分离得到,也是首次从海金沙属中分离得到。
3-氯-4-羟基-苯甲酸(6)是一个较为少见的卤素取代化合物[20-21],其生理活性鲜见报道。4-甲氧基-6-(3’,4’-二羟基苯乙烯基)-2-吡喃(13)与抗癌活性显著的hispidin 化合物具有高度的结构相似性[22-25]。原儿茶醛能通过抑制丝裂原活化蛋白激酶信号通路降低肿瘤坏死因子-α、白细胞介素-6、白细胞介素-1β 等炎症因子的水平,发挥抗骨关节作用。(E)-3,4-二羟基苯亚甲基丙酮(4)、对羟基亚苄基丙酮(10)作为苯亚甲基丙酮类化合物可以作为潜在的抗骨质疏松类药物。本文建立了铜丝藤根成分的分离工艺,可为以上化合物的后续研究提供借鉴。
