达格列净联合前列地尔治疗糖尿病肾病的安全性分析
2022-06-08石建霞彭永德
刘 奇,石建霞,林 毅,彭永德
1.上海交通大学附属第一人民医院内分泌代谢科,上海 200080;2.上海市浦东新区浦南医院内分泌科,上海 200125
糖尿病肾病(DN)是糖尿病最常见的并发症,已成为终末期肾病的主要原因。DN治疗主要以延缓或逆转肾脏损害,降低心血管系统、神经系统等并发症发生率,改善患者生存质量为目标[1-2]。合理地控制血糖,可有效预防并延缓DN发生、进展,故选择科学的降糖方案是治疗DN的重要基础[3]。肾小球高灌注及高压力等血流动力学因素改变,在DN发生、进展中起关键作用[4]。前列地尔是一种血管扩张剂与血小板聚集抑制剂,可有效促进血管扩张,抑制血小板聚集,调节血液动力学与流变学,进而有利于改善肾脏微循环,在DN治疗中发挥着重要作用[5]。达格列净属钠-葡萄糖协同转运蛋白-2(SGLT-2)抑制剂,可通过抑制SGLT-2减少滤过葡萄糖重吸收,促使葡萄糖肾阈值降低,增加尿糖排泄,进而达到降低血糖的目的[6]。本研究试分析达格列净联合前列地尔治疗DN的临床价值,以期为DN患者寻求一种安全、有效的治疗方案。
1 资料与方法
1.1 临床资料
经医院伦理委员会审核批准,选择120例DN患者作为研究对象。纳入标准:(1)符合DN临床诊断标准[7];(2)无心、肺功能障碍;(3)未合并脑血管疾病;(4)无认知或视听障碍,能进行有效沟通;(5)自愿签署研究知情同意书。排除标准:(1)原发性肾病综合征或过敏性紫癜肾炎;(2)合并血液系统、自身免疫系统疾病;(3)合并未控制的急慢性感染;(4)合并糖尿病足、糖尿病视网膜病变等其他糖尿病继发疾病;(5)合并恶性肿瘤疾病;(6)入组前已接受DN系统治疗;(7)妊娠期或哺乳期女性。按照随机数字表法分为2组,2组基线临床资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
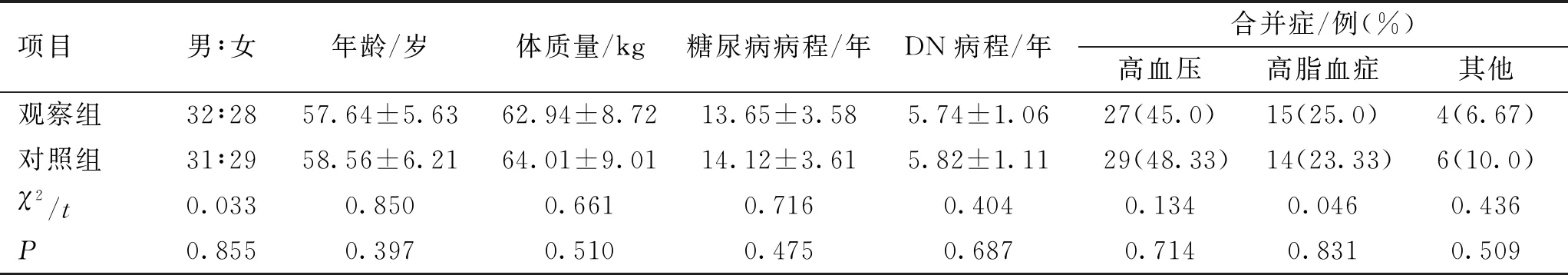
表1 2组基线临床资料比较 (n=60)
1.2 治疗方案
2组均给予控制血压、调脂、限制蛋白质摄入量、积极治疗并发症、生活方式指导等常规对症支持治疗与干预。在此基础上,对照组给予注射用前列地尔(北京德泰制药股份有限公司,规格:2 mL∶10 μg)10 μg前列地尔与10 mL生理盐水混合稀释,静脉滴注,每日1次;观察组采取达格列净(AstraZeneca Pharmaceuticals LP,规格:10 mg·片-1)联合前列地尔治疗,前列地尔用法用量同对照组,口服达格列净10 mg,每日1次。2组均治疗8周。
1.3 观察指标
1.3.1血糖控制水平 对比2组治疗前后糖化血红蛋白(HbA1c)、空腹血糖(FPG)、餐后2 h血糖(2 h PG)水平。
1.3.2肾功能 抽取患者空腹状态下外周静脉血3 mL,离心处理后取上层血清送检,以苦味酸法检测血清肌酐(Scr),用迈瑞200全自动生化仪(武汉精诚伟业医疗设备有限公司)以酶偶联速率法检测血清尿素氮(BUN);采用中国人群改良的肾脏病膳食改良试验(MDRD)公式计算肾小球滤过率(eGFR):eGFR[mL/(min·1.73 m2)]=186×(Scr)-1.154×年龄-0.203×(女性0.742)×(中国人1.233);用酶偶联速率法检测微量蛋白尿肌酐,计算尿微量蛋白/尿肌酐(ACR)。
1.3.3血清炎症因子水平 抽取患者空腹状态下外周静脉血3 mL,离心处理后分离上层血清送检,以酶联免疫吸附(ELISA)法检测肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)和单核细胞趋化因子-1(MCP-1)水平,仪器为美国Bio-RAD 550型酶标仪。
1.3.4生活质量 用肾脏疾病生活质量简表(KDQOL-36)评估患者生活质量,量表包含肾脏疾病及透析相关生存质量(KDTA,共11个条目)与一般健康相关生存质量(SF-36,共8个条目)2个部分,分值为0~100分,分值越高表示患者生存质量越高[8]。
1.3.5安全性 治疗期间,监测患者的血常规、尿常规、肝功能及心电图,同时统计2组治疗期间不良反应发生率,记录不良反应临床表现、严重程度、处理方案及缓解时间,客观评价其治疗安全性。
1.4 统计学方法
2 结果
2.1 血糖控制
治疗前2组HbA1c、FPG和2 h PG水平比较差异无统计学意义(P>0.05);治疗后2组以上指标均较治疗前降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表2。

表2 2组血糖水平比较
2.2 肾功能
治疗前2组血清Scr、BUN、eGFR和尿ACR比较差异无统计学意义(P>0.05);治疗后2组以上指标均较治疗前改善,且观察组优于对照组,差异有统计学意义(P<0.05)。见表3。
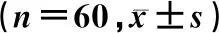
表3 2组肾功能比较
2.3 炎症因子
治疗前2组血清TNF-α、IL-6和MCP-1水平比较差异无统计学意义(P>0.05);治疗后2组以上指标均较治疗前降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表4。
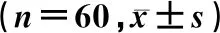
表4 2组血清炎症因子水平比较
2.4 生活质量
治疗前2组KDQOL-36各部分评分比较差异无统计学意义(P>0.05);治疗后2组KDQOL-36各部分评分均较治疗前升高,且观察组高于对照组,差异有统计学意义(P<0.05)。见表5。
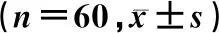
表5 2组KDQOL-36评分比较
2.5 安全性
治疗期间,监测患者血常规、尿常规、肝功能和心电图,未见异常;观察组不良反应发生率与对照组比较差异无统计学意义(P>0.05)。见表6。且2组不良反应均为轻度、一过性,未给予特殊干预自行缓解,未影响治疗进程。

表6 2组不良反应发生率比较 (n=60)
3 讨论
DN是由糖尿病引起的肾脏疾病,已成为终末期肾脏疾病的第二位原因,仅次于肾小球肾炎[9-10]。随着疾病进展,可出现蛋白尿、水肿和高血压等,严重者甚至引发肾衰竭,并累及心血管系统、消化系统和神经系统[11]。因此,应重视DN的早期防治,延缓或逆转肾功能损害。
前列地尔是临床常用的血管扩张剂,可有效扩张肾脏血管,改善微循环,促进肾脏血运系统恢复,进而提高eGFR[12]。合理控制血糖是临床治疗DN的重要措施,而达格列净是新型降糖药物,可通过尿液排出糖分,降低血糖水平[13]。本研究结果显示,治疗后观察组血糖水平、肾功能指标及KDQOL-36评分均优于对照组(P<0.05),且2组不良反应比较差异无统计学意义,提示上述联合方案治疗DN安全、有效,有利于患者血糖控制在合理水平,逆转肾功能损害,进而改善生活质量。血管活性物质增多、系统性血压增高和肾小球高压力等血流动力学因素可进一步加重DN的病情进展[14]。前列地尔属于天然前列腺素类物质,可通过扩张肾脏血管增加肾脏血流量及eGFR,促进肾脏血液循环改善,且可改善肾脏缺氧缺血状态,减少细胞脂质过氧化而保护肾脏,同时对肾小球基底膜细胞增生有显著抑制作用,有利于改善膜通透性,减少尿蛋白,进而延缓DN进展[15]。此外,高血糖状态下,钠-葡萄糖协同转运蛋白2(SGLT-2)表达上调,介导近端肾小管约90%尿糖重吸收,进而增加体液,上调血糖水平,加重肾脏负担[16]。SGLT-2抑制剂可通过降低肾脏葡萄糖重吸收阈值,增加尿葡萄糖排泄,控制血糖水平[17]。此外,SGLT-2抑制剂可下调血管紧张素Ⅱ受体1表达,增加抗氧化酶水平,减少氧化应激产物,有利于阻止肾间质纤维化,且可通过增加肾小球体积、减少远端肾小管糖原积累和改善肾小球系膜扩张,进而减轻肾损伤[18]。因而达格列净作为SGLT-2抑制剂,在DN治疗中发挥着降糖、降压和保护肾脏的多效作用,已成为DN治疗的新选择。因此,达格列净联合前列地尔治疗DN,通过不同机制发挥协同肾脏保护作用,进而延缓或逆转肾损伤。
近年来,随着临床对DN的深入研究发现,慢性炎症反应参与了DN的发生、进展。相关资料显示,TNF-α、IL-6可促使内皮细胞增殖,增加过氧化脂质代谢产物产生,并诱导血管内皮因子释放,致使肾小球基底膜通透性增加,造成蛋白尿,同时可促进血小板活化因子、前列腺素E2合成和释放,进而加重肾脏损害[19-20]。此外,资料还显示,单核细胞趋化因子-1(MCP-1)在DN慢性炎症过程中发挥着关键作用,并可通过促炎反应增加肾小球系膜外基质堆积,导致血管内皮细胞增生及基底膜增厚,进而加速肾小球硬化与肾间质纤维化[21-22]。本研究结果显示,治疗后观察组血清TNF-α、IL-6和MCP-1水平均低于对照组(P<0.05),提示达格列净联合前列地尔可通过下调TNF-α、IL-6和MCP-1等炎症介质表达,发挥肾脏保护作用。目前,已有研究证实达格列净与前列地尔具有抗炎作用,而本研究则进一步证明二者联合应用可通过抗炎作用降低TNF-α、IL-6和MCP-1等炎症因子水平,进而减轻由炎症因子诱发的肾脏损害,有利于保护肾功能。
综上,达格列净联合前列地尔治疗DN安全、有效,有利于控制血糖,改善患者的肾功能及生活质量,且可能与下调血清TNF-α、IL-6和MCP-1等炎症介质表达有关。
