2016-2020年重庆地区单采血小板献血者血液筛查结果的回顾性研究*
2022-05-27张巧琳韩凤娇杨冬燕
张巧琳,韩凤娇,王 娟,魏 兰,杨冬燕,王 芳
重庆市血液中心检验科,重庆 400000
血小板制剂在临床输血治疗中具有重要作用,因血小板功能障碍、大量失血、放疗和化疗等处理导致血小板减少的患者,均需进行血小板输注治疗[1]。单采血小板具有纯度高、不良反应少等特点,在临床上运用广泛。与其他血液制品不同,血小板离体后需(22±2)℃震荡保存,因面临细菌污染风险,有效期仅为5d。极短的保质期及临床大量需求经常导致其用血紧缺[2]。因此,分析单采血小板献血者的血液筛查结果,分析不合格项目及其危险因素,可为建立有效的招募策略,从低危人群中建立长期、固定的单采血小板献血者队伍提供有效的数据支持。本研究将回顾性分析重庆市血液中心2016-2020年单采血小板献血者的血液筛查结果,分析不同分组中各筛查项目的不合格情况。现将结果报道如下。
1 资料与方法
1.1一般资料 选取2016-2020年于重庆市血液中心捐赠单采血小板的18 473例献血者为研究对象,共计捐献68 755次,献血量107 774 U;其中男11 165例,女7 308例;年龄18~55岁。所有献血者按相关要求进行献血前体检及初筛,并且于献血前签署《献血者知情同意书》。
1.2仪器与试剂 全自动酶联免疫检测分析仪(FAME24/20)、全自动加样仪(HAMILTON STAR)、奥林巴斯全自动生化分析仪(AU680)、PROCLEIX Ultrio、PROCLEIX Ultrio Plus和Procleix Panther核酸检测系统均购自美国诺华公司;主要筛查项目试剂:乙肝表面抗原(HBsAg)诊断试剂盒(北京万泰,索林);抗-丙型肝炎病毒(HCV)试剂(北京万泰,强生Ortho-Clinical Diagnostics Inc);抗-人类免疫缺陷病毒(HIV)1/2试剂(法国伯乐);抗-梅毒螺旋体(TP)试剂(北京万泰);谷氨酸氨基转移酶(ALT,烟台奥斯邦),筛查试剂均经国家批检合格并在有效期内使用;核酸检测试剂:使用核酸仪器厂家配套原装试剂盒,该试剂可同时定性检测人类血浆中的 HIV-RNA、HCV-RNA和乙型肝炎病毒(HBV)-DNA,试剂盒内含有配套的HBV、HIV、HCV核酸鉴别试剂。
1.3方法
1.3.1血液筛查 献血者捐献单采血小板时留取两管抗凝血标本分别进行血清学血液筛查和核酸检测,项目包括ABO血型正反定型、RHD血型定型、ALT,以两种不同厂家酶联免疫吸附试验(ELISA)试剂盒检测HBsAg、抗-HCV、抗-HIV1/2、抗-TP,所有检测均严格按照试剂说明书进行操作与判定。
1.3.2核酸检测 本研究的所有献血者标本的核酸检测均采用核酸等温扩增原理,采用单人份标本进行HBV-DNA、HCV-RNA、HIV-RNA核酸联合检测,当检测结果呈反应性时,采用配套试剂盒进行HBV-DNA、HCV-RNA、HIV-RNA的鉴别检测。
1.4统计学处理 采用SPSS22.0统计软件对数据进行处理和分析,计数资料以例数和百分率表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1单采血小板献血者筛查项目不合格分布 2016-2020年单采血小板献血者每年献血次数和献血量分布情况见表1。筛查项目中ALT不合格率最高,为0.307%(211/68 755);抗-TP不合格率为0.079%(54/68 755);HBsAg/HBV-DNA不合格率为0.238%(164/68 755);抗-HCV/HCV-RNA不合格率为0.103%(71/68 755);抗-HIV/HIV-RNA不合格率为0.096%(66/68 755);2016-2020年年度筛查不合格率分别为0.70%、1.28%、0.96%、0.95%、0.83%;经核酸检测HBV为反应性,但ELISA检测为无反应性31例(0.045%);HIV血清学窗口期(最初检测时ELISA阴性,但核酸检测阳性)1例。筛查项目不合格详细分布情况见表2。
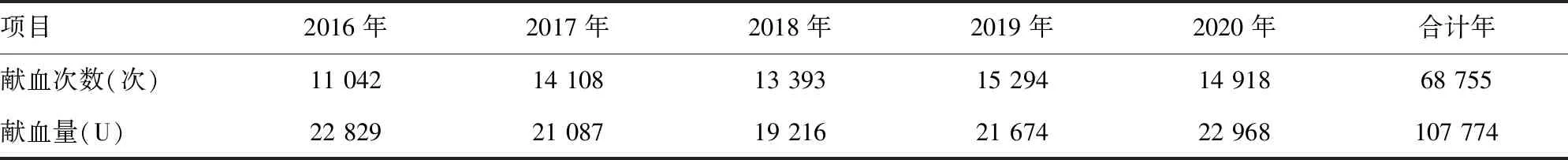
表1 2016-2020年重庆市单采血小板献血情况
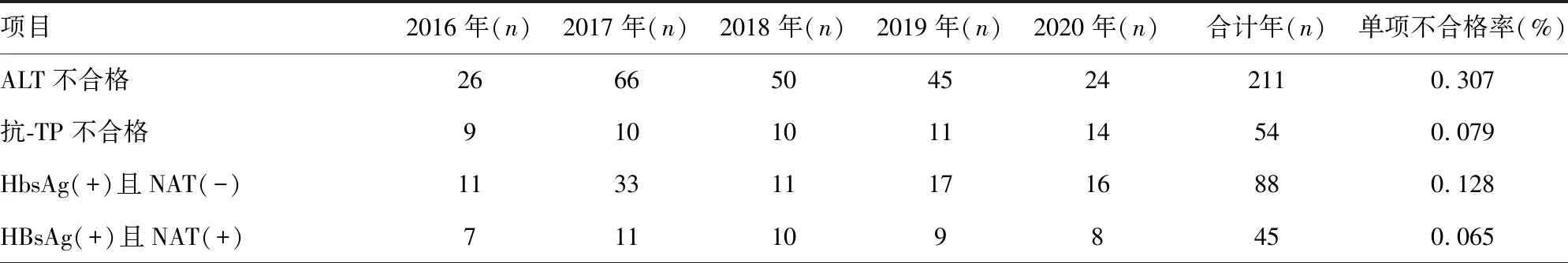
表2 2016-2020年重庆市单采血小板筛查项目不合格分布情况
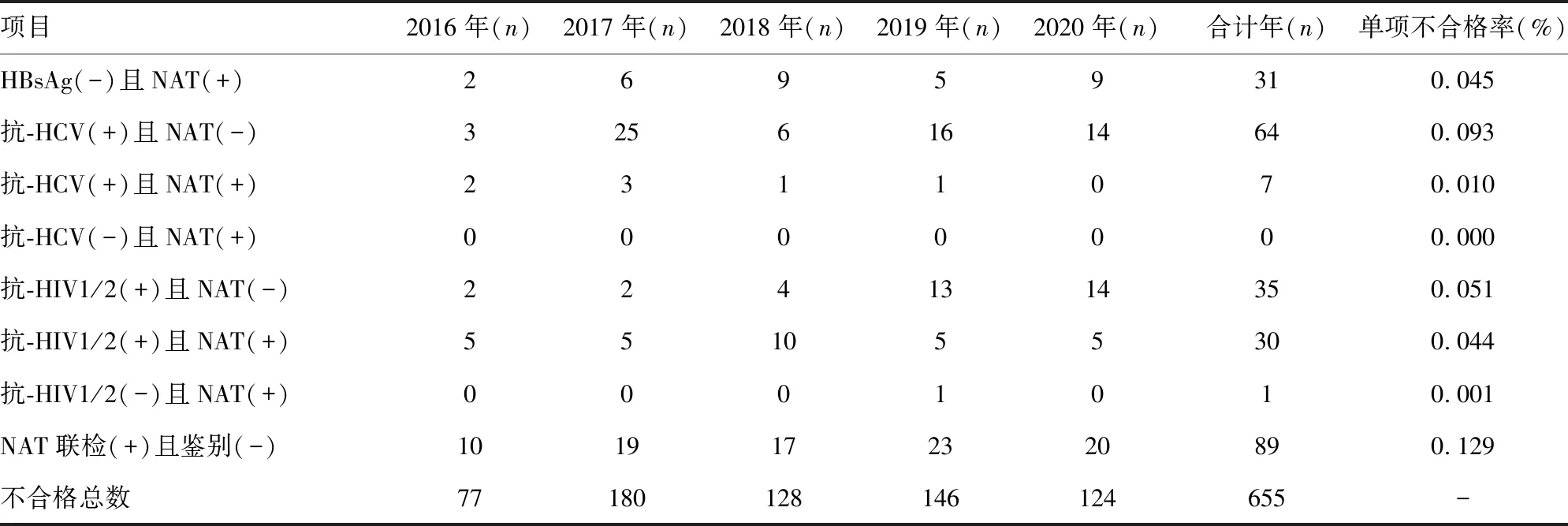
续表2 2016-2020年重庆市单采血小板筛查项目不合格分布情况
2.2各项目筛查不合格率年度趋势 根据血液筛查策略,抗-TP项目采用两种厂家的ELISA试剂血清学检测两次,HBV、HCV、HIV外加核酸进行了相应标志物检测,HBV、HCV、HIV不合格率包含了ELISA和核酸检测不合格之和,2016-2020年筛查不合格率年度趋势见图1。
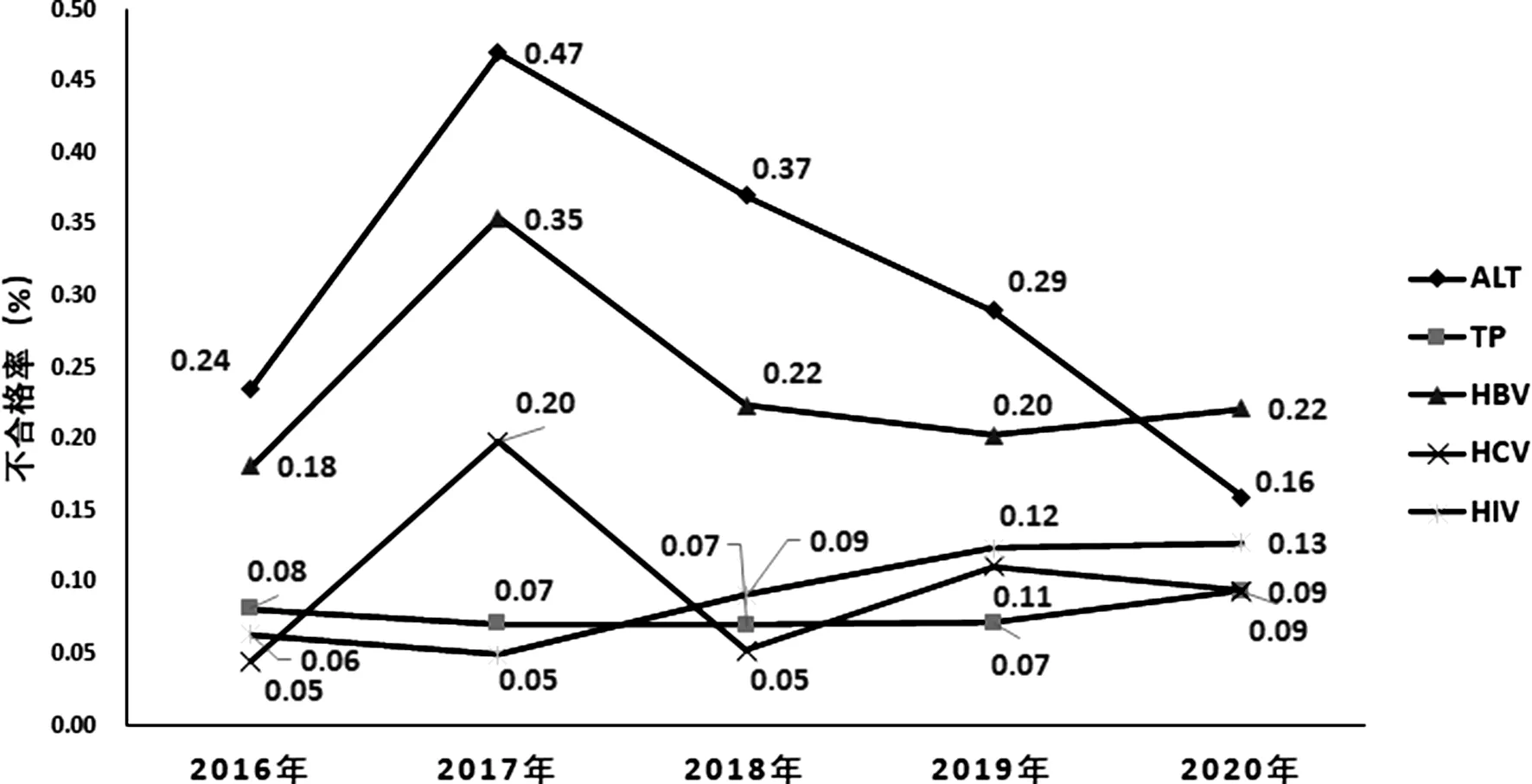
图1 各筛查项目2016-2020年总不合格率年度趋势图
2.3首次与重复献血者中抗-TP不合格情况 2016-2020年单采血小板献血者中共检出抗-TP不合格52例,其中首次献血者32例,重复献血者20例,差异有统计学意义(χ2=3.311,P<0.05);52例抗-TP不合格献血者中,男30例,女22例,不合格率比较,差异有统计学意义(χ2=8.066,P<0.05)。
2.4不同分组中核酸检测结果情况 2016-2020年,本中心单采血小板的首次献血者有9 041例,重复献血者(≥2次)有9 432例,核酸检测鉴定结果中,首次献血者和重复献血者HBV-DNA不合格率比较,差异有统计学意义(χ2=11.580,P<0.01),HCV-RNA和HIV-RNA不合格率比较,差异无统计学意义(P>0.05);HBV-DNA在不同年龄段比较,差异有统计学意义(P<0.05),年龄>45岁者HBV-DNA不合格率最高,HCV-RNA和HIV-RNA不合格率在不同年龄段中比较,差异无统计学意义(P>0.05);男性HIV-RNA不合格率明显高于女性(χ2=8.645,P<0.05);16例HIV核酸鉴定不合格重复献血者(经重庆疾病预防控制中心确认为阳性)共计献血225次,平均每人捐赠14次。见表2。
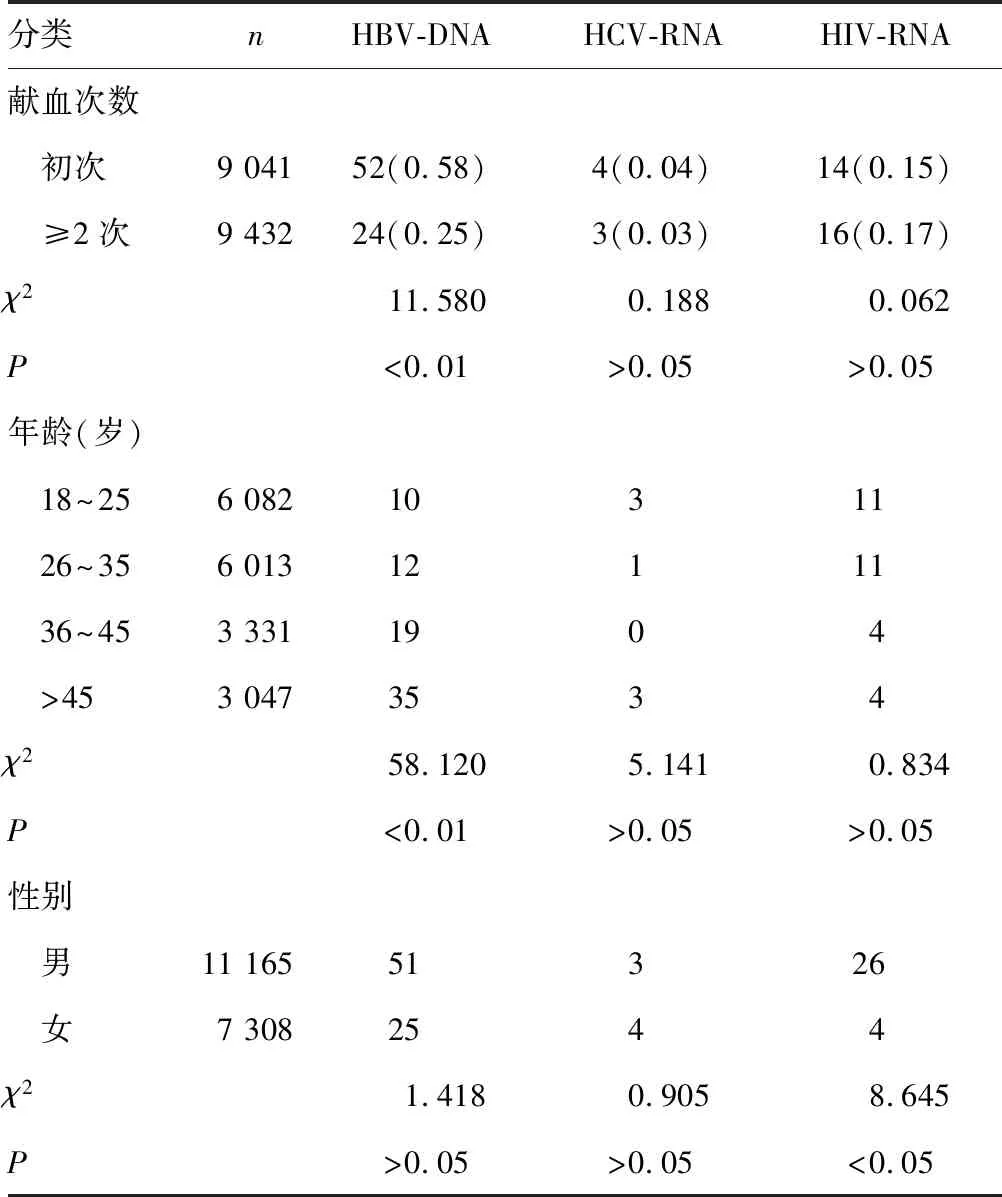
表2 2016-2020年核酸检测鉴定不合格情况分布[n(%)]
3 讨 论
近年来,临床对单采血小板的需求不断增加,而单采血小板献血者招募难度大,其产品保存有效期短,致其临床血小板供应非常紧缺。建立一支固定的、低风险的单采血小板献血者队伍迫在眉睫。分析历年单采血小板献血者血液筛查结果,可为献血招募和固定献血者队伍提供客观数据支持。
本研究回顾性分析了重庆市2016-2020年单采血小板数据,其中首次献血者有9 041例,重复献血者有9 432例,共计献血68 755次,献血量107 774 U。2016-2020年血液筛查总不合格率依次为0.70%、1.28%、0.96%、0.95%、0.83%。据报道,成都市血液中心2015-2019年44 508例单采血小板无偿献血者的血液检测总不合格率为4.96%[3];韶关血站2015年6月至2018年6月单采血小板捐献者血液检测不合格率为0.60%[4];广州2014年1月至2018年3月共检测单采血小板献血者标本157 692份,共检出1 495份不合格标本,总体不合格率为0.95%[5];郑州地区单采血小板不合格率为5.84%[6];西安地区单采血小板不合格率为4.05%[7];重庆单采血小板血液筛查不合格率在已报道的大部分数据中相对处于较低水平。
本研究的单采血小板献血者单项检测不合格项目中,ALT不合格率最高,为0.307%,占比近50%。导致ALT水平升高的原因有很多,据报道,和单采血小板献血者相关的主要因素为非病理性因素[8]。依据相关要求,在单采血小板献血前,ALT虽不是必检项目,但采集前对ALT项目进行筛查,合格后再献血可有效避免不必要的血液资源浪费和献血者流失。
2015年来,中国基本实现血站血液筛查核酸全覆盖。目前,HBV、HIV和HCV除采用ELISA进行血清学检测外,还需进行一次核酸检测。已有研究表明,核酸检测可缩短血液筛查窗口期[9-10]。本中心2016-2020年单采血小板献血者标本经核酸联检,检出反应性标本203例,经进一步鉴别实验,HBV核酸单反应性31例,这部分献血者血清学结果为无反应性,据已有的数据研究,这部分献血者为隐匿性乙型肝炎感染者,或者是急性感染者[11];本中心还检出1例HIV核酸单反应性献血者,经进一步追踪证实为HIV血清学窗口期献血者;HCV流行率较低,各项分组比较差异均无统计学意义(P>0.05)。据报道,HBV、HIV和HCV核酸联检在血液筛查中存在一定的假阳性结果,但其进一步的鉴别结果假阳性率较低,而ELISA单反应性结果(ELISA反应性而NAT无反应性)中假阳性率占比90%以上[12]。本研究将ELISA和核酸同时反应性的标本及HBV、HIV和HCV核酸单项鉴别反应性结果标本进一步在不同分组中进行比较。经分析,HBV-DNA在首次献血者的不合格率高于重复献血者,且年龄>45岁以上HBV-DNA不合格率最高,这与相关报道结果相似[13]。中国自1992年乙型肝炎疫苗接种计划以来,HBV感染者较疫苗接种普及之前有所降低,临床研究表明<30岁的HBV感染者占比最低[14]。
本研究数据显示男性献血者HIV筛查不合格率明显高于女性,而首次和重复献血者中HIV-RNA不合格率没有明显差异,本研究在9 041例首次献血者中,检出HIV(血清学和核酸同时不合格)14例,9 432例重复献血中检出HIV不合格16例(血清学和核酸同时不合格15例,1例核酸不合格),两者不合格率比较,差异无统计学意义(P>0.05);而16例重复献血者共计献血225次,平均每人捐赠14次。这其中可能原因为:献血者以检测身体为目的而参加献血,故意隐瞒身体真实状况;性教育知识缺乏,发生不安全性行为;已知感染HIV,仍去献血[15]。这提示,针对HIV筛查项目,在本地区重复血小板捐献者中,尤其是在男性群体中,无论是否是长期、固定捐赠者,献血间隔时间小于检测窗口期的情况下对其献血前的征询应视为重点关注点;此外,全国血站与疾病控制中心共享HIV阳性确认者信息,可有效阻止HIV确证阳性者参与献血,保障血液安全和资源浪费[16]。
综上所述,在本地区单采血小板献血者中,HBV、TP筛查项目在重复献血者中不合格率较低,在年龄>45岁中不合格率较高;HIV筛查不合格率在首次和重复献血者、不同年龄段中比较无明显差异,男性献血者HIV-RNA、抗-TP不合格率明显高于女性;建议本地区的单采血小板献血者固定队伍应在低龄、长期献血的队伍中建立,并重点注意献血前生活史方面的征询。
