基于生物信息学分析糖尿病肾病相关基因及信号通路的研究①
2022-05-25栾海艳张慧明王李鸣郑小鹏单洪超江智慧
谭 晶,栾海艳,张慧明,王 琳,王李鸣,郑小鹏,孙 跞,单洪超,江智慧,辛 华
(1.佳木斯大学附属第一医院,黑龙江 佳木斯 154003;2.佳木斯大学基础医学院,黑龙江 佳木斯 154007)
糖尿病肾病(diabetic nephropathy,DN)是糖尿病最常见的微血管并发症之一[1],也是世界范围内的一个重大公共卫生问题。据统计全球约有 4.2亿的糖尿病患者,平均每4名女性和每5名男性中就有1名患有2型糖尿病糖尿病肾病,这种现象在1型糖尿病中更为常见[2]。近年来,随着人们生活质量的提高,糖尿病的发病率在全世界范围内更是呈现突飞猛进的上升现象。约20%~30%的2型糖尿病(T2DM)患者有肾功能损害。在高血糖的持续刺激状态下,肾小球肾小管功能收到破坏。糖尿病患者胰岛素分泌不足,导致机体产生大量且稳定的糖基化终末产物(Advanced Glycation End products, AGEs)。AGEs在肾脏中的沉积导致肾小球基底膜逐渐变厚,系膜细胞大量增殖,肾小球硬化,肾间质出现纤维化等病变,同时引起基底膜增厚,细胞受损,肾小球滤过率增加。AGEs具有比高糖更强的胰岛β细胞毒性作用,是导致糖尿病持续恶化的重要因素。另一方面,AGEs大量积累,促进炎症因子释放,激活炎症反应,进一步促进糖尿病肾病的发生发展。糖尿病肾病主要临床表现为蛋白尿、水肿、高血压、肾衰竭、贫血,同时会引起心肌梗死、神经源性膀胱炎等并发症。有研究表明[3],糖尿病晚期100%并发视网膜病变,并伴随其病程加速视网膜恶化。糖尿病肾病患者常常合并代谢综合征,高血糖,高血脂症、高尿酸症等代谢疾病又进一步加重肾脏损伤,导致糖尿病肾病患者的5年生存率低于20%[4]。严重影响患者生活及生存质量。DN的致病因素和发病机制主要代谢紊乱、遗传因素、氧化应激、炎症影响等[5]。糖尿病肾病是由于胰岛素分泌不足或细胞对胰岛素反应无效而引起的肾脏微血管并发症,是终末期肾脏疾病的主要病因[6]。目前,治疗方法主要为药物治疗,其中以胰岛素注射治疗为主。这一疾病尚不能完全治愈,只能缓解相关症状及并发症,也不能改善糖尿病肾病病变的最终结果[7]。
1 资料与方法
1.1 一般资料
随着分子生物学技术的不断发展,芯片技术已经成为医学研究领域的重要研究手段之一,大量的基因芯片数据为临床治疗提供了更多可靠的治疗依据。本研究从Gene Expression Omnibus数据库(https://www.ncbi.nlm.nih.gov/)中下载编号为“GSE30122”、“GSE142153”的芯片数据,采用R语言(https://www.r-project.org/)中GEO query包下载GEO芯片矩阵及临床信息。其中,GSE30122芯片数据的原始文件有69个样本,健康组50例,糖尿病肾病组19例,所有样本全部为肾组织,并采用“GPL570”平台进行检测。GSE142153芯片数据的原始文件有40个样本,其中健康组10例,糖尿病肾病组23例,终末期糖尿病肾病7例,去除终末期糖尿病肾病后,对其余33例样本进行分析,所有样本全部为外周血,并采用“GPL6480”平台进行检测。
1.2 方法
1.2.1 差异基因
采用eBayes检验,通过R语言中Limma包对合并数据集进行差异分析,选取|logFC|>0.4。正常应该采用|logFC|>1,由于联合了不同的数据集,通过去批次效应后,会将部分差异基因|logFC|值降低,直接使用|logFC|>1,差异基因数较少。因此采取|logFC|>0.4,P<0.05为阈值。
1.2.2 KEGG通路富集
将“1.2.1”项下获取差异基因以gene symbol及logFC导入R,使用富集的clusterProfiler、ID转换的org.Hs.eg.db和绘图的ggplot2等加载包进行分析,以pvalueCutoff≤0.05和qvalueCutoff ≤0.05进行筛选。
2 结果
2.1 差异基因分析
通过limma包进行差异分析,共得到251个差异基因,其中上调基因174个,下调基因77个,对差异分析结果进行绘制火山图,红色部分为上调基因,绿色部分为下调基因,黑色部分为无差异基因,见图1;按|logFC|进行排序,选取前50个差异基因进行热图绘制可知,GSE30122、GSE142153采集样本为肾脏和外周血,结果显示前50个差异基因中,健康组和糖尿病肾病组存在一定差异,见图2。

图1 差异基因火山图(up: 上调基因;down: 下调基因;stable: 无差异基因)

图2 差异基因热图
2.2 KEGG通路富集分析
通过对差异基因KEGG通路富集分析,共得到37条KEGG通路富集结果,表明糖尿病肾病发病主要与Rheumatoid arthritis、Pertussis、NF-kappa B 等信号通路有关,见图3。

图3 KEGG通路富集分析结果图(A.气泡图;B.弦表图)
由图3 A-B可知,Rheumatoid arthritis信号通路主要有CXCL6、CCL5、ITGB2等12个基因参与,Pertussis信号通路主要有IL1B、LY96、IRF8等10个基因参与,NF-kappa B 信号通路主要有CXCL3、LTB、IL1B等11个基因参与。通过图4可知,Rheumatoid arthritis、Pertussis、NF-kappa B 信号通路等具有相同的基因。使用pathview加载包对通路关系图中关联度度值较高的结果进行染色,见图5。由图5 A-D可知,4条信号通路相互影响,除PLCy2基因为下调基因,其余都为上调基因。KEGG结果表明DN发病机制并非单一的,而是多靶点-多通路共同导致的。
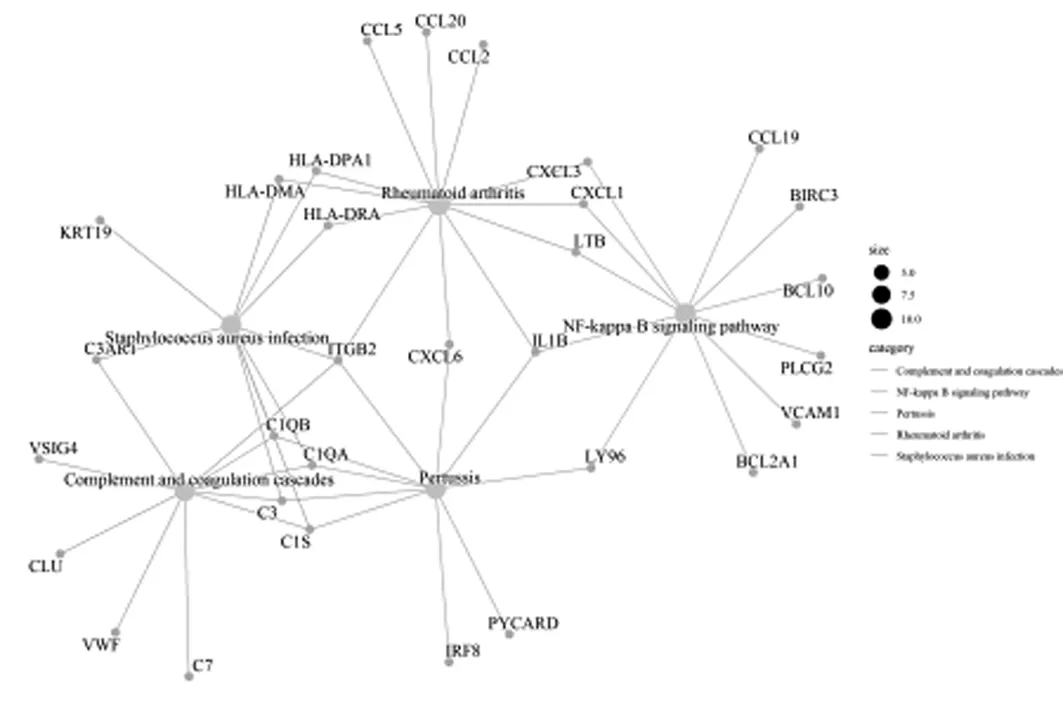
图4 通路-基因网络图

图5 KEGG通路富集结果染色图(A.Staphylococcus aureus infection信号通路;B.Rheumatoid arthritis信号通路;C.NF-kappa B 信号通路;D.TNF 信号通路)
3 讨论
本研究通过GEO数据库下载GSE30122数据,经过limmma包中normalizeBetweenArrays函数进行标准化,得到中位数齐,样品分布均匀,密度统一的质量分析结果。将GSE142153和GSE30122数据集进行合并,去除批次效应,使用limma包共获取251个差异基因,其中174个上调基因,77个下调基因。对差异基因进行KEGG富集分析,共得到37条KEGG通路富集结果。
分析结果显示,糖尿病肾病发病机制与Rheumatoid arthritis、Pertussis、NF-kappa B 等信号通路有关,Rheumatoid arthritis信号通路主要有CXCL6、CCL5、ITGB2等12个基因参与,Pertussis信号通路主要有IL1B、LY96、IRF8等10个基因参与,NF-kappa B 信号通路主要有CXCL3、LTB、IL1B等11个基因参与。通过可视化分析后的结果表明,糖尿病肾病发病机制是由多条通路相互影响导致的,发病机制复杂,需要多靶点-多通路综合分析。对统计结果的前10条通路进行关联性分析发现,影响最大的为炎症信号通路的相关基因,多种炎性因子介导的炎症反应有可能是造成血管内皮功能减退和肾小球内皮细胞损害的重要因素之一,是糖尿病肾病发病的重要机制。
糖尿病肾病是2型糖尿病患者发病和死亡的主要原因之一,也糖尿病患者发展为终末期肾病的主要原因。氧化和炎症损伤在糖尿病肾病的发病机制中起重要作用,病理上可见肾小球基底膜增厚等病变,临床上主要表现为白蛋白排泄增加和肾小球滤过率降低。因此,严格的控制血糖和血压是治疗糖尿病的重点,炎症的相关治疗可以有效地保护肾功能正常运行,延缓糖尿病肾病的发生发展。糖尿病肾病及其并发症的治疗尚未完全被人类所掌握,很大比例的糖尿病患者发展为终末期肾病,最后需要透析治疗,给患者及其家庭带来很多心理和经济上的压力。在寻找该疾病的潜在靶点和药物研究上我们还需进一步研发和开创,需要新的治疗方案,我们相信终有一天能攻克难关,为糖尿病肾病患者带来很多希望。
