MoS2/g-C3N4复合光催化剂催化降解H2S的研究*
2022-04-27张春灵
张春灵
(烟台国邦化工机械科技有限公司,山东烟台 264000)
H2S是石化企业尾气中的一种典型易燃、有毒、有害的酸性气体,也是造成大气污染的因素之一。H2S不仅对金属设备和石化管道有较强的腐蚀作用,而且会对环境造成严重的危害。因此,必须开发快速高效的H2S降解技术以解决其污染问题[1-2]。
在众多的污染物处理和净化技术中,光催化技术因其可以直接利用太阳光降解有机物,具有节能、高效、易操作、无二次污染等优点,有望成为治理H2S污染的一条廉价可行的途径[3-4]。TiO2及TiO2基复合物是目前研究最多的光催化降解H2S材料[5-6],但较宽的禁带宽度和较低的光催化性能限制了TiO2在光催化降解H2S方面的应用。
作为一种非金属型光催化剂类石墨相g-C3N4,因具有较窄的禁带宽度、合适的价带/导带位置、二维层状结构、化学稳定性好等优点,受到了很多研究者的关注[7-10]。但是,对于单一g-C3N4而言,尽管可以通过调控其尺寸、维度、晶化度和缺陷浓度等来改善其性能,但较高的光生载流子复合几率导致其光催化降解H2S性能偏低。
为了提高g-C3N4光催化降解H2S的性能,采用光照沉积法将生成的MoS2原位沉积到g-C3N4表面的活性位点,制备了MoS2/g-C3N4复合光催化剂,在分析MoS2/g-C3N4结构的基础上,探讨了MoS2的负载量、光催化剂的用量以及光源的强度对光催化降解H2S制取氢气性能的影响,为g-C3N4基复合光催化剂在光催化降解H2S的开发和应用上提供一定的技术指导。
1 试验部分
1.1 g-C3N4和MoS2/g-C3N4的合成
g-C3N4粉末的制备采用简单的三聚氰胺热处理法,具体试验过程如下:将10 g的三聚氰胺放入带盖子的坩埚中,然后通过高温炉加热,以5℃/min的升温速率从室温升至550 ℃,然后在550℃下保温2 h,最后将取得的试样中研钵中研磨为细粉,记得到淡黄色的g-C3N4粉末试样。
MoS2/g-C3N4的合成采用传统的光照沉积法,具体试验过程如下:在含有100 mL去离子水的烧杯中加入一定量的g-C3N4和H8MoN2S4,搅拌30 min后转移到光催化反应器中,在可见光下反应4 h。将得到的产物进行过滤、洗涤和烘干,最后得到不同负载量(w,下同)的MoS2/g-C3N4复合光催化剂。根据MoS2负载量的不同,制备的复合光催化剂分别表示为1% MoS2/g-C3N4,3% MoS2/g-C3N4,5% MoS2/g-C3N4,10% MoS2/g-C3N4。
1.2 结构表征
采用日本岛津公司的XRD-600型X射线衍射仪表征复合光催化剂的物相组成;采用美国赛默飞世尔公司的ESCALAB-250型X射线光电子能谱仪表征复合光催化剂的电子结构;采用美国麦克仪器公司ASAP 2020 M+C型全自动微孔比表面积和孔隙度分析仪检测复合光催化剂的比表面积,并利用BET理论计算得到最终的比表面积。
1.3 光催化性能表征
光催化降解H2S制取氢气的性能在中教金源的CEL-APR100H-3光化学控温一体化反应器中进行,氙灯采用的是中教金源的CEL-PF300-T8型氙灯,光功率从0到300 W可调,反应中生成的H2采用岛津GC-2014C型气相色谱仪进行在线检测(不锈钢填充柱、TCD检测器)。光催化降解H2S的试验如下:称取一定量的光催化剂粉末分散到100 mL的去离子水中,再加入1 mol/L的NaOH溶液和0.35 mol/L的Na2SO3溶液,然后将反应器封闭,通入(φ)20% H2S/Ar混合气体,使NaOH溶液饱和吸附H2S。开始光催化反应,每隔1 h通过气相色谱仪在线检测生成的氢气。
2 结果与讨论
2.1 XRD
g-C3N4和MoS2/g-C3N4试样的XRD谱图如图1所示。

图1 g-C3N4和MoS2/g-C3N4的XRD谱图
由图1可见:g-C3N4试样衍射角2θ=27.4°的特征峰对应于g-C3N4的(002)晶面,表明g-C3N4存在层间堆叠结构。光照沉积MoS2后,MoS2/g-C3N4试样的XRD特征峰与纯的g-C3N4一致,未观察到MoS2的衍射峰,这与MoS2/g-C3N4试样中MoS2的含量较低以及均匀负载有关。此外,在MoS2/g-C3N4试样的XRD谱图中,也未观察到其他新的衍射峰,说明MoS2的沉积并未对g-C3N4试样的晶体结构造成影响。
近年来关于特殊用途英语语篇和学术语篇的名物化研究有所增加。对于不同用途的英语语篇,研究者主要根据语篇的词汇特征提出翻译建议或探讨名物化在语篇中所起的特殊作用。而对于学术语篇,研究者更感兴趣的是名物化与阅读效率和写作质量方面的关系,考察名物化在诸如期刊论文、学位论文摘要、书评、学生作文、课本、讲座等类型的语篇中的使用频率、分布规律、功能,以及句法特征等,因此更多采用实证研究方法。
2.2 XPS
利用XPS能谱仪分析了3% MoS2/g-C3N4试样中Mo和S的元素组成和化学状态,结果如图2所示。
由图2可见:结合能在232.3,229.1,226.5 eV的3个特征峰分别对应于MoS2中的Mo 3d5/2,Mo 3d3/2,S 2s,而S 2p1/2和2p3/2的结合能分别为163.2,162.1 eV。结果表明,通过光照沉积法成功地将MoS2负载到g-C3N4表面。

图2 3% MoS2/g-C3N4试样中Mo和S的XPS谱图
2.3 BET
使用N2吸附-脱附表征g-C3N4和MoS2/g-C3N4试样的比表面积和孔体积,结果见表1。
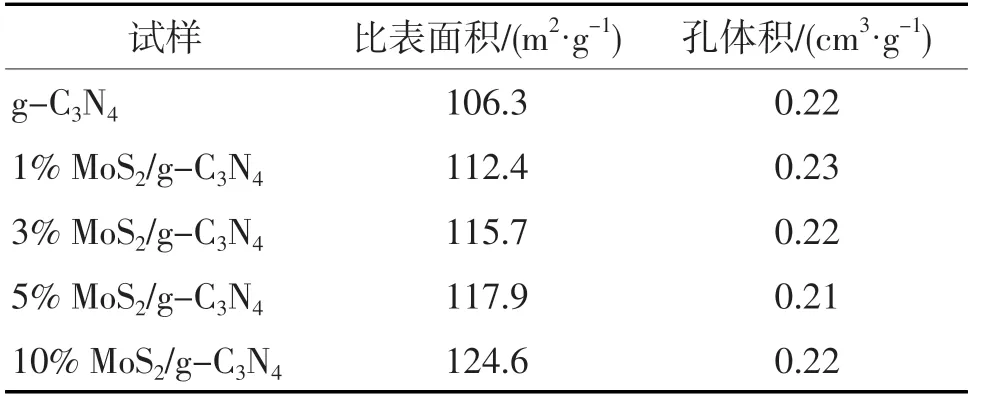
表1 g-C3N4和MoS2/g-C3N4试样的物化性质
由表1可见:采用热处理合成的g-C3N4试样,其比表面积为106.3 m2/g,孔体积为0.22 cm3/g。经过光照沉积MoS2后,MoS2/g-C3N4试样的比表面积逐渐增大,而孔体积基本保持不变,表明MoS2的负载并未破坏g-C3N4的孔结构。同时,较大的比表面积有利于在光催化反应中提供更多的吸附位和活性位。
2.4 光催化降解H2S性能
2.4.1 MoS2含量的影响
在g-C3N4和MoS2/g-C3N4试样光催化降解H2S制取H2的试验中,固定氙灯光源的功率300 W,光催化剂用量20 mg,分别记录光催化反应过程中产物H2的产量随光照时间的变化,结果见图3。

图3 MoS2负载量对光催化降解H2S制取H2的影响
由图3可见:随着光照时间的延长,H2的产量逐渐增加,表明所制备的光催化剂均具有良好的光催化稳定性。对于纯g-C3N4光催化剂,经过6 h的可见光反应后,H2的产量为6 235 μmol/g,对应的产氢速率为1 039.2 μmol/(h·g);通过在表面活性位点原位沉积MoS2后,MoS2/g-C3N4光催化降解H2S制取H2的性能明显增强。对于1% MoS2/g-C3N4光催化剂,经过6 h可见光反应后,H2产量为11 020 μmol/g,对应产氢速率为1 836.7 μmol/(h·g),是纯g-C3N4光催化反应的1.8倍;当MoS2的负载量达到3%时,3% MoS2/g-C3N4光催化降解H2S制取H2的活性最高,相应的产氢速率为3 205 μmol/(h·g),是纯g-C3N4光催化反应的3.1倍;进一步增大MoS2的负载量,光催化降解H2S制取H2的性能逐渐降低,但仍然高于纯g-C3N4光催化性能。结果表明,MoS2在g-C3N4表面的最佳负载量为3%,且MoS2的负载可以显著增强g-C3N4光催化降解H2S制取H2的性能。
在3% MoS2/g-C3N4试样光催化降解H2S制取H2的试验中,固定氙灯光源的功率为300 W,考察不同的光催化剂用量对光催化降解H2S制氢H2性能的影响,结果如图4所示。
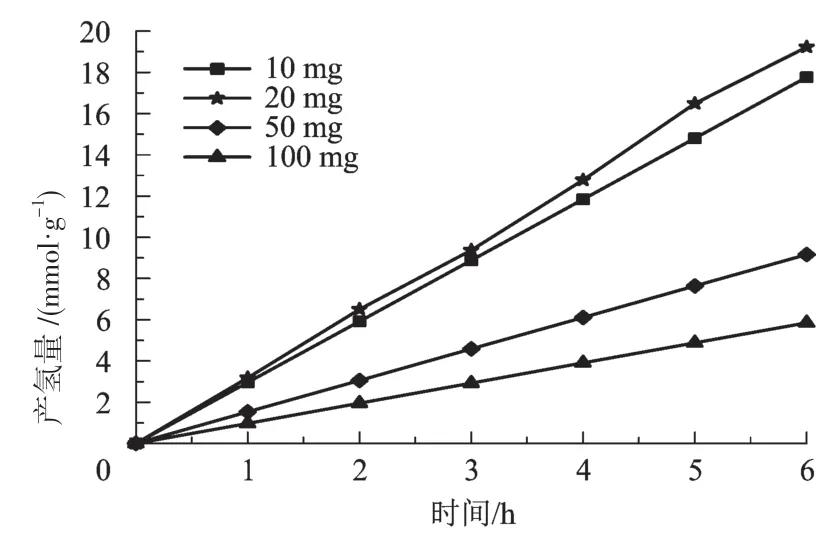
图4 光催化剂用量对光催化降解H2S制取H2的影响
由图4可见:当光催化剂用量为10 mg时,其绝对产氢速率为29.6 μmol/h,相对质量单位的产氢速率为2 960 μmol/(h·g);当光催化剂的用量增加至20 mg时,其绝对产氢速率和相对质量单位产氢速率分别为63.7 μmol/h和3 185 μmol/(h·g);当光催化剂的用量再增加至50 mg时,其绝对产氢速率和相对质量单位产氢速率分别为76.4 μmol/h和1 528 μmol/(h·g);当光催化剂的用量进一步增加至100 mg时,其绝对产氢速率和相对质量单位产氢速率分别为97.6 μmol/h和976 μmol/(h·g)。结果说明,对于光催化降解H2S制氢H2反应而言,在一定的光催化用量范围内,增加光催化剂的用量,其绝对产氢速率逐渐增大,但相对质量单位的产氢速率可能会降低。
2.4.3 光源强度的影响
对于光催化降解H2S制氢H2反应而言,光催化剂吸收光后首先产生光生载流子,随后光生载流子在复合之前会迁移至光催化剂表面,并与表面吸附的H2S发生光催化反应,生成H2。光源的强度会影响光催化剂产生光生载流子的数量,因此会影响光催化剂降解H2S制氢H2的性能。在3% MoS2/g-C3N4试样光催化降解H2S制取H2的试验中,光催化剂的用量20 mg,考察不同氙灯功率对光催化降解H2S制氢H2性能的影响,结果如图5所示。
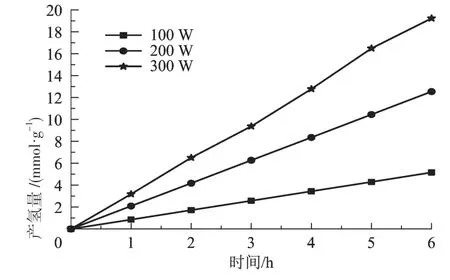
图5 氙灯功率对光催化降解H2S制取H2的影响
由图5可见:当氙灯的功率为300 W时,3%MoS2/g-C3N4试样光催化降解H2S制氢H2的速率为3 185 μmol/(h·g)。当氙灯的功率减至200 W时,其产氢速率降低2 090 μmol/(h·g)。当氙灯的功率进一步降低至100 W时,其产氢速率则降低到860 μmol/(h·g)。由此可见,随着氙灯功率的降低,产氢速率也随之降低。
2.5 光催化增强机理
根据上述结构表征分析和试验结果,提出了在MoS2/g-C3N4光催化体系中MoS2的增强机理,如图6所示。

图6 MoS2/g-C3N4复合光催化剂的光催化降解H2S的增强机理
由图6可见:在可见光激发下,复合光催化剂中g-C3N4的组分被可见光激发,分别在价带和导带产生光生空穴和光生电子。由于MoS2的费米能级低于g-C3N4的导带电位,光生电子可以从g-C3N4的表面迁移至MoS2的表面,从而提高了光生载流子的分离几率,这有利于光催化性能的增强。同时,在MoS2/g-C3N4的制备过程中,前驱体H8MoN2S4被g-C3N4表面的光生电子原位还原,生成的MoS2则直接负载在g-C3N4表面的活性位点,这是MoS2/g-C3N4体系光催化降解H2S制氢H2性能增强的主要原因。此外,MoS2的原位沉积还能增加光催化剂的比表面积,这也可以为光催化降解H2S的反应提供更多的吸附位和活性位。
3 结论
利用光照沉积法将MoS2原位负载到光催化剂g-C3N4表面的活性位点,生成的MoS2/g-C3N4复合光催化剂不仅未改变g-C3N4的晶体结构,还会增加光催化剂的比表面积。在光催化降解H2S制氢H2的反应中,当氙灯的功率为300 W、光催化剂的用量为20 mg以及MoS2的负载量为3%时,3%MoS2/g-C3N4试样光催化降解H2S制取H2的活性最高,产氢速率最高可达到3 205 μmol/(h·g),是纯g-C3N4光催化反应产氢速率的3.1倍,且表现出较好的光催化稳定性。通过对MoS2/g-C3N4复合光催化剂的结构表征分析和光催化试验结果,提出了在MoS2/g-C3N4光催化体系中MoS2的增强机理。该研究工作为石化企业尾气H2S的催化降解以及绿色氢能的光催化制取提供了一定的参考。
