艾立布林联合特瑞普利单抗治疗多线化疗失败的晚期乳腺癌的初步探索
2022-04-18桑蝶王依盟顾子凡范善民张育荣
桑蝶,王依盟,顾子凡,范善民,张育荣
北京市朝阳区三环肿瘤医院肿瘤内科,北京 100122
乳腺癌的发病率居全球女性恶性肿瘤第一位,极大地威胁女性的身心健康[1]。尽管约90%的乳腺癌患者接受了根治性手术及综合治疗,但仍有30%~40%的患者出现复发转移,转移性乳腺癌患者的中位生存期为2~3年[2]。然而针对紫杉类、蒽环类、长春瑞滨、吉西他滨、卡培他滨及铂类等药物已经产生耐药的乳腺癌患者,如何选择治疗方案仍是临床医师面临的一大挑战。艾立布林是非紫杉烷类微管抑制剂,用于已经接受过蒽环类及紫杉类药物治疗的转移性乳腺癌[3]。近些年来免疫检查点抑制剂程序性死亡受体1(programmed cell death 1,PDCD1,也称PD-1)单抗在实体瘤治疗中取得了突破性进展[4],但在中国乳腺癌的免疫治疗中应用仍较少。特瑞普利单抗是中国首个上市的国产PD-1单抗,本研究总结艾立布林联合特瑞普利单抗治疗多线化疗失败的晚期乳腺癌的疗效和安全性,以期为临床选择治疗方案提供一定参考,现报道如下。
1 资料与方法
1.1 一般资料
收集2020年1月至2021年1月于北京市朝阳区三环肿瘤医院接受艾立布林联合特瑞普利单抗治疗的多线化疗失败的晚期乳腺癌患者的病历资料。纳入标准:①经病理检查和影像学检查确诊为晚期乳腺癌,经多线化疗失败;②全面检查提示发生远处转移,至少有1个可测量病灶;③美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力状况评分≤2分;④生存期>3个月;⑤接受艾立布林联合特瑞普利单抗治疗;⑥重要脏器功能正常,化疗前血象、肝肾功能、心电图基本正常,无化疗禁忌证。排除标准:①脑转移灶未控制;②临床资料不全;③双原发恶性肿瘤。依据纳入和排除标准,本研究共纳入9例患者,病理类型均为浸润性导管癌;年龄为30~74岁,中位年龄为55岁,年龄>50岁7例,年龄≤50岁2例;Luminal型乳腺癌4例,三阴性乳腺癌5例;转移脏器或组织包括肝、肺、骨、脑、胸膜、淋巴结、盆腔、皮肤等,有内脏转移6例,无内脏转移3例;艾立布林联合特瑞普利单抗治疗线数:三线3例,四至九线6例;ECOG体力状况评分:0分5例,1分2例,2分2例。本研究经医院伦理委员会审核通过,所有患者均知情同意并签署知情同意书。
1.2 治疗方法
艾立布林1.4 mg/m2,第1天和第8天静脉滴注;特瑞普利单抗240 mg,第2天静脉滴注,21天为1个周期。每2个周期治疗后采用CT或MRI复查原发灶和转移灶,评价疗效,监测乳腺癌标志物变化;每3周复查甲状腺功能、肝肾功能及心电图,每周复查血常规1~2次,评估不良反应,直至肿瘤进展或患者不能耐受不良反应。
1.3 观察指标及评价标准
①临床疗效。依据实体瘤疗效评价标准(response evaluation criteria in solid tumor,RECIST)1.1版[5]进行疗效评估。完全缓解(complete response,CR):所有靶病灶及非靶病灶均消失;部分缓解(partial response,PR):靶病灶最大长径之和减少30%以上且非靶病灶未进展;疾病稳定(stable disease,SD):靶病灶最大长径之和减少不超过30%或增加不超过20%且非靶病灶未进展;疾病进展(progressive disease,PD):靶病灶最大长径之和增加20%以上或出现新病灶,非靶病灶进展。客观缓解率(objective response rate,ORR)(%)=(CR+PR)例数/总例数×100%,临床获益率(clinical benefit rate,CBR)(%)=(CR+PR+SD)例 数/总 例 数 ×100%。②不良反应发生情况。依据美国国立癌症研究所常见不良反应事件评价标准(National Cancer Institute-common toxicity criteria,NCI-CTC)4.0版[6]评估患者的不良反应。③生存情况。采用电话、门诊随访的方式对9例患者进行随访,随访截止时间为2021年9月1日,记录9例患者的疾病转归及生存情况。无进展生存期(progression-free survival,PFS)定义为从接受艾立布林联合特瑞普利单抗治疗开始至首次出现疾病进展或患者死亡时间。总生存期(overall survival,OS)定义为从接受艾立布林联合特瑞普利单抗治疗开始至患者死亡或随访截止时间。
1.4 统计学方法
采用SPSS 25.0软件对数据进行统计分析,计数资料以例数和率(%)表示,采用Kaplan-Meier法绘制生存曲线,组间比较采用Log-rank检验;以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效
9例患者的中位治疗周期为4个周期,PR 2例,SD 5例,PD 2例,ORR为22.2%,CBR为77.8%。亚组分析结果显示:三线接受艾立布林联合特瑞普利单抗治疗3例,PR 1例,SD 1例,PD 1例,ORR为33.3%,CBR为66.7%;四至九线接受艾立布林联合特瑞普利单抗治疗6例,PR 1例,SD 4例,PD 1例,ORR为16.7%,CBR为83.3%,其中1例三阴性乳腺癌患者第九线接受艾立布林联合特瑞普利单抗治疗,至末次随访时间2021年9月1日,已完成23个周期治疗,最佳疗效为PR,已缓解16个月。Luminal型乳腺癌患者4例,其中PR 1例,SD 2例,PD 1例,ORR为25.0%,CBR为75.0%;三阴性乳腺癌患者5例,其中PR 1例,SD 3例,PD 1例,ORR为20.0%,CBR为80.0%。存在内脏转移的乳腺癌患者6例,PR 1例,SD 4例,PD 1例,ORR为16.7%,CBR为83.3%;无内脏转移的乳腺癌患者3例,PR 1例,SD 1例,PD 1例,ORR为33.3%,CBR为66.7%。
2.2 不良反应分析
主要不良反应为中性粒细胞减少,发生率为66.7%,其中3~4级中性粒细胞减少发生率为33.3%;恶心呕吐发生率为33.3%,其中3~4级恶心呕吐发生率为11.1%;手足麻木发生率为22.2%,均为1~2级;甲状腺功能减退发生率为22.2%,均为1~2级。经对症处理后患者均恢复正常,未影响治疗。(表 1)
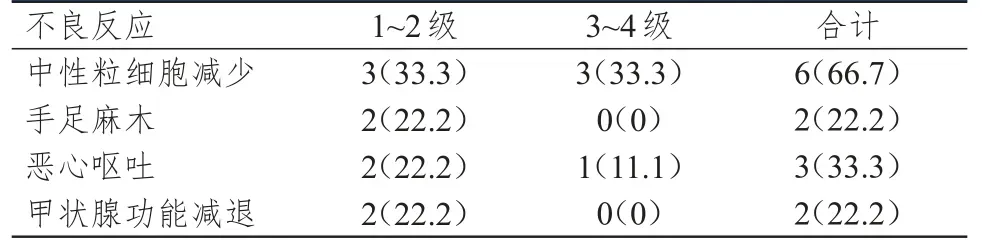
表1 艾立布林联合特瑞普利单抗治疗9例晚期乳腺癌患者的不良反应[n(%)]
2.3 生存分析
截至2021年9月1日,所有患者均未失访,随访率为100%,中位随访时间为7个月,患者的中位PFS为4个月,中位OS未达到。(图1、图2)
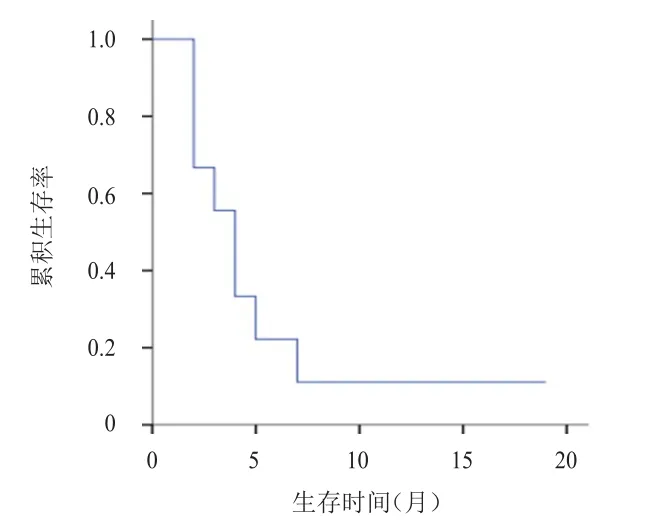
图1 9例接受艾立布林联合特瑞普利单抗治疗的晚期乳腺癌患者的PFS曲线
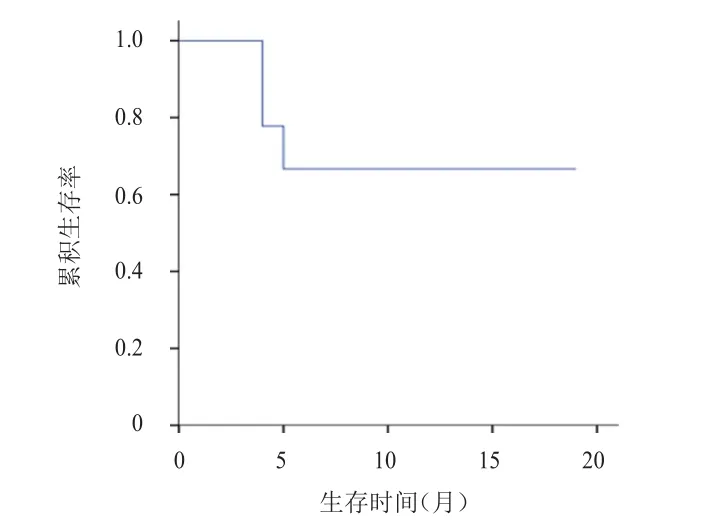
图2 9例接受艾立布林联合特瑞普利单抗治疗的晚期乳腺癌患者的OS曲线
3 讨论
晚期乳腺癌的治疗目标是延长患者的总生存期并改善生活质量。多项Ⅲ期临床研究证实艾立布林在乳腺癌治疗中具有兼顾疗效和安全性的优势[7-9]。因此,美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)、欧洲肿瘤内科学会(European Society for Medical Oncology,ESMO)、中国临床肿瘤学会(Chinese Society of Clinical Oncology,CSCO)等权威指南一致推荐艾立布林作为晚期乳腺癌新的化疗选择。近年来的临床研究显示,免疫治疗联合化疗治疗乳腺癌获得了较好的疗效[10-11]。KEYNOTE-355研究共纳入847例未经治疗的转移性三阴性乳腺癌患者,结果发现,在PD-L1联合阳性分数(combined positive score,CPS)≥10亚组中,帕博利珠单抗联合化疗组与单纯化疗组患者的中位PFS分别为9.7个月和5.6个月(HR=0.65,95%CI:0.49~0.86),ORR分别为53.2%和39.8%,疾病控制率(disease control rate,DCR)分别为65.0%和54.4%,该研究证实帕博利珠单抗联合化疗可改善转移性三阴性乳腺癌患者的PFS,PD-L1表达水平较高的患者ORR、DCR更高[12]。IMpassion130研究共纳入902例未经治疗的转移性三阴性乳腺癌患者,按1∶1随机分为阿特利珠单抗+白蛋白紫杉醇组和安慰剂+白蛋白紫杉醇组,分层因素中包括PD-L1表达阳性和PD-L1表达阴性,结果显示,PD-L1阳性组患者的中位OS为25个月,而PD-L1阴性组患者的中位OS为18个月,PD-L1阳性组患者的中位OS延长7个月,死亡风险降低33%,不良反应事件相似且可控[13]。I-SPY2研究针对Ⅱ/Ⅲ期高危人表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阴性乳腺癌患者进行新辅助治疗,结果发现,免疫治疗联合化疗相比单纯化疗可以提高早期HER2阴性乳腺癌患者的病理学完全缓解率(34.1%vs19.9%),亚组分析提示激素受体(hormone receptor,HR)阴性和HR阳性患者的病理学完全缓解率分别为43.7%和25.9%[14]。本研究中晚期乳腺癌多线治疗失败再接受免疫治疗联合化疗,其中2例患者PD-L1表达>1%,其余7例患者由于条件所限未能检测PD-1或PD-L1的表达情况。结果显示,Luminal型乳腺癌患者接受艾立布林联合特瑞普利单抗治疗后ORR为25.0%,CBR为75.0%,三阴性乳腺癌患者接受艾立布林联合特瑞普利单抗治疗后ORR为20.0%,CBR为80.0%,在两种分子亚型中均具有一定疗效,其ORR和PFS低于KEYNOTE-355和IMPassion130的结果,分析原因为本研究纳入的均为三线及以上治疗的患者,治疗的线数较晚,而KEYNOTE-355和IMPassion130研究纳入的均为一线治疗的患者。本研究中,三线接受艾立布林联合特瑞普利单抗治疗的患者3例,PR 1例,SD 1例,PD 1例,ORR为33.3%,CBR为66.7%,四至九线接受艾立布林联合特瑞普利单抗治疗的患者6例,PR 1例,SD 4例,PD 1例,ORR为16.7%,CBR为83.3%,提示三线选择艾立布林联合特瑞普利单抗治疗在ORR上较后线治疗有更优的趋势。本研究中1例三阴性乳腺癌患者在第九线接受艾立布林联合特瑞普利单抗治疗,至随访截止时间,已完成23个周期治疗,最佳疗效为PR,已缓解16个月,治疗中出现1级甲状腺功能减退。本研究结果显示,存在内脏转移的患者6例,PR 1例,SD 4例,PD 1例,ORR为16.7%,CBR为83.3%;无内脏转移的患者3例,PR 1例,SD 1例,PD 1例,ORR为33.3%,CBR为66.7%。
安全性分析,艾立布林联合特瑞普利单抗治疗的不良反应发生率:1~2级中性粒细胞减少为33.3%,3~4级中性粒细胞减少为33.3%,1~2级手足麻木为22.2%,1~2级恶心呕吐为22.2%,3~4级恶心呕吐为11.1%,1~2级甲状腺功能减退为22.2%。不良反应均可控可管理。Kim等[15]研究对比了吉西他滨+艾立布林与紫杉醇+吉西他滨治疗晚期HER2阴性乳腺癌的疗效和安全性,该研究共纳入118例患者,结果显示,两组患者的疗效相似,但艾立布林可延迟并减少神经毒性,其中30%的患者出现神经病变,而紫杉醇导致90%的患者出现神经病变。本研究神经毒性为1~2级,未影响治疗。化疗药物及免疫治疗引起骨髓抑制、消化道反应及甲状腺功能异常与文献报道相似[16-17]。
综上,艾立布林联合特瑞普利单抗治疗多线化疗失败的Luminal型和三阴性乳腺癌具有一定疗效,且不良反应可控,具有一定的应用前景。但是在精准治疗时代,需要扩大样本量探索化疗联合免疫治疗的最佳人群,从而提高疗效,减轻不良反应。
